2023-2024学年九年级化学人教版下册第十二单元化学与生活达标练习(含解析)
文档属性
| 名称 | 2023-2024学年九年级化学人教版下册第十二单元化学与生活达标练习(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 842.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-02-29 00:00:00 | ||
图片预览




文档简介
第十二单元化学与生活
学校:___________姓名:___________班级:___________考号:___________
一、选择题
1.学习化学最重要的是对知识进行归纳和整理,下列选项中不完全正确的是( )
A B C D
①农药和化肥的大量使用——不会引起土壤污染 ②塑料制品的大量使用——会造成“白色污染” ③化石燃料的大量使用——会造成空气污染 ①NaCl——俗称食盐 ②Na2CO3——俗称纯碱 ③NaOH——俗称火碱 ①CaO——氧化物 ②Ca(OH)2——碱 ③CaCO3——盐 ①人体缺碘——甲状腺肿大 ②人体缺铁——贫血 ③人体缺钙——骨质疏松
A.A B.B C.C D.D
2.“绿水青山就是金山银山”,水是人类不可缺少的宝贵资源。人人都要树立节约用水的意识。下列标志与节约用水有关的是
A. B. C. D.
3.安徽省2035远景目标:围绕地域传统美食,做响安徽绿色农食品品牌,下列安徽传统美食富含糖类的是
A.八公山豆腐 B.巢湖银鱼
C.太和板面 D.芜湖露仙酱泡菜
4.小明同学在复习阶段在笔记本上对化学知识进行了归纳整理:
①加热固体有气体产生的变化一定是化学变化
②可燃冰是混合物,开采其导致的温室效应,比二氧化碳更严重
③人呼出气体中含量最多的气体是CO2
④石油是一种重要的化工产品,是不可再生能源
⑤图书、档案、精密仪器等失火可用CO2灭火器
⑥物质与氧气发生的反应都是氧化反应,则氧化反应一定要有氧气参加。
上述说法正确的个数是
A.1 B.2 C.3 D.4
5.维生素C(化学式为C6H8O6)是一种水溶性维生素,也是一种常见的食品添加剂,能够阻止空气中的氧气将食品氧化变质。下列有关维生素C的说法正确的是
A.由3个元素组成 B.可以预防夜盲症
C.含有6个一氧化碳分子 D.其中氧元素的质量分数最大
6.下列有关生活中的做法正确的是
A.用刷漆的方式防止自行车链条生锈
B.炒菜时如油锅不慎着火,立即用冰水扑灭
C.蚊虫叮咬后在叮咬处涂抹适量肥皂水可得到缓解
D.焚烧废弃塑料解决“白色污染”问题
7.下列说法正确的是
A.回收废弃塑料可减少“白色污染”
B.缺钙引起贫血
C.用氯化钠固体配制50克10%的氯化钠溶液的主要步骤:计算、量取、溶解
D.合金的熔点和硬度均高于组成它们的纯金属
8.下列说法中,不正确的是
A.玻璃钢是常用的复合材料之一
B.糖类和维生素是人体中重要的供能营养素
C.氮肥、磷肥、钾肥及复合肥是农业生产中主要的化学肥料
D.重金属盐可使蛋白质发生化学变化,失去生理活性
9.继“食盐加碘”后,我国又将启动“酱油加铁”工程。“酱油加铁”的意义是
①补充人体需要的铁元素 ②预防缺铁性贫血病 ③改善酱油的味道 ④增加黑色素 ⑤减少厨房污染物 ⑥提高人民的健康水平
A.①②③
B.④⑤⑥
C.③④⑤
D.①②⑥
10.学校食堂为保证师生营养需求,每天提供几十道菜品,下列提供的食品中富含蛋白质的是
A.滑蛋虾仁 B.蒸青菜包 C.清炒菜心 D.水果拼盘
二、判断题
11.用工业酒精配制饮用酒( )
12.塑料、合成橡胶、合金都属于合成有机高分子材料( )
13.纤维素不能被人体吸收,所以食物中的纤维素对人体毫无意义( )
14.食物淀粉在人体内经酶的催化作用,与水反应最终变为葡萄糖( )
15.为减少“白色污染”,可将塑料垃圾集中焚烧处理( )
三、综合应用题
16.2022年1月31日,"三星堆遗址"出土青铜大面具,亮相春晚舞台。同时出土的还有黄金面具、青铜艺术品、象牙、残存丝织品等重要文物。
(1)下列物质中属于金属材料的有______。
A.象牙 B.黄金 C.丝织品 D.青铜
(2)青铜是铜的合金,其硬度比纯铜 (填“大”或“小”)。
(3)铜制品长期暴露在空气中能与空气中的O2、H2O和 化合生成铜锈【主要成分是Cu2(OH)2CO3】。
(4)黄铜是铜锌合金,用稀硫酸区分黄铜和纯铜的化学方程式为 。
(5)铜制品在生活中有广泛的应用。下图装置可做一氧化碳还原氧化铜的实验,并检验生成的气体产物。
①B装置玻璃管里可观察到的现象是 。
②C装置中反应的化学方程式为 。
③实验结束后,若要确定A装置的溶液中溶质的成分,请设计合理的实验方案,简要写出实验步骤、现象和结论。(提示:Na2CO3溶液呈碱性)。 。
④为测定A装置的溶液中Na2CO3的质量分数,取A装置的溶液100g,并向其中加入过量的BaCl2溶液,生成沉淀的质量是19.7g。计算A装置的溶液中Na2CO3的质量分数 。
17.珍珠粉是由珍珠经加工制成的白色粉末,含有碳酸钙、蛋白质等成分,是重要的药品、化妆品原料。但市场上出现的假珍珠粉外观上与真珍珠粉差不多,肉眼往往无法辨别它们。
(1)为了寻找区分真假珍珠粉的方法,科学兴趣小组的同学进行了如图1实验:
实验一:分别取真假珍珠粉适量置于两支试管中,加一定量的稀盐酸并将产生的气体通入澄清石灰水中,发现澄清石灰水均变浑浊,写出石灰水变浑浊的化学方程式 。说明真假珍珠粉均含有 。
实验二:分别取真假珍珠粉少量置于铁片上灼烧,发现真珍珠粉能闻到烧焦羽毛气味;假珍珠粉未闻到烧焦羽毛气味,由此可得出结论:假珍珠粉中不含 。
(2)为了比较真假珍珠粉中碳酸钙的含量,共进行了三次实验,每次各取5g真假珍珠粉,分别置于如图2实验装置中(稀盐酸足量且真假珍珠粉中只有碳酸钙与稀盐酸会反应生成气体),测定生成气体体积数据如下表:
样品 气体体积ml 次数 第一次 第二次 第三次
假珍珠粉 117.50 117.28 117.05
真珍珠粉 111.52 111.66 111.86
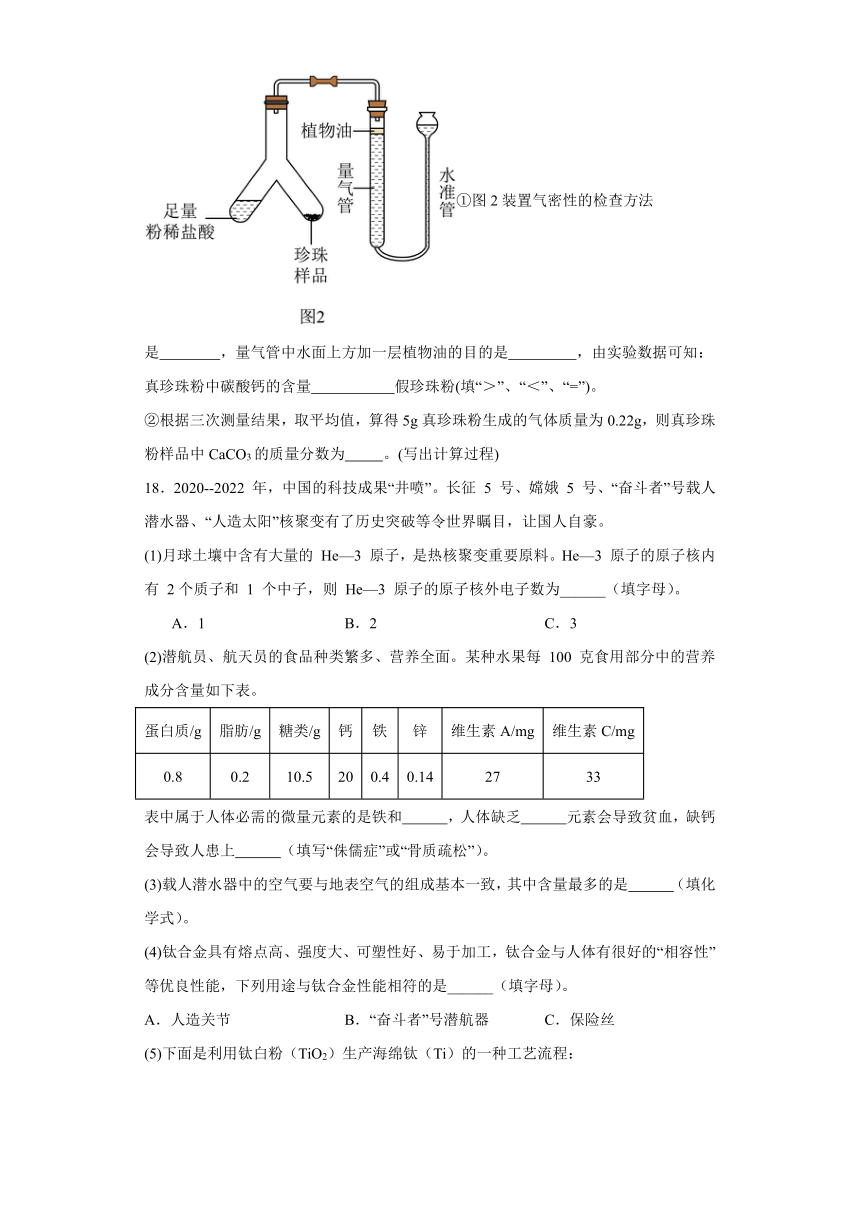
①图2装置气密性的检查方法是 ,量气管中水面上方加一层植物油的目的是 ,由实验数据可知:真珍珠粉中碳酸钙的含量 假珍珠粉(填“>”、“<”、“=”)。
②根据三次测量结果,取平均值,算得5g真珍珠粉生成的气体质量为0.22g,则真珍珠粉样品中CaCO3的质量分数为 。(写出计算过程)
18.2020--2022 年,中国的科技成果“井喷”。长征 5 号、嫦娥 5 号、“奋斗者”号载人潜水器、“人造太阳”核聚变有了历史突破等令世界瞩目,让国人自豪。
(1)月球土壤中含有大量的 He—3 原子,是热核聚变重要原料。He—3 原子的原子核内有 2个质子和 1 个中子,则 He—3 原子的原子核外电子数为______(填字母)。
A.1 B.2 C.3
(2)潜航员、航天员的食品种类繁多、营养全面。某种水果每 100 克食用部分中的营养成分含量如下表。
蛋白质/g 脂肪/g 糖类/g 钙 铁 锌 维生素A/mg 维生素C/mg
0.8 0.2 10.5 20 0.4 0.14 27 33
表中属于人体必需的微量元素的是铁和 ,人体缺乏 元素会导致贫血,缺钙会导致人患上 (填写“侏儒症”或“骨质疏松”)。
(3)载人潜水器中的空气要与地表空气的组成基本一致,其中含量最多的是 (填化学式)。
(4)钛合金具有熔点高、强度大、可塑性好、易于加工,钛合金与人体有很好的“相容性”等优良性能,下列用途与钛合金性能相符的是______(填字母)。
A.人造关节 B.“奋斗者”号潜航器 C.保险丝
(5)下面是利用钛白粉(TiO2)生产海绵钛(Ti)的一种工艺流程:
①右上图为镁元素的某种微粒结构示意图,该图表示 (填字母)。
A.原子 B.阳离子 C.阴离子
②已知:镁除了能与氧气反应,还可与氮气,二氧化碳反应。镁在氮气中燃烧能生成氮化镁(氮元素化合价为-3 价),则此反应的化学符号表达式为 。
③反应Ⅱ需在下列哪种环境中进行 (填字母)。
A.稀有气体中 B.空气中 C.氮气中 D.CO2气体中
四、填空与简答
19.化学来源于生活服务于生活。请回答下列生活中的有关化学问题:
(1)厨房中有下列几种食物:①黄瓜;②牛奶;③大米。其中富含维生素的是 。
(2)泡茶时,可在茶杯内装上纱网,该设计利用的化学实验操作原理是 。
(3)某品牌口罩中加入了活性炭滤片,利用了活性炭的 性。
(4)厨房中用洗洁精能去除餐具上的油污,是因为洗洁精具有 功能。
20.防疫情,测体温。体温测量仪功不可没。
(1)传统型 体温计、含汞血压计将在2026年起全面禁止生产,因为汞是人体中的 (选填“必需”或“有害”)元素。汞的元素符号是 。
(2)方便型——额温枪。某种额温枪的红外温度传感器所用材料含有钽酸锂(LiTaO3),钽酸锂中锂元素(Li)的化合价为+1价,则钽元素(Ta)的化合价为 价。在惰性气氛中制取钽的原理为:5Na+K2TaF7=Ta+2KF+5R,则R的化学式为 。
(3)快捷型——红外热成像测温仪。该测温仪可实现远距离、多目标、非接触式测温,可用于快速筛查人群中的高温个体。
①该测温仪还可用于 (填字母)。
A.测量物质溶解时的温度变化
B.分析鸡龙河水质
C.检测室内甲醛含量是否超标
②该测温仪外壳的塑料一经加工成型,受热不再熔化,是热 性塑料。
21.下列用字母表示的是初中化学常见的7种物质,其中A~E均为无色气体,A和B为单质。请根据下列叙述回答问题。
(1)A是一种理想的清洁燃料,其原因可以用化学方程式表示为 。
(2)X、Y的组成相同,在一定条件下均能分解产生B。X、Y分别是 。
(3)C、D的组成相同,C与B反应时生成D,C、D均由 元素组成。
(4)E中两种元素的质量比为3:1。A与D在催化剂作用下可生成E和B,该反应的化学方程式为 。E能在空气中燃烧,反应的化学方程式为 。
22.随着社会进步,饮食、材料、环境等成为人们关注的热点话题。
【舌尖上的化学】
(1)2023年3月15日是第41个国际消费者权益日,“舌尖上的安全”成为民生热词。下列做法不正确的是______。
A.用霉变的花生制作鱼皮豆
B.烹调食物时,放入一些加铁酱油
C.为防止海鲜腐烂,可用甲醛溶液浸泡
D.加工火腿肠时加入过量的亚硝酸盐防腐
【环境中的化学】
我国承诺在2030年前实现“碳达峰”,2060年前实现“碳中和”。
(2)化石燃料燃烧是造成碳排放量增加的主要因素。化石燃料包括煤、石油和天然气,石油主要含有 元素。
(3)科学家在高温、高压下以二氧化碳和氨气为原料制得尿素[CO(NH2)2],同时有水生成,这是固定和利用二氧化碳的成功范例。请写出该反应的化学方程式: 。
【材料中的化学】
(4)“手撕钢”的厚度不足0.02mm,用于“折叠屏手机”屏。将钢板轧成“手撕钢”,利用了金属的 性。
(5)碳酸锂(Li2CO3)是制备手机锂电池的重要原料,工业上以锂辉石精矿(主要成分为Li2O,其余成分不溶于水,也不参与反应)为原料制取Li2CO3,其主要工艺流程如图所示:提示:Li2CO3溶解度随温度的升高而减小。
①Li2CO3中锂元素的化合价为 。
②在投入酸浸槽前,锂辉石需进行粉碎研磨的预处理,其目的是 。
③反应器加入的Na2CO3溶液是饱和溶液,其作用是 。
④洗涤槽中使用热水,原因是 。证明Li2CO3洗涤干净的方法是 。(写操作,现象和结论)
23.阅读下面科普短文。
酱油是中国传统发酵调味品。酱油的鲜味和营养价值取决于氨基酸态氮含量的高低。氨基酸态氮是指以氨基酸形式存在的氮元素,其含量是衡量酱油营养价值的一项重要指标。氨基酸态氮含量越高,酱油品质越好,等级越高,标准见表1。
表1酿造酱油等级标准
项目 指标
氨基酸态氮g/100mL 特级 一级 二级 三级
≥0.80 0.70~0.79 0.55~0.69 0.40~0.54
酿造酱油是以大豆或脱脂大豆,小麦或麸皮为原料,经微生物发酵而成。食盐也是酱油酿造的重要原料之一、选用的食盐以氯化钠含量高、卤汁(氯化钾、氯化镁、硫酸钙等的混合物)少的品质为宜。酱油在酿造过程中会产生一系列带有特殊风味的物质。风味是传统发酵食品重要的质量指标,经实验测定发现。杀菌工艺对酱油风味物质的形成有一定影响。研究人员做了如下实验:将2份等量的生酱油分别加热到不同灭菌温度(90°C、98°C)并保温20min,灭菌后快速降温到45°C,保持24小时后检测酱油鲜、咸、甜等9项风味,实验结果如图。
酱油营养丰富,但由于含盐量高,亦不可过量食用。依据文章内容,回答下列问题。
(1)衡量酱油营养价值的重要指标是 。
(2)某酿造的酱油氨基酸态氮含量为0.90g/100mL,则该酱油的等级为 。
(3)卤汁(氯化钾、氯化镁等的混合物)其中含有的阴离子有氯离子其符号为 。
(4)由图可知,98℃灭菌条件下的酱油的 强于90℃灭菌条件下的酱油。
(5)下列说法正确的是 (填序号)。
A.酱油酿造过程发生了化学变化
B.购买酱油时应关注标签上氨基酸态氮的含量
C.酱油的风味指的是酱油的香气、后味、协调感、浓厚感等
参考答案:
1.A
【详解】A、农药和化肥的大量使用会引起土壤污染;塑料制品不易降解,大量使用会造成“白色污染”;化石燃料的大量使用会造成空气污染,故A错误;
B、NaCl俗称食盐,Na2CO3俗称纯碱,NaOH俗称火碱,故B正确;
C、CaO,是由两种元素组成,其中一种是氧元素,所以属于氧化物;Ca(OH)2电离出的阴离子只有氢氧根离子,所以属于碱;CaCO3是由钙离子和碳酸根离子构成的化合物,所以属于盐,故C正确;
D、人体缺碘会患甲状腺肿大;人体缺铁会患贫血;人体缺钙会患骨质疏松,故D正确.
故选A.
【点睛】化学来源于生产和生活,也服务于人类的生产和生活,因此与人类生产和生活相关的化学知识就成了中考的热点之一.
2.D
【详解】A、图为禁止吸烟标志,故A错误;
B、图为腐蚀品标志,故B错误;
C、图为塑料回收循环利用标志,故C错误;
D、图为节约用水标志,故D正确。
故选D。
【点睛】
3.C
【详解】A、八公山豆腐中高含蛋白质,故A选项不符合题意;
B、巢湖银鱼中富含蛋白质,故B选项不符合题意;
C、太和板面中富含淀粉,淀粉属于糖类,故C选项符合题意;
D、芜湖露仙酱泡菜富含维生素,故D选项不符合题意。
故选C。
4.B
【详解】①加热固体有气体产生的变化不一定是化学变化,例如加热固体碘生成碘蒸气,该变化没有新物质生成,属于物理变化,故错误;
②可燃冰主要含有甲烷水合物(由甲烷分子和水分子组成),属于混合物;如果开采不当,甲烷气体将大量泄漏于空气中,其造成的温室效应将比二氧化碳更加严重,故正确;
③空气中含量最多的气体是氮气(约占空气体积的78%),氮气不参与呼吸作用,因此人呼出气体中含量最多的是N2,故错误;
④石油是一种重要的化工原料,在短期内不能得到补充,是不可再生能源,故错误;
⑤图书、档案、精密仪器等失火可用CO2灭火器,不会留下痕迹,减小损失,故正确;
⑥物质与氧气发生的反应都是氧化反应,但是氧化反应不一定要有氧气参加,如一氧化碳在加热条件下与氧化铜反应生成铜和二氧化碳,一氧化碳发生了氧化反应,故错误;
其中②⑤两个正确;
故选:B。
5.D
【详解】A、如题根据维生素C的化学式可知维生素C是由碳元素、氢元素和氧元素,三种元素组成的化合物,选项说法错误;
B、人体缺少维生素C会患坏血病,选项错误;
C、一个维生素C分子是由6个碳原子、8个氧原子和6个氧原子构成,不含其他物质的分子,选项错误;
D、维生素C中碳元素、氢元素和氧元素的质量比是,说明其中氧元素的质量分数最大,选项正确;
答案为:D。
6.C
【详解】A、生活中用涂油的方式防止自行车链条生锈,A错误。
B、炒菜时如油锅不慎着火,立即锅盖盖灭,B错误。
C、蚊虫叮咬处有酸性物质,肥皂水显碱性,蚊虫叮咬后在叮咬处涂抹适量肥皂水可得到缓解,C正确。
D、焚烧废弃塑料会产生大量烟尘,污染空气,D错误。
故选:C。
7.A
【详解】A、“白色污染”是由废弃塑料难处理、难降解导致的,回收废弃的塑料,能有效降低废弃塑料的污染,减少“白色污染”,该选项正确;
B、钙主要存在于骨骼和牙齿中,使骨和牙齿具有坚硬的结构支架,缺乏钙元素主要会导致幼儿和青少年患佝偻病、软骨症等,贫血往往是因为缺少铁元素导致的,该选项错误;
C、用氯化钠固体配制50克10%的氯化钠溶液的主要步骤:计算、称量、量取、溶解、装瓶贴标签,该选项错误;
D、根据合金的特性可知,合金的硬度高于组成它们的纯金属,熔点低于组成它们的纯金属,该选项错误。
故选A。
8.B
【详解】A、玻璃钢是玻璃与塑料叠合在一起形成的具有金属性能的新型材料,属于复合材料,选项正确;
B、糖类能为人体提供能量,属于供能营养素,而维生素能够参与人体的代谢活动,不能为人体提供能量,不是人体中的供能营养素,选项错误;
C、氮肥、磷肥、钾肥及复合肥能够为农作物提供营养元素,是农业生产中主要的化学肥料,选项正确;
D、重金属盐可使蛋白质发生化学变化,失去生理活性,选项正确,故选B。
9.D
【详解】“酱油加铁”工程能①补充人体需要的铁元素;②预防缺铁性贫血病;⑥提高人民的健康水平,故①②⑥组合正确。故选D。
10.A
【详解】A、滑蛋虾仁富含蛋白质,故选项符合题意;
B、蒸青菜包中富含糖类和维生素,故选项不符合题意;
C、清炒菜心富含维生素,故选项不符合题意;
D、水果拼盘富含维生素,故选项不符合题意;
故选A。
11.错误
【详解】工业酒精的主要成分是甲醇,甲醇有毒,不能饮用,故不能用于配制饮用酒,此说法不正确。
12.错误
【详解】塑料、合成橡胶于合成有机高分子材料,而合金并不属于有机高分子材料,题目说法错误。
13.错误
【详解】纤维素不能被人体吸收,但是食物中的纤维素对人体有重要作用,故填:错误。
14.正确
【详解】淀粉经过消化,最终变化为能被小肠吸收的葡萄糖,正确。
15.错误
【详解】“白色污染”是指废塑料对环境的污染,塑料垃圾集中焚烧会产生大量废气,污染空气。
16.(1)BD
(2)大
(3)二氧化碳/CO2
(4)
(5) 黑色固体变红色 取少量A装置中的溶液,加入足量的BaCl2溶液,若有白色沉淀生成,则溶质中含有Na2CO3;静置,向上层清液中滴加无色酚酞溶液,若溶液变红色,则溶质中还含有NaOH。不变红则无NaOH 解:设A装置的溶液中碳酸钠的质量分数为x
x=10.6%
答:A装置的溶液中Na2CO3的质量分数为10.6%
【详解】(1)A、象牙不属于金属材料,不符合题意;
B、黄金是纯金属,属于金属材料,符合题意;
C、丝织品属于天然材料,不符合题意;
D、青铜是铜的合金,属于金属材料,符合题意。
故选BD;
(2)合金比组成它的纯金属硬度大, 耐腐性,青铜是铜的合金,其硬度比纯铜大;
(3)根据质量守恒定律,化学反应前后,元素的种类不变,生成物中含Cu、C、O、H,反应物中含Cu、O、H,故反应物中还应含碳元素,空气中含碳元素的物质是二氧化碳,故二氧化碳参与了反应;
(4)黄铜是铜锌合金,锌能与稀硫酸反应生成硫酸锌和氢气,产生气泡,铜与稀硫酸不反应,故可用稀硫酸区分黄铜和纯铜,该反应的化学方程式为:;
(5)①B装置中一氧化碳和氧化铜在加热的条件下反应生成铜和二氧化碳,故观察到的现象是:黑色固体逐渐变红;
②C装置中反应为二氧化碳和氢氧化钙反应生成碳酸钙和水,该反应的化学方程式为:;
③氢氧化钠能与二氧化碳反应生成碳酸钠和水,氯化钡能与碳酸钠反应生成碳酸钡和氯化钠,可加入过量的氯化钡检验碳酸钠,且将碳酸钠除尽(防止影响氢氧化钠的检验),氢氧化钠显碱性,能使无色酚酞试液变红,故可用无色酚酞试液检验是否含氢氧化钠,故实验方案为:取少量A装置中的溶液,加入足量的BaCl2溶液,若有白色沉淀生成,则溶质中含有Na2CO3;静置,向上层清液中滴加无色酚酞溶液,若溶液变红色,则溶质中还含有NaOH。不变红则无NaOH;
④见答案。
17.(1) 碳酸钙/CaCO3 蛋白质
(2) 将图中的长颈漏斗向下移动,造成和试管内的水柱差,如果水柱的高度不变,说明气密性良好 防止CO2溶于水 < 设5g真珍珠粉样品中碳酸钙的质量为x,则
解得x=0.5g
则真珍珠粉样品中CaCO3的质量分数为
答:真珍珠粉样品中CaCO3的质量分数为10%。
【详解】(1)实验一:二氧化碳能与石灰水中的氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为;
碳酸钙能与盐酸反应生成氯化钙、二氧化碳和水,则说明真假珍珠粉均含有碳酸钙。
实验二:蛋白质灼烧时有烧焦羽毛的气味,而假珍珠粉未闻到烧焦羽毛气味,则说明假珍珠粉中不含蛋白质。
(2)①图2装置气密性的检查方法是将图中的长颈漏斗向下移动,造成和试管内的水柱差,如果水柱的高度不变,说明气密性良好;
由于二氧化碳能溶于水,则量气管中水面上方加一层植物油的目的是防止CO2溶于水;
由表中数据可知,假珍珠粉产生的气体体积更多,则说明真珍珠粉中碳酸钙的含量小于假珍珠粉。
②见答案。
18.(1)B
(2) 锌 铁 骨质疏松
(3)N2
(4)AB
(5) B A
【详解】(1)在原子中,质子数=核外电子数,则 He—3 原子的原子核外电子数为2,故选B。
(2)表中铁、锌属于人体必需的微量元素;人体缺铁会导致贫血;缺钙会导致人患上骨质疏松。
(3)载人潜水器中的空气要与地表空气的组成基本一致,则其中含量最多的气体为氮气,符号为N2。
(4)A、钛合金与人体有很好的“相容性”,可用于人造关节,该选项符合题意;
B、钛合金强度大、可塑性好、易于加工,可作“奋斗者”号潜航器,该选项符合题意;
C、钛合金熔点高,不能作保险丝,该选项不符合题意。
故选AB。
(5)①图中,质子数>核外电子数,则该粒子为阳离子,故选B;
②在氮化镁中,镁元素化合价为+2价,氮元素化合价为-3价,则氮化镁的化学式为Mg3N2,镁在氮气中燃烧能生成氮化镁,符号表达式为;
③由于镁与氧气、氮气、二氧化碳中均能反应,则反应Ⅱ需在稀有气体中进行,故选A。
19. 黄瓜或① 过滤 吸附 乳化
【详解】(1)黄瓜中富含维生素,牛奶富含蛋白质,大米富含淀粉,淀粉属于糖类,故填:黄瓜或①。
(2)茶杯内装上纱网是将茶叶和水分离,故该操作原理是过滤,故填:过滤。
(3)活性炭具有吸附性,可以吸附色素和异味,故填:吸附。
(4)洗洁精具有乳化功能,可以清洗餐具上的油污,故填乳化。
20.(1) 含汞 有害 Hg
(2) +5 NaF
(3) A 固
【分析】化学式中元素的化合价之和是零;
【详解】(1)现在所使用的含汞温度计较多,汞属于有害元素,应减少生产,汞的元素符号是Hg;
(2)LiTaO3中Li是+1价,氧是-2价,设Ta的化合价为x,列式子:+1+x+(-2)×3=0,解得x=+5价。
化学方程式:5Na+K2TaF7=Ta+2KF+5R,反应物共含有5个钠原子,2个钾原子,1个钽原子,7个氟原子,生成物中含有2个钾原子,1个钽原子,2个氟原子,故5R中含有5个钠原子,5个氟原子,R中含有1个钠原子,1个氟原子,金属元素在左,非金属元素在右,故化学式为:NaF;
(3)①测温计主要用于测定温度的改变,故选A;
②热塑性塑料受热后可改变其形状,热固性塑料受热后不能改变形状,故填热固性;
【点睛】热塑性塑料是链状结构,热固性塑料是网状结构。
21.(1)
(2)H2O、H2O2
(3)碳和氧
(4)
【分析】A是一种理想的清洁燃料,说明A是氢气,X、Y的组成相同,在一定条件下均能分解产生B,说明B是氧气,X和Y分别是水和过氧化氢,C、D的组成相同,C与B反应时生成D,说明C是,D是CO2,代入原题验证,符合题意。
【详解】(1)根据分析A是氢气,氢气燃烧后只生成水,化学方程式为:;
(2)根据分析可知,X、Y分别是水和过氧化氢,化学式是:;
(3)根据分析可知,C、D分别是一氧化碳和二氧化碳,故都是由碳元素和氧元素组成;
(4)E中两种元素的质量比为3:1。A与D在催化剂作用下可生成E和B,根据质量守恒定律,反应前后元素种类不变,由甲烷中碳氢元素的质量比是,该反应是氢气和二氧化碳在催化剂的条件下反应生成甲烷和水,化学方程式为:;
E能在空气中燃烧,即甲烷和氧气点燃生成二氧化碳和水,化学方程式为:。
22.(1)ACD
(2)C、H
(3)
(4)延展性
(5) +1 增大矿物与酸的接触面积,加快酸浸的速率,使矿物充分反应 为了提高反应物的浓度,有利于Li2SO4转化为Li2CO3 碳酸锂在热水中溶解度小,避免了洗涤过程中碳酸锂的损耗 取少量洗涤后的溶液于试管中,滴入足量稀盐酸,充分反应后滴入氯化钡溶液,若无明显现象,则已洗涤干净
【详解】(1)A、霉变的花生含有黄曲霉素,有毒,不能食用,选项错误;
B、烹调食物时,放入一些加铁酱油,可以补铁元素,选项正确;
C、甲醛有毒,不能食用,选项错误;
D、亚硝酸钠有毒,不能食用,选项错误;
故选:ACD;
(2)石油主要含有碳元素和氢元素;
(3)高压下以二氧化碳和氨气为原料制得尿素[CO(NH2)2],同时有水生成,化学方程式为:;
(4)将钢板轧成“手撕钢”,利用了金属的延展性;
(5)①化合物中化合价代数和为0,由碳酸根离子显-2价,则锂元素显+1价;
②在投入酸浸槽前,锂辉石需进行粉碎研磨的预处理,可以使物质之间接触更充分,故填:增大矿物与酸的接触面积,加快酸浸的速率,使矿物充分反应;
③反应器加入的Na2CO3溶液是饱和溶液,其作用是为了提高反应物的浓度,有利于Li2SO4转化为Li2CO3
④洗涤槽中使用热水,根据题意,碳酸锂溶解度随温度的升高而减小因此碳酸锂在热水中溶解度小,避免了洗涤过程中碳酸锂的损耗;
根据碳酸盐能与酸反应生成二氧化碳,则:取少量洗涤后的溶液于试管中,滴入足量稀盐酸,充分反应后滴入氯化钡溶液,若无明显现象,则已洗涤干净
23. 氨基酸态氮的含量 特级 协调性、浓厚感 ABC
【详解】(1)从文中可知,衡量酱油营养价值的重要指标是氨基酸态氮的含量。
(2)根据表1数据可知,某酿造的酱油氨基酸态氮含量为0.90g/100mL,则该酱油的等级为特级。
(3)卤汁(氯化钾、氯化镁等的混合物)其中含有的阴离子有氯离子,一个氯离子带一个单位负电荷,其符号为。
(4)由图可知,98℃灭菌条件下的酱油的协调性、浓厚感强于90℃灭菌条件下的酱油。
(5)A、酱油酿造过程有新物质生成,发生了化学变化,说法正确;
B、衡量酱油营养价值的重要指标是氨基酸态氮含量,购买酱油时应关注标签上氨基酸态氮的含量,说法正确;
C、酱油的风味指的是酱油的香气、后味、协调感、浓厚感等,说法正确;
故选:ABC。
学校:___________姓名:___________班级:___________考号:___________
一、选择题
1.学习化学最重要的是对知识进行归纳和整理,下列选项中不完全正确的是( )
A B C D
①农药和化肥的大量使用——不会引起土壤污染 ②塑料制品的大量使用——会造成“白色污染” ③化石燃料的大量使用——会造成空气污染 ①NaCl——俗称食盐 ②Na2CO3——俗称纯碱 ③NaOH——俗称火碱 ①CaO——氧化物 ②Ca(OH)2——碱 ③CaCO3——盐 ①人体缺碘——甲状腺肿大 ②人体缺铁——贫血 ③人体缺钙——骨质疏松
A.A B.B C.C D.D
2.“绿水青山就是金山银山”,水是人类不可缺少的宝贵资源。人人都要树立节约用水的意识。下列标志与节约用水有关的是
A. B. C. D.
3.安徽省2035远景目标:围绕地域传统美食,做响安徽绿色农食品品牌,下列安徽传统美食富含糖类的是
A.八公山豆腐 B.巢湖银鱼
C.太和板面 D.芜湖露仙酱泡菜
4.小明同学在复习阶段在笔记本上对化学知识进行了归纳整理:
①加热固体有气体产生的变化一定是化学变化
②可燃冰是混合物,开采其导致的温室效应,比二氧化碳更严重
③人呼出气体中含量最多的气体是CO2
④石油是一种重要的化工产品,是不可再生能源
⑤图书、档案、精密仪器等失火可用CO2灭火器
⑥物质与氧气发生的反应都是氧化反应,则氧化反应一定要有氧气参加。
上述说法正确的个数是
A.1 B.2 C.3 D.4
5.维生素C(化学式为C6H8O6)是一种水溶性维生素,也是一种常见的食品添加剂,能够阻止空气中的氧气将食品氧化变质。下列有关维生素C的说法正确的是
A.由3个元素组成 B.可以预防夜盲症
C.含有6个一氧化碳分子 D.其中氧元素的质量分数最大
6.下列有关生活中的做法正确的是
A.用刷漆的方式防止自行车链条生锈
B.炒菜时如油锅不慎着火,立即用冰水扑灭
C.蚊虫叮咬后在叮咬处涂抹适量肥皂水可得到缓解
D.焚烧废弃塑料解决“白色污染”问题
7.下列说法正确的是
A.回收废弃塑料可减少“白色污染”
B.缺钙引起贫血
C.用氯化钠固体配制50克10%的氯化钠溶液的主要步骤:计算、量取、溶解
D.合金的熔点和硬度均高于组成它们的纯金属
8.下列说法中,不正确的是
A.玻璃钢是常用的复合材料之一
B.糖类和维生素是人体中重要的供能营养素
C.氮肥、磷肥、钾肥及复合肥是农业生产中主要的化学肥料
D.重金属盐可使蛋白质发生化学变化,失去生理活性
9.继“食盐加碘”后,我国又将启动“酱油加铁”工程。“酱油加铁”的意义是
①补充人体需要的铁元素 ②预防缺铁性贫血病 ③改善酱油的味道 ④增加黑色素 ⑤减少厨房污染物 ⑥提高人民的健康水平
A.①②③
B.④⑤⑥
C.③④⑤
D.①②⑥
10.学校食堂为保证师生营养需求,每天提供几十道菜品,下列提供的食品中富含蛋白质的是
A.滑蛋虾仁 B.蒸青菜包 C.清炒菜心 D.水果拼盘
二、判断题
11.用工业酒精配制饮用酒( )
12.塑料、合成橡胶、合金都属于合成有机高分子材料( )
13.纤维素不能被人体吸收,所以食物中的纤维素对人体毫无意义( )
14.食物淀粉在人体内经酶的催化作用,与水反应最终变为葡萄糖( )
15.为减少“白色污染”,可将塑料垃圾集中焚烧处理( )
三、综合应用题
16.2022年1月31日,"三星堆遗址"出土青铜大面具,亮相春晚舞台。同时出土的还有黄金面具、青铜艺术品、象牙、残存丝织品等重要文物。
(1)下列物质中属于金属材料的有______。
A.象牙 B.黄金 C.丝织品 D.青铜
(2)青铜是铜的合金,其硬度比纯铜 (填“大”或“小”)。
(3)铜制品长期暴露在空气中能与空气中的O2、H2O和 化合生成铜锈【主要成分是Cu2(OH)2CO3】。
(4)黄铜是铜锌合金,用稀硫酸区分黄铜和纯铜的化学方程式为 。
(5)铜制品在生活中有广泛的应用。下图装置可做一氧化碳还原氧化铜的实验,并检验生成的气体产物。
①B装置玻璃管里可观察到的现象是 。
②C装置中反应的化学方程式为 。
③实验结束后,若要确定A装置的溶液中溶质的成分,请设计合理的实验方案,简要写出实验步骤、现象和结论。(提示:Na2CO3溶液呈碱性)。 。
④为测定A装置的溶液中Na2CO3的质量分数,取A装置的溶液100g,并向其中加入过量的BaCl2溶液,生成沉淀的质量是19.7g。计算A装置的溶液中Na2CO3的质量分数 。
17.珍珠粉是由珍珠经加工制成的白色粉末,含有碳酸钙、蛋白质等成分,是重要的药品、化妆品原料。但市场上出现的假珍珠粉外观上与真珍珠粉差不多,肉眼往往无法辨别它们。
(1)为了寻找区分真假珍珠粉的方法,科学兴趣小组的同学进行了如图1实验:
实验一:分别取真假珍珠粉适量置于两支试管中,加一定量的稀盐酸并将产生的气体通入澄清石灰水中,发现澄清石灰水均变浑浊,写出石灰水变浑浊的化学方程式 。说明真假珍珠粉均含有 。
实验二:分别取真假珍珠粉少量置于铁片上灼烧,发现真珍珠粉能闻到烧焦羽毛气味;假珍珠粉未闻到烧焦羽毛气味,由此可得出结论:假珍珠粉中不含 。
(2)为了比较真假珍珠粉中碳酸钙的含量,共进行了三次实验,每次各取5g真假珍珠粉,分别置于如图2实验装置中(稀盐酸足量且真假珍珠粉中只有碳酸钙与稀盐酸会反应生成气体),测定生成气体体积数据如下表:
样品 气体体积ml 次数 第一次 第二次 第三次
假珍珠粉 117.50 117.28 117.05
真珍珠粉 111.52 111.66 111.86
①图2装置气密性的检查方法是 ,量气管中水面上方加一层植物油的目的是 ,由实验数据可知:真珍珠粉中碳酸钙的含量 假珍珠粉(填“>”、“<”、“=”)。
②根据三次测量结果,取平均值,算得5g真珍珠粉生成的气体质量为0.22g,则真珍珠粉样品中CaCO3的质量分数为 。(写出计算过程)
18.2020--2022 年,中国的科技成果“井喷”。长征 5 号、嫦娥 5 号、“奋斗者”号载人潜水器、“人造太阳”核聚变有了历史突破等令世界瞩目,让国人自豪。
(1)月球土壤中含有大量的 He—3 原子,是热核聚变重要原料。He—3 原子的原子核内有 2个质子和 1 个中子,则 He—3 原子的原子核外电子数为______(填字母)。
A.1 B.2 C.3
(2)潜航员、航天员的食品种类繁多、营养全面。某种水果每 100 克食用部分中的营养成分含量如下表。
蛋白质/g 脂肪/g 糖类/g 钙 铁 锌 维生素A/mg 维生素C/mg
0.8 0.2 10.5 20 0.4 0.14 27 33
表中属于人体必需的微量元素的是铁和 ,人体缺乏 元素会导致贫血,缺钙会导致人患上 (填写“侏儒症”或“骨质疏松”)。
(3)载人潜水器中的空气要与地表空气的组成基本一致,其中含量最多的是 (填化学式)。
(4)钛合金具有熔点高、强度大、可塑性好、易于加工,钛合金与人体有很好的“相容性”等优良性能,下列用途与钛合金性能相符的是______(填字母)。
A.人造关节 B.“奋斗者”号潜航器 C.保险丝
(5)下面是利用钛白粉(TiO2)生产海绵钛(Ti)的一种工艺流程:
①右上图为镁元素的某种微粒结构示意图,该图表示 (填字母)。
A.原子 B.阳离子 C.阴离子
②已知:镁除了能与氧气反应,还可与氮气,二氧化碳反应。镁在氮气中燃烧能生成氮化镁(氮元素化合价为-3 价),则此反应的化学符号表达式为 。
③反应Ⅱ需在下列哪种环境中进行 (填字母)。
A.稀有气体中 B.空气中 C.氮气中 D.CO2气体中
四、填空与简答
19.化学来源于生活服务于生活。请回答下列生活中的有关化学问题:
(1)厨房中有下列几种食物:①黄瓜;②牛奶;③大米。其中富含维生素的是 。
(2)泡茶时,可在茶杯内装上纱网,该设计利用的化学实验操作原理是 。
(3)某品牌口罩中加入了活性炭滤片,利用了活性炭的 性。
(4)厨房中用洗洁精能去除餐具上的油污,是因为洗洁精具有 功能。
20.防疫情,测体温。体温测量仪功不可没。
(1)传统型 体温计、含汞血压计将在2026年起全面禁止生产,因为汞是人体中的 (选填“必需”或“有害”)元素。汞的元素符号是 。
(2)方便型——额温枪。某种额温枪的红外温度传感器所用材料含有钽酸锂(LiTaO3),钽酸锂中锂元素(Li)的化合价为+1价,则钽元素(Ta)的化合价为 价。在惰性气氛中制取钽的原理为:5Na+K2TaF7=Ta+2KF+5R,则R的化学式为 。
(3)快捷型——红外热成像测温仪。该测温仪可实现远距离、多目标、非接触式测温,可用于快速筛查人群中的高温个体。
①该测温仪还可用于 (填字母)。
A.测量物质溶解时的温度变化
B.分析鸡龙河水质
C.检测室内甲醛含量是否超标
②该测温仪外壳的塑料一经加工成型,受热不再熔化,是热 性塑料。
21.下列用字母表示的是初中化学常见的7种物质,其中A~E均为无色气体,A和B为单质。请根据下列叙述回答问题。
(1)A是一种理想的清洁燃料,其原因可以用化学方程式表示为 。
(2)X、Y的组成相同,在一定条件下均能分解产生B。X、Y分别是 。
(3)C、D的组成相同,C与B反应时生成D,C、D均由 元素组成。
(4)E中两种元素的质量比为3:1。A与D在催化剂作用下可生成E和B,该反应的化学方程式为 。E能在空气中燃烧,反应的化学方程式为 。
22.随着社会进步,饮食、材料、环境等成为人们关注的热点话题。
【舌尖上的化学】
(1)2023年3月15日是第41个国际消费者权益日,“舌尖上的安全”成为民生热词。下列做法不正确的是______。
A.用霉变的花生制作鱼皮豆
B.烹调食物时,放入一些加铁酱油
C.为防止海鲜腐烂,可用甲醛溶液浸泡
D.加工火腿肠时加入过量的亚硝酸盐防腐
【环境中的化学】
我国承诺在2030年前实现“碳达峰”,2060年前实现“碳中和”。
(2)化石燃料燃烧是造成碳排放量增加的主要因素。化石燃料包括煤、石油和天然气,石油主要含有 元素。
(3)科学家在高温、高压下以二氧化碳和氨气为原料制得尿素[CO(NH2)2],同时有水生成,这是固定和利用二氧化碳的成功范例。请写出该反应的化学方程式: 。
【材料中的化学】
(4)“手撕钢”的厚度不足0.02mm,用于“折叠屏手机”屏。将钢板轧成“手撕钢”,利用了金属的 性。
(5)碳酸锂(Li2CO3)是制备手机锂电池的重要原料,工业上以锂辉石精矿(主要成分为Li2O,其余成分不溶于水,也不参与反应)为原料制取Li2CO3,其主要工艺流程如图所示:提示:Li2CO3溶解度随温度的升高而减小。
①Li2CO3中锂元素的化合价为 。
②在投入酸浸槽前,锂辉石需进行粉碎研磨的预处理,其目的是 。
③反应器加入的Na2CO3溶液是饱和溶液,其作用是 。
④洗涤槽中使用热水,原因是 。证明Li2CO3洗涤干净的方法是 。(写操作,现象和结论)
23.阅读下面科普短文。
酱油是中国传统发酵调味品。酱油的鲜味和营养价值取决于氨基酸态氮含量的高低。氨基酸态氮是指以氨基酸形式存在的氮元素,其含量是衡量酱油营养价值的一项重要指标。氨基酸态氮含量越高,酱油品质越好,等级越高,标准见表1。
表1酿造酱油等级标准
项目 指标
氨基酸态氮g/100mL 特级 一级 二级 三级
≥0.80 0.70~0.79 0.55~0.69 0.40~0.54
酿造酱油是以大豆或脱脂大豆,小麦或麸皮为原料,经微生物发酵而成。食盐也是酱油酿造的重要原料之一、选用的食盐以氯化钠含量高、卤汁(氯化钾、氯化镁、硫酸钙等的混合物)少的品质为宜。酱油在酿造过程中会产生一系列带有特殊风味的物质。风味是传统发酵食品重要的质量指标,经实验测定发现。杀菌工艺对酱油风味物质的形成有一定影响。研究人员做了如下实验:将2份等量的生酱油分别加热到不同灭菌温度(90°C、98°C)并保温20min,灭菌后快速降温到45°C,保持24小时后检测酱油鲜、咸、甜等9项风味,实验结果如图。
酱油营养丰富,但由于含盐量高,亦不可过量食用。依据文章内容,回答下列问题。
(1)衡量酱油营养价值的重要指标是 。
(2)某酿造的酱油氨基酸态氮含量为0.90g/100mL,则该酱油的等级为 。
(3)卤汁(氯化钾、氯化镁等的混合物)其中含有的阴离子有氯离子其符号为 。
(4)由图可知,98℃灭菌条件下的酱油的 强于90℃灭菌条件下的酱油。
(5)下列说法正确的是 (填序号)。
A.酱油酿造过程发生了化学变化
B.购买酱油时应关注标签上氨基酸态氮的含量
C.酱油的风味指的是酱油的香气、后味、协调感、浓厚感等
参考答案:
1.A
【详解】A、农药和化肥的大量使用会引起土壤污染;塑料制品不易降解,大量使用会造成“白色污染”;化石燃料的大量使用会造成空气污染,故A错误;
B、NaCl俗称食盐,Na2CO3俗称纯碱,NaOH俗称火碱,故B正确;
C、CaO,是由两种元素组成,其中一种是氧元素,所以属于氧化物;Ca(OH)2电离出的阴离子只有氢氧根离子,所以属于碱;CaCO3是由钙离子和碳酸根离子构成的化合物,所以属于盐,故C正确;
D、人体缺碘会患甲状腺肿大;人体缺铁会患贫血;人体缺钙会患骨质疏松,故D正确.
故选A.
【点睛】化学来源于生产和生活,也服务于人类的生产和生活,因此与人类生产和生活相关的化学知识就成了中考的热点之一.
2.D
【详解】A、图为禁止吸烟标志,故A错误;
B、图为腐蚀品标志,故B错误;
C、图为塑料回收循环利用标志,故C错误;
D、图为节约用水标志,故D正确。
故选D。
【点睛】
3.C
【详解】A、八公山豆腐中高含蛋白质,故A选项不符合题意;
B、巢湖银鱼中富含蛋白质,故B选项不符合题意;
C、太和板面中富含淀粉,淀粉属于糖类,故C选项符合题意;
D、芜湖露仙酱泡菜富含维生素,故D选项不符合题意。
故选C。
4.B
【详解】①加热固体有气体产生的变化不一定是化学变化,例如加热固体碘生成碘蒸气,该变化没有新物质生成,属于物理变化,故错误;
②可燃冰主要含有甲烷水合物(由甲烷分子和水分子组成),属于混合物;如果开采不当,甲烷气体将大量泄漏于空气中,其造成的温室效应将比二氧化碳更加严重,故正确;
③空气中含量最多的气体是氮气(约占空气体积的78%),氮气不参与呼吸作用,因此人呼出气体中含量最多的是N2,故错误;
④石油是一种重要的化工原料,在短期内不能得到补充,是不可再生能源,故错误;
⑤图书、档案、精密仪器等失火可用CO2灭火器,不会留下痕迹,减小损失,故正确;
⑥物质与氧气发生的反应都是氧化反应,但是氧化反应不一定要有氧气参加,如一氧化碳在加热条件下与氧化铜反应生成铜和二氧化碳,一氧化碳发生了氧化反应,故错误;
其中②⑤两个正确;
故选:B。
5.D
【详解】A、如题根据维生素C的化学式可知维生素C是由碳元素、氢元素和氧元素,三种元素组成的化合物,选项说法错误;
B、人体缺少维生素C会患坏血病,选项错误;
C、一个维生素C分子是由6个碳原子、8个氧原子和6个氧原子构成,不含其他物质的分子,选项错误;
D、维生素C中碳元素、氢元素和氧元素的质量比是,说明其中氧元素的质量分数最大,选项正确;
答案为:D。
6.C
【详解】A、生活中用涂油的方式防止自行车链条生锈,A错误。
B、炒菜时如油锅不慎着火,立即锅盖盖灭,B错误。
C、蚊虫叮咬处有酸性物质,肥皂水显碱性,蚊虫叮咬后在叮咬处涂抹适量肥皂水可得到缓解,C正确。
D、焚烧废弃塑料会产生大量烟尘,污染空气,D错误。
故选:C。
7.A
【详解】A、“白色污染”是由废弃塑料难处理、难降解导致的,回收废弃的塑料,能有效降低废弃塑料的污染,减少“白色污染”,该选项正确;
B、钙主要存在于骨骼和牙齿中,使骨和牙齿具有坚硬的结构支架,缺乏钙元素主要会导致幼儿和青少年患佝偻病、软骨症等,贫血往往是因为缺少铁元素导致的,该选项错误;
C、用氯化钠固体配制50克10%的氯化钠溶液的主要步骤:计算、称量、量取、溶解、装瓶贴标签,该选项错误;
D、根据合金的特性可知,合金的硬度高于组成它们的纯金属,熔点低于组成它们的纯金属,该选项错误。
故选A。
8.B
【详解】A、玻璃钢是玻璃与塑料叠合在一起形成的具有金属性能的新型材料,属于复合材料,选项正确;
B、糖类能为人体提供能量,属于供能营养素,而维生素能够参与人体的代谢活动,不能为人体提供能量,不是人体中的供能营养素,选项错误;
C、氮肥、磷肥、钾肥及复合肥能够为农作物提供营养元素,是农业生产中主要的化学肥料,选项正确;
D、重金属盐可使蛋白质发生化学变化,失去生理活性,选项正确,故选B。
9.D
【详解】“酱油加铁”工程能①补充人体需要的铁元素;②预防缺铁性贫血病;⑥提高人民的健康水平,故①②⑥组合正确。故选D。
10.A
【详解】A、滑蛋虾仁富含蛋白质,故选项符合题意;
B、蒸青菜包中富含糖类和维生素,故选项不符合题意;
C、清炒菜心富含维生素,故选项不符合题意;
D、水果拼盘富含维生素,故选项不符合题意;
故选A。
11.错误
【详解】工业酒精的主要成分是甲醇,甲醇有毒,不能饮用,故不能用于配制饮用酒,此说法不正确。
12.错误
【详解】塑料、合成橡胶于合成有机高分子材料,而合金并不属于有机高分子材料,题目说法错误。
13.错误
【详解】纤维素不能被人体吸收,但是食物中的纤维素对人体有重要作用,故填:错误。
14.正确
【详解】淀粉经过消化,最终变化为能被小肠吸收的葡萄糖,正确。
15.错误
【详解】“白色污染”是指废塑料对环境的污染,塑料垃圾集中焚烧会产生大量废气,污染空气。
16.(1)BD
(2)大
(3)二氧化碳/CO2
(4)
(5) 黑色固体变红色 取少量A装置中的溶液,加入足量的BaCl2溶液,若有白色沉淀生成,则溶质中含有Na2CO3;静置,向上层清液中滴加无色酚酞溶液,若溶液变红色,则溶质中还含有NaOH。不变红则无NaOH 解:设A装置的溶液中碳酸钠的质量分数为x
x=10.6%
答:A装置的溶液中Na2CO3的质量分数为10.6%
【详解】(1)A、象牙不属于金属材料,不符合题意;
B、黄金是纯金属,属于金属材料,符合题意;
C、丝织品属于天然材料,不符合题意;
D、青铜是铜的合金,属于金属材料,符合题意。
故选BD;
(2)合金比组成它的纯金属硬度大, 耐腐性,青铜是铜的合金,其硬度比纯铜大;
(3)根据质量守恒定律,化学反应前后,元素的种类不变,生成物中含Cu、C、O、H,反应物中含Cu、O、H,故反应物中还应含碳元素,空气中含碳元素的物质是二氧化碳,故二氧化碳参与了反应;
(4)黄铜是铜锌合金,锌能与稀硫酸反应生成硫酸锌和氢气,产生气泡,铜与稀硫酸不反应,故可用稀硫酸区分黄铜和纯铜,该反应的化学方程式为:;
(5)①B装置中一氧化碳和氧化铜在加热的条件下反应生成铜和二氧化碳,故观察到的现象是:黑色固体逐渐变红;
②C装置中反应为二氧化碳和氢氧化钙反应生成碳酸钙和水,该反应的化学方程式为:;
③氢氧化钠能与二氧化碳反应生成碳酸钠和水,氯化钡能与碳酸钠反应生成碳酸钡和氯化钠,可加入过量的氯化钡检验碳酸钠,且将碳酸钠除尽(防止影响氢氧化钠的检验),氢氧化钠显碱性,能使无色酚酞试液变红,故可用无色酚酞试液检验是否含氢氧化钠,故实验方案为:取少量A装置中的溶液,加入足量的BaCl2溶液,若有白色沉淀生成,则溶质中含有Na2CO3;静置,向上层清液中滴加无色酚酞溶液,若溶液变红色,则溶质中还含有NaOH。不变红则无NaOH;
④见答案。
17.(1) 碳酸钙/CaCO3 蛋白质
(2) 将图中的长颈漏斗向下移动,造成和试管内的水柱差,如果水柱的高度不变,说明气密性良好 防止CO2溶于水 < 设5g真珍珠粉样品中碳酸钙的质量为x,则
解得x=0.5g
则真珍珠粉样品中CaCO3的质量分数为
答:真珍珠粉样品中CaCO3的质量分数为10%。
【详解】(1)实验一:二氧化碳能与石灰水中的氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为;
碳酸钙能与盐酸反应生成氯化钙、二氧化碳和水,则说明真假珍珠粉均含有碳酸钙。
实验二:蛋白质灼烧时有烧焦羽毛的气味,而假珍珠粉未闻到烧焦羽毛气味,则说明假珍珠粉中不含蛋白质。
(2)①图2装置气密性的检查方法是将图中的长颈漏斗向下移动,造成和试管内的水柱差,如果水柱的高度不变,说明气密性良好;
由于二氧化碳能溶于水,则量气管中水面上方加一层植物油的目的是防止CO2溶于水;
由表中数据可知,假珍珠粉产生的气体体积更多,则说明真珍珠粉中碳酸钙的含量小于假珍珠粉。
②见答案。
18.(1)B
(2) 锌 铁 骨质疏松
(3)N2
(4)AB
(5) B A
【详解】(1)在原子中,质子数=核外电子数,则 He—3 原子的原子核外电子数为2,故选B。
(2)表中铁、锌属于人体必需的微量元素;人体缺铁会导致贫血;缺钙会导致人患上骨质疏松。
(3)载人潜水器中的空气要与地表空气的组成基本一致,则其中含量最多的气体为氮气,符号为N2。
(4)A、钛合金与人体有很好的“相容性”,可用于人造关节,该选项符合题意;
B、钛合金强度大、可塑性好、易于加工,可作“奋斗者”号潜航器,该选项符合题意;
C、钛合金熔点高,不能作保险丝,该选项不符合题意。
故选AB。
(5)①图中,质子数>核外电子数,则该粒子为阳离子,故选B;
②在氮化镁中,镁元素化合价为+2价,氮元素化合价为-3价,则氮化镁的化学式为Mg3N2,镁在氮气中燃烧能生成氮化镁,符号表达式为;
③由于镁与氧气、氮气、二氧化碳中均能反应,则反应Ⅱ需在稀有气体中进行,故选A。
19. 黄瓜或① 过滤 吸附 乳化
【详解】(1)黄瓜中富含维生素,牛奶富含蛋白质,大米富含淀粉,淀粉属于糖类,故填:黄瓜或①。
(2)茶杯内装上纱网是将茶叶和水分离,故该操作原理是过滤,故填:过滤。
(3)活性炭具有吸附性,可以吸附色素和异味,故填:吸附。
(4)洗洁精具有乳化功能,可以清洗餐具上的油污,故填乳化。
20.(1) 含汞 有害 Hg
(2) +5 NaF
(3) A 固
【分析】化学式中元素的化合价之和是零;
【详解】(1)现在所使用的含汞温度计较多,汞属于有害元素,应减少生产,汞的元素符号是Hg;
(2)LiTaO3中Li是+1价,氧是-2价,设Ta的化合价为x,列式子:+1+x+(-2)×3=0,解得x=+5价。
化学方程式:5Na+K2TaF7=Ta+2KF+5R,反应物共含有5个钠原子,2个钾原子,1个钽原子,7个氟原子,生成物中含有2个钾原子,1个钽原子,2个氟原子,故5R中含有5个钠原子,5个氟原子,R中含有1个钠原子,1个氟原子,金属元素在左,非金属元素在右,故化学式为:NaF;
(3)①测温计主要用于测定温度的改变,故选A;
②热塑性塑料受热后可改变其形状,热固性塑料受热后不能改变形状,故填热固性;
【点睛】热塑性塑料是链状结构,热固性塑料是网状结构。
21.(1)
(2)H2O、H2O2
(3)碳和氧
(4)
【分析】A是一种理想的清洁燃料,说明A是氢气,X、Y的组成相同,在一定条件下均能分解产生B,说明B是氧气,X和Y分别是水和过氧化氢,C、D的组成相同,C与B反应时生成D,说明C是,D是CO2,代入原题验证,符合题意。
【详解】(1)根据分析A是氢气,氢气燃烧后只生成水,化学方程式为:;
(2)根据分析可知,X、Y分别是水和过氧化氢,化学式是:;
(3)根据分析可知,C、D分别是一氧化碳和二氧化碳,故都是由碳元素和氧元素组成;
(4)E中两种元素的质量比为3:1。A与D在催化剂作用下可生成E和B,根据质量守恒定律,反应前后元素种类不变,由甲烷中碳氢元素的质量比是,该反应是氢气和二氧化碳在催化剂的条件下反应生成甲烷和水,化学方程式为:;
E能在空气中燃烧,即甲烷和氧气点燃生成二氧化碳和水,化学方程式为:。
22.(1)ACD
(2)C、H
(3)
(4)延展性
(5) +1 增大矿物与酸的接触面积,加快酸浸的速率,使矿物充分反应 为了提高反应物的浓度,有利于Li2SO4转化为Li2CO3 碳酸锂在热水中溶解度小,避免了洗涤过程中碳酸锂的损耗 取少量洗涤后的溶液于试管中,滴入足量稀盐酸,充分反应后滴入氯化钡溶液,若无明显现象,则已洗涤干净
【详解】(1)A、霉变的花生含有黄曲霉素,有毒,不能食用,选项错误;
B、烹调食物时,放入一些加铁酱油,可以补铁元素,选项正确;
C、甲醛有毒,不能食用,选项错误;
D、亚硝酸钠有毒,不能食用,选项错误;
故选:ACD;
(2)石油主要含有碳元素和氢元素;
(3)高压下以二氧化碳和氨气为原料制得尿素[CO(NH2)2],同时有水生成,化学方程式为:;
(4)将钢板轧成“手撕钢”,利用了金属的延展性;
(5)①化合物中化合价代数和为0,由碳酸根离子显-2价,则锂元素显+1价;
②在投入酸浸槽前,锂辉石需进行粉碎研磨的预处理,可以使物质之间接触更充分,故填:增大矿物与酸的接触面积,加快酸浸的速率,使矿物充分反应;
③反应器加入的Na2CO3溶液是饱和溶液,其作用是为了提高反应物的浓度,有利于Li2SO4转化为Li2CO3
④洗涤槽中使用热水,根据题意,碳酸锂溶解度随温度的升高而减小因此碳酸锂在热水中溶解度小,避免了洗涤过程中碳酸锂的损耗;
根据碳酸盐能与酸反应生成二氧化碳,则:取少量洗涤后的溶液于试管中,滴入足量稀盐酸,充分反应后滴入氯化钡溶液,若无明显现象,则已洗涤干净
23. 氨基酸态氮的含量 特级 协调性、浓厚感 ABC
【详解】(1)从文中可知,衡量酱油营养价值的重要指标是氨基酸态氮的含量。
(2)根据表1数据可知,某酿造的酱油氨基酸态氮含量为0.90g/100mL,则该酱油的等级为特级。
(3)卤汁(氯化钾、氯化镁等的混合物)其中含有的阴离子有氯离子,一个氯离子带一个单位负电荷,其符号为。
(4)由图可知,98℃灭菌条件下的酱油的协调性、浓厚感强于90℃灭菌条件下的酱油。
(5)A、酱油酿造过程有新物质生成,发生了化学变化,说法正确;
B、衡量酱油营养价值的重要指标是氨基酸态氮含量,购买酱油时应关注标签上氨基酸态氮的含量,说法正确;
C、酱油的风味指的是酱油的香气、后味、协调感、浓厚感等,说法正确;
故选:ABC。
同课章节目录
