9.3 溶液的浓度 达标检测(含答案) -2023-2024学年九年级化学人教版下册
文档属性
| 名称 | 9.3 溶液的浓度 达标检测(含答案) -2023-2024学年九年级化学人教版下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 282.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-02-29 00:00:00 | ||
图片预览



文档简介
9.3 溶液的浓度 达标检测-2023-2024学年九年级化学人教版下册
一、单选题
1.溶液与人们的生活息息相关。下列有关溶液说法正确的是( )
A.溶液一定是无色透明的液体
B.将面粉与水充分混合,得到的是溶液
C.将5%的某溶液倒出一半,剩余溶液中溶质的质量分数为10%
D.某饱和溶液降温到t℃析出晶体后,得到的溶液仍是t℃时该物质的饱和溶液
2.同学们在一定温度下进行KNO3的溶解实验,实验数据如下。根据数据分析,下列叙述正确的是( )
实验序号 实验1 实验2 实验3 实验4
水的质量(g) 100 100 100 100
加入KNO3的质量(g) 80 100 120 140
溶液质量(g) 180 200 210 210
A.实验1所得溶液的溶质质量分数=
B.实验2所得溶液为饱和溶液
C.实验4所得溶液的溶质质量分数比实验3大
D.该温度下,KNO3饱和溶液的溶质质量分数=
3.欲用溶质质量分数为5%的次氯酸钠溶液配制1000g溶质质量分数为0.5%的溶液,需加水( )
A.900g B.500g C.200g D.100g
4.如图为KCl和Na2CO3的溶解度曲线,下列说法正确的是( )
A.T2℃时,Na2CO3饱和溶液质量分数为49.0%
B.将Na2CO3的饱和溶液由T3℃降温至T1℃的过程中,一直有固体不断析出
C.T4℃时,分别将等质量的KCl和Na2CO3溶于水配成饱和溶液,所得溶液的质量前者等于后者
D.KCl溶液中含有少量Na2CO3,可采取控制温度T3℃以上降温结晶、过滤的方法
5.生理盐水是0.9%的氯化钠溶液,关于生理盐水的说法正确的是( )
A.每100g水中溶解了0.9g 氯化钠
B.溶质与溶液的质量比为0.9:100
C.氯化钠的溶解度为0.9g/100g水
D.加入0.1g氯化钠完全溶解后得到1%的氯化钠溶液
6.已知20℃时,氯化钠的溶解度为36g,20℃时,各盛50g水的A、B烧杯中分别加入氯化钠20g、40g,充分搅拌后,两烧杯溶液中溶质的质量分数的关系是( )。
A.mA>mB B.mA=mB C.mA7.农业上常用溶质质量分数为16%的氯化钠溶液进行选种,实验室用氯化钠固体配制100g溶质质量分数为16%的氯化钠溶液。下列说法正确的是( )
A.所配溶液溶质和溶剂质量之比为16:100
B.称量氯化钠时砝码生锈了,所配溶液的溶质质量分数偏大
C.装瓶时的标签为“NaCl溶液100g”
D.用量筒量取水时仰视读数,所配溶液的溶质质量分数偏大
8.如图所示的四个图像,分别对应四种过程,其中正确的是( )
A.HCl和Na2SO4混合液中加入Ba(OH)2溶液
B.在等质量的镁、铁里分别加入足量的稀硫酸
C.恒温下,往一定量的KNO3不饱和溶液中加入KNO3固体
D.浓硫酸长久露置在空气中
9.如图为某物质在溶剂1、溶剂2中的溶解度曲线,下列说法正确的是( )
A.t2℃时,P点对应该物质在两种溶剂中形成的溶液均为不饱和溶液
B.将t2℃的该物质与溶剂1形成的溶液降温至t1℃,析出4g该物质
C.t2℃时,该物质与溶剂1形成的饱和溶液中溶质的质量分数为26%
D.t3℃时,该物质与溶剂2形成的饱和溶液中溶质与溶剂的质量比为6:25
10.甲、乙两种固体的溶解度曲线如图所示,下列说法正确的是( )
A.甲物质的溶解度大于乙物质的溶解度
B.t1℃时,100g 甲、乙两种物质的溶液中所含溶质的质量相等
C.将 a 点的乙溶液转化为饱和溶液,溶质质量分数一定改变
D.t2℃时,在 50g 水中加入 20g 甲物质所得溶液的质量为 65g
11.碳酸镁和氢氧化镁的混合物10g,经测定混合物中镁元素的质量分数为36%,向其中加入100g溶质质量分数为14.7%的稀硫酸,恰好完全反应得到不饱和溶液,将溶液蒸干后得到的固体质量为( )
A.12g B.18g C.24g D.36g
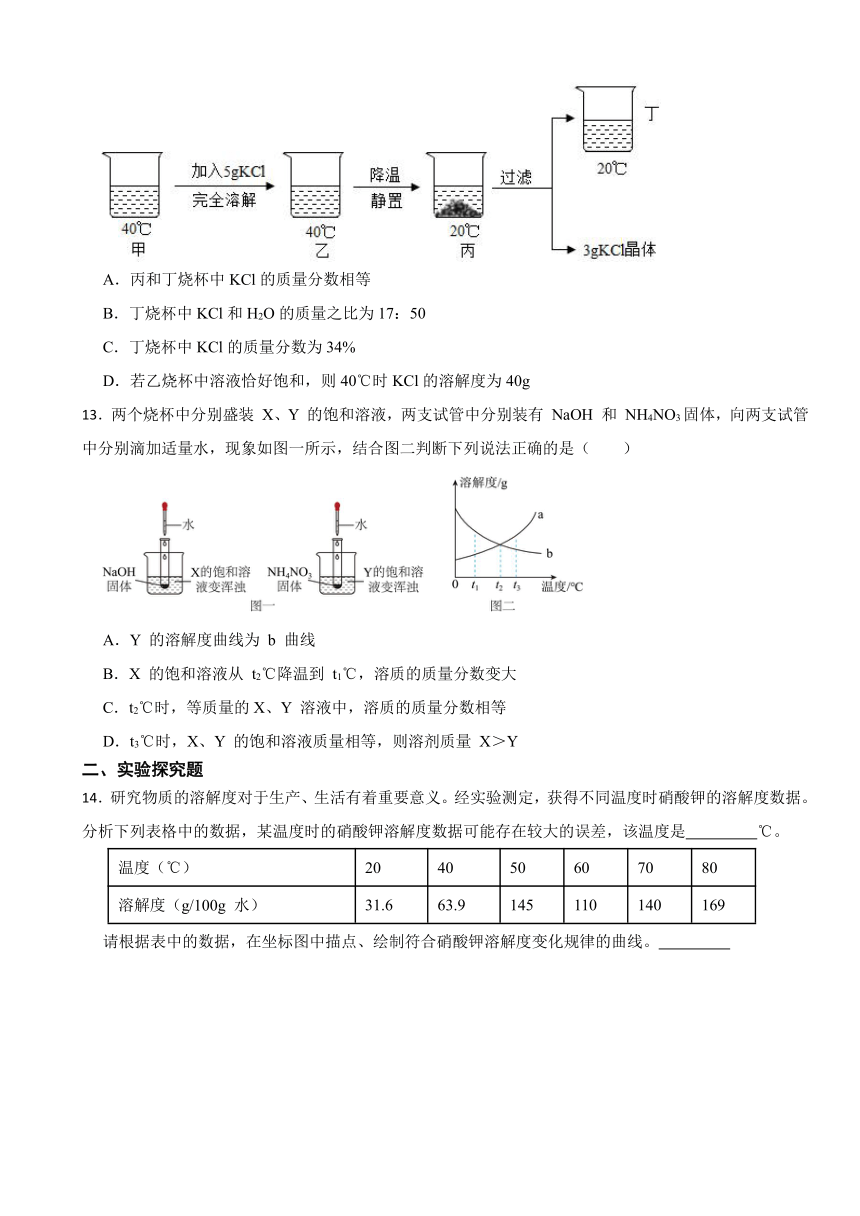
12.20℃时KCl的溶解度是34g。取65gKCl溶液放入甲烧杯中,按如图所示进行操作(整个过程中无溶剂损失)。以下说法错误的是( )
A.丙和丁烧杯中KCl的质量分数相等
B.丁烧杯中KCl和H2O的质量之比为17:50
C.丁烧杯中KCl的质量分数为34%
D.若乙烧杯中溶液恰好饱和,则40℃时KCl的溶解度为40g
13.两个烧杯中分别盛装 X、Y 的饱和溶液,两支试管中分别装有 NaOH 和 NH4NO3固体,向两支试管中分别滴加适量水,现象如图一所示,结合图二判断下列说法正确的是( )
A.Y 的溶解度曲线为 b 曲线
B.X 的饱和溶液从 t2℃降温到 t1℃,溶质的质量分数变大
C.t2℃时,等质量的X、Y 溶液中,溶质的质量分数相等
D.t3℃时,X、Y 的饱和溶液质量相等,则溶剂质量 X>Y
二、实验探究题
14.研究物质的溶解度对于生产、生活有着重要意义。经实验测定,获得不同温度时硝酸钾的溶解度数据。分析下列表格中的数据,某温度时的硝酸钾溶解度数据可能存在较大的误差,该温度是 ℃。
温度(℃) 20 40 50 60 70 80
溶解度(g/100g 水) 31.6 63.9 145 110 140 169
请根据表中的数据,在坐标图中描点、绘制符合硝酸钾溶解度变化规律的曲线。
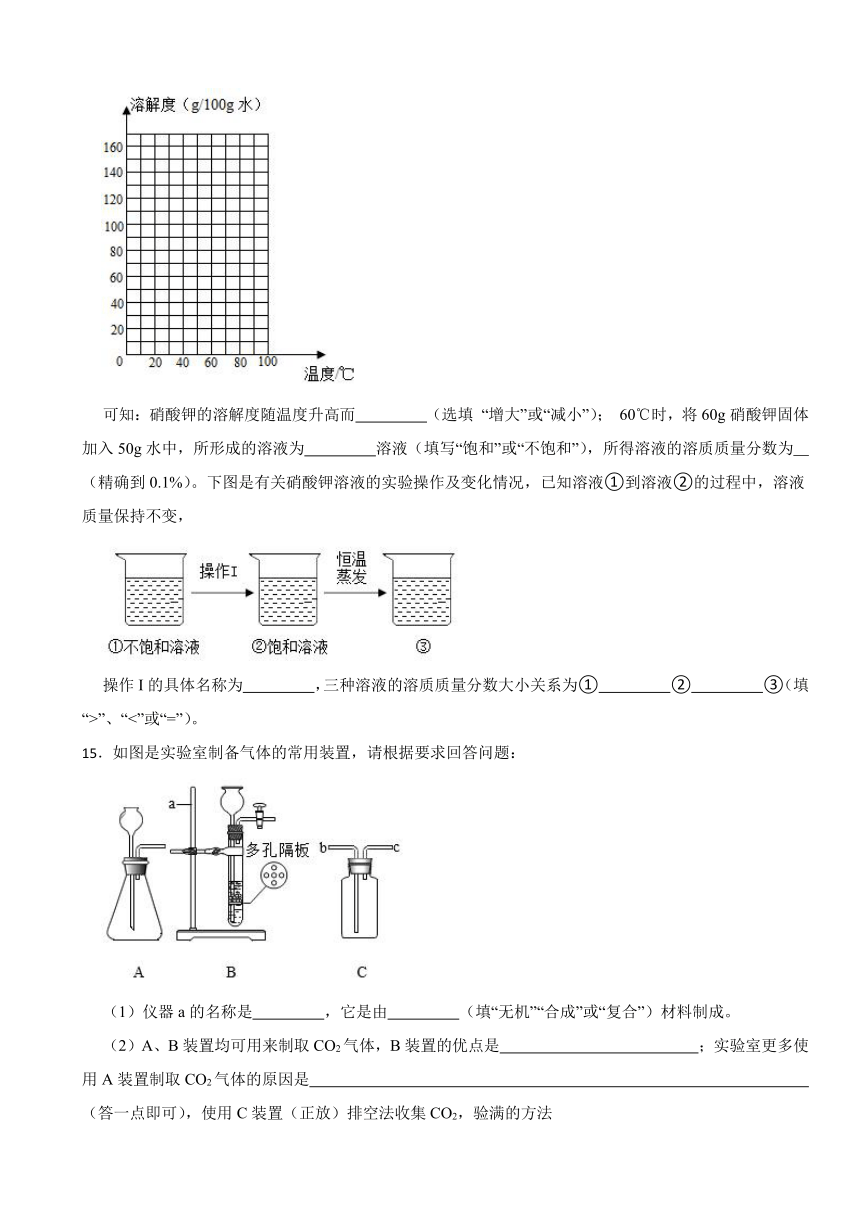
可知:硝酸钾的溶解度随温度升高而 (选填 “增大”或“减小”); 60℃时,将60g硝酸钾固体加入50g水中,所形成的溶液为 溶液(填写“饱和”或“不饱和”),所得溶液的溶质质量分数为 (精确到0.1%)。下图是有关硝酸钾溶液的实验操作及变化情况,已知溶液①到溶液②的过程中,溶液质量保持不变,
操作I的具体名称为 ,三种溶液的溶质质量分数大小关系为① ② ③(填“>”、“<”或“=”)。
15.如图是实验室制备气体的常用装置,请根据要求回答问题:
(1)仪器a的名称是 ,它是由 (填“无机”“合成”或“复合”)材料制成。
(2)A、B装置均可用来制取CO2气体,B装置的优点是 ;实验室更多使用A装置制取CO2气体的原因是 (答一点即可),使用C装置(正放)排空法收集CO2,验满的方法是 。
(3)制备CO2常用1:3的稀盐酸(用体积比为1:3的浓盐酸与水混合配制),已知浓盐酸的溶质质量分数为37%,密度为1.19g·mL-1,1:3的稀盐酸溶质质量分数为 (计算结果保留一位小数)。
三、填空题
16.甲、乙两种固体物质的溶解度曲线如图所示(已知两种物质溶解时互不影响),请回答下列问题。
(1)甲、乙溶解度曲线交点的意义 。
(2)40℃时分别溶解甲、乙两种固体,所得溶液中质量分数的最大值是 (精确到0.1%)。
(3)图中的饱和溶液有 (填序号),③到④实验过程中析出晶体质量为 g。
(4)40℃时,将等质量的甲、乙两种物质的饱和溶液分别蒸发等质量的水后,恢复到40℃,所得溶液质量的大小关系是甲 乙(填“大于”、“等于”或“小于”)。
17.A,B,C三种物质的溶解度随温度的变化情况如图:
(1)温度为 ℃时,A、C物质的溶解度相等。
(2)t1℃时A,B,C三种物质的溶解度由大到小的顺序是 。
(3)t1℃时,将50g的A物质溶于100g水中,所得溶液的质量为 g,溶质的质量分数为 。(保留到小数点后一位)
(4)t2℃时,将等质量的A,B,C三种物质的饱和溶液同时降温至t1℃时,析出晶体最多的是 。
四、计算题
18.洁厕灵的有效成分为HCl,某化学实验小组同学欲测定某品牌洁厕灵中的HCl的质量分数。同学们将100.0g洁厕灵倒入锥形瓶中,逐次加入一定量质量分数的碳酸钠溶液,至不在产生气体为止,共消耗80g碳酸钠溶液,并测得反应后溶液的质量为175.6g.请计算。
(1)生成二氧化碳的质量为 g。
(2)恰好完全反应时,所得溶液的溶质质量分数是多少?(写出计算过程,计算结果精确到0.1%)
19.某化学活动小组需要用溶质质量分数为19.6%的稀硫酸测量黄铜中铜的质量分数,但实验室现有的是溶质质量分数为98%的浓硫酸。试计算:
(1)将10g浓硫酸配制成所需的稀硫酸,需要水的质量为 g。
(2)上述配制好的稀硫酸20g与8g黄铜恰好完全反应,黄铜中铜的质量分数为多少?
五、综合题
20.如图是甲、乙、丙三种固体物质的溶解度曲线,回答问题:
(1)t1℃时,甲、乙、丙三种物质溶解度由大到小的顺序是: 。
(2)t2℃时,将45g甲加入到50g水中,充分溶解,所得溶液的质量为 g;
(3)要使t1℃时,接近饱和的乙溶液变成该温度下的饱和溶液,可采取的方法是 (写一种即可)。
21.如图1为甲、乙两种固体物质的溶解度曲线。
(1)某同学按图2所示进行实验,得到相应温度下的A、B、C溶液,在A、B、C三种溶液中属于饱和溶液的是 (填字母)。向溶液C中再加入25g甲,充分搅拌,恢复到t2℃时,所得溶液中溶质的质量为 g。
(2)将t2℃时等质量的甲、乙两种物质的饱和溶液降温至t1℃,下列说法正确的是__________。
A.降温后,甲溶液的质量大于乙溶液的质量
B.降温前,甲溶液中溶剂的质量比乙溶液中溶剂的质量小
C.降温后,甲溶液的质量分数大于乙溶液的质量分数
D.降温前后乙溶液的质量分数保持不变
答案解析部分
1.【答案】D
2.【答案】D
3.【答案】A
4.【答案】D
5.【答案】B
6.【答案】B
7.【答案】B
8.【答案】B
9.【答案】D
10.【答案】D
11.【答案】B
12.【答案】C
13.【答案】D
14.【答案】50;;增大;饱和;52.4%;降温;=;=
15.【答案】(1)铁架台;无机
(2)控制反应的开始和停止;A装置的反应容器为锥形瓶,能装的药品较多,则可制取大量的二氧化碳气体;将燃着的木条放在c口处,若木条熄灭,则瓶中二氧化碳收集满
(3)10.5%
16.【答案】(1)20℃时,甲、乙溶解度相同
(2)28.6%
(3)①②④;10
(4)大于
17.【答案】(1)t2
(2)C>B>A
(3)140;28.6%
(4)A
18.【答案】(1)4.4
(2)解:设生成NaCl的质量为x
x=11.7g
×100%≈6.7℅
答:恰好完全反应时,所得溶液的溶质质量分数为6.7%。
19.【答案】(1)40
(2)解:20g稀硫酸中溶质的质量=,设:8g黄铜中锌的质量为x。
8g黄铜中铜的质量分数=;
答:黄铜中铜的质量分数为67.5%。
20.【答案】(1)甲>乙>丙
(2)70g
(3)加入乙物质或降低温度、蒸发溶剂(写一种即可)
21.【答案】(1)B;40
(2)B;C;D
一、单选题
1.溶液与人们的生活息息相关。下列有关溶液说法正确的是( )
A.溶液一定是无色透明的液体
B.将面粉与水充分混合,得到的是溶液
C.将5%的某溶液倒出一半,剩余溶液中溶质的质量分数为10%
D.某饱和溶液降温到t℃析出晶体后,得到的溶液仍是t℃时该物质的饱和溶液
2.同学们在一定温度下进行KNO3的溶解实验,实验数据如下。根据数据分析,下列叙述正确的是( )
实验序号 实验1 实验2 实验3 实验4
水的质量(g) 100 100 100 100
加入KNO3的质量(g) 80 100 120 140
溶液质量(g) 180 200 210 210
A.实验1所得溶液的溶质质量分数=
B.实验2所得溶液为饱和溶液
C.实验4所得溶液的溶质质量分数比实验3大
D.该温度下,KNO3饱和溶液的溶质质量分数=
3.欲用溶质质量分数为5%的次氯酸钠溶液配制1000g溶质质量分数为0.5%的溶液,需加水( )
A.900g B.500g C.200g D.100g
4.如图为KCl和Na2CO3的溶解度曲线,下列说法正确的是( )
A.T2℃时,Na2CO3饱和溶液质量分数为49.0%
B.将Na2CO3的饱和溶液由T3℃降温至T1℃的过程中,一直有固体不断析出
C.T4℃时,分别将等质量的KCl和Na2CO3溶于水配成饱和溶液,所得溶液的质量前者等于后者
D.KCl溶液中含有少量Na2CO3,可采取控制温度T3℃以上降温结晶、过滤的方法
5.生理盐水是0.9%的氯化钠溶液,关于生理盐水的说法正确的是( )
A.每100g水中溶解了0.9g 氯化钠
B.溶质与溶液的质量比为0.9:100
C.氯化钠的溶解度为0.9g/100g水
D.加入0.1g氯化钠完全溶解后得到1%的氯化钠溶液
6.已知20℃时,氯化钠的溶解度为36g,20℃时,各盛50g水的A、B烧杯中分别加入氯化钠20g、40g,充分搅拌后,两烧杯溶液中溶质的质量分数的关系是( )。
A.mA>mB B.mA=mB C.mA
A.所配溶液溶质和溶剂质量之比为16:100
B.称量氯化钠时砝码生锈了,所配溶液的溶质质量分数偏大
C.装瓶时的标签为“NaCl溶液100g”
D.用量筒量取水时仰视读数,所配溶液的溶质质量分数偏大
8.如图所示的四个图像,分别对应四种过程,其中正确的是( )
A.HCl和Na2SO4混合液中加入Ba(OH)2溶液
B.在等质量的镁、铁里分别加入足量的稀硫酸
C.恒温下,往一定量的KNO3不饱和溶液中加入KNO3固体
D.浓硫酸长久露置在空气中
9.如图为某物质在溶剂1、溶剂2中的溶解度曲线,下列说法正确的是( )
A.t2℃时,P点对应该物质在两种溶剂中形成的溶液均为不饱和溶液
B.将t2℃的该物质与溶剂1形成的溶液降温至t1℃,析出4g该物质
C.t2℃时,该物质与溶剂1形成的饱和溶液中溶质的质量分数为26%
D.t3℃时,该物质与溶剂2形成的饱和溶液中溶质与溶剂的质量比为6:25
10.甲、乙两种固体的溶解度曲线如图所示,下列说法正确的是( )
A.甲物质的溶解度大于乙物质的溶解度
B.t1℃时,100g 甲、乙两种物质的溶液中所含溶质的质量相等
C.将 a 点的乙溶液转化为饱和溶液,溶质质量分数一定改变
D.t2℃时,在 50g 水中加入 20g 甲物质所得溶液的质量为 65g
11.碳酸镁和氢氧化镁的混合物10g,经测定混合物中镁元素的质量分数为36%,向其中加入100g溶质质量分数为14.7%的稀硫酸,恰好完全反应得到不饱和溶液,将溶液蒸干后得到的固体质量为( )
A.12g B.18g C.24g D.36g
12.20℃时KCl的溶解度是34g。取65gKCl溶液放入甲烧杯中,按如图所示进行操作(整个过程中无溶剂损失)。以下说法错误的是( )
A.丙和丁烧杯中KCl的质量分数相等
B.丁烧杯中KCl和H2O的质量之比为17:50
C.丁烧杯中KCl的质量分数为34%
D.若乙烧杯中溶液恰好饱和,则40℃时KCl的溶解度为40g
13.两个烧杯中分别盛装 X、Y 的饱和溶液,两支试管中分别装有 NaOH 和 NH4NO3固体,向两支试管中分别滴加适量水,现象如图一所示,结合图二判断下列说法正确的是( )
A.Y 的溶解度曲线为 b 曲线
B.X 的饱和溶液从 t2℃降温到 t1℃,溶质的质量分数变大
C.t2℃时,等质量的X、Y 溶液中,溶质的质量分数相等
D.t3℃时,X、Y 的饱和溶液质量相等,则溶剂质量 X>Y
二、实验探究题
14.研究物质的溶解度对于生产、生活有着重要意义。经实验测定,获得不同温度时硝酸钾的溶解度数据。分析下列表格中的数据,某温度时的硝酸钾溶解度数据可能存在较大的误差,该温度是 ℃。
温度(℃) 20 40 50 60 70 80
溶解度(g/100g 水) 31.6 63.9 145 110 140 169
请根据表中的数据,在坐标图中描点、绘制符合硝酸钾溶解度变化规律的曲线。
可知:硝酸钾的溶解度随温度升高而 (选填 “增大”或“减小”); 60℃时,将60g硝酸钾固体加入50g水中,所形成的溶液为 溶液(填写“饱和”或“不饱和”),所得溶液的溶质质量分数为 (精确到0.1%)。下图是有关硝酸钾溶液的实验操作及变化情况,已知溶液①到溶液②的过程中,溶液质量保持不变,
操作I的具体名称为 ,三种溶液的溶质质量分数大小关系为① ② ③(填“>”、“<”或“=”)。
15.如图是实验室制备气体的常用装置,请根据要求回答问题:
(1)仪器a的名称是 ,它是由 (填“无机”“合成”或“复合”)材料制成。
(2)A、B装置均可用来制取CO2气体,B装置的优点是 ;实验室更多使用A装置制取CO2气体的原因是 (答一点即可),使用C装置(正放)排空法收集CO2,验满的方法是 。
(3)制备CO2常用1:3的稀盐酸(用体积比为1:3的浓盐酸与水混合配制),已知浓盐酸的溶质质量分数为37%,密度为1.19g·mL-1,1:3的稀盐酸溶质质量分数为 (计算结果保留一位小数)。
三、填空题
16.甲、乙两种固体物质的溶解度曲线如图所示(已知两种物质溶解时互不影响),请回答下列问题。
(1)甲、乙溶解度曲线交点的意义 。
(2)40℃时分别溶解甲、乙两种固体,所得溶液中质量分数的最大值是 (精确到0.1%)。
(3)图中的饱和溶液有 (填序号),③到④实验过程中析出晶体质量为 g。
(4)40℃时,将等质量的甲、乙两种物质的饱和溶液分别蒸发等质量的水后,恢复到40℃,所得溶液质量的大小关系是甲 乙(填“大于”、“等于”或“小于”)。
17.A,B,C三种物质的溶解度随温度的变化情况如图:
(1)温度为 ℃时,A、C物质的溶解度相等。
(2)t1℃时A,B,C三种物质的溶解度由大到小的顺序是 。
(3)t1℃时,将50g的A物质溶于100g水中,所得溶液的质量为 g,溶质的质量分数为 。(保留到小数点后一位)
(4)t2℃时,将等质量的A,B,C三种物质的饱和溶液同时降温至t1℃时,析出晶体最多的是 。
四、计算题
18.洁厕灵的有效成分为HCl,某化学实验小组同学欲测定某品牌洁厕灵中的HCl的质量分数。同学们将100.0g洁厕灵倒入锥形瓶中,逐次加入一定量质量分数的碳酸钠溶液,至不在产生气体为止,共消耗80g碳酸钠溶液,并测得反应后溶液的质量为175.6g.请计算。
(1)生成二氧化碳的质量为 g。
(2)恰好完全反应时,所得溶液的溶质质量分数是多少?(写出计算过程,计算结果精确到0.1%)
19.某化学活动小组需要用溶质质量分数为19.6%的稀硫酸测量黄铜中铜的质量分数,但实验室现有的是溶质质量分数为98%的浓硫酸。试计算:
(1)将10g浓硫酸配制成所需的稀硫酸,需要水的质量为 g。
(2)上述配制好的稀硫酸20g与8g黄铜恰好完全反应,黄铜中铜的质量分数为多少?
五、综合题
20.如图是甲、乙、丙三种固体物质的溶解度曲线,回答问题:
(1)t1℃时,甲、乙、丙三种物质溶解度由大到小的顺序是: 。
(2)t2℃时,将45g甲加入到50g水中,充分溶解,所得溶液的质量为 g;
(3)要使t1℃时,接近饱和的乙溶液变成该温度下的饱和溶液,可采取的方法是 (写一种即可)。
21.如图1为甲、乙两种固体物质的溶解度曲线。
(1)某同学按图2所示进行实验,得到相应温度下的A、B、C溶液,在A、B、C三种溶液中属于饱和溶液的是 (填字母)。向溶液C中再加入25g甲,充分搅拌,恢复到t2℃时,所得溶液中溶质的质量为 g。
(2)将t2℃时等质量的甲、乙两种物质的饱和溶液降温至t1℃,下列说法正确的是__________。
A.降温后,甲溶液的质量大于乙溶液的质量
B.降温前,甲溶液中溶剂的质量比乙溶液中溶剂的质量小
C.降温后,甲溶液的质量分数大于乙溶液的质量分数
D.降温前后乙溶液的质量分数保持不变
答案解析部分
1.【答案】D
2.【答案】D
3.【答案】A
4.【答案】D
5.【答案】B
6.【答案】B
7.【答案】B
8.【答案】B
9.【答案】D
10.【答案】D
11.【答案】B
12.【答案】C
13.【答案】D
14.【答案】50;;增大;饱和;52.4%;降温;=;=
15.【答案】(1)铁架台;无机
(2)控制反应的开始和停止;A装置的反应容器为锥形瓶,能装的药品较多,则可制取大量的二氧化碳气体;将燃着的木条放在c口处,若木条熄灭,则瓶中二氧化碳收集满
(3)10.5%
16.【答案】(1)20℃时,甲、乙溶解度相同
(2)28.6%
(3)①②④;10
(4)大于
17.【答案】(1)t2
(2)C>B>A
(3)140;28.6%
(4)A
18.【答案】(1)4.4
(2)解:设生成NaCl的质量为x
x=11.7g
×100%≈6.7℅
答:恰好完全反应时,所得溶液的溶质质量分数为6.7%。
19.【答案】(1)40
(2)解:20g稀硫酸中溶质的质量=,设:8g黄铜中锌的质量为x。
8g黄铜中铜的质量分数=;
答:黄铜中铜的质量分数为67.5%。
20.【答案】(1)甲>乙>丙
(2)70g
(3)加入乙物质或降低温度、蒸发溶剂(写一种即可)
21.【答案】(1)B;40
(2)B;C;D
同课章节目录
