8.2金属的化学性质(第二课时) 达标检测(含答案)2023-2024学年人教版九年级化学下册
文档属性
| 名称 | 8.2金属的化学性质(第二课时) 达标检测(含答案)2023-2024学年人教版九年级化学下册 |

|
|
| 格式 | doc | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-01 00:00:00 | ||
图片预览


文档简介
中小学教育资源及组卷应用平台
8.2金属的化学性质(第二课时) 达标检测
一、选择题
1.在金属Cu、Al、Ag、Zn中,能与硝酸银溶液反应,但不能与稀硫酸反应的金属是( )
A.Al B.Zn C.Cu D.Ag
2.有甲、乙、丙、丁四种金属,只有丙在自然界能以单质形态存在。含甲化合物的水溶液不能用乙制的容器盛放。将甲和丁分别放入硝酸铜溶液中,在甲表面有铜析出,而丁没有变化。这四种金属活动性由强到弱的顺序是( )
A.丙>丁>甲>乙 B.乙>甲>丁>丙 C.丁>甲>乙>丙 D.丙>乙>甲>丁
3.以下实验能比较出铜和银的金属活动性强弱的是( )
A.测定两金属的密度 B.铜片放入硝酸银溶液中
C.将两种金属相互刻画 D.铜片、银片分别放入稀硫酸中
4.化学小组探究铝、铜、银三种金属的活动性顺序时,设计了如图所示实验方案。下列说法不正确的是( )
A.由实验甲可知金属活动性:Al>Cu
B.由实验乙可知金属活动性:Cu>Ag
C.丙中铜丝表面没有明显变化
D.实验甲中的CuSO4溶液改为CuCl2溶液,不能完成本实验探究
5.金属R与硫酸铜溶液反应的化学方程式是R+CuSO4=Cu+RSO4,下列说法正确的是( )
A.该反应属于置换反应 B.金属R的活泼性比Cu弱
C.该金属可以是铝 D.该金属一定是铁
6.下列各组物质不能验证Mg、Fe、Cu三种金属活动性强弱的是( )
A.稀盐酸、Mg、Fe、Cu B.MgSO4溶液、Fe、Cu
C.Mg、FeSO4 溶液、Cu D.MgSO4溶液、Fe、Cu(NO3)2溶液
7.下列事实不能用金属的活动性顺序加以解释的是( )
A.不能用铜与稀硫酸反应制取氢气
B.铁能置换出硫酸铜溶液中的铜
C.在化合物中,铁显+2、+3价,铜显+1、+2价
D.相同条件下,锌和铁与稀硫酸反应的剧烈程度不同
8.锡(Sn)是五金之一,它在金属活动性顺序中位于铁和铜之间,则下列反应不会发生的是( )
A.Zn+Sn(NO3)2=Zn(NO3)2+Sn B.Sn+2HCl=SnCl2+H2↑
C.Sn+2AgNO3=Sn(NO3)2+2Ag D.Sn+MgSO4=SnSO4+Mg
9.某学生为了验证锌、银、铜三种金属的活动性顺序,设计了五个实验:
①将Zn、Cu分别放入稀盐酸中;②将Ag放入Cu(NO3)2溶液中;③将Cu放入AgNO3溶液中;④将Cu放入ZnSO4溶液中;⑤将Zn放入AgNO3溶液中。
下列实验组合不能验证锌、银、铜三种金属活动性顺序的是( )
A.①② B.①③ C.②④ D.①⑤
10.在学习了金属活动性顺序的知识后,化学兴趣小组同学进行了如下实验:取足量的Zn、Fe、Ag三种金属分别放入盛有等质量的CuSO4溶液的①②③三支试管中,其反应前后溶液质量变化如图所示。下列有关说法正确的是( )
A.①②③三支试管中均发生置换反应
B.①中加入的是Fe,③中加入的是Zn
C.反应后③试管的溶液为浅绿色
D.三支试管中金属的活动性顺序为③>②>①
二、填空与简答题
11.实验课上,同学们设计并完成了以下几个实验,如下图所示,请回答问题。
(1)甲组实验中能观察到金属_________的表面产生气泡速率最快,金属_________的表面产生气泡缓慢,金属_________的表面没有气泡产生。有一支试管中的溶液变为浅绿色,写出该试管中发生反应的化学方程式: 。
(2)乙实验中铝与CuSO4溶液反应的现象为_________。 铜与AgNO3溶液反应的化学方程式为_________。通过乙实验,可得出Al、Cu、Ag三种金属活动性由弱到强的顺序为_________。
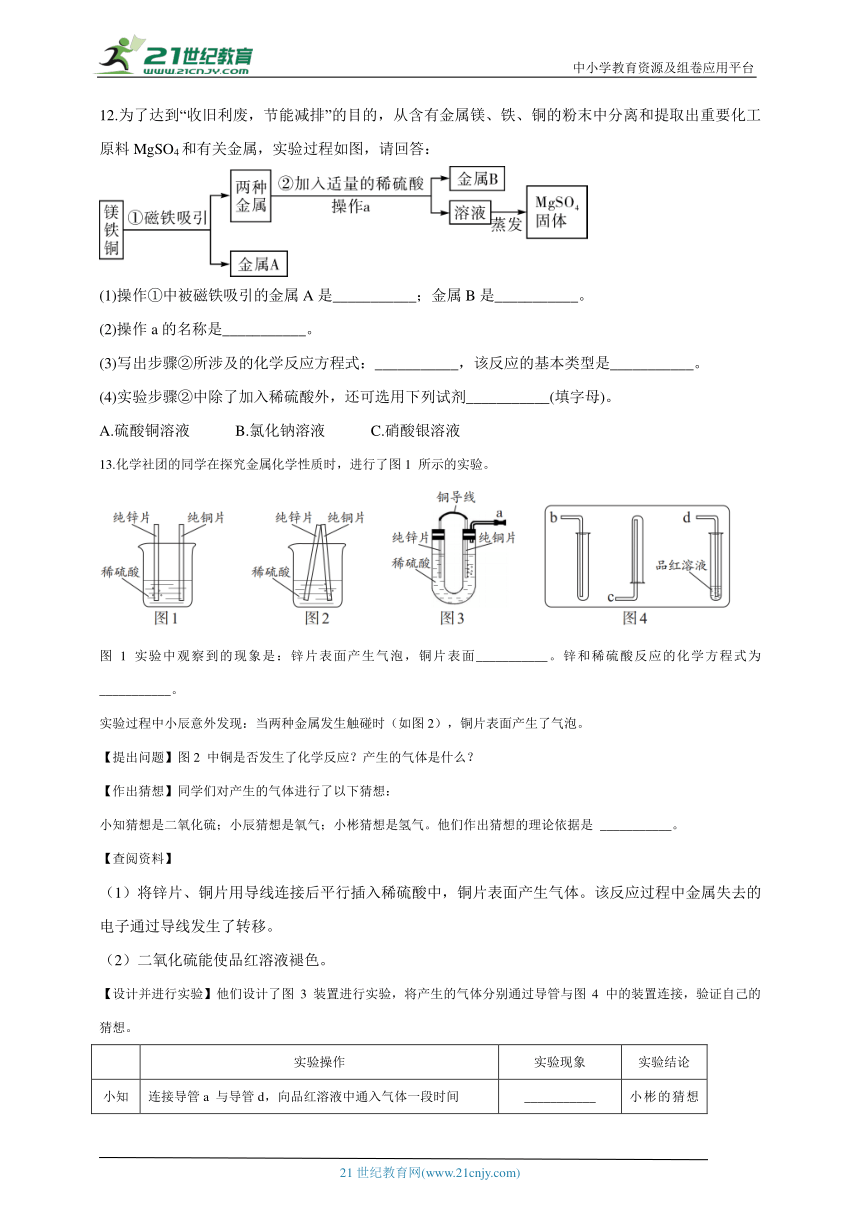
12.为了达到“收旧利废,节能减排”的目的,从含有金属镁、铁、铜的粉末中分离和提取出重要化工原料MgSO4和有关金属,实验过程如图,请回答:
(1)操作①中被磁铁吸引的金属A是___________;金属B是___________。
(2)操作a的名称是___________。
(3)写出步骤②所涉及的化学反应方程式:___________,该反应的基本类型是___________。
(4)实验步骤②中除了加入稀硫酸外,还可选用下列试剂___________(填字母)。
A.硫酸铜溶液 B.氯化钠溶液 C.硝酸银溶液
13.化学社团的同学在探究金属化学性质时,进行了图1 所示的实验。
图1 实验中观察到的现象是:锌片表面产生气泡,铜片表面___________。锌和稀硫酸反应的化学方程式为___________。
实验过程中小辰意外发现:当两种金属发生触碰时(如图2),铜片表面产生了气泡。
【提出问题】图2 中铜是否发生了化学反应?产生的气体是什么?
【作出猜想】同学们对产生的气体进行了以下猜想:
小知猜想是二氧化硫;小辰猜想是氧气;小彬猜想是氢气。他们作出猜想的理论依据是 ___________。
【查阅资料】
(1)将锌片、铜片用导线连接后平行插入稀硫酸中,铜片表面产生气体。该反应过程中金属失去的电子通过导线发生了转移。
(2)二氧化硫能使品红溶液褪色。
【设计并进行实验】他们设计了图3 装置进行实验,将产生的气体分别通过导管与图4 中的装置连接,验证自己的猜想。
实验操作 实验现象 实验结论
小知 连接导管a 与导管d,向品红溶液中通入气体一段时间 ___________ 小彬的猜想正确
小辰 选用正确方法收集气体一段时间后,向试管内伸入带火星的木条 木条不复燃
小彬 连接导管a 与导管________(填序号),收集气体后用拇指堵住试管口,靠近酒精灯火焰,移开拇指点火 气体燃烧,听到轻微的“噗”声
【教师释疑】图1 实验中,锌与稀硫酸反应,锌失去电子,酸溶液中氢离子在锌片表面获得电子生成氢气。
【学生感悟】图3 实验中,酸溶液中的氢离子从铜片表面获得___________(选填“锌”或“铜”)失去的电子生成了氢气。
【得出结论】图2 中两种金属触碰后铜___________(选填“有”或“没有”)发生化学反应。
【延伸应用】制造钢制船闸门时,为防止铁被腐蚀,常在钢闸门表面安装比铁更活泼的金属。这种金属可以是___________(填序号)。
A.锌 B.铜 C.银
参考答案
1.C 2.B 3.B 4.D 5.A 6.B 7.C 8.D 9.D 10.C
11.(1)Mg Fe Cu Fe+2HCl=FeCl2+H2↑ (2)铝丝的表面附着一层紫红色物质,溶液由蓝色逐渐变为无色 Cu+2AgNO3=2Ag+Cu(NO3)2 Ag12.(1)铁 铜 (2)过滤 (3)Mg+H2SO4=MgSO4+H2↑ 置换反应 (4)A
13.无气泡产生(或无明显现象) Zn+ H2SO4==ZnSO4+ H2↑
【作出猜想】质量守恒定律(或反应前后元素种类不变等)
【设计并进行实验】品红溶液不褪色(或无明显现象) c
【学生感悟】锌
【得出结论】没有
【延伸应用】A
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
8.2金属的化学性质(第二课时) 达标检测
一、选择题
1.在金属Cu、Al、Ag、Zn中,能与硝酸银溶液反应,但不能与稀硫酸反应的金属是( )
A.Al B.Zn C.Cu D.Ag
2.有甲、乙、丙、丁四种金属,只有丙在自然界能以单质形态存在。含甲化合物的水溶液不能用乙制的容器盛放。将甲和丁分别放入硝酸铜溶液中,在甲表面有铜析出,而丁没有变化。这四种金属活动性由强到弱的顺序是( )
A.丙>丁>甲>乙 B.乙>甲>丁>丙 C.丁>甲>乙>丙 D.丙>乙>甲>丁
3.以下实验能比较出铜和银的金属活动性强弱的是( )
A.测定两金属的密度 B.铜片放入硝酸银溶液中
C.将两种金属相互刻画 D.铜片、银片分别放入稀硫酸中
4.化学小组探究铝、铜、银三种金属的活动性顺序时,设计了如图所示实验方案。下列说法不正确的是( )
A.由实验甲可知金属活动性:Al>Cu
B.由实验乙可知金属活动性:Cu>Ag
C.丙中铜丝表面没有明显变化
D.实验甲中的CuSO4溶液改为CuCl2溶液,不能完成本实验探究
5.金属R与硫酸铜溶液反应的化学方程式是R+CuSO4=Cu+RSO4,下列说法正确的是( )
A.该反应属于置换反应 B.金属R的活泼性比Cu弱
C.该金属可以是铝 D.该金属一定是铁
6.下列各组物质不能验证Mg、Fe、Cu三种金属活动性强弱的是( )
A.稀盐酸、Mg、Fe、Cu B.MgSO4溶液、Fe、Cu
C.Mg、FeSO4 溶液、Cu D.MgSO4溶液、Fe、Cu(NO3)2溶液
7.下列事实不能用金属的活动性顺序加以解释的是( )
A.不能用铜与稀硫酸反应制取氢气
B.铁能置换出硫酸铜溶液中的铜
C.在化合物中,铁显+2、+3价,铜显+1、+2价
D.相同条件下,锌和铁与稀硫酸反应的剧烈程度不同
8.锡(Sn)是五金之一,它在金属活动性顺序中位于铁和铜之间,则下列反应不会发生的是( )
A.Zn+Sn(NO3)2=Zn(NO3)2+Sn B.Sn+2HCl=SnCl2+H2↑
C.Sn+2AgNO3=Sn(NO3)2+2Ag D.Sn+MgSO4=SnSO4+Mg
9.某学生为了验证锌、银、铜三种金属的活动性顺序,设计了五个实验:
①将Zn、Cu分别放入稀盐酸中;②将Ag放入Cu(NO3)2溶液中;③将Cu放入AgNO3溶液中;④将Cu放入ZnSO4溶液中;⑤将Zn放入AgNO3溶液中。
下列实验组合不能验证锌、银、铜三种金属活动性顺序的是( )
A.①② B.①③ C.②④ D.①⑤
10.在学习了金属活动性顺序的知识后,化学兴趣小组同学进行了如下实验:取足量的Zn、Fe、Ag三种金属分别放入盛有等质量的CuSO4溶液的①②③三支试管中,其反应前后溶液质量变化如图所示。下列有关说法正确的是( )
A.①②③三支试管中均发生置换反应
B.①中加入的是Fe,③中加入的是Zn
C.反应后③试管的溶液为浅绿色
D.三支试管中金属的活动性顺序为③>②>①
二、填空与简答题
11.实验课上,同学们设计并完成了以下几个实验,如下图所示,请回答问题。
(1)甲组实验中能观察到金属_________的表面产生气泡速率最快,金属_________的表面产生气泡缓慢,金属_________的表面没有气泡产生。有一支试管中的溶液变为浅绿色,写出该试管中发生反应的化学方程式: 。
(2)乙实验中铝与CuSO4溶液反应的现象为_________。 铜与AgNO3溶液反应的化学方程式为_________。通过乙实验,可得出Al、Cu、Ag三种金属活动性由弱到强的顺序为_________。
12.为了达到“收旧利废,节能减排”的目的,从含有金属镁、铁、铜的粉末中分离和提取出重要化工原料MgSO4和有关金属,实验过程如图,请回答:
(1)操作①中被磁铁吸引的金属A是___________;金属B是___________。
(2)操作a的名称是___________。
(3)写出步骤②所涉及的化学反应方程式:___________,该反应的基本类型是___________。
(4)实验步骤②中除了加入稀硫酸外,还可选用下列试剂___________(填字母)。
A.硫酸铜溶液 B.氯化钠溶液 C.硝酸银溶液
13.化学社团的同学在探究金属化学性质时,进行了图1 所示的实验。
图1 实验中观察到的现象是:锌片表面产生气泡,铜片表面___________。锌和稀硫酸反应的化学方程式为___________。
实验过程中小辰意外发现:当两种金属发生触碰时(如图2),铜片表面产生了气泡。
【提出问题】图2 中铜是否发生了化学反应?产生的气体是什么?
【作出猜想】同学们对产生的气体进行了以下猜想:
小知猜想是二氧化硫;小辰猜想是氧气;小彬猜想是氢气。他们作出猜想的理论依据是 ___________。
【查阅资料】
(1)将锌片、铜片用导线连接后平行插入稀硫酸中,铜片表面产生气体。该反应过程中金属失去的电子通过导线发生了转移。
(2)二氧化硫能使品红溶液褪色。
【设计并进行实验】他们设计了图3 装置进行实验,将产生的气体分别通过导管与图4 中的装置连接,验证自己的猜想。
实验操作 实验现象 实验结论
小知 连接导管a 与导管d,向品红溶液中通入气体一段时间 ___________ 小彬的猜想正确
小辰 选用正确方法收集气体一段时间后,向试管内伸入带火星的木条 木条不复燃
小彬 连接导管a 与导管________(填序号),收集气体后用拇指堵住试管口,靠近酒精灯火焰,移开拇指点火 气体燃烧,听到轻微的“噗”声
【教师释疑】图1 实验中,锌与稀硫酸反应,锌失去电子,酸溶液中氢离子在锌片表面获得电子生成氢气。
【学生感悟】图3 实验中,酸溶液中的氢离子从铜片表面获得___________(选填“锌”或“铜”)失去的电子生成了氢气。
【得出结论】图2 中两种金属触碰后铜___________(选填“有”或“没有”)发生化学反应。
【延伸应用】制造钢制船闸门时,为防止铁被腐蚀,常在钢闸门表面安装比铁更活泼的金属。这种金属可以是___________(填序号)。
A.锌 B.铜 C.银
参考答案
1.C 2.B 3.B 4.D 5.A 6.B 7.C 8.D 9.D 10.C
11.(1)Mg Fe Cu Fe+2HCl=FeCl2+H2↑ (2)铝丝的表面附着一层紫红色物质,溶液由蓝色逐渐变为无色 Cu+2AgNO3=2Ag+Cu(NO3)2 Ag
13.无气泡产生(或无明显现象) Zn+ H2SO4==ZnSO4+ H2↑
【作出猜想】质量守恒定律(或反应前后元素种类不变等)
【设计并进行实验】品红溶液不褪色(或无明显现象) c
【学生感悟】锌
【得出结论】没有
【延伸应用】A
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
同课章节目录
