《8.3金属资源的利用和保护(第一课时)》课后作业(含答案)2023-2024学年人教版九年级化学下册
文档属性
| 名称 | 《8.3金属资源的利用和保护(第一课时)》课后作业(含答案)2023-2024学年人教版九年级化学下册 |

|
|
| 格式 | doc | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-01 00:00:00 | ||
图片预览

文档简介
中小学教育资源及组卷应用平台
《8.3金属资源的利用和保护(第一课时)》课后作业
一、选择题
1.下列原料不是高炉炼铁所需的是( )
A.孔雀石 B.焦炭 C.石灰石 D.铁矿石
2.铁是应用最广泛的金属之一。下列物质中不能与氧化铁反应生成铁的是( )
A.木炭 B.氢气 C.一氧化碳 D.氧气
3.块炼铁以炭和铁矿石为原料,反应之一为Fe2O3+3CO2Fe+3CO2,该反应中,化合价降低的元素是( )
A.铁元素 B.碳元素 C.氧元素 D.铁元素和碳元素
4.下列有关高炉炼铁的说法正确的一组是( )
①高炉中焦炭的作用是产生一氧化碳 ②高炉中焦炭的作用是供热 ③高炉炼铁得到的产品是钢 ④高炉炼铁的原料有铁矿石、焦炭、石灰石、空气等
A.①②③ B.②③④ C.①③④ D.①②④
5.物质X与Y能够由如图反应生成,下列各组物质不符合该反应的是( )
选项 X Y
A Fe CO2
B H2 CuSO4
C Zn MgSO4
D CO2 H2O
6.实验室里,用如图所示装置还原氧化铁的过程中,可能生成四氧化三铁、氧化亚铁或铁等固体物质。关于该实验,下列说法错误的是( )
A.实验时,澄清的石灰水变浑浊,证明该反应有二氧化碳生成
B.实验结束时,玻璃管中红色的氧化铁粉末变成黑色,该产物不一定是铁
C.实验结束时,应先停止通一氧化碳气体,后停止加热
D.为了减少空气污染,应增加尾气处理装置
7.下列关于工业炼铁的叙述中错误的是( )
A.使用的设备是高炉
B.主要原理是:2Fe2O3+3C4Fe+3CO2↑
C.主要原料为铁矿石、石灰石、焦炭和热空气等
D.主要产物为生铁
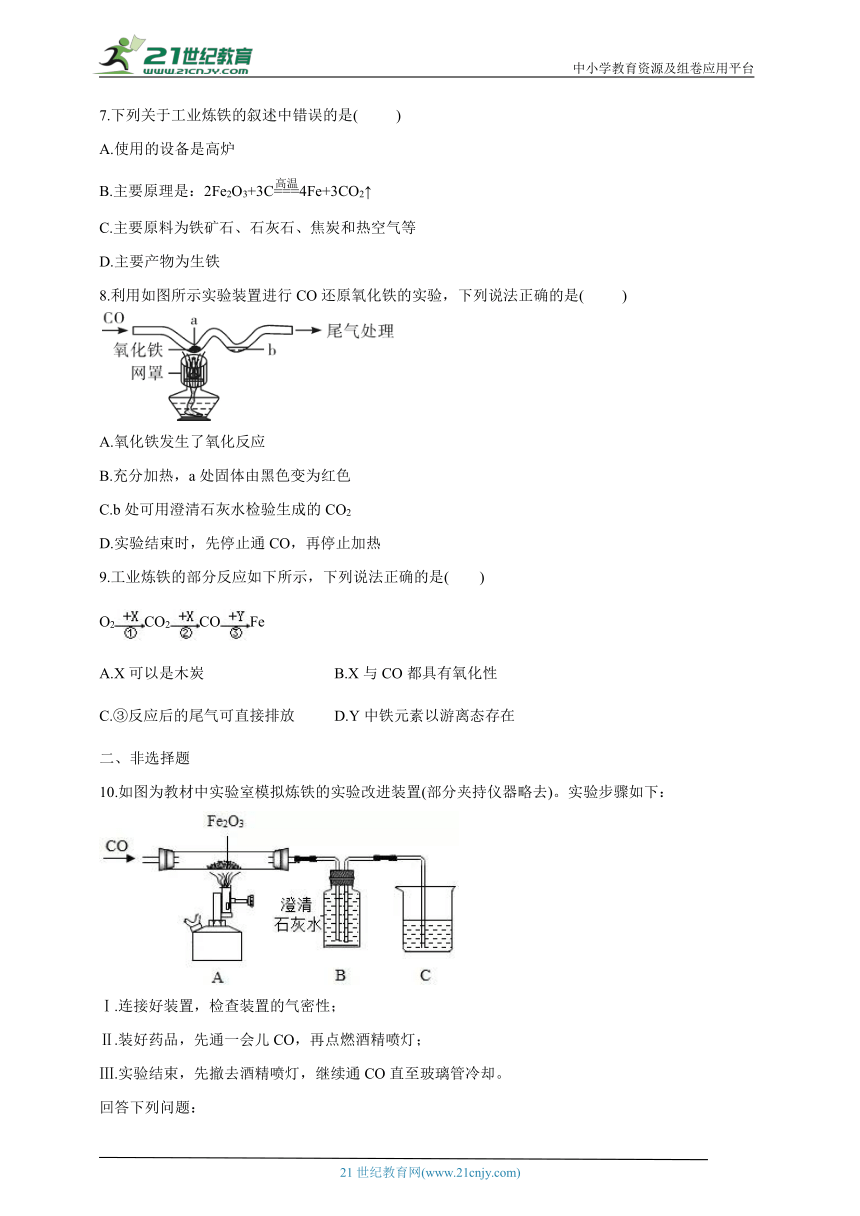
8.利用如图所示实验装置进行CO还原氧化铁的实验,下列说法正确的是( )
A.氧化铁发生了氧化反应
B.充分加热,a处固体由黑色变为红色
C.b处可用澄清石灰水检验生成的CO2
D.实验结束时,先停止通CO,再停止加热
9.工业炼铁的部分反应如下所示,下列说法正确的是( )
O2CO2COFe
A.X可以是木炭 B.X与CO都具有氧化性
C.③反应后的尾气可直接排放 D.Y中铁元素以游离态存在
二、非选择题
10.如图为教材中实验室模拟炼铁的实验改进装置(部分夹持仪器略去)。实验步骤如下:
Ⅰ.连接好装置,检查装置的气密性;
Ⅱ.装好药品,先通一会儿CO,再点燃酒精喷灯;
Ⅲ.实验结束,先撤去酒精喷灯,继续通CO直至玻璃管冷却。
回答下列问题:
(1)实验中可看到A处玻璃管里的粉末由红色逐渐变黑,说明Fe2O3转化为______(填化学式),B瓶中澄清石灰水变浑浊,该反应的化学方程式为____________。
(2)步骤Ⅲ中先撤去酒精喷灯,继续通CO直至玻璃管冷却的目的是____________。
(3)盛满石灰水的B装置在此实验中的作用有下列说法:
①收集多余的CO ②检验并吸收反应生成的CO2
上述说法中正确的____________。
A.只有① B.只有② C.是①和②
11.早在春秋战国时期,我国就开始生产和使用铁器。某实验小组利用焦炭和Fe2O3模拟早期炼铁并检验可能的产物,实验装置如下:
【查阅资料】①铁粉为黑色;常温下,Fe、Fe3O4可被磁铁吸引;
②PbCl2,溶液可用于检验CO,原理是:PdCl2+CO+H2O=Pd↓+CO2+2HCl;
③Fe3O4与硫酸反应: Fe3O4+4H2SO4=FeSO4+Fe2(SO4)3+4H2O
【实验现象】澄清石灰水变浑浊,PdCl2溶液中产生黑色沉淀,玻璃管内粉末全部变成黑色。冷却后,用磁铁靠近黑色固体,黑色固体被部分吸引。
(1)仪器A的名称是___________。
(2)为了检验气体产物,装置从左到右的接口连接顺序为a→_____→_____ →_____ →____。
(3)澄清石灰水变浑浊的化学方程式___________。
【实验结论】反应生成CO 和CO2,磁铁上的黑色固体可能是 Fe、Fe3O4。
【提出猜想】磁铁上的黑色固体是什么?
猜想一:Fe 猜想二:Fe3O4 猜想三:Fe 和Fe3O4
【设计实验】
设计思路 操作 现象 结论
定性实验 取少量黑色固体于试管中,加入足量稀硫酸,充分反应 固体完全溶解,产生气泡 猜想_______不成立
定量实验 取一定质量的稀硫酸(足量)放入烧杯中,加入5.6g黑色固体,充分反应后称量溶液的质量 固体完全溶解,产生气泡,溶液增加的质量为___________ 猜想一成立
【归纳总结】根据实验结论和探究结果C与Fe2O3反应的化学方程式为___________。
12.用500 t含氧化铁质量分数为70%的赤铁矿,可以炼出多少吨含杂质4%的生铁 (写出计算过程,结果保留一位小数)
参考答案
1.A 2.D 3.A 4.D 5.B 6.C 7.B 8.C 9.A
10.(1)Fe CO2+Ca(OH)2=CaCO3↓+H2O (2)防止生成的铁被空气中的氧气氧化 (3)C
11.(1)酒精灯 (2)d e b c (3)CO2+Ca(OH)2=CaCO3↓+H2O 【设计实验】二 5.4g 【归纳总结】Fe2O3+2C2Fe+CO↑+CO2↑
12.解:设可以炼出含杂质4%的生铁的质量为x。
Fe2O3+3CO2Fe+3CO2
160 112
500 t×70% x (1-4%)
x≈255.2 t
答:可以炼出含杂质4%的生铁255.2 t。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
《8.3金属资源的利用和保护(第一课时)》课后作业
一、选择题
1.下列原料不是高炉炼铁所需的是( )
A.孔雀石 B.焦炭 C.石灰石 D.铁矿石
2.铁是应用最广泛的金属之一。下列物质中不能与氧化铁反应生成铁的是( )
A.木炭 B.氢气 C.一氧化碳 D.氧气
3.块炼铁以炭和铁矿石为原料,反应之一为Fe2O3+3CO2Fe+3CO2,该反应中,化合价降低的元素是( )
A.铁元素 B.碳元素 C.氧元素 D.铁元素和碳元素
4.下列有关高炉炼铁的说法正确的一组是( )
①高炉中焦炭的作用是产生一氧化碳 ②高炉中焦炭的作用是供热 ③高炉炼铁得到的产品是钢 ④高炉炼铁的原料有铁矿石、焦炭、石灰石、空气等
A.①②③ B.②③④ C.①③④ D.①②④
5.物质X与Y能够由如图反应生成,下列各组物质不符合该反应的是( )
选项 X Y
A Fe CO2
B H2 CuSO4
C Zn MgSO4
D CO2 H2O
6.实验室里,用如图所示装置还原氧化铁的过程中,可能生成四氧化三铁、氧化亚铁或铁等固体物质。关于该实验,下列说法错误的是( )
A.实验时,澄清的石灰水变浑浊,证明该反应有二氧化碳生成
B.实验结束时,玻璃管中红色的氧化铁粉末变成黑色,该产物不一定是铁
C.实验结束时,应先停止通一氧化碳气体,后停止加热
D.为了减少空气污染,应增加尾气处理装置
7.下列关于工业炼铁的叙述中错误的是( )
A.使用的设备是高炉
B.主要原理是:2Fe2O3+3C4Fe+3CO2↑
C.主要原料为铁矿石、石灰石、焦炭和热空气等
D.主要产物为生铁
8.利用如图所示实验装置进行CO还原氧化铁的实验,下列说法正确的是( )
A.氧化铁发生了氧化反应
B.充分加热,a处固体由黑色变为红色
C.b处可用澄清石灰水检验生成的CO2
D.实验结束时,先停止通CO,再停止加热
9.工业炼铁的部分反应如下所示,下列说法正确的是( )
O2CO2COFe
A.X可以是木炭 B.X与CO都具有氧化性
C.③反应后的尾气可直接排放 D.Y中铁元素以游离态存在
二、非选择题
10.如图为教材中实验室模拟炼铁的实验改进装置(部分夹持仪器略去)。实验步骤如下:
Ⅰ.连接好装置,检查装置的气密性;
Ⅱ.装好药品,先通一会儿CO,再点燃酒精喷灯;
Ⅲ.实验结束,先撤去酒精喷灯,继续通CO直至玻璃管冷却。
回答下列问题:
(1)实验中可看到A处玻璃管里的粉末由红色逐渐变黑,说明Fe2O3转化为______(填化学式),B瓶中澄清石灰水变浑浊,该反应的化学方程式为____________。
(2)步骤Ⅲ中先撤去酒精喷灯,继续通CO直至玻璃管冷却的目的是____________。
(3)盛满石灰水的B装置在此实验中的作用有下列说法:
①收集多余的CO ②检验并吸收反应生成的CO2
上述说法中正确的____________。
A.只有① B.只有② C.是①和②
11.早在春秋战国时期,我国就开始生产和使用铁器。某实验小组利用焦炭和Fe2O3模拟早期炼铁并检验可能的产物,实验装置如下:
【查阅资料】①铁粉为黑色;常温下,Fe、Fe3O4可被磁铁吸引;
②PbCl2,溶液可用于检验CO,原理是:PdCl2+CO+H2O=Pd↓+CO2+2HCl;
③Fe3O4与硫酸反应: Fe3O4+4H2SO4=FeSO4+Fe2(SO4)3+4H2O
【实验现象】澄清石灰水变浑浊,PdCl2溶液中产生黑色沉淀,玻璃管内粉末全部变成黑色。冷却后,用磁铁靠近黑色固体,黑色固体被部分吸引。
(1)仪器A的名称是___________。
(2)为了检验气体产物,装置从左到右的接口连接顺序为a→_____→_____ →_____ →____。
(3)澄清石灰水变浑浊的化学方程式___________。
【实验结论】反应生成CO 和CO2,磁铁上的黑色固体可能是 Fe、Fe3O4。
【提出猜想】磁铁上的黑色固体是什么?
猜想一:Fe 猜想二:Fe3O4 猜想三:Fe 和Fe3O4
【设计实验】
设计思路 操作 现象 结论
定性实验 取少量黑色固体于试管中,加入足量稀硫酸,充分反应 固体完全溶解,产生气泡 猜想_______不成立
定量实验 取一定质量的稀硫酸(足量)放入烧杯中,加入5.6g黑色固体,充分反应后称量溶液的质量 固体完全溶解,产生气泡,溶液增加的质量为___________ 猜想一成立
【归纳总结】根据实验结论和探究结果C与Fe2O3反应的化学方程式为___________。
12.用500 t含氧化铁质量分数为70%的赤铁矿,可以炼出多少吨含杂质4%的生铁 (写出计算过程,结果保留一位小数)
参考答案
1.A 2.D 3.A 4.D 5.B 6.C 7.B 8.C 9.A
10.(1)Fe CO2+Ca(OH)2=CaCO3↓+H2O (2)防止生成的铁被空气中的氧气氧化 (3)C
11.(1)酒精灯 (2)d e b c (3)CO2+Ca(OH)2=CaCO3↓+H2O 【设计实验】二 5.4g 【归纳总结】Fe2O3+2C2Fe+CO↑+CO2↑
12.解:设可以炼出含杂质4%的生铁的质量为x。
Fe2O3+3CO2Fe+3CO2
160 112
500 t×70% x (1-4%)
x≈255.2 t
答:可以炼出含杂质4%的生铁255.2 t。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
同课章节目录
