2024年河北化学中考备考重难专题:小实验到实验探究题(课件)(共29张PPT)
文档属性
| 名称 | 2024年河北化学中考备考重难专题:小实验到实验探究题(课件)(共29张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-01 00:00:00 | ||
图片预览






文档简介
(共29张PPT)
河北 化学
小实验到实验探究题
2024中考备考重难专题课件
课件说明
一、课件设计初衷
基于老师在总复习过程中对重难题型有较大的需求,难易结合化学学科的重难点,为此设计重难专题复习课件,助力高效课堂
二、课件亮点
1.对专题知识体系的构建
侧重专题知识体系分解再构建,根据本区域近五年的中考真题提炼知识点,通过知识点讲授方法和技巧,并进一步形成对应体系,再让学生尝试应用已有体系中的方法与技巧去解决问题,在复习过程中构建自己的重难专题知识体系。会对难题进行分解,降低梯度,准确、高效攻克重难专题。
2.过程性分析设置分步动画
对方法讲解、解题步骤设置分步动画,按步骤播放,更清晰有条理。
三、课件使用场景
适用于中考二轮专题复习
1
模型构建
典例精析
2
巩固练习
3
模型构建
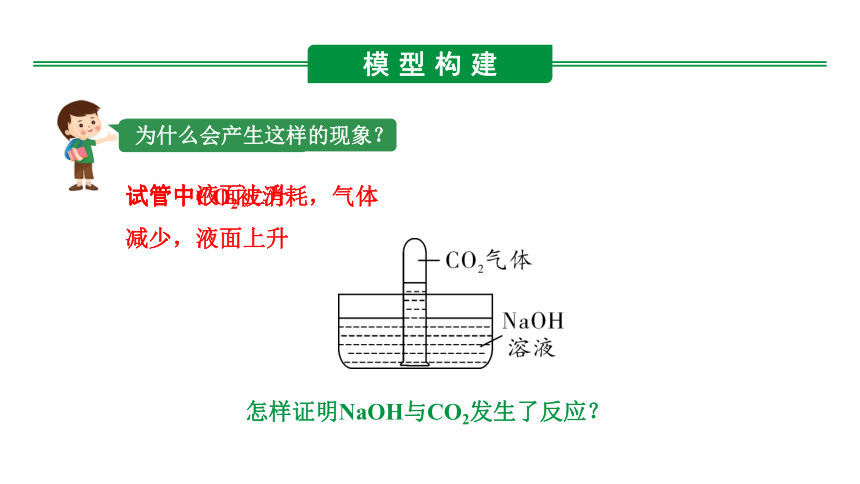
观察到什么现象?
试管中液面上升
试管中CO2被消耗,气体减少,液面上升
为什么会产生这样的现象?
怎样证明NaOH与CO2发生了反应?
观察与问题
假设与预测
怎样证明NaOH与CO2发生了反应?
①能发生化学反应
②不能发生化学反应
设计实验
证明反应物减少或消失
科学探究
证明CO2与氢氧化钠溶液反应消耗
CO2消耗
CO2未消耗
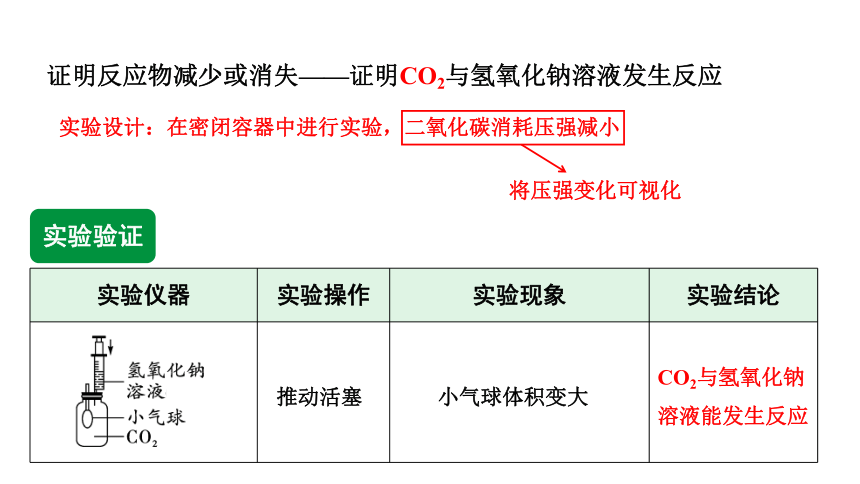
证明反应物减少或消失——证明CO2与氢氧化钠溶液发生反应
实验设计:在密闭容器中进行实验,二氧化碳消耗压强减小
将压强变化可视化
实验验证
实验仪器 实验操作 实验现象 实验结论
推动活塞
小气球体积变大
CO2与氢氧化钠溶液能发生反应
该实验能证明CO2与氢氧化钠溶液发生反应吗?原因是什么?
实验反思
不能,可能只是与溶液中水发生了化学反应,需要设计对比实验,对比CO2与氢氧化钠溶液和水溶液反应现象的区别证明
实验验证
实验仪器 实验操作 实验现象 实验结论
推动活塞
小气球体积变大
CO2与氢氧化钠溶液能发生反应
水
推动活塞
小气球体积变大,但没有实验①的体积变化明显
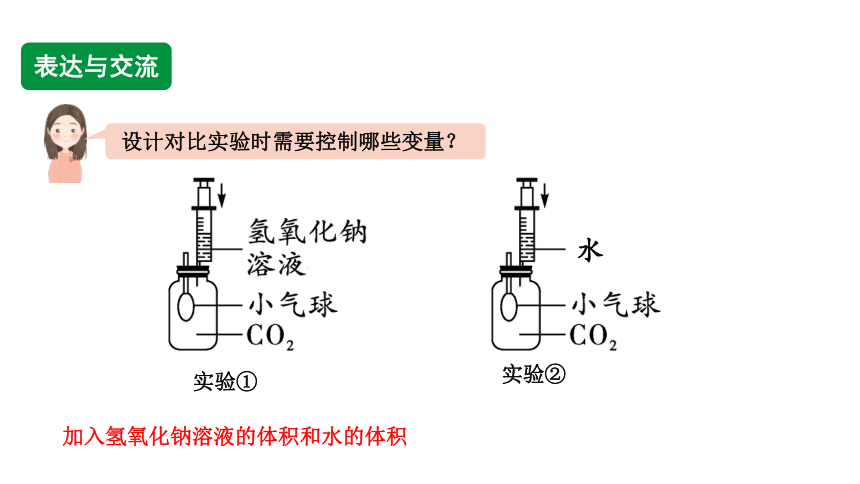
实验②
实验①
设计对比实验时需要控制哪些变量?
水
实验②
实验①
表达与交流
加入氢氧化钠溶液的体积和水的体积
科学探究的思维模型
观察与问题
猜想与假设
设计实验
实验验证
实验反思
发现问题深入探究
①发生反应
②未发生反应
表达与交流
→CO2消耗
→CO2未消耗
单一实验为何不能得到正确结论?
分析原因、设计对比实验
拓展延伸
化学反应的本质特征是什么?
有新物质生成
证明发生化学反应的新思路
证明是否有Na2CO3存在
碳酸钠的化学性质:
①溶于水显碱性
②与酸、碱、盐反应
沉
气
Ba2+
Ca2+
H+
实验验证
试剂选择 实验操作 实验现象 实验结论
(取样→试剂→现象→结论)
取样于试管中,滴加过量稀盐酸或稀硫酸
取样于试管中,滴加Ca(OH)2溶液或Ba(OH)2溶液
取样于试管中,滴加CaCl2溶液或BaCl2溶液
有气泡产生
有白色沉淀产生
有白色沉淀产生
发生化学变化
发生化学变化
发生化学变化
实验②:滴加碱溶液
实验③:滴加盐溶液
实验①:滴加过量稀酸溶液
探究“CO2能否与NaOH溶液发生化学反应”
无明显现象实验探究的一般思路
证明有碳酸钠生成
证明二氧化碳减少或消失
思路2:证明有新物质生成
思路1:证明反应物减少或消失
(利用性质,现象明显)
(对比实验,控制变量)
典例精析
1.(2022逆袭卷)钙尔奇D片是常见的补钙剂,小明不小心将手中的钙尔奇D片掉入装有白醋的碗碟中,观察到有气泡出现,于是他对该现象产生兴趣,进行如下探究。
【查阅资料】①钙尔奇D片的主要成分是CaCO3;白醋的主要成分是
醋酸(CH3COOH),醋酸是一种常见的酸,能与碳酸钙发生化学反应。
②无水硫酸铜遇水变蓝色。
探究一:钙尔奇D片遇白醋后产生的气体是什么?
【提出问题】产生的气体是什么?
【作出猜想】可能是CO2、H2、O2中的一种或两种。
【设计实验】为了验证气体成分,小明同学将一定量的钙尔奇D片加入到白醋中,并收集两试管气体。
(1)小明将燃着的木条伸入其中一支试管中,观察到________________;
(2)小明向另一支试管中加入澄清石灰水,观察到澄清石灰水变浑浊。因此小明推断出该气体为CO2。写出(2)中发生反应的化学方程式__________________________________。
实验过程中,小明发现有同学将钙尔奇D片加入到白醋中产生气泡的速度较快,在老师的帮助下,小明对影响产生气体速率的因素展开探究。
二氧化碳不燃烧也不支持燃烧
燃着的木条熄灭
CO2+Ca(OH)2===CaCO3↓+H2O
探究二:影响产生CO2速率的因素是什么?
老师提醒小明可通过单位时间内产生二氧化碳的浓度判断产生气体的速率。
【作出猜想】猜想1:与反应物间的接触面积有关
猜想2:与反应温度有关
【进行实验】将等质量的钙尔奇D片与等体积、等浓度的白醋充分反应,用数字传感器测得二氧化碳浓度随时间的变化曲线如图所示,实验记录如表所示。
实验编号 反应物形状 温度/℃ 曲线斜率
① 片状 100 1151
② 片状 25 389
③ 粉末状 100 1621
④ 粉末状 25 877
相同温度下不同的形状对比
相同形状下不同的温度对比
实验编号 反应物形状 温度/℃ 曲线斜率
① 片状 100 1151
② 片状 25 389
③ 粉末状 100 1621
④ 粉末状 25 877
【实验结论】(1)若验证猜想2成立,需要选择的对比实验是____________(填实验编号)。
(2)设计实验②④的目的是_________________________________________。
猜想1:与反应物间的接触面积有关
猜想2:与反应温度有关
①②或③④
证明反应物间的接触面积影响产生CO2的速率
温度相同,形状不同
实验编号 反应物形状 温度/℃ 曲线斜率
① 片状 100 1151
② 片状 25 389
③ 粉末状 100 1621
④ 粉末状 25 877
(3)由上述实验可得出的结论是_________________________________________
_______________________________________________________________。
猜想1:与反应物间的接触面积有关
猜想2:与反应温度有关
相同条件下,温度越高,产生CO2的速率越快(或相同条件下,反应物间的接触面积越大,产生CO2的速率越快)
【交流反思】(1)白醋的浓度也可能影响产生气体的速率,请你设计实验方案____________________________________________________________________________________________________________________。
(2)根据图1和图2可知,等质量不同形状的钙尔奇D片与等体积等浓度的白醋反应,产生CO2的量______(选填“相等”或“不相等”)。
变量
室温下,将等质量的片状钙尔奇D片分别与等体积、浓度为5%和25%的白醋反应,用传感器检测产生CO2浓度随时间的变化曲线
相等
温度、形状影响的都是CO2的反应速率,产生CO2的量是由反应物的量决定的
巩固练习
1.2021年10月16日,搭载神舟十三号的长征二号F遥十三运载火箭亮相,航天工作者给它贴了“暖宝宝”。 某社会实践小组的同学们对此产生浓厚的兴趣,并对火箭贴“暖宝宝”的原因、“暖宝宝”中的主要成分及作用展开了一系列探究活动。
【查阅资料】①“暖宝宝”中含有铁粉、氯化钠、水等物质,可持续发热12 小时左右。
②返回器推进剂肼(N2H4) 的熔点为1.4℃,且有剧毒,一旦在低温环境下凝固,会产生很多潜在的问题,甚至发生危险。
【查阅资料】①“暖宝宝”中含有铁粉、氯化钠、水等物质,可持续发热12
小时左右。
②返回器推进剂肼(N2H4) 的熔点为1.4℃,且有剧毒,一旦在低温环境下凝固,会产生很多潜在的问题,甚至发生危险。
探究一:探究贴“暖宝宝”的原因。
【交流讨论】分析资料,火箭贴“暖宝宝”的原因是____________________
_________。
防止返回器推进剂肼遇冷凝固
探究二:验证“暖宝宝”中的主要成分。
【实验准备】剪开“暖宝宝”外包装,取出其中固体。
实验操作 实验现象 实验结论
①取少量固体于试管中,加入足量稀盐酸 ______________________________________________ 固体中含有铁粉
②另取少量固体于试管中,加足量水,充分溶解后过滤_____________________ __________ 产生白色沉淀且白色沉淀不溶解 固体中含有氯化钠
固体逐渐溶解,产生气泡,溶液由无色变为浅绿色
向滤液中加入AgNO3溶液和稀硝酸
氯化银沉淀不溶于酸
【实验总结】步骤①中发生反应的化学方程式为_______________________。
Fe+2HCl===FeCl2+H2↑
探究三:探究成分中氯化钠的作用
【实验2】小王同学设计并进行如图所示的实验,观察一段时间,发现铁粉均生锈,且B中铁粉生锈较快。
【交流讨论】该实验设计的不足之处是__________________________。
【得出结论】经改正后仍然是加氯化钠的铁粉生锈更快,则发热贴中氯化钠的作用是____________________。
A、B 烧杯中的加水量不同
控制变量法应只有一个变量,水的量不同,无法形成对比
加快铁粉的生锈速率
【拓展交流】“暖宝宝”中的铁粉在氧气、水的作用下能发生缓慢氧化,同时放出热量。 由此可见,人们可以利用化学反应放出的能量,请再举一例:
_____________。
煤燃烧取暖
2.同学们了解到碳酸钠与氢氧化钙能发生反应,实验中可观察到溶液变浑浊的现象,但小明同学进行如图所示实验时却未观察到预期现象,于是小组同学对此异常现象进行如下探究。
【知识回顾】 碳酸钠与氢氧化钙溶液反应的化学方程式是____________________________________
Na2CO3+Ca(OH)2===CaCO3↓+2NaOH
【提出问题】 小明实验中未观察到浑浊现象的原因是什么
【猜想与假设】同学们提出了如下猜想:
猜想一:氢氧化钙溶液的浓度偏低;
猜想二:碳酸钠溶液的浓度偏低;
猜想三:生成的碳酸钙沉淀溶解了。
经讨论,同学们认为猜想一不合理,____________________________________。
溶液已经饱和
饱和澄清石灰水是该条件下的最大浓度
【进行实验】小组同学设计如下实验。
编号 1 2 3
实验方案
现象 浑浊 浑浊 不浑浊
【解释与结论】(1)实验1中X的值为_____。
(2)由上述实验过程可知,猜想二___________(填“成立”或“不成立”)。
2
不成立
实验2和实验3的变量是什么?
编号 2 3
实验方案
现象 浑浊 不浑浊
加入的碳酸钠溶液浓度不同
说明碳酸钙沉淀溶解与碳酸钠的浓度有关,再做进一步探究
【继续探究】为进一步验证猜想三,小明将实验1所得的浑浊液过滤,将滤渣分为两等份,分别加入 A、B 两支试管中,向 A 试管中加入2 mL 水,向 B 试管中加入______________________,振荡,观察到________________________
________________,说明猜想三成立
2mL10%的碳酸钠溶液
试管 A中滤渣不溶解,试管 B 中滤渣溶解
【拓展延伸】由上述实验方案可知,反应物浓度不同可能会影响反应的现象或结果,请你举出一个此类现象的例子________________________________
__________________________________________________________________
_____。
氧气的浓度越大,可燃物燃烧越剧烈,如硫在空气中燃烧发出微弱的淡蓝色火焰,在氧气中燃烧发出明亮的蓝紫色火焰
河北 化学
小实验到实验探究题
2024中考备考重难专题课件
课件说明
一、课件设计初衷
基于老师在总复习过程中对重难题型有较大的需求,难易结合化学学科的重难点,为此设计重难专题复习课件,助力高效课堂
二、课件亮点
1.对专题知识体系的构建
侧重专题知识体系分解再构建,根据本区域近五年的中考真题提炼知识点,通过知识点讲授方法和技巧,并进一步形成对应体系,再让学生尝试应用已有体系中的方法与技巧去解决问题,在复习过程中构建自己的重难专题知识体系。会对难题进行分解,降低梯度,准确、高效攻克重难专题。
2.过程性分析设置分步动画
对方法讲解、解题步骤设置分步动画,按步骤播放,更清晰有条理。
三、课件使用场景
适用于中考二轮专题复习
1
模型构建
典例精析
2
巩固练习
3
模型构建
观察到什么现象?
试管中液面上升
试管中CO2被消耗,气体减少,液面上升
为什么会产生这样的现象?
怎样证明NaOH与CO2发生了反应?
观察与问题
假设与预测
怎样证明NaOH与CO2发生了反应?
①能发生化学反应
②不能发生化学反应
设计实验
证明反应物减少或消失
科学探究
证明CO2与氢氧化钠溶液反应消耗
CO2消耗
CO2未消耗
证明反应物减少或消失——证明CO2与氢氧化钠溶液发生反应
实验设计:在密闭容器中进行实验,二氧化碳消耗压强减小
将压强变化可视化
实验验证
实验仪器 实验操作 实验现象 实验结论
推动活塞
小气球体积变大
CO2与氢氧化钠溶液能发生反应
该实验能证明CO2与氢氧化钠溶液发生反应吗?原因是什么?
实验反思
不能,可能只是与溶液中水发生了化学反应,需要设计对比实验,对比CO2与氢氧化钠溶液和水溶液反应现象的区别证明
实验验证
实验仪器 实验操作 实验现象 实验结论
推动活塞
小气球体积变大
CO2与氢氧化钠溶液能发生反应
水
推动活塞
小气球体积变大,但没有实验①的体积变化明显
实验②
实验①
设计对比实验时需要控制哪些变量?
水
实验②
实验①
表达与交流
加入氢氧化钠溶液的体积和水的体积
科学探究的思维模型
观察与问题
猜想与假设
设计实验
实验验证
实验反思
发现问题深入探究
①发生反应
②未发生反应
表达与交流
→CO2消耗
→CO2未消耗
单一实验为何不能得到正确结论?
分析原因、设计对比实验
拓展延伸
化学反应的本质特征是什么?
有新物质生成
证明发生化学反应的新思路
证明是否有Na2CO3存在
碳酸钠的化学性质:
①溶于水显碱性
②与酸、碱、盐反应
沉
气
Ba2+
Ca2+
H+
实验验证
试剂选择 实验操作 实验现象 实验结论
(取样→试剂→现象→结论)
取样于试管中,滴加过量稀盐酸或稀硫酸
取样于试管中,滴加Ca(OH)2溶液或Ba(OH)2溶液
取样于试管中,滴加CaCl2溶液或BaCl2溶液
有气泡产生
有白色沉淀产生
有白色沉淀产生
发生化学变化
发生化学变化
发生化学变化
实验②:滴加碱溶液
实验③:滴加盐溶液
实验①:滴加过量稀酸溶液
探究“CO2能否与NaOH溶液发生化学反应”
无明显现象实验探究的一般思路
证明有碳酸钠生成
证明二氧化碳减少或消失
思路2:证明有新物质生成
思路1:证明反应物减少或消失
(利用性质,现象明显)
(对比实验,控制变量)
典例精析
1.(2022逆袭卷)钙尔奇D片是常见的补钙剂,小明不小心将手中的钙尔奇D片掉入装有白醋的碗碟中,观察到有气泡出现,于是他对该现象产生兴趣,进行如下探究。
【查阅资料】①钙尔奇D片的主要成分是CaCO3;白醋的主要成分是
醋酸(CH3COOH),醋酸是一种常见的酸,能与碳酸钙发生化学反应。
②无水硫酸铜遇水变蓝色。
探究一:钙尔奇D片遇白醋后产生的气体是什么?
【提出问题】产生的气体是什么?
【作出猜想】可能是CO2、H2、O2中的一种或两种。
【设计实验】为了验证气体成分,小明同学将一定量的钙尔奇D片加入到白醋中,并收集两试管气体。
(1)小明将燃着的木条伸入其中一支试管中,观察到________________;
(2)小明向另一支试管中加入澄清石灰水,观察到澄清石灰水变浑浊。因此小明推断出该气体为CO2。写出(2)中发生反应的化学方程式__________________________________。
实验过程中,小明发现有同学将钙尔奇D片加入到白醋中产生气泡的速度较快,在老师的帮助下,小明对影响产生气体速率的因素展开探究。
二氧化碳不燃烧也不支持燃烧
燃着的木条熄灭
CO2+Ca(OH)2===CaCO3↓+H2O
探究二:影响产生CO2速率的因素是什么?
老师提醒小明可通过单位时间内产生二氧化碳的浓度判断产生气体的速率。
【作出猜想】猜想1:与反应物间的接触面积有关
猜想2:与反应温度有关
【进行实验】将等质量的钙尔奇D片与等体积、等浓度的白醋充分反应,用数字传感器测得二氧化碳浓度随时间的变化曲线如图所示,实验记录如表所示。
实验编号 反应物形状 温度/℃ 曲线斜率
① 片状 100 1151
② 片状 25 389
③ 粉末状 100 1621
④ 粉末状 25 877
相同温度下不同的形状对比
相同形状下不同的温度对比
实验编号 反应物形状 温度/℃ 曲线斜率
① 片状 100 1151
② 片状 25 389
③ 粉末状 100 1621
④ 粉末状 25 877
【实验结论】(1)若验证猜想2成立,需要选择的对比实验是____________(填实验编号)。
(2)设计实验②④的目的是_________________________________________。
猜想1:与反应物间的接触面积有关
猜想2:与反应温度有关
①②或③④
证明反应物间的接触面积影响产生CO2的速率
温度相同,形状不同
实验编号 反应物形状 温度/℃ 曲线斜率
① 片状 100 1151
② 片状 25 389
③ 粉末状 100 1621
④ 粉末状 25 877
(3)由上述实验可得出的结论是_________________________________________
_______________________________________________________________。
猜想1:与反应物间的接触面积有关
猜想2:与反应温度有关
相同条件下,温度越高,产生CO2的速率越快(或相同条件下,反应物间的接触面积越大,产生CO2的速率越快)
【交流反思】(1)白醋的浓度也可能影响产生气体的速率,请你设计实验方案____________________________________________________________________________________________________________________。
(2)根据图1和图2可知,等质量不同形状的钙尔奇D片与等体积等浓度的白醋反应,产生CO2的量______(选填“相等”或“不相等”)。
变量
室温下,将等质量的片状钙尔奇D片分别与等体积、浓度为5%和25%的白醋反应,用传感器检测产生CO2浓度随时间的变化曲线
相等
温度、形状影响的都是CO2的反应速率,产生CO2的量是由反应物的量决定的
巩固练习
1.2021年10月16日,搭载神舟十三号的长征二号F遥十三运载火箭亮相,航天工作者给它贴了“暖宝宝”。 某社会实践小组的同学们对此产生浓厚的兴趣,并对火箭贴“暖宝宝”的原因、“暖宝宝”中的主要成分及作用展开了一系列探究活动。
【查阅资料】①“暖宝宝”中含有铁粉、氯化钠、水等物质,可持续发热12 小时左右。
②返回器推进剂肼(N2H4) 的熔点为1.4℃,且有剧毒,一旦在低温环境下凝固,会产生很多潜在的问题,甚至发生危险。
【查阅资料】①“暖宝宝”中含有铁粉、氯化钠、水等物质,可持续发热12
小时左右。
②返回器推进剂肼(N2H4) 的熔点为1.4℃,且有剧毒,一旦在低温环境下凝固,会产生很多潜在的问题,甚至发生危险。
探究一:探究贴“暖宝宝”的原因。
【交流讨论】分析资料,火箭贴“暖宝宝”的原因是____________________
_________。
防止返回器推进剂肼遇冷凝固
探究二:验证“暖宝宝”中的主要成分。
【实验准备】剪开“暖宝宝”外包装,取出其中固体。
实验操作 实验现象 实验结论
①取少量固体于试管中,加入足量稀盐酸 ______________________________________________ 固体中含有铁粉
②另取少量固体于试管中,加足量水,充分溶解后过滤_____________________ __________ 产生白色沉淀且白色沉淀不溶解 固体中含有氯化钠
固体逐渐溶解,产生气泡,溶液由无色变为浅绿色
向滤液中加入AgNO3溶液和稀硝酸
氯化银沉淀不溶于酸
【实验总结】步骤①中发生反应的化学方程式为_______________________。
Fe+2HCl===FeCl2+H2↑
探究三:探究成分中氯化钠的作用
【实验2】小王同学设计并进行如图所示的实验,观察一段时间,发现铁粉均生锈,且B中铁粉生锈较快。
【交流讨论】该实验设计的不足之处是__________________________。
【得出结论】经改正后仍然是加氯化钠的铁粉生锈更快,则发热贴中氯化钠的作用是____________________。
A、B 烧杯中的加水量不同
控制变量法应只有一个变量,水的量不同,无法形成对比
加快铁粉的生锈速率
【拓展交流】“暖宝宝”中的铁粉在氧气、水的作用下能发生缓慢氧化,同时放出热量。 由此可见,人们可以利用化学反应放出的能量,请再举一例:
_____________。
煤燃烧取暖
2.同学们了解到碳酸钠与氢氧化钙能发生反应,实验中可观察到溶液变浑浊的现象,但小明同学进行如图所示实验时却未观察到预期现象,于是小组同学对此异常现象进行如下探究。
【知识回顾】 碳酸钠与氢氧化钙溶液反应的化学方程式是____________________________________
Na2CO3+Ca(OH)2===CaCO3↓+2NaOH
【提出问题】 小明实验中未观察到浑浊现象的原因是什么
【猜想与假设】同学们提出了如下猜想:
猜想一:氢氧化钙溶液的浓度偏低;
猜想二:碳酸钠溶液的浓度偏低;
猜想三:生成的碳酸钙沉淀溶解了。
经讨论,同学们认为猜想一不合理,____________________________________。
溶液已经饱和
饱和澄清石灰水是该条件下的最大浓度
【进行实验】小组同学设计如下实验。
编号 1 2 3
实验方案
现象 浑浊 浑浊 不浑浊
【解释与结论】(1)实验1中X的值为_____。
(2)由上述实验过程可知,猜想二___________(填“成立”或“不成立”)。
2
不成立
实验2和实验3的变量是什么?
编号 2 3
实验方案
现象 浑浊 不浑浊
加入的碳酸钠溶液浓度不同
说明碳酸钙沉淀溶解与碳酸钠的浓度有关,再做进一步探究
【继续探究】为进一步验证猜想三,小明将实验1所得的浑浊液过滤,将滤渣分为两等份,分别加入 A、B 两支试管中,向 A 试管中加入2 mL 水,向 B 试管中加入______________________,振荡,观察到________________________
________________,说明猜想三成立
2mL10%的碳酸钠溶液
试管 A中滤渣不溶解,试管 B 中滤渣溶解
【拓展延伸】由上述实验方案可知,反应物浓度不同可能会影响反应的现象或结果,请你举出一个此类现象的例子________________________________
__________________________________________________________________
_____。
氧气的浓度越大,可燃物燃烧越剧烈,如硫在空气中燃烧发出微弱的淡蓝色火焰,在氧气中燃烧发出明亮的蓝紫色火焰
同课章节目录
