4.1 醇和酚 随堂检测(含解析) 2023-2024学年高二下学期化学苏教版(2019)选择性必修3
文档属性
| 名称 | 4.1 醇和酚 随堂检测(含解析) 2023-2024学年高二下学期化学苏教版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 542.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-02 00:00:00 | ||
图片预览



文档简介
4.1 醇和酚 随堂检测 2023-2024学年高二下学期化学苏教版(2019)选择性必修3
一、单选题
1.乙醇分子中不同的化学键如图。下列关于乙醇在不同的反应中断裂化学键的说法错误的是
A.与金属钠反应时,只有键①断裂
B.在Ag催化下与O2反应时,键①、③断裂
C.与CuO反应时,只有键①断裂
D.与浓硫酸共热至170℃时,键②、⑤断裂
2.下列各组物质中能用分液漏斗分离的是
A.苯和苯酚 B.环己烷和水 C.乙醇和水 D.乙醇和四氯化碳
3.下列反应不属于取代反应的是
A.CH3Cl+Cl2CH2Cl2+HCl
B.C2H5OH+HBr→C2H5Br+H2O
C.C2H5Br+NaOH→C2H5OH+NaBr
D.CaCl2+Na2CO3=CaCO3↓+2NaCl
4.下列关于元素及其化合物的性质说法不正确的是
A.将Cl2通入冷的石灰乳可制得漂白粉
B.用FeCl3溶液可检验工业废水中是否含有酚类物质
C.Al与氨水反应可生成H2
D.工业上可用Na2CO3溶液吸收氮氧化物,防止其污染环境
5.新冠疫情期间,医院常用甲基苯酚(化学式为C7H8O)对空气进行消毒,下列说法错误的
A.甲基苯酚由C、H、O三种元素组成
B.一个甲基苯酚分子中含有16个原子
C.甲基苯酚中氧元素的质量分数最小
D.甲基苯酚中氢元素与氧元素的质量比为1:2
6.下列说法中不正确的是
A.甲烷是一种清洁能源 B.乙烯属于烃的衍生物
C.苯是一种有毒液体 D.饮酒过量对身体有害
7.下列化学用语表示正确的是( )
A.乙醇的结构简式:C2H6O
B.甲烷分子的比例模型:
C.乙烯的电子式:
D.氢氧化钠的电离方程式:NaOH=Na++O2-+H+
8.下列实验过程能达到实验目的的是
选项 实验目的 实验过程
A 检验某铁的氧化物含二价铁 将该氧化物溶于浓盐酸,滴入KMnO4溶液,紫色褪去
B 检验乙醇中含有水 用试管取少量的乙醇,加入一小块钠,产生无色气体
C 证明酸性:H2SO3>HClO 在Ca(ClO)2溶液中通入SO2气体,观察是否有沉淀生成
D 证明CO2有氧化性 将点燃的镁条,迅速伸入盛满CO2的集气瓶中,产生大量白烟且瓶内有黑色颗粒产生
A.A B.B C.C D.D
9.下列涉及有机物的性质的说法错误的是
A.乙烯和聚氯乙烯都能发生加成反应
B.乙醇在红热铜丝作用下被氧化成乙醛
C.黄酒中某些微生物使乙醇氧化成乙酸
D.能与苯、纤维素等发生反应,常用浓硫酸作催化剂
10.下列有关苯酚的叙述中正确的是
A.苯酚是羧酸,它能与NaOH溶液反应 B.苯酚比苯容易发生苯环上的取代反应
C.苯中混有的少量苯酚可用乙醇除去 D.苯酚有毒,不能配成洗涤剂和软膏
11.杯芳烃在医药、分子识别、催化剂、模拟酶等领域均有重要的应用。某大学团队合成类杯芳烃结构窄光谱蓝光分子硼氮掺杂杯[4]芳烃的反应如图。下列叙述正确的是
已知:-Ph为苯基。
A.甲能与溴水发生加成反应 B.甲分子在核磁共振氢谱上有4组峰
C.乙分子不能使酸性KMnO4溶液褪色 D.共价键键能大小决定甲、乙的熔点高低
12.已知咖啡酸的结构如图所示。关于咖啡酸的描述正确的是
A.与咖啡酸的物质类别完全相同(含咖啡酸),且苯环上只有3个取代基的同分异构体(包括顺反异构)有18种
B.1mol咖啡酸最多可与3molBr2反应
C.咖啡酸与互为同系物
D.1mol咖啡酸与足量NaHCO3溶液反应产生3mol气体
13.乙醇的分子结构如下图所示,“箭头”表示乙醇发生化学反应时可能断键的位置,下列叙述不正确的是
A.与钠反应时断裂①键 B.与HBr发生取代反应时断裂②键
C.发生分子间脱水时断裂①键或②键 D.发生催化氧化反应时断裂③、④键
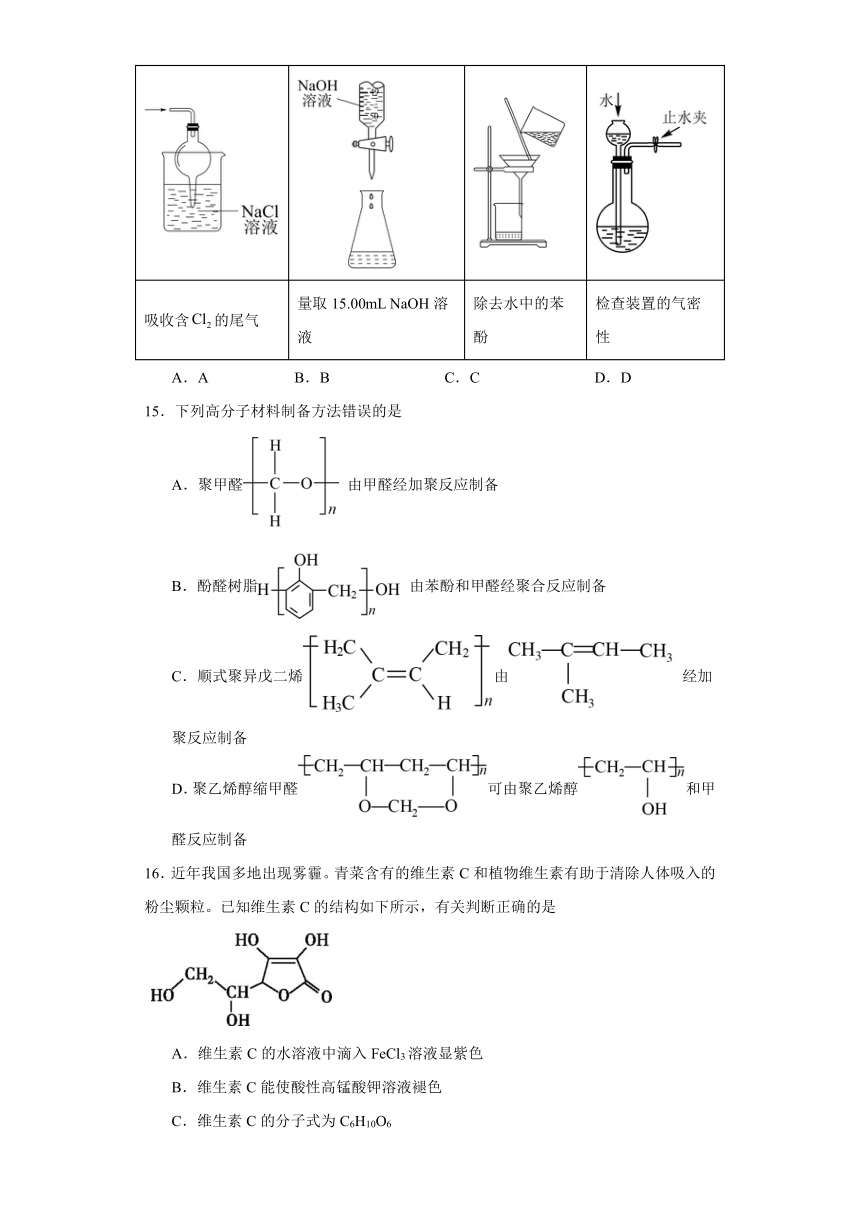
14.下列装置可达到预期实验目的的是
A B C D
吸收含的尾气 量取15.00mL NaOH溶液 除去水中的苯酚 检查装置的气密性
A.A B.B C.C D.D
15.下列高分子材料制备方法错误的是
A.聚甲醛 由甲醛经加聚反应制备
B.酚醛树脂 由苯酚和甲醛经聚合反应制备
C.顺式聚异戊二烯由 经加聚反应制备
D.聚乙烯醇缩甲醛可由聚乙烯醇和甲醛反应制备
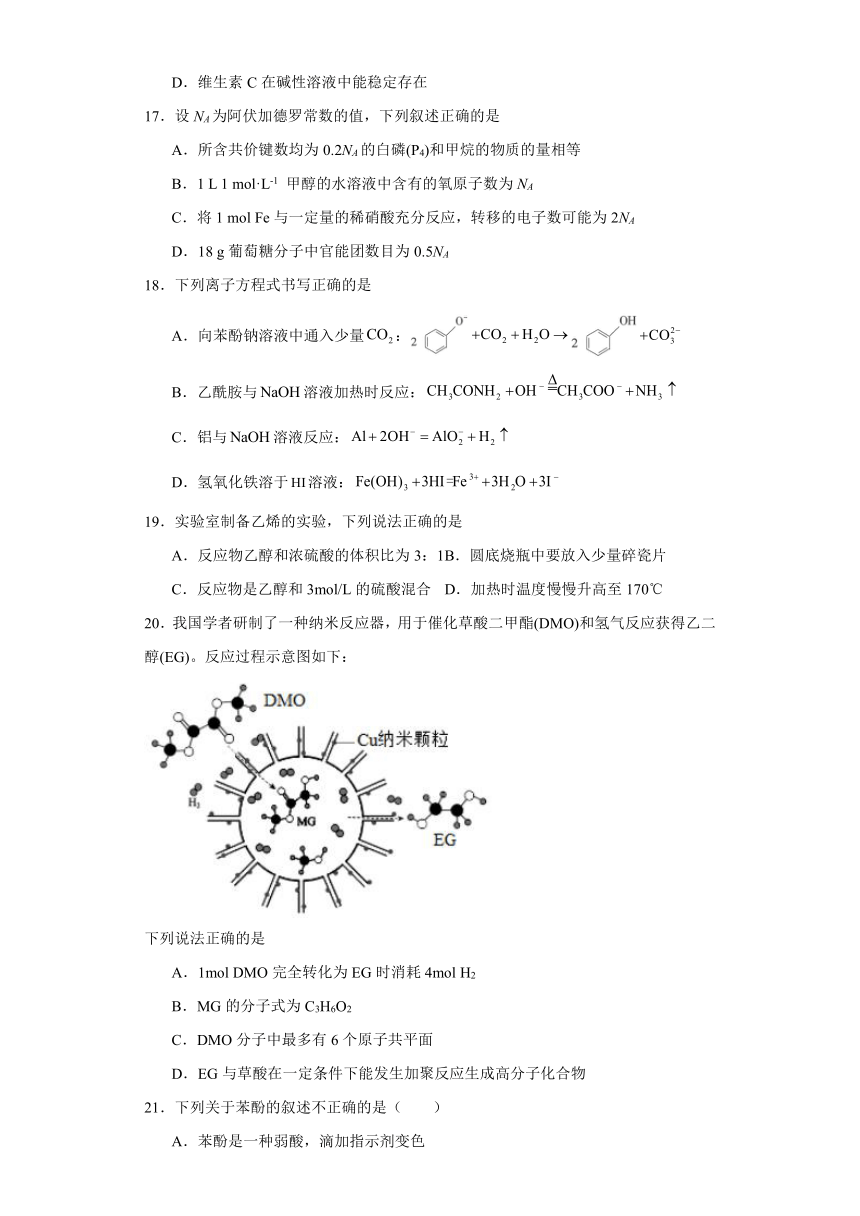
16.近年我国多地出现雾霾。青菜含有的维生素C和植物维生素有助于清除人体吸入的粉尘颗粒。已知维生素C的结构如下所示,有关判断正确的是
A.维生素C的水溶液中滴入FeCl3溶液显紫色
B.维生素C能使酸性高锰酸钾溶液褪色
C.维生素C的分子式为C6H10O6
D.维生素C在碱性溶液中能稳定存在
17.设NA为阿伏加德罗常数的值,下列叙述正确的是
A.所含共价键数均为0.2NA的白磷(P4)和甲烷的物质的量相等
B.1 L 1 mol·L-1 甲醇的水溶液中含有的氧原子数为NA
C.将1 mol Fe与一定量的稀硝酸充分反应,转移的电子数可能为2NA
D.18 g葡萄糖分子中官能团数目为0.5NA
18.下列离子方程式书写正确的是
A.向苯酚钠溶液中通入少量:
B.乙酰胺与溶液加热时反应:
C.铝与溶液反应:
D.氢氧化铁溶于溶液:
19.实验室制备乙烯的实验,下列说法正确的是
A.反应物乙醇和浓硫酸的体积比为3:1 B.圆底烧瓶中要放入少量碎瓷片
C.反应物是乙醇和3mol/L的硫酸混合 D.加热时温度慢慢升高至170℃
20.我国学者研制了一种纳米反应器,用于催化草酸二甲酯(DMO)和氢气反应获得乙二醇(EG)。反应过程示意图如下:
下列说法正确的是
A.1mol DMO完全转化为EG时消耗4mol H2
B.MG的分子式为C3H6O2
C.DMO分子中最多有6个原子共平面
D.EG与草酸在一定条件下能发生加聚反应生成高分子化合物
21.下列关于苯酚的叙述不正确的是( )
A.苯酚是一种弱酸,滴加指示剂变色
B.苯酚在水溶液中能按下式电离:+H2O+H3O+
C.苯酚钠在水溶液中几乎不能存在,会水解生成苯酚,所以苯酚钠溶液显碱性
D.苯酚有腐蚀性,溅在皮肤上可用酒精冲洗
22.某有机物的结构如图所示,关于该有机物下列说法错误的是
A.该物质的熔沸点主要由范德华力决定
B.该分子可以在浓硫酸、加热条件下发生消去反应
C.该分子中最少有12个原子共平面
D.该分子完全水解后所得有机物分子中手性碳原子数目为1个
23.漆酚是我国特产漆的主要成分,漆酚不应具有的化学性质是
A.可以跟FeCl3溶液发生显色反应
B.可以使酸性KMnO4溶液褪色
C.可以跟Na2CO3溶液反应放出CO2
D.可以跟溴水发生取代和加成反应
24.已知是阿伏加德罗常数的值,下列说法正确的的是
A.46g乙醇中插入刚灼烧后的铜丝,液体中碳氢键的数目依然为
B.与混合,光照充分反应,生成分子数小于
C.在中充分燃烧,消耗的分子数为
D.常温下28g铁粉放入浓硝酸中,充分反应,转移电子数为
25.中医的急救三宝分别是安宫牛黄丸、紫雪丹、至宝丹。安宫牛黄丸的主要药材是黄芩,黄芩素能抑制新冠病毒的活性。黄芩素结构如图所示,下列说法正确的是
A.黄芩素的核磁共振氢谱显示有八组峰
B.分子中碳原子均为杂化
C.1mol黄芩素分别与足量的浓溴水和NaOH溶液反应,最多能够消耗和NaOH分别为:2mol、4mol
D.黄岑素与足量氢气加成后,连有氧原子的碳原子中有5个手性碳原子
二、填空题
26.醇发生的反应主要涉及分子中的 键和 键:断裂碳氧键脱掉羟基,发生 或 反应;断裂氢氧键脱掉氢原子,发生 反应或 反应。
27.狄尔斯和阿尔德在研究1,3 丁二烯的性质时发现如下反应:;回答下列问题:
(1)狄尔斯 阿尔德反应属于 (填反应类型)。
(2)下列不能发生狱尔斯 阿尔德反应的有机物是_______(填字母)。
A. B. C. D.
(3)工业上通常以甲醛、乙炔为原料制取1,3 丁二烯,生产流程如下:
①X的结构简式为 ;
②X转化成1,3 丁二烯的化学方程式为 。
28.探究物质的结构有助于对物质的性质进行研究。
(1)① 下列物质中含有羧基的是 (填字母)。
a. b. c.
② 下列物质分子中所有原子处于同一平面的是 (填字母)。
a.苯 b.丙烯 c.甲醇
(2)乙烯使溴水或溴的四氯化碳溶液褪色的化学方程式 ,属于 反应,
(3)灼热的铜丝多次反复地插入乙醇中的现象是: ,属于 反应。
试卷第1页,共3页
参考答案:
1.C
【详解】A.与金属钠反应时,羟基上氢原子变为氢气,只有键①断裂,A正确;
B.在Ag催化下与O2反应时生成乙醛,键①、③断裂,B正确;
C.与CuO反应时生成乙醛,只有键①、③断裂,C错误;
D.与浓硫酸共热至170℃时发生消去反应生成乙烯,键②、⑤断裂,D正确;
答案选C。
2.B
【分析】互不相溶的两种液体可以用分液漏斗分离,以此解题。
【详解】A.苯和苯酚都是常见的有机溶剂,相互混溶,溶液不分层,不能用分液的方法分离,故A错误;
B.环己烷和水不混溶,能用分液漏斗进行分离,故B正确;
C.乙醇和水能互溶,不能用分液漏斗分离,故C错误;
D.乙醇和四氯化碳能互溶,不能用分液漏斗分离,故D错误;
故选B。
3.D
【详解】A.一氯甲烷中H被Cl取代,为取代反应,故A不选;
B.-OH被-Br取代,为取代反应,故B不选;
C.-Br被-OH取代,为取代反应,故C不选;
D.为典型的复分解反应,故D正确;
答案选D。
4.C
【详解】A.氯气和石灰乳反应生成氯化钙、次氯酸钙和水,反应方程式为,漂白粉的有效成分是,故A正确;
B.FeCl3与酚类物质会发生显色反应,使溶液变紫色,所以可用来检验工业废水中是否含有酚类物质,故B正确;
C.铝与氨水不反应,铝只能与强碱反应,生成偏铝酸根,故C错误;
D. Na2CO3溶液可与氮氧化物反应生成硝酸盐和二氧化碳等物质,氮氧化物得以被转化为无害化合物,防止其污染环境,故D正确;
故选C。
5.C
【详解】A.由化学式可知,甲基苯酚由C、H、O三种元素组成,A正确;
B.由化学式可知,一个甲基苯酚分子中含7个碳原子、8个氢原子、1个氧原子共16个原子,B正确;
C.甲基苯酚中C、H、O元素的质量比为(12×7):8:16=21:2:4,故氢元素的质量分数最小,C错误;
D.甲基苯酚中氢元素与氧元素的质量比为8:16=1:2,D正确。
故选C。
6.B
【详解】A.甲烷分子式是CH4,燃烧产生CO2、H2O,燃烧产物无污染,因此甲烷是一种清洁能源,A正确;
B.乙烯分子式是C2H4,仅有C、H两种元素,属于烃,不属于烃的衍生物,B错误;
C.苯是一种无色有刺激性气味的有毒的液态物质,是一种常用的有机溶剂,C正确;
D.酒是一种常用的饮品,若饮酒过量,会对人体的胃、肝脏造成一定的伤害,因此饮酒过量有害身体健康,D正确;
故合理选项是B。
7.C
【详解】A. 乙醇的官能团是羟基,乙醇的结构简式为:CH3CH2OH,故A错误;
B.图中所给是甲烷的球棍模型,不是比例模型,故B错误;
C. 乙烯的电子式:,故C正确;
D. 氢氧化钠是由钠离子和氢氧根离子构成的,电离方程式为:NaOH=Na++OH-,故D错误。
故答案选C。
8.D
【详解】A.高锰酸钾可氧化浓盐酸,紫色褪去,不能检验二价铁,故A错误;
B.乙醇、水均与Na反应生成氢气,有气体生成,不能检验是否有水,故B错误;
C.Ca(ClO)2溶液中通入SO2,发生氧化还原反应生成硫酸钙沉淀,不能比较H2SO3、HClO的酸性强弱,故C错误;
D.点燃时Mg与二氧化碳反应生成氧化镁和C,则产生大量白烟且瓶内有黑色颗粒产生,C元素的化合价降低,可知二氧化碳具有氧化性,故D正确。
答案选D。
9.A
【详解】A.氯乙烯发生加聚反应生成聚氯乙烯,聚氯乙烯分子结构中不含碳碳双键,不能发生加成反应,A错误;
B.加热条件下,铜和氧气反应生成氧化铜,氧化铜能将乙醇氧化乙醛,B正确;
C.黄酒中的乙醇能在某些微生物作用下被氧化生成乙酸,C正确;
D.在浓H2SO4的催化作用下,HNO3能与苯、纤维素等有机物发生取代反应,D正确;
故选A。
10.B
【详解】A.苯酚是酚类,不是羧酸,A错误;
B.苯酚中苯环与羟基直接相连,由于羟基的存在影响苯酚中苯环羟基的邻、对位H原子,使得苯酚中羟基的邻、对位H原子比较活泼,使得苯酚比苯更容易发生苯环上的取代反应,B正确;
C.苯酚在乙醇中微溶,且苯与乙醇也在一定程度上互溶,因此无法用乙醇除去苯中的苯酚,C错误;
D.苯酚是一种有毒的物质,对皮肤、黏膜有强烈的腐蚀作用,但苯酚也是很多医药(如水杨酸、阿司匹林及磺胺药等)、香料、染料的原料,也能配成洗涤剂和软膏,D错误;
故选B。
11.B
【详解】A.甲中不含碳碳双键等能与溴水发生加成反应官能团,A错误;
B.甲分子高度对称,苯环上只有一种氢,甲基相同,羟基相同,亚甲基相同,在核磁共振氢谱上有4组峰,B正确;
C.乙分子苯环上含有甲基,能使酸性KMnO4 溶液褪色,C错误;
D.甲乙为分子晶体,其熔点高低由分子间作用力决定,与化学键键能无关,D错误;
故选B。
12.A
【详解】A.分子可看成是乙烯分子上的一个氢被羧基取代(用X代替),一个氢被苯二酚取代(用Y代替),则顺反异构的位置有:、、三种,而羧基只有一种结构,苯二酚两个羟基有邻、间、对三种位置,上面的氢被取代后加在乙烯上的位置有:邻位两种,间位三种,对位有一种,故同分异构体总共3×6=18种,选项A正确;
B.1mol咖啡酸最多可与3molBr2发生取代反应和1 molBr2发生加成反应共4molBr2反应,选项B错误;
C.分子中只有一个酚羟基,而咖啡酸分子中含有两个酚羟基,不可能互为同系物,选项C错误;
D.咖啡酸中只含有一个羧基能与NaHCO3反应产生气体,1mol咖啡酸与足量NaHCO3溶液反应产生1mol气体,选项D错误。
答案选A。
13.D
【详解】A.乙醇与钠反应生成乙醇钠,断裂①键,A正确;
B.与HBr发生取代反应生成溴乙烷,断裂②键,B正确;
C.乙醇发生分子间脱水生成CH3CH2OCH2CH3,断裂①键或②键,C正确;
D.乙醇发生催化氧化反应生成乙醛,断裂①③键,D错误;
答案选D。
14.D
【详解】A.应用NaOH溶液吸收含的尾气,在NaCl中的溶解度较小,A项不选;
B.量取15.00mL NaOH溶液,应用碱式滴定管,不能用酸式滴定管量取碱液,B项不选;
C.苯酚微溶于水,不能用过滤的方法除去水中的苯酚,C项不选;
D.关闭止水夹,长颈漏斗中的液面下降到一定程度后不再下降,则气密性良好,该装置可达到预期实验目的,D项选;
答案选D。
15.C
【详解】A.聚甲醛的单体是HCHO,聚甲醛 由甲醛经加聚反应制备,故A正确;
B.苯酚和甲醛在酸性条件下发生缩聚反应生成 和水,酚醛树脂由苯酚和甲醛经缩聚反应制备,故B正确;
C.顺式聚异戊二烯由 经加聚反应制备,故C错误;
D.聚乙烯醇和甲醛反应生成聚乙烯醇缩甲醛和水,故D正确;
选C。
16.B
【详解】A.根据维生素C的结构简式可知其不含酚羟基,所以滴入FeCl3溶液不会显紫色,故A错误;
B.维生素C中含有碳碳双键,且部分羟基相连的碳原子上有氢原子,可以被酸性高锰酸钾氧化从而使其褪色,故B正确;
C.根据维生素C的结构简式可知其分子式为C6H8O6,故C错误;
D.维生素C含有酯基,在碱性溶液中会发生酯基的水解,不能稳定存在,故D错误;
综上所述答案为B。
17.C
【详解】A.P4是正四面体结构,分子中含有6个P-P共价键;CH4分子中含有4个C-H键,因此所含共价键数目相同时,白磷(P4)和甲烷的物质的量不相等,A错误;
B.1 L 1 mol·L-1 甲醇的水溶液中,溶质的物质的量是1 mol,由于1个甲醇分子中含有1个O原子,所以1 mol甲醇分子中含有的氧原子数为NA;但在甲醇水溶液中溶解水中也含有O元素,因此该溶液中含有的O原子数大于NA,B错误;
C.Fe是变价金属,与硝酸反应时可能失去2个电子生成Fe2+,也可能失去3个电子生成Fe3+,故将1 mol Fe与一定量的稀硝酸充分反应,转移的电子数可能为2NA,C正确;
D.葡萄糖分子式是C6H12O6,相对分子质量是180,分子中含有5个-OH,1个-CHO,共6个官能团,18 g葡萄糖的物质的量是0.1 mol,则其所含分子中官能团数目为0.6NA,D错误;
故合理选项是C。
18.B
【详解】A.由于苯酚的酸性弱于碳酸,强于碳酸氢根,则向苯酚钠溶液中通入少量,生成苯酚和碳酸氢钠,该反应的离子方程式为,A错误;
B.乙酰胺与溶液加热时发生水解反应生成乙酸钠和,B正确;
C.铝与溶液反应生成和,则该反应的离子方程式为,C错误;
D.氢氧化铁与氢离子反应生成的能与继续反应,离子方程式为,D错误;
故答案为:B。
19.B
【详解】A.实验室制备乙烯时反应物乙醇和浓硫酸的体积比为1:3,故A错误;
B.圆底烧瓶中要放入少量碎瓷片防止暴沸,故B正确;
C.3mol/L的硫酸是稀硫酸,应用18.4mol/L的浓硫酸,故C错误;
D.温度要迅速上升到170℃,防止140℃时生成副产物乙醚,故D错误;
答案选B。
20.A
【详解】A.由图可知,CH3OOC-COOCH3和氢气反应生成乙二醇(C2H6O2)和甲醇,化学方程式为CH3OOC-COOCH3+4H2HOCH2CH2OH+CH3OH,则1mol DMO完全转化为EG时消耗4mol H2,A项正确;
B.由图可知,MG的分子式为C3H6O3,B项错误;
C.由图可知,DMO分子中含有酯基和甲基,分子中最多有8个原子共平面,C项错误;
D.EG为HOCH2CH2OH,分子中含有2个羟基,能和草酸在一定条件下能发生缩聚反应生成高分子化合物,D项错误;
答案选A。
21.A
【详解】A.苯酚的酸性比碳酸还要弱,在溶液中只能微弱电离出氢离子,不能使指示剂变色,故A错误;
B.水分子作用下,苯酚在溶液中微弱电离出氢离子和苯氧根离子,电离方程式为+H2O+H3O+,故B正确;
C.苯酚的酸性比碳酸还要弱,所以苯酚钠在溶液中的水解程度非常大,使溶液显碱性,故C正确;
D.常温下,苯酚微溶于水,易溶于酒精,所以有腐蚀性的苯酚溅在皮肤上应立即用酒精冲洗,故D正确;
故选A。
22.A
【详解】A.该物质分子间除了范德华力外,还有分子间氢键,该物质的熔沸点主要由氢键决定,A错误;
B.该分子含有羟基,与羟基相连碳原子相邻碳原子上有氢原子,可以在浓硫酸、加热条件下发生消去反应,B正确;
C.与苯环碳原子直接相连的6个原子和苯环上的6个碳原子一定共平面,故该分子中至少有12个原子共平面,C正确;
D.手性碳原子为碳原子周围连有四个不同原子团称为手性碳原子,该分子水解肽键断裂,其中只有与氨基直接相连的碳原子为手性碳原子,即手性碳原子数目为1个,D正确;
故答案为A。
23.C
【详解】A.由结构简式可知,漆酚中含有酚羟基,能与氯化铁溶液发生显色反应使溶液变为紫色,故A正确;
B.由结构简式可知,漆酚中含有的酚羟基和烃基中含有的碳碳不饱和键都能与酸性高锰酸钾溶液发生氧化反应使溶液褪色,故B正确;
C.酚的酸性弱于碳酸,所以漆酚中含有的酚羟基不能与碳酸钠溶液反应生成二氧化碳气体,故C错误;
D.由结构简式可知,漆酚中含有酚羟基,能与溴水发生取代反应,烃基中含有的碳碳不饱和键能与溴水发生加成反应,故D正确;
故选C。
24.B
【详解】A.46g乙醇的物质的量是1mol,插入刚灼烧后的铜丝发生催化氧化生成乙醛,因此液体中碳氢键的数目不是,A错误;
B.与混合,光照充分反应,生成多种卤代烃,则生成分子数小于,B正确;
C.的物质的量不能确定,在中充分燃烧,消耗的分子数不一定为,C错误;
D.常温下28g铁粉放入浓硝酸中发生钝化,充分反应,无法计算转移电子数,D错误;
答案选B。
25.A
【详解】A.如图 ,黄芩素分子中含有8种H原子,其核磁共振氢谱显示有八组峰,故A正确;
B.黄芩素分子中含有4种官能团,分别为酚羟基、酮羰基、醚键和碳碳双键,分子中碳原子均为杂化,故B错误;
C.碳碳双键能与溴水发生加成反应,苯环上酚羟基的邻位、对位氢原子可以溴水发生取代反应,1mol黄芩素与足量溴水反应可消耗2molBr2,该有机物分子含有的官能团中,只有酚羟基与氢氧化钠溶液反应,1mol黄芩素最多能够消耗3mol的NaOH,故C错误;
D.如图 ,黄芩参素与足量氢气加成后,连有氧原子的碳原子中有6个手性碳原子,故D错误;
故选:A。
26. 碳氧 氢氧 取代 消去 取代 氧化
【解析】略
27.(1)加成反应
(2)C
(3) ↑+2H2O
【详解】(1)狄尔斯 阿尔德反应是两种物质变为一种物质,该反应属于加成反应;故答案为:加成反应。
(2)、 、都存在相邻的两个碳碳双键,能发生加成反应,而不存在碳碳双键,因此不能发生狱尔斯 阿尔德反应,故答案为:C。
(3)①1mol与2mol氢气发生加成反应,得到,则X的结构简式为;故答案为:。
②根据题中信息X失去两分子水得到1,3 丁二烯,则X转化成1,3 丁二烯的化学方程式为↑+2H2O;故答案为:↑+2H2O。
28. c a CH2=CH2+Br2 CH2BrCH2Br 加成 铜丝红黑交替,有刺激性气味 氧化
【分析】(1)①羧基为-COOH;
②在常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行判断;
(2)乙烯分子结构中含有碳碳双键,易发生加成反应;
(3)乙醇在Cu的催化作用下加热生成乙醛。
【详解】(1)①a. 分子结构中含有酚羟基,故a错误;
b. 分子结构中含有醇羟基,故b错误;
c. 分子结构中含有羧基,故c正确;
故答案为c;
②苯是平面型结构,所有原子都处于同一平面内;丙烯含有甲基,具有甲烷的结构特点,所有原子不可能在同一个平面上;甲醇含有甲基,具有甲烷的结构特点,所有原子不可能在同一个平面上,故答案为:a;
(2)乙烯使溴水或溴的四氯化碳溶液褪色发生的是加成反应,反应化学方程式为CH2=CH2+Br2 CH2BrCH2Br;
(3)钢丝加热时生成黑色的CuO,能被乙醇还原生成Cu,同时生成有刺激性气味的乙醛,则灼热的铜丝多次反复地插入乙醇中的现象是铜丝红黑交替,有刺激性气味,此反应属于氧化反应。
【点睛】分析有机物的原子共面问题时,重点掌握C-C、C=C、C≡C和苯的空间结构特点,有机物中的原子共平面问题可以直接联想甲烷的正四面体结构、乙烯的平面型结构、乙炔的直线型结构和苯的平面型结构,对有机物进行肢解,分部分析,特别注意由于甲烷是四面体结构,有机物分子中只要含有饱和碳原子(包括:-CH3、-CH2-、 、)中的一种,分子中的所有原子就不可能处于同一平面内
一、单选题
1.乙醇分子中不同的化学键如图。下列关于乙醇在不同的反应中断裂化学键的说法错误的是
A.与金属钠反应时,只有键①断裂
B.在Ag催化下与O2反应时,键①、③断裂
C.与CuO反应时,只有键①断裂
D.与浓硫酸共热至170℃时,键②、⑤断裂
2.下列各组物质中能用分液漏斗分离的是
A.苯和苯酚 B.环己烷和水 C.乙醇和水 D.乙醇和四氯化碳
3.下列反应不属于取代反应的是
A.CH3Cl+Cl2CH2Cl2+HCl
B.C2H5OH+HBr→C2H5Br+H2O
C.C2H5Br+NaOH→C2H5OH+NaBr
D.CaCl2+Na2CO3=CaCO3↓+2NaCl
4.下列关于元素及其化合物的性质说法不正确的是
A.将Cl2通入冷的石灰乳可制得漂白粉
B.用FeCl3溶液可检验工业废水中是否含有酚类物质
C.Al与氨水反应可生成H2
D.工业上可用Na2CO3溶液吸收氮氧化物,防止其污染环境
5.新冠疫情期间,医院常用甲基苯酚(化学式为C7H8O)对空气进行消毒,下列说法错误的
A.甲基苯酚由C、H、O三种元素组成
B.一个甲基苯酚分子中含有16个原子
C.甲基苯酚中氧元素的质量分数最小
D.甲基苯酚中氢元素与氧元素的质量比为1:2
6.下列说法中不正确的是
A.甲烷是一种清洁能源 B.乙烯属于烃的衍生物
C.苯是一种有毒液体 D.饮酒过量对身体有害
7.下列化学用语表示正确的是( )
A.乙醇的结构简式:C2H6O
B.甲烷分子的比例模型:
C.乙烯的电子式:
D.氢氧化钠的电离方程式:NaOH=Na++O2-+H+
8.下列实验过程能达到实验目的的是
选项 实验目的 实验过程
A 检验某铁的氧化物含二价铁 将该氧化物溶于浓盐酸,滴入KMnO4溶液,紫色褪去
B 检验乙醇中含有水 用试管取少量的乙醇,加入一小块钠,产生无色气体
C 证明酸性:H2SO3>HClO 在Ca(ClO)2溶液中通入SO2气体,观察是否有沉淀生成
D 证明CO2有氧化性 将点燃的镁条,迅速伸入盛满CO2的集气瓶中,产生大量白烟且瓶内有黑色颗粒产生
A.A B.B C.C D.D
9.下列涉及有机物的性质的说法错误的是
A.乙烯和聚氯乙烯都能发生加成反应
B.乙醇在红热铜丝作用下被氧化成乙醛
C.黄酒中某些微生物使乙醇氧化成乙酸
D.能与苯、纤维素等发生反应,常用浓硫酸作催化剂
10.下列有关苯酚的叙述中正确的是
A.苯酚是羧酸,它能与NaOH溶液反应 B.苯酚比苯容易发生苯环上的取代反应
C.苯中混有的少量苯酚可用乙醇除去 D.苯酚有毒,不能配成洗涤剂和软膏
11.杯芳烃在医药、分子识别、催化剂、模拟酶等领域均有重要的应用。某大学团队合成类杯芳烃结构窄光谱蓝光分子硼氮掺杂杯[4]芳烃的反应如图。下列叙述正确的是
已知:-Ph为苯基。
A.甲能与溴水发生加成反应 B.甲分子在核磁共振氢谱上有4组峰
C.乙分子不能使酸性KMnO4溶液褪色 D.共价键键能大小决定甲、乙的熔点高低
12.已知咖啡酸的结构如图所示。关于咖啡酸的描述正确的是
A.与咖啡酸的物质类别完全相同(含咖啡酸),且苯环上只有3个取代基的同分异构体(包括顺反异构)有18种
B.1mol咖啡酸最多可与3molBr2反应
C.咖啡酸与互为同系物
D.1mol咖啡酸与足量NaHCO3溶液反应产生3mol气体
13.乙醇的分子结构如下图所示,“箭头”表示乙醇发生化学反应时可能断键的位置,下列叙述不正确的是
A.与钠反应时断裂①键 B.与HBr发生取代反应时断裂②键
C.发生分子间脱水时断裂①键或②键 D.发生催化氧化反应时断裂③、④键
14.下列装置可达到预期实验目的的是
A B C D
吸收含的尾气 量取15.00mL NaOH溶液 除去水中的苯酚 检查装置的气密性
A.A B.B C.C D.D
15.下列高分子材料制备方法错误的是
A.聚甲醛 由甲醛经加聚反应制备
B.酚醛树脂 由苯酚和甲醛经聚合反应制备
C.顺式聚异戊二烯由 经加聚反应制备
D.聚乙烯醇缩甲醛可由聚乙烯醇和甲醛反应制备
16.近年我国多地出现雾霾。青菜含有的维生素C和植物维生素有助于清除人体吸入的粉尘颗粒。已知维生素C的结构如下所示,有关判断正确的是
A.维生素C的水溶液中滴入FeCl3溶液显紫色
B.维生素C能使酸性高锰酸钾溶液褪色
C.维生素C的分子式为C6H10O6
D.维生素C在碱性溶液中能稳定存在
17.设NA为阿伏加德罗常数的值,下列叙述正确的是
A.所含共价键数均为0.2NA的白磷(P4)和甲烷的物质的量相等
B.1 L 1 mol·L-1 甲醇的水溶液中含有的氧原子数为NA
C.将1 mol Fe与一定量的稀硝酸充分反应,转移的电子数可能为2NA
D.18 g葡萄糖分子中官能团数目为0.5NA
18.下列离子方程式书写正确的是
A.向苯酚钠溶液中通入少量:
B.乙酰胺与溶液加热时反应:
C.铝与溶液反应:
D.氢氧化铁溶于溶液:
19.实验室制备乙烯的实验,下列说法正确的是
A.反应物乙醇和浓硫酸的体积比为3:1 B.圆底烧瓶中要放入少量碎瓷片
C.反应物是乙醇和3mol/L的硫酸混合 D.加热时温度慢慢升高至170℃
20.我国学者研制了一种纳米反应器,用于催化草酸二甲酯(DMO)和氢气反应获得乙二醇(EG)。反应过程示意图如下:
下列说法正确的是
A.1mol DMO完全转化为EG时消耗4mol H2
B.MG的分子式为C3H6O2
C.DMO分子中最多有6个原子共平面
D.EG与草酸在一定条件下能发生加聚反应生成高分子化合物
21.下列关于苯酚的叙述不正确的是( )
A.苯酚是一种弱酸,滴加指示剂变色
B.苯酚在水溶液中能按下式电离:+H2O+H3O+
C.苯酚钠在水溶液中几乎不能存在,会水解生成苯酚,所以苯酚钠溶液显碱性
D.苯酚有腐蚀性,溅在皮肤上可用酒精冲洗
22.某有机物的结构如图所示,关于该有机物下列说法错误的是
A.该物质的熔沸点主要由范德华力决定
B.该分子可以在浓硫酸、加热条件下发生消去反应
C.该分子中最少有12个原子共平面
D.该分子完全水解后所得有机物分子中手性碳原子数目为1个
23.漆酚是我国特产漆的主要成分,漆酚不应具有的化学性质是
A.可以跟FeCl3溶液发生显色反应
B.可以使酸性KMnO4溶液褪色
C.可以跟Na2CO3溶液反应放出CO2
D.可以跟溴水发生取代和加成反应
24.已知是阿伏加德罗常数的值,下列说法正确的的是
A.46g乙醇中插入刚灼烧后的铜丝,液体中碳氢键的数目依然为
B.与混合,光照充分反应,生成分子数小于
C.在中充分燃烧,消耗的分子数为
D.常温下28g铁粉放入浓硝酸中,充分反应,转移电子数为
25.中医的急救三宝分别是安宫牛黄丸、紫雪丹、至宝丹。安宫牛黄丸的主要药材是黄芩,黄芩素能抑制新冠病毒的活性。黄芩素结构如图所示,下列说法正确的是
A.黄芩素的核磁共振氢谱显示有八组峰
B.分子中碳原子均为杂化
C.1mol黄芩素分别与足量的浓溴水和NaOH溶液反应,最多能够消耗和NaOH分别为:2mol、4mol
D.黄岑素与足量氢气加成后,连有氧原子的碳原子中有5个手性碳原子
二、填空题
26.醇发生的反应主要涉及分子中的 键和 键:断裂碳氧键脱掉羟基,发生 或 反应;断裂氢氧键脱掉氢原子,发生 反应或 反应。
27.狄尔斯和阿尔德在研究1,3 丁二烯的性质时发现如下反应:;回答下列问题:
(1)狄尔斯 阿尔德反应属于 (填反应类型)。
(2)下列不能发生狱尔斯 阿尔德反应的有机物是_______(填字母)。
A. B. C. D.
(3)工业上通常以甲醛、乙炔为原料制取1,3 丁二烯,生产流程如下:
①X的结构简式为 ;
②X转化成1,3 丁二烯的化学方程式为 。
28.探究物质的结构有助于对物质的性质进行研究。
(1)① 下列物质中含有羧基的是 (填字母)。
a. b. c.
② 下列物质分子中所有原子处于同一平面的是 (填字母)。
a.苯 b.丙烯 c.甲醇
(2)乙烯使溴水或溴的四氯化碳溶液褪色的化学方程式 ,属于 反应,
(3)灼热的铜丝多次反复地插入乙醇中的现象是: ,属于 反应。
试卷第1页,共3页
参考答案:
1.C
【详解】A.与金属钠反应时,羟基上氢原子变为氢气,只有键①断裂,A正确;
B.在Ag催化下与O2反应时生成乙醛,键①、③断裂,B正确;
C.与CuO反应时生成乙醛,只有键①、③断裂,C错误;
D.与浓硫酸共热至170℃时发生消去反应生成乙烯,键②、⑤断裂,D正确;
答案选C。
2.B
【分析】互不相溶的两种液体可以用分液漏斗分离,以此解题。
【详解】A.苯和苯酚都是常见的有机溶剂,相互混溶,溶液不分层,不能用分液的方法分离,故A错误;
B.环己烷和水不混溶,能用分液漏斗进行分离,故B正确;
C.乙醇和水能互溶,不能用分液漏斗分离,故C错误;
D.乙醇和四氯化碳能互溶,不能用分液漏斗分离,故D错误;
故选B。
3.D
【详解】A.一氯甲烷中H被Cl取代,为取代反应,故A不选;
B.-OH被-Br取代,为取代反应,故B不选;
C.-Br被-OH取代,为取代反应,故C不选;
D.为典型的复分解反应,故D正确;
答案选D。
4.C
【详解】A.氯气和石灰乳反应生成氯化钙、次氯酸钙和水,反应方程式为,漂白粉的有效成分是,故A正确;
B.FeCl3与酚类物质会发生显色反应,使溶液变紫色,所以可用来检验工业废水中是否含有酚类物质,故B正确;
C.铝与氨水不反应,铝只能与强碱反应,生成偏铝酸根,故C错误;
D. Na2CO3溶液可与氮氧化物反应生成硝酸盐和二氧化碳等物质,氮氧化物得以被转化为无害化合物,防止其污染环境,故D正确;
故选C。
5.C
【详解】A.由化学式可知,甲基苯酚由C、H、O三种元素组成,A正确;
B.由化学式可知,一个甲基苯酚分子中含7个碳原子、8个氢原子、1个氧原子共16个原子,B正确;
C.甲基苯酚中C、H、O元素的质量比为(12×7):8:16=21:2:4,故氢元素的质量分数最小,C错误;
D.甲基苯酚中氢元素与氧元素的质量比为8:16=1:2,D正确。
故选C。
6.B
【详解】A.甲烷分子式是CH4,燃烧产生CO2、H2O,燃烧产物无污染,因此甲烷是一种清洁能源,A正确;
B.乙烯分子式是C2H4,仅有C、H两种元素,属于烃,不属于烃的衍生物,B错误;
C.苯是一种无色有刺激性气味的有毒的液态物质,是一种常用的有机溶剂,C正确;
D.酒是一种常用的饮品,若饮酒过量,会对人体的胃、肝脏造成一定的伤害,因此饮酒过量有害身体健康,D正确;
故合理选项是B。
7.C
【详解】A. 乙醇的官能团是羟基,乙醇的结构简式为:CH3CH2OH,故A错误;
B.图中所给是甲烷的球棍模型,不是比例模型,故B错误;
C. 乙烯的电子式:,故C正确;
D. 氢氧化钠是由钠离子和氢氧根离子构成的,电离方程式为:NaOH=Na++OH-,故D错误。
故答案选C。
8.D
【详解】A.高锰酸钾可氧化浓盐酸,紫色褪去,不能检验二价铁,故A错误;
B.乙醇、水均与Na反应生成氢气,有气体生成,不能检验是否有水,故B错误;
C.Ca(ClO)2溶液中通入SO2,发生氧化还原反应生成硫酸钙沉淀,不能比较H2SO3、HClO的酸性强弱,故C错误;
D.点燃时Mg与二氧化碳反应生成氧化镁和C,则产生大量白烟且瓶内有黑色颗粒产生,C元素的化合价降低,可知二氧化碳具有氧化性,故D正确。
答案选D。
9.A
【详解】A.氯乙烯发生加聚反应生成聚氯乙烯,聚氯乙烯分子结构中不含碳碳双键,不能发生加成反应,A错误;
B.加热条件下,铜和氧气反应生成氧化铜,氧化铜能将乙醇氧化乙醛,B正确;
C.黄酒中的乙醇能在某些微生物作用下被氧化生成乙酸,C正确;
D.在浓H2SO4的催化作用下,HNO3能与苯、纤维素等有机物发生取代反应,D正确;
故选A。
10.B
【详解】A.苯酚是酚类,不是羧酸,A错误;
B.苯酚中苯环与羟基直接相连,由于羟基的存在影响苯酚中苯环羟基的邻、对位H原子,使得苯酚中羟基的邻、对位H原子比较活泼,使得苯酚比苯更容易发生苯环上的取代反应,B正确;
C.苯酚在乙醇中微溶,且苯与乙醇也在一定程度上互溶,因此无法用乙醇除去苯中的苯酚,C错误;
D.苯酚是一种有毒的物质,对皮肤、黏膜有强烈的腐蚀作用,但苯酚也是很多医药(如水杨酸、阿司匹林及磺胺药等)、香料、染料的原料,也能配成洗涤剂和软膏,D错误;
故选B。
11.B
【详解】A.甲中不含碳碳双键等能与溴水发生加成反应官能团,A错误;
B.甲分子高度对称,苯环上只有一种氢,甲基相同,羟基相同,亚甲基相同,在核磁共振氢谱上有4组峰,B正确;
C.乙分子苯环上含有甲基,能使酸性KMnO4 溶液褪色,C错误;
D.甲乙为分子晶体,其熔点高低由分子间作用力决定,与化学键键能无关,D错误;
故选B。
12.A
【详解】A.分子可看成是乙烯分子上的一个氢被羧基取代(用X代替),一个氢被苯二酚取代(用Y代替),则顺反异构的位置有:、、三种,而羧基只有一种结构,苯二酚两个羟基有邻、间、对三种位置,上面的氢被取代后加在乙烯上的位置有:邻位两种,间位三种,对位有一种,故同分异构体总共3×6=18种,选项A正确;
B.1mol咖啡酸最多可与3molBr2发生取代反应和1 molBr2发生加成反应共4molBr2反应,选项B错误;
C.分子中只有一个酚羟基,而咖啡酸分子中含有两个酚羟基,不可能互为同系物,选项C错误;
D.咖啡酸中只含有一个羧基能与NaHCO3反应产生气体,1mol咖啡酸与足量NaHCO3溶液反应产生1mol气体,选项D错误。
答案选A。
13.D
【详解】A.乙醇与钠反应生成乙醇钠,断裂①键,A正确;
B.与HBr发生取代反应生成溴乙烷,断裂②键,B正确;
C.乙醇发生分子间脱水生成CH3CH2OCH2CH3,断裂①键或②键,C正确;
D.乙醇发生催化氧化反应生成乙醛,断裂①③键,D错误;
答案选D。
14.D
【详解】A.应用NaOH溶液吸收含的尾气,在NaCl中的溶解度较小,A项不选;
B.量取15.00mL NaOH溶液,应用碱式滴定管,不能用酸式滴定管量取碱液,B项不选;
C.苯酚微溶于水,不能用过滤的方法除去水中的苯酚,C项不选;
D.关闭止水夹,长颈漏斗中的液面下降到一定程度后不再下降,则气密性良好,该装置可达到预期实验目的,D项选;
答案选D。
15.C
【详解】A.聚甲醛的单体是HCHO,聚甲醛 由甲醛经加聚反应制备,故A正确;
B.苯酚和甲醛在酸性条件下发生缩聚反应生成 和水,酚醛树脂由苯酚和甲醛经缩聚反应制备,故B正确;
C.顺式聚异戊二烯由 经加聚反应制备,故C错误;
D.聚乙烯醇和甲醛反应生成聚乙烯醇缩甲醛和水,故D正确;
选C。
16.B
【详解】A.根据维生素C的结构简式可知其不含酚羟基,所以滴入FeCl3溶液不会显紫色,故A错误;
B.维生素C中含有碳碳双键,且部分羟基相连的碳原子上有氢原子,可以被酸性高锰酸钾氧化从而使其褪色,故B正确;
C.根据维生素C的结构简式可知其分子式为C6H8O6,故C错误;
D.维生素C含有酯基,在碱性溶液中会发生酯基的水解,不能稳定存在,故D错误;
综上所述答案为B。
17.C
【详解】A.P4是正四面体结构,分子中含有6个P-P共价键;CH4分子中含有4个C-H键,因此所含共价键数目相同时,白磷(P4)和甲烷的物质的量不相等,A错误;
B.1 L 1 mol·L-1 甲醇的水溶液中,溶质的物质的量是1 mol,由于1个甲醇分子中含有1个O原子,所以1 mol甲醇分子中含有的氧原子数为NA;但在甲醇水溶液中溶解水中也含有O元素,因此该溶液中含有的O原子数大于NA,B错误;
C.Fe是变价金属,与硝酸反应时可能失去2个电子生成Fe2+,也可能失去3个电子生成Fe3+,故将1 mol Fe与一定量的稀硝酸充分反应,转移的电子数可能为2NA,C正确;
D.葡萄糖分子式是C6H12O6,相对分子质量是180,分子中含有5个-OH,1个-CHO,共6个官能团,18 g葡萄糖的物质的量是0.1 mol,则其所含分子中官能团数目为0.6NA,D错误;
故合理选项是C。
18.B
【详解】A.由于苯酚的酸性弱于碳酸,强于碳酸氢根,则向苯酚钠溶液中通入少量,生成苯酚和碳酸氢钠,该反应的离子方程式为,A错误;
B.乙酰胺与溶液加热时发生水解反应生成乙酸钠和,B正确;
C.铝与溶液反应生成和,则该反应的离子方程式为,C错误;
D.氢氧化铁与氢离子反应生成的能与继续反应,离子方程式为,D错误;
故答案为:B。
19.B
【详解】A.实验室制备乙烯时反应物乙醇和浓硫酸的体积比为1:3,故A错误;
B.圆底烧瓶中要放入少量碎瓷片防止暴沸,故B正确;
C.3mol/L的硫酸是稀硫酸,应用18.4mol/L的浓硫酸,故C错误;
D.温度要迅速上升到170℃,防止140℃时生成副产物乙醚,故D错误;
答案选B。
20.A
【详解】A.由图可知,CH3OOC-COOCH3和氢气反应生成乙二醇(C2H6O2)和甲醇,化学方程式为CH3OOC-COOCH3+4H2HOCH2CH2OH+CH3OH,则1mol DMO完全转化为EG时消耗4mol H2,A项正确;
B.由图可知,MG的分子式为C3H6O3,B项错误;
C.由图可知,DMO分子中含有酯基和甲基,分子中最多有8个原子共平面,C项错误;
D.EG为HOCH2CH2OH,分子中含有2个羟基,能和草酸在一定条件下能发生缩聚反应生成高分子化合物,D项错误;
答案选A。
21.A
【详解】A.苯酚的酸性比碳酸还要弱,在溶液中只能微弱电离出氢离子,不能使指示剂变色,故A错误;
B.水分子作用下,苯酚在溶液中微弱电离出氢离子和苯氧根离子,电离方程式为+H2O+H3O+,故B正确;
C.苯酚的酸性比碳酸还要弱,所以苯酚钠在溶液中的水解程度非常大,使溶液显碱性,故C正确;
D.常温下,苯酚微溶于水,易溶于酒精,所以有腐蚀性的苯酚溅在皮肤上应立即用酒精冲洗,故D正确;
故选A。
22.A
【详解】A.该物质分子间除了范德华力外,还有分子间氢键,该物质的熔沸点主要由氢键决定,A错误;
B.该分子含有羟基,与羟基相连碳原子相邻碳原子上有氢原子,可以在浓硫酸、加热条件下发生消去反应,B正确;
C.与苯环碳原子直接相连的6个原子和苯环上的6个碳原子一定共平面,故该分子中至少有12个原子共平面,C正确;
D.手性碳原子为碳原子周围连有四个不同原子团称为手性碳原子,该分子水解肽键断裂,其中只有与氨基直接相连的碳原子为手性碳原子,即手性碳原子数目为1个,D正确;
故答案为A。
23.C
【详解】A.由结构简式可知,漆酚中含有酚羟基,能与氯化铁溶液发生显色反应使溶液变为紫色,故A正确;
B.由结构简式可知,漆酚中含有的酚羟基和烃基中含有的碳碳不饱和键都能与酸性高锰酸钾溶液发生氧化反应使溶液褪色,故B正确;
C.酚的酸性弱于碳酸,所以漆酚中含有的酚羟基不能与碳酸钠溶液反应生成二氧化碳气体,故C错误;
D.由结构简式可知,漆酚中含有酚羟基,能与溴水发生取代反应,烃基中含有的碳碳不饱和键能与溴水发生加成反应,故D正确;
故选C。
24.B
【详解】A.46g乙醇的物质的量是1mol,插入刚灼烧后的铜丝发生催化氧化生成乙醛,因此液体中碳氢键的数目不是,A错误;
B.与混合,光照充分反应,生成多种卤代烃,则生成分子数小于,B正确;
C.的物质的量不能确定,在中充分燃烧,消耗的分子数不一定为,C错误;
D.常温下28g铁粉放入浓硝酸中发生钝化,充分反应,无法计算转移电子数,D错误;
答案选B。
25.A
【详解】A.如图 ,黄芩素分子中含有8种H原子,其核磁共振氢谱显示有八组峰,故A正确;
B.黄芩素分子中含有4种官能团,分别为酚羟基、酮羰基、醚键和碳碳双键,分子中碳原子均为杂化,故B错误;
C.碳碳双键能与溴水发生加成反应,苯环上酚羟基的邻位、对位氢原子可以溴水发生取代反应,1mol黄芩素与足量溴水反应可消耗2molBr2,该有机物分子含有的官能团中,只有酚羟基与氢氧化钠溶液反应,1mol黄芩素最多能够消耗3mol的NaOH,故C错误;
D.如图 ,黄芩参素与足量氢气加成后,连有氧原子的碳原子中有6个手性碳原子,故D错误;
故选:A。
26. 碳氧 氢氧 取代 消去 取代 氧化
【解析】略
27.(1)加成反应
(2)C
(3) ↑+2H2O
【详解】(1)狄尔斯 阿尔德反应是两种物质变为一种物质,该反应属于加成反应;故答案为:加成反应。
(2)、 、都存在相邻的两个碳碳双键,能发生加成反应,而不存在碳碳双键,因此不能发生狱尔斯 阿尔德反应,故答案为:C。
(3)①1mol与2mol氢气发生加成反应,得到,则X的结构简式为;故答案为:。
②根据题中信息X失去两分子水得到1,3 丁二烯,则X转化成1,3 丁二烯的化学方程式为↑+2H2O;故答案为:↑+2H2O。
28. c a CH2=CH2+Br2 CH2BrCH2Br 加成 铜丝红黑交替,有刺激性气味 氧化
【分析】(1)①羧基为-COOH;
②在常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行判断;
(2)乙烯分子结构中含有碳碳双键,易发生加成反应;
(3)乙醇在Cu的催化作用下加热生成乙醛。
【详解】(1)①a. 分子结构中含有酚羟基,故a错误;
b. 分子结构中含有醇羟基,故b错误;
c. 分子结构中含有羧基,故c正确;
故答案为c;
②苯是平面型结构,所有原子都处于同一平面内;丙烯含有甲基,具有甲烷的结构特点,所有原子不可能在同一个平面上;甲醇含有甲基,具有甲烷的结构特点,所有原子不可能在同一个平面上,故答案为:a;
(2)乙烯使溴水或溴的四氯化碳溶液褪色发生的是加成反应,反应化学方程式为CH2=CH2+Br2 CH2BrCH2Br;
(3)钢丝加热时生成黑色的CuO,能被乙醇还原生成Cu,同时生成有刺激性气味的乙醛,则灼热的铜丝多次反复地插入乙醇中的现象是铜丝红黑交替,有刺激性气味,此反应属于氧化反应。
【点睛】分析有机物的原子共面问题时,重点掌握C-C、C=C、C≡C和苯的空间结构特点,有机物中的原子共平面问题可以直接联想甲烷的正四面体结构、乙烯的平面型结构、乙炔的直线型结构和苯的平面型结构,对有机物进行肢解,分部分析,特别注意由于甲烷是四面体结构,有机物分子中只要含有饱和碳原子(包括:-CH3、-CH2-、 、)中的一种,分子中的所有原子就不可能处于同一平面内
