广东省深圳中学2023-2024学年高二上学期期末考试化学试题
文档属性
| 名称 | 广东省深圳中学2023-2024学年高二上学期期末考试化学试题 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-03 00:00:00 | ||
图片预览




文档简介
试卷类型:A
深圳中学2023-2024学年度第一学期期末考试试题
年级:高二 科目:化学
考试时长:75分钟 卷面总分:100分
注意事项:
1.答案写在答题卡指定的位置上,写在试题卷上无效。选择题作答必须用2B铅笔,修改时用橡皮擦干净。
可能用到的相对原子质量:H-1 C-12 O-16 N-14 S-32 Ni-59 Zn-65
一、单项选择题(每小题只有一个答案符合题意,共16小题,1-10小题每小题2分,11-16小题每小题4分,共44分)
1.自由能的变化△G=△H-T△S是判断反应进行方向的复合判据。△G<0时,反应能自发进行。已知工业上常利用和来制备水煤气,化学方程式为,△H>0 则下列说法正确的是
A.△S>0,低温下该反应能自发进行 B.△S<0,高温下该反应能自发进行
C.△S<0,低温下该反应能自发进行 D.△S>0,高温下该反应能自发进行
2.下列热化学方程式及其描述正确的是
A. (燃烧热)
B. (中和热)
C. (燃烧热)
D.C(金刚石、s)=C(石墨、s) (反应热)(已知石墨比金刚石稳定)
3.是一种具有高催化活性的新型光催化剂,下列相关说法错误的是
A.Zn处于元素周期表中的ds区 B.基态Ge存在7种不同能量的电子
C.基态O原子中含有3对成对电子 D.电负性大小顺序O>Ge>Zn
4.下列离子的VSEPR模型与其空间结构一致的是
A. B. C. D.
5.下列化学用语不正确的是
A.次氯酸的电子式: B.正丁烷的球棍模型:
C.乙烯的结构简式: D.中碳的杂化类型:
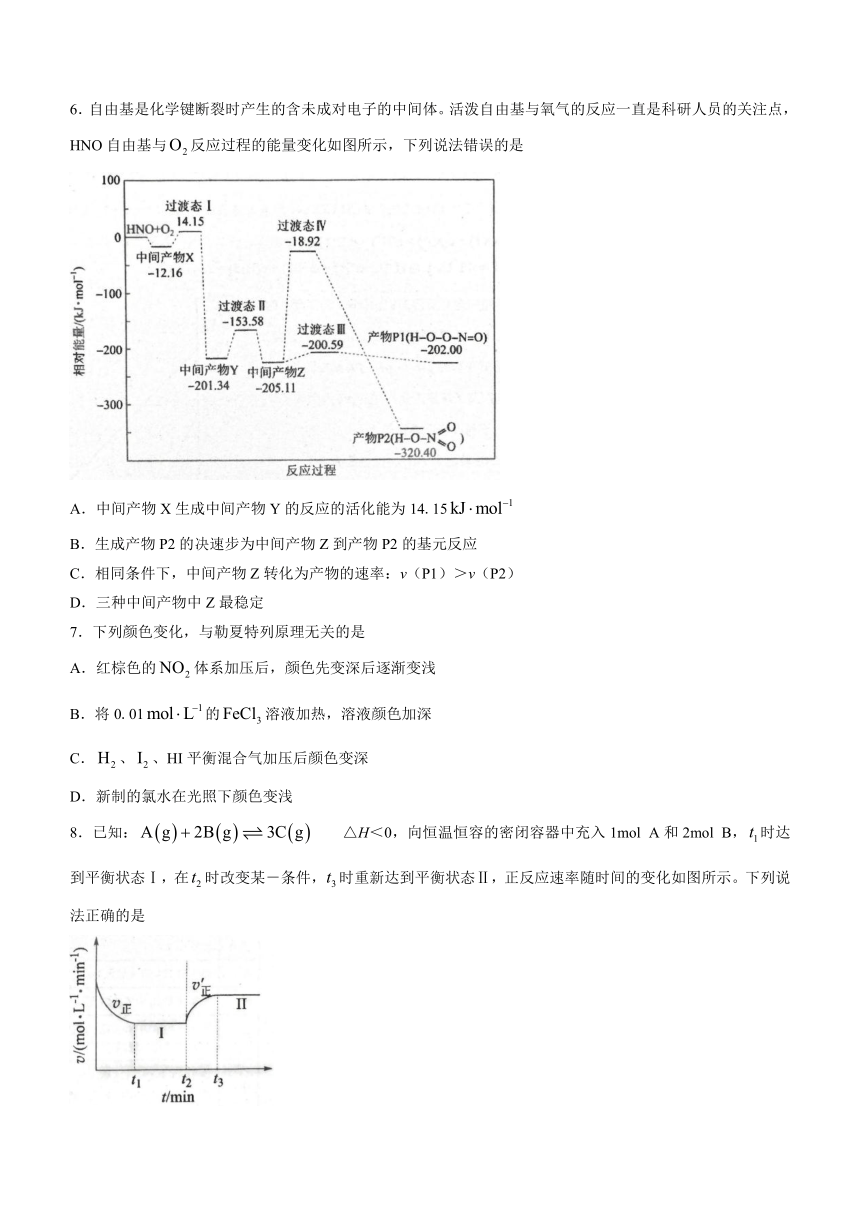
6.自由基是化学键断裂时产生的含未成对电子的中间体。活泼自由基与氧气的反应一直是科研人员的关注点,HNO自由基与反应过程的能量变化如图所示,下列说法错误的是
A.中间产物X生成中间产物Y的反应的活化能为14.15
B.生成产物P2的决速步为中间产物Z到产物P2的基元反应
C.相同条件下,中间产物Z转化为产物的速率:v(P1)>v(P2)
D.三种中间产物中Z最稳定
7.下列颜色变化,与勒夏特列原理无关的是
A.红棕色的体系加压后,颜色先变深后逐渐变浅
B.将0.01的溶液加热,溶液颜色加深
C.、、HI平衡混合气加压后颜色变深
D.新制的氯水在光照下颜色变浅
8.已知: △H<0,向恒温恒容的密闭容器中充入1mol A和2mol B,时达到平衡状态Ⅰ,在时改变某-条件,时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
A.时刻改变的条件可能是升高温度B.~时,平衡向逆反应方向移动
C.平衡时A的体积分数φ(Ⅱ)>φ(Ⅰ)D.平衡常数K(Ⅰ)>K(Ⅱ)
9.常温下,下列有关电解质溶液的说法正确的是
A.相同浓度的HCOONa和NaF溶液,前者的pH较大,则
B.已知FeS溶于稀硫酸,而CuS不溶于稀硫酸,则
C.相同浓度的和溶液等体积混合后pH约为4.7,则溶液中
D.在1mol/L 溶液中,
10.秦俑彩绘中含有难溶的铅白()和黄色的。常温下,和在水溶液中各自分别达到沉淀溶解平衡时pM与pR的关系如图所示,其中pM为阳离子浓度的负对数,pR为阴离子浓度的负对数。下列说法正确的是
A.转化为的反应趋势很大 B.z点溶液对于来说尚未饱和
C.的数量级为 D.完全沉淀废液中的,的效果不如
11.化合物可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族,且Y的原子半径小于M。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为,X与M同周期,E在地壳中含量最多。下列说法正确的是
A.元素电负性:E>Y>Z B.简单氢化物沸点:M>Y>E
C.第一电离能:X>E>Y D.和的空间结构均为三角锥形
12.根据下列实验现象所得出的实验结论正确的是:
选项 实验现象 实验结论
A 将少量HA溶液加入溶液,未产生气泡。 酸性:HA<
B 臭氧在中的溶解度高于在水中的溶解度 为非极性分子
C 向含有酚酞的溶液中加入少量固体,溶液红色变浅。 溶液中存在水解平衡
D 向10mL 溶液中滴加5mL等浓度的KI溶液,再滴加KSCN溶液,溶液最终变为血红色。 溶液与KI溶液的反应为可逆反应
13.多位化学家用简单的偶联反应合成了右图这个有趣的“纳米小人”分子。关于该小人的结构,以下说法错误的是
A.小人眼睛的两个O原子,杂化方式为
B.构成帽子的6个C原子,不可能同时处于同一个平面上
C.与足量氢气发生加成反应后,人“腰部”的两个C原子杂化方式会发生改变
D.该分子所有碳原子都不是手性碳原子
14.碱性锌—铁液流电池(如图)具有电压高、成本低的优点。
该电池的总反应为:。
下列叙述正确的是
A.放电时,右侧贮液器中溶液浓度减小
B.充电时,M电极与电源负极相连
C.充电时,M极电极反应式为
D.放电时,电路中转移2mol电子时,负极区电解质溶液增加65g
15.合成氨反应: △H<0。图1表示在2L恒容密闭容器中的物质的量浓度随时间的变化曲线。图2表示在其他条件不变时,平衡时的体积分数随起始时的物质的量的变化曲线。下列说法正确的是
图1 图2
A.图1中,其他条件不变,第11min改用更为高效的催化剂,则-t的变化趋势为曲线b所示
B.图1中,其他条件不变,第11min迅速压缩容器体积为1L,则-t的变化趋势为曲线a所示
C.图2中,反应物的平衡转化率:b>a>c
D.图2中,、表示温度,则
16.25℃时,用0.2mol/L NaOH溶液滴定10mL 0.2mol/L的某二元弱酸溶液,溶液中pH,、及的物质的量浓度随滴加NaOH溶液体积的变化关系如图所示,下列说法错误的是
A.的
B.X、Y、Z三点中,Z点时水的电离程度最大
C.0.1mol/L NaHA溶液中:
D.在Y点时,
二、非选择题(共4小题,共56分,每空2分)
17.根据所学知识,回答下列问题:
(1)Cu的简化电子排布式为 。的价电子轨道表示式为 。
(2)乙炔分子中σ键与π键个数之比为 。
(3)吡啶()是一种常用的有机溶剂。已知吡啶中所有原子共面,且分子中含有与苯类似的大π键,由此可知,吡啶中N原子的价层孤电子对占据 轨道。
(4)、、按照沸点由高到低排序,依次为 。
(5)、、按照键角由大到小排序,依次为 。
(6)科学家合成了一种新型离子化合物,其所有原子最外层都符合相应稀有气体原子电子层结构,该物质遇水会发生水解,生成一种一元弱碱和一种单质气体。
该反应的化学方程式为 。
18.(1)某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。
①反应从开始至2min,用Z的浓度变化表示的平均反应速率为 。
②由图中所给数据进行分析,该反应的化学方程式为 。
③下列措施能加快反应速率的有 。
A.恒压时充入He B.恒容时充入He C.恒容时充入X D.升高温度
(2)已知25℃时的各级电离平衡常数如表所示:
平衡常数
①水解反应的离子方程式为 ;其水解常数 (保留3位有效数字),溶液呈 性。(填“酸”、“碱”或“中”)
②计算的平衡常数K= (保留2位有效数字)。
19.对和的高效利用能够有效缓解全球变暖。
(1)在两个体积均为1L的恒容密闭容器中,在相同温度下进行反应(不发生其他反应),起始时按表中相应的量加入物质。的平衡转化率如表所示。
容器 起始物质的量/mol 的平衡转化率
CO
X 1 1 0 0 50%
Y 2 2 0 0 —
①该温度下,反应的平衡常数K= 。
②下列条件能说明反应达到平衡状态的是 (填标号)。
A.
B.容器内混合气体的总压强不再变化
C.容器内混合气体的密度保持不变
D.容器内各物质的浓度满足
③达到平衡时,容器Y内的平衡转化率 50%。(填“>”,“<”或“=”)
(2)还可以通过催化加氢合成乙醇: △H<0
设m为起始时的投料比,即。通过实验得到下列图像:
①若图1中m相同,则温度从高到低排序为 。
图1
②图2表示在m=3时,平衡状态各物质的物质的量分数与温度的关系,则d曲线表示的是 的物质的量分数。在温度、总压为5MPa的恒压条件下,该反应压强平衡常数的计算式(带入数据,不用化简)为 。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数),的平衡转化率为 (保留3位有效数字)。
图2
20.镍及其化合物在工业上有广泛用途,以某地红土镍矿(主要成分NiO、MgO、、和FeO)为原料,采用酸溶法制取和,工业流程如图所示:
已知:
①常温下,易溶于水,和NiOOH不溶于水。
②在上述流程中,某些金属离子开始沉淀和沉淀完全时的pH如下:
沉淀物
开始沉淀时的pH 7.1 7.6 2.7 3.4 9.2
沉淀完全()时的pH 9.0 9.6 3.2 4.7 11.1
回答下列问题:
(1)“滤液1”中加入的作用是 (用离子反应方程式表示)。
(2)操作Ⅱ为达到实验目的,由表中的数据判断通入调节溶液pH的范围是 。
(3),“沉镍”中pH调为8.5,则滤液中的浓度为 mol/L。
(4)工业上使用在碱性溶液中电解,在电解池的阳极可制得电极材料NiOOH,该电极反应方程式为 。
(5)用滴定法测定产品中镍元素含量。取5.90g样品,酸溶后配成100mL溶液,取20.00mL于锥形瓶中进行滴定,滴入几滴紫脲酸胺指示剂,用浓度为0.100的标准液滴定,重复操作2~3次,消耗标准液平均值为12.00mL。
已知:
ⅰ.;
ⅱ.紫脲酸胺;紫色试剂,遇显橙黄色。
①滴定终点的颜色变化为 。
②样品中镍元素的质量分数为 %(保留3位有效数字);
③以下操作,会使测定结果偏低的有 。
A.滴定终点读数时,俯视滴定管刻度。
B.盛装标准液的滴定管未润洗。
C.滴定前,发现装有滴定管尖嘴处有一个气泡,滴定后,气泡消失。
D.滴定终点读数后,发现尖嘴处悬挂了一滴溶液。
深圳中学2023-2024学年度第一学期期末考试试题
参考答案
一、选择题(1-10题每题2分,11-16题每题4分)
A卷:DBBBA ACBCD ACDCBC
B卷:DBBCA ACBBD ACDCBC
二、非选择题(每空2分)
17.
(1)
(2)3∶2
(3)杂化
(4)
(5)
(6)
18.
(1)0.05 CD
(2) (或) 酸
19.
(1)4 B <
(2)
(单位不写不扣分,或或或或)
66.7%
20.
(1)
(2)4.7-7.1(或4.7<pH<7.1)
(3)
(4)
(5)橙黄色(黄色、浅黄色)变为浅紫色(紫色、粉红色、浅红色)
6.00
A
深圳中学2023-2024学年度第一学期期末考试试题
年级:高二 科目:化学
考试时长:75分钟 卷面总分:100分
注意事项:
1.答案写在答题卡指定的位置上,写在试题卷上无效。选择题作答必须用2B铅笔,修改时用橡皮擦干净。
可能用到的相对原子质量:H-1 C-12 O-16 N-14 S-32 Ni-59 Zn-65
一、单项选择题(每小题只有一个答案符合题意,共16小题,1-10小题每小题2分,11-16小题每小题4分,共44分)
1.自由能的变化△G=△H-T△S是判断反应进行方向的复合判据。△G<0时,反应能自发进行。已知工业上常利用和来制备水煤气,化学方程式为,△H>0 则下列说法正确的是
A.△S>0,低温下该反应能自发进行 B.△S<0,高温下该反应能自发进行
C.△S<0,低温下该反应能自发进行 D.△S>0,高温下该反应能自发进行
2.下列热化学方程式及其描述正确的是
A. (燃烧热)
B. (中和热)
C. (燃烧热)
D.C(金刚石、s)=C(石墨、s) (反应热)(已知石墨比金刚石稳定)
3.是一种具有高催化活性的新型光催化剂,下列相关说法错误的是
A.Zn处于元素周期表中的ds区 B.基态Ge存在7种不同能量的电子
C.基态O原子中含有3对成对电子 D.电负性大小顺序O>Ge>Zn
4.下列离子的VSEPR模型与其空间结构一致的是
A. B. C. D.
5.下列化学用语不正确的是
A.次氯酸的电子式: B.正丁烷的球棍模型:
C.乙烯的结构简式: D.中碳的杂化类型:
6.自由基是化学键断裂时产生的含未成对电子的中间体。活泼自由基与氧气的反应一直是科研人员的关注点,HNO自由基与反应过程的能量变化如图所示,下列说法错误的是
A.中间产物X生成中间产物Y的反应的活化能为14.15
B.生成产物P2的决速步为中间产物Z到产物P2的基元反应
C.相同条件下,中间产物Z转化为产物的速率:v(P1)>v(P2)
D.三种中间产物中Z最稳定
7.下列颜色变化,与勒夏特列原理无关的是
A.红棕色的体系加压后,颜色先变深后逐渐变浅
B.将0.01的溶液加热,溶液颜色加深
C.、、HI平衡混合气加压后颜色变深
D.新制的氯水在光照下颜色变浅
8.已知: △H<0,向恒温恒容的密闭容器中充入1mol A和2mol B,时达到平衡状态Ⅰ,在时改变某-条件,时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
A.时刻改变的条件可能是升高温度B.~时,平衡向逆反应方向移动
C.平衡时A的体积分数φ(Ⅱ)>φ(Ⅰ)D.平衡常数K(Ⅰ)>K(Ⅱ)
9.常温下,下列有关电解质溶液的说法正确的是
A.相同浓度的HCOONa和NaF溶液,前者的pH较大,则
B.已知FeS溶于稀硫酸,而CuS不溶于稀硫酸,则
C.相同浓度的和溶液等体积混合后pH约为4.7,则溶液中
D.在1mol/L 溶液中,
10.秦俑彩绘中含有难溶的铅白()和黄色的。常温下,和在水溶液中各自分别达到沉淀溶解平衡时pM与pR的关系如图所示,其中pM为阳离子浓度的负对数,pR为阴离子浓度的负对数。下列说法正确的是
A.转化为的反应趋势很大 B.z点溶液对于来说尚未饱和
C.的数量级为 D.完全沉淀废液中的,的效果不如
11.化合物可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族,且Y的原子半径小于M。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为,X与M同周期,E在地壳中含量最多。下列说法正确的是
A.元素电负性:E>Y>Z B.简单氢化物沸点:M>Y>E
C.第一电离能:X>E>Y D.和的空间结构均为三角锥形
12.根据下列实验现象所得出的实验结论正确的是:
选项 实验现象 实验结论
A 将少量HA溶液加入溶液,未产生气泡。 酸性:HA<
B 臭氧在中的溶解度高于在水中的溶解度 为非极性分子
C 向含有酚酞的溶液中加入少量固体,溶液红色变浅。 溶液中存在水解平衡
D 向10mL 溶液中滴加5mL等浓度的KI溶液,再滴加KSCN溶液,溶液最终变为血红色。 溶液与KI溶液的反应为可逆反应
13.多位化学家用简单的偶联反应合成了右图这个有趣的“纳米小人”分子。关于该小人的结构,以下说法错误的是
A.小人眼睛的两个O原子,杂化方式为
B.构成帽子的6个C原子,不可能同时处于同一个平面上
C.与足量氢气发生加成反应后,人“腰部”的两个C原子杂化方式会发生改变
D.该分子所有碳原子都不是手性碳原子
14.碱性锌—铁液流电池(如图)具有电压高、成本低的优点。
该电池的总反应为:。
下列叙述正确的是
A.放电时,右侧贮液器中溶液浓度减小
B.充电时,M电极与电源负极相连
C.充电时,M极电极反应式为
D.放电时,电路中转移2mol电子时,负极区电解质溶液增加65g
15.合成氨反应: △H<0。图1表示在2L恒容密闭容器中的物质的量浓度随时间的变化曲线。图2表示在其他条件不变时,平衡时的体积分数随起始时的物质的量的变化曲线。下列说法正确的是
图1 图2
A.图1中,其他条件不变,第11min改用更为高效的催化剂,则-t的变化趋势为曲线b所示
B.图1中,其他条件不变,第11min迅速压缩容器体积为1L,则-t的变化趋势为曲线a所示
C.图2中,反应物的平衡转化率:b>a>c
D.图2中,、表示温度,则
16.25℃时,用0.2mol/L NaOH溶液滴定10mL 0.2mol/L的某二元弱酸溶液,溶液中pH,、及的物质的量浓度随滴加NaOH溶液体积的变化关系如图所示,下列说法错误的是
A.的
B.X、Y、Z三点中,Z点时水的电离程度最大
C.0.1mol/L NaHA溶液中:
D.在Y点时,
二、非选择题(共4小题,共56分,每空2分)
17.根据所学知识,回答下列问题:
(1)Cu的简化电子排布式为 。的价电子轨道表示式为 。
(2)乙炔分子中σ键与π键个数之比为 。
(3)吡啶()是一种常用的有机溶剂。已知吡啶中所有原子共面,且分子中含有与苯类似的大π键,由此可知,吡啶中N原子的价层孤电子对占据 轨道。
(4)、、按照沸点由高到低排序,依次为 。
(5)、、按照键角由大到小排序,依次为 。
(6)科学家合成了一种新型离子化合物,其所有原子最外层都符合相应稀有气体原子电子层结构,该物质遇水会发生水解,生成一种一元弱碱和一种单质气体。
该反应的化学方程式为 。
18.(1)某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。
①反应从开始至2min,用Z的浓度变化表示的平均反应速率为 。
②由图中所给数据进行分析,该反应的化学方程式为 。
③下列措施能加快反应速率的有 。
A.恒压时充入He B.恒容时充入He C.恒容时充入X D.升高温度
(2)已知25℃时的各级电离平衡常数如表所示:
平衡常数
①水解反应的离子方程式为 ;其水解常数 (保留3位有效数字),溶液呈 性。(填“酸”、“碱”或“中”)
②计算的平衡常数K= (保留2位有效数字)。
19.对和的高效利用能够有效缓解全球变暖。
(1)在两个体积均为1L的恒容密闭容器中,在相同温度下进行反应(不发生其他反应),起始时按表中相应的量加入物质。的平衡转化率如表所示。
容器 起始物质的量/mol 的平衡转化率
CO
X 1 1 0 0 50%
Y 2 2 0 0 —
①该温度下,反应的平衡常数K= 。
②下列条件能说明反应达到平衡状态的是 (填标号)。
A.
B.容器内混合气体的总压强不再变化
C.容器内混合气体的密度保持不变
D.容器内各物质的浓度满足
③达到平衡时,容器Y内的平衡转化率 50%。(填“>”,“<”或“=”)
(2)还可以通过催化加氢合成乙醇: △H<0
设m为起始时的投料比,即。通过实验得到下列图像:
①若图1中m相同,则温度从高到低排序为 。
图1
②图2表示在m=3时,平衡状态各物质的物质的量分数与温度的关系,则d曲线表示的是 的物质的量分数。在温度、总压为5MPa的恒压条件下,该反应压强平衡常数的计算式(带入数据,不用化简)为 。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数),的平衡转化率为 (保留3位有效数字)。
图2
20.镍及其化合物在工业上有广泛用途,以某地红土镍矿(主要成分NiO、MgO、、和FeO)为原料,采用酸溶法制取和,工业流程如图所示:
已知:
①常温下,易溶于水,和NiOOH不溶于水。
②在上述流程中,某些金属离子开始沉淀和沉淀完全时的pH如下:
沉淀物
开始沉淀时的pH 7.1 7.6 2.7 3.4 9.2
沉淀完全()时的pH 9.0 9.6 3.2 4.7 11.1
回答下列问题:
(1)“滤液1”中加入的作用是 (用离子反应方程式表示)。
(2)操作Ⅱ为达到实验目的,由表中的数据判断通入调节溶液pH的范围是 。
(3),“沉镍”中pH调为8.5,则滤液中的浓度为 mol/L。
(4)工业上使用在碱性溶液中电解,在电解池的阳极可制得电极材料NiOOH,该电极反应方程式为 。
(5)用滴定法测定产品中镍元素含量。取5.90g样品,酸溶后配成100mL溶液,取20.00mL于锥形瓶中进行滴定,滴入几滴紫脲酸胺指示剂,用浓度为0.100的标准液滴定,重复操作2~3次,消耗标准液平均值为12.00mL。
已知:
ⅰ.;
ⅱ.紫脲酸胺;紫色试剂,遇显橙黄色。
①滴定终点的颜色变化为 。
②样品中镍元素的质量分数为 %(保留3位有效数字);
③以下操作,会使测定结果偏低的有 。
A.滴定终点读数时,俯视滴定管刻度。
B.盛装标准液的滴定管未润洗。
C.滴定前,发现装有滴定管尖嘴处有一个气泡,滴定后,气泡消失。
D.滴定终点读数后,发现尖嘴处悬挂了一滴溶液。
深圳中学2023-2024学年度第一学期期末考试试题
参考答案
一、选择题(1-10题每题2分,11-16题每题4分)
A卷:DBBBA ACBCD ACDCBC
B卷:DBBCA ACBBD ACDCBC
二、非选择题(每空2分)
17.
(1)
(2)3∶2
(3)杂化
(4)
(5)
(6)
18.
(1)0.05 CD
(2) (或) 酸
19.
(1)4 B <
(2)
(单位不写不扣分,或或或或)
66.7%
20.
(1)
(2)4.7-7.1(或4.7<pH<7.1)
(3)
(4)
(5)橙黄色(黄色、浅黄色)变为浅紫色(紫色、粉红色、浅红色)
6.00
A
同课章节目录
