化学人教版(2019)必修第一册2.2.2氯气的实验室制法 氯离子的检验(共17张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册2.2.2氯气的实验室制法 氯离子的检验(共17张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 12.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-03 00:00:00 | ||
图片预览





文档简介
(共17张PPT)
第二节
氯及其化合物
第二章 海水中的重要元素——钠和氯
第2课时 氯气的实验室制法
01 氯气的实验室制法
02 氯离子的检验
舍勒与氯气的制备
世间最大的快乐,莫过于发现世人从未见过的新物质。 ——舍勒
1774年,瑞典化学家舍勒在研究软锰矿(主要成分MnO2)的过程中,发现软锰矿与浓盐酸混合加热,产生了黄绿色气体、伴有强烈的刺激性气味。
——氯气。
世间最大的快乐,莫过于发现世人从未见过的新物质。 —舍勒
反应原理
使用浓盐酸与足量的MnO2共热制Cl2,实际产生的Cl2总比理论值低,其主要原因是什么?
原理一:软锰矿(MnO2)与浓盐酸混合加热
MnO2 + 4HCl(浓) MnCl2 +Cl2 + 2H2O
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
原理二:高锰酸钾与浓盐酸混合
1.浓盐酸的作用?
2.使用浓盐酸与足量的MnO2共热制Cl2,实际产生的Cl2总比理论值低,其主要原因是什么?
不浓不热不反应
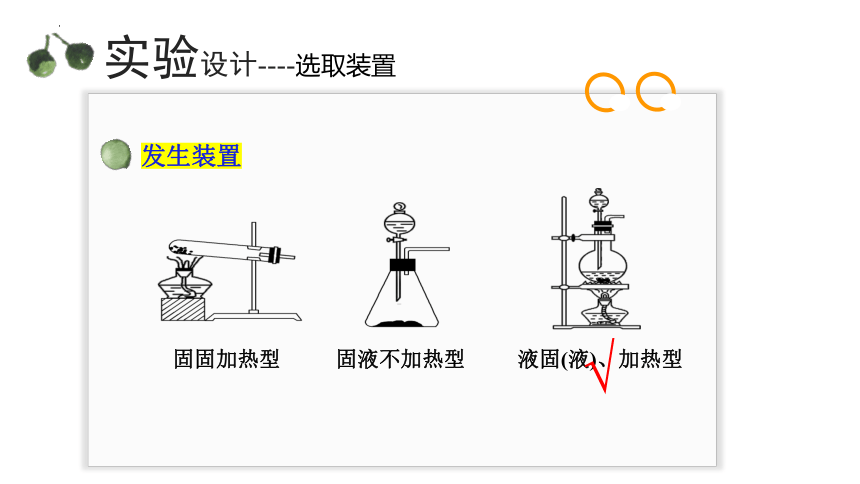
实验设计----选取装置
发生装置
固固加热型
固液不加热型
液固(液)、加热型
√
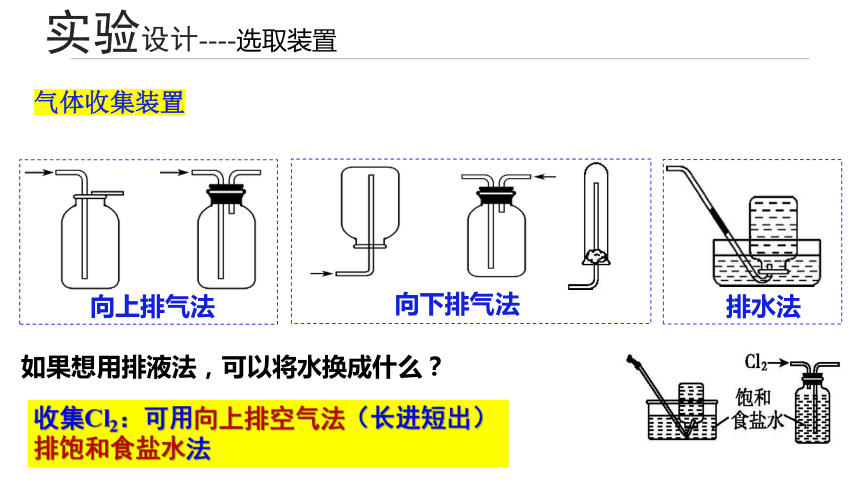
气体收集装置
向上排气法
向下排气法
排水法
如果想用排液法,可以将水换成什么?
收集Cl2:可用向上排空气法(长进短出)排饱和食盐水法
实验设计----选取装置
用NaOH等强碱进行吸收
Cl2 + 2NaOH == NaCl + NaClO + H2O
氢氧化钠溶液
资料
尾气处理
Cl2在水中的溶解度为1:2
【思考与讨论】能否用澄清石灰水代替?
尾气处理时,不能用澄清石灰水吸收氯气,因为澄清石灰水中Ca(OH)2的含量少,吸收不完全。
实验设计----选取装置
收集装置
尾气处理装置
发生装置
这样收集到的氯气纯净吗?有哪些杂质?如何除去?有没有先后顺序?
评价装置
思考讨论
问题一 一套完整的气体制取装置应该包括哪几步?
问题二 实验室制备氯气过程中,会产生哪些杂质气体,如何除去杂质气体,需要什么装置?
尾气处理装置
净化
发生装置
收集
先除杂后干燥
HCl
水蒸气
饱和食盐水
浓硫酸
实验设计
除杂装置
装置(洗气瓶):盛液体除杂试剂,气流方向是长管进,短管出。
装置(干燥管):盛固体除杂试剂,气流方向是粗口进,细口出。
装置(U形管):盛固体除杂试剂
实验设计
【思考与讨论】如何验满?
淀粉碘化钾试纸
2KI+Cl2=2KCl+I2
方法一:观察,集气瓶中充满黄绿色气体
方法二:将湿润的淀粉-KI试纸放在瓶口,观察试纸是否变蓝
方法三:湿润的蓝色石蕊试纸放在瓶口,是否先变红后褪色
实验设计----选取装置
实验过程
02
氯离子的检验
【实验2-9】在三支试管中分别加入稀盐酸、氯化钠溶液和碳酸钠溶液,再各滴入几滴硝酸银溶液,观察现象,再加入稀硝酸观察现象。
HCl
NaCl
AgNO3溶液
AgNO3溶液
AgNO3溶液
HNO3溶液
HNO3溶液
HNO3溶液
Cl- + Ag+ = AgCl↓
CO32- + 2Ag+ = Ag2CO3↓
Ag2CO3 + 2H+ = 2Ag+ + CO2↑ + H2O
Na2CO3
氯离子的检验
氯离子的检验
待测液
滴加稀硝酸
排除CO32-等的干扰
酸化液
滴加AgNO3溶液
白色沉淀
结论
含有Cl-
取少量待测液于试管中,先加入稀硝酸酸化,再加入硝酸银溶液,若有白色沉淀生成,说明溶液中含有Cl-,否则无。
或者硝酸酸化的硝酸银溶液
1.检验原理
Ag++Cl-===AgCl↓
2.检验步骤
课堂小结
氯气的
实验室制法
原理
装置
氯离子的检验
试剂
(稀硝酸酸化的AgNO3)
现象
(白色沉淀)
第二节
氯及其化合物
第二章 海水中的重要元素——钠和氯
第2课时 氯气的实验室制法
01 氯气的实验室制法
02 氯离子的检验
舍勒与氯气的制备
世间最大的快乐,莫过于发现世人从未见过的新物质。 ——舍勒
1774年,瑞典化学家舍勒在研究软锰矿(主要成分MnO2)的过程中,发现软锰矿与浓盐酸混合加热,产生了黄绿色气体、伴有强烈的刺激性气味。
——氯气。
世间最大的快乐,莫过于发现世人从未见过的新物质。 —舍勒
反应原理
使用浓盐酸与足量的MnO2共热制Cl2,实际产生的Cl2总比理论值低,其主要原因是什么?
原理一:软锰矿(MnO2)与浓盐酸混合加热
MnO2 + 4HCl(浓) MnCl2 +Cl2 + 2H2O
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
原理二:高锰酸钾与浓盐酸混合
1.浓盐酸的作用?
2.使用浓盐酸与足量的MnO2共热制Cl2,实际产生的Cl2总比理论值低,其主要原因是什么?
不浓不热不反应
实验设计----选取装置
发生装置
固固加热型
固液不加热型
液固(液)、加热型
√
气体收集装置
向上排气法
向下排气法
排水法
如果想用排液法,可以将水换成什么?
收集Cl2:可用向上排空气法(长进短出)排饱和食盐水法
实验设计----选取装置
用NaOH等强碱进行吸收
Cl2 + 2NaOH == NaCl + NaClO + H2O
氢氧化钠溶液
资料
尾气处理
Cl2在水中的溶解度为1:2
【思考与讨论】能否用澄清石灰水代替?
尾气处理时,不能用澄清石灰水吸收氯气,因为澄清石灰水中Ca(OH)2的含量少,吸收不完全。
实验设计----选取装置
收集装置
尾气处理装置
发生装置
这样收集到的氯气纯净吗?有哪些杂质?如何除去?有没有先后顺序?
评价装置
思考讨论
问题一 一套完整的气体制取装置应该包括哪几步?
问题二 实验室制备氯气过程中,会产生哪些杂质气体,如何除去杂质气体,需要什么装置?
尾气处理装置
净化
发生装置
收集
先除杂后干燥
HCl
水蒸气
饱和食盐水
浓硫酸
实验设计
除杂装置
装置(洗气瓶):盛液体除杂试剂,气流方向是长管进,短管出。
装置(干燥管):盛固体除杂试剂,气流方向是粗口进,细口出。
装置(U形管):盛固体除杂试剂
实验设计
【思考与讨论】如何验满?
淀粉碘化钾试纸
2KI+Cl2=2KCl+I2
方法一:观察,集气瓶中充满黄绿色气体
方法二:将湿润的淀粉-KI试纸放在瓶口,观察试纸是否变蓝
方法三:湿润的蓝色石蕊试纸放在瓶口,是否先变红后褪色
实验设计----选取装置
实验过程
02
氯离子的检验
【实验2-9】在三支试管中分别加入稀盐酸、氯化钠溶液和碳酸钠溶液,再各滴入几滴硝酸银溶液,观察现象,再加入稀硝酸观察现象。
HCl
NaCl
AgNO3溶液
AgNO3溶液
AgNO3溶液
HNO3溶液
HNO3溶液
HNO3溶液
Cl- + Ag+ = AgCl↓
CO32- + 2Ag+ = Ag2CO3↓
Ag2CO3 + 2H+ = 2Ag+ + CO2↑ + H2O
Na2CO3
氯离子的检验
氯离子的检验
待测液
滴加稀硝酸
排除CO32-等的干扰
酸化液
滴加AgNO3溶液
白色沉淀
结论
含有Cl-
取少量待测液于试管中,先加入稀硝酸酸化,再加入硝酸银溶液,若有白色沉淀生成,说明溶液中含有Cl-,否则无。
或者硝酸酸化的硝酸银溶液
1.检验原理
Ag++Cl-===AgCl↓
2.检验步骤
课堂小结
氯气的
实验室制法
原理
装置
氯离子的检验
试剂
(稀硝酸酸化的AgNO3)
现象
(白色沉淀)
