第8单元 课题3第2课时 金属资源的保护 学案 (含答案)2023-2024学年初中化学人教版九年级下册
文档属性
| 名称 | 第8单元 课题3第2课时 金属资源的保护 学案 (含答案)2023-2024学年初中化学人教版九年级下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 63.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-03 00:00:00 | ||
图片预览

文档简介
课题3第2课时 金属资源的保护
学习目标
1.了解导致钢铁锈蚀的因素以及减缓钢铁锈蚀的办法。
2.知道废旧金属对环境的污染,认识回收利用废旧金属对环境及金属资源保护的重要性,树立珍惜资源、爱护环境的意识。
3.通过对钢铁锈蚀条件的探究,进一步加深对科学探究各要素的理解,提高学生的科学素养。
◎素养要求:1.了解防止金属腐蚀的简单方法。
2.认识废弃金属对环境的影响和回收金属的重要性。
【预习导学】
课时线索
铁锈蚀的条件→金属资源的保护
自主学习
阅读教材,回答下列问题:
1.铁在 中容易生锈,钢铁的锈蚀主要是铁与空气中的 、 等物质发生化学反应的结果;铁锈的成分比较复杂,主要成分是 (填化式),铁锈疏松多孔,不仅不能阻止钢铁制品与 和 接触,还会把空气和 保留在钢铁制品的表面,进一步加快钢铁的锈蚀。
2.防止铁生锈的实质就是破坏铁生锈的条件,即让铁与 或 隔绝,可采用的方法有 。
3.废弃金属回收的意义: 。
保护金属资源的途径: ; ;
; 。
【答案】
1.潮湿的空气 氧气 水蒸气 Fe2O3 氧气 水蒸气 水蒸气
2.氧气 水蒸气 ①保持铁制品表面的清洁、干燥;②表面涂保护膜:如涂油、刷漆、电镀、烤蓝等;③制成不锈钢
3.节约金属资源,减少环境污染 ①防止金属腐蚀 ②回收利用废旧金属 ③合理开采矿物 ④寻找金属的代替品
【合作探究】
任务驱动一:金属的腐蚀和防护
【提出问题】钢铁锈蚀是生活中常见的现象,钢铁的锈蚀与哪些因素有关
【猜想假设】猜想1:钢铁生锈可能与氧气有关。
猜想2:钢铁生锈可能与水有关。
猜想3:钢铁生锈可能是空气、水与铁共同作用的结果。
猜想4:酸溶液或盐溶液能加快钢铁生锈的速率。
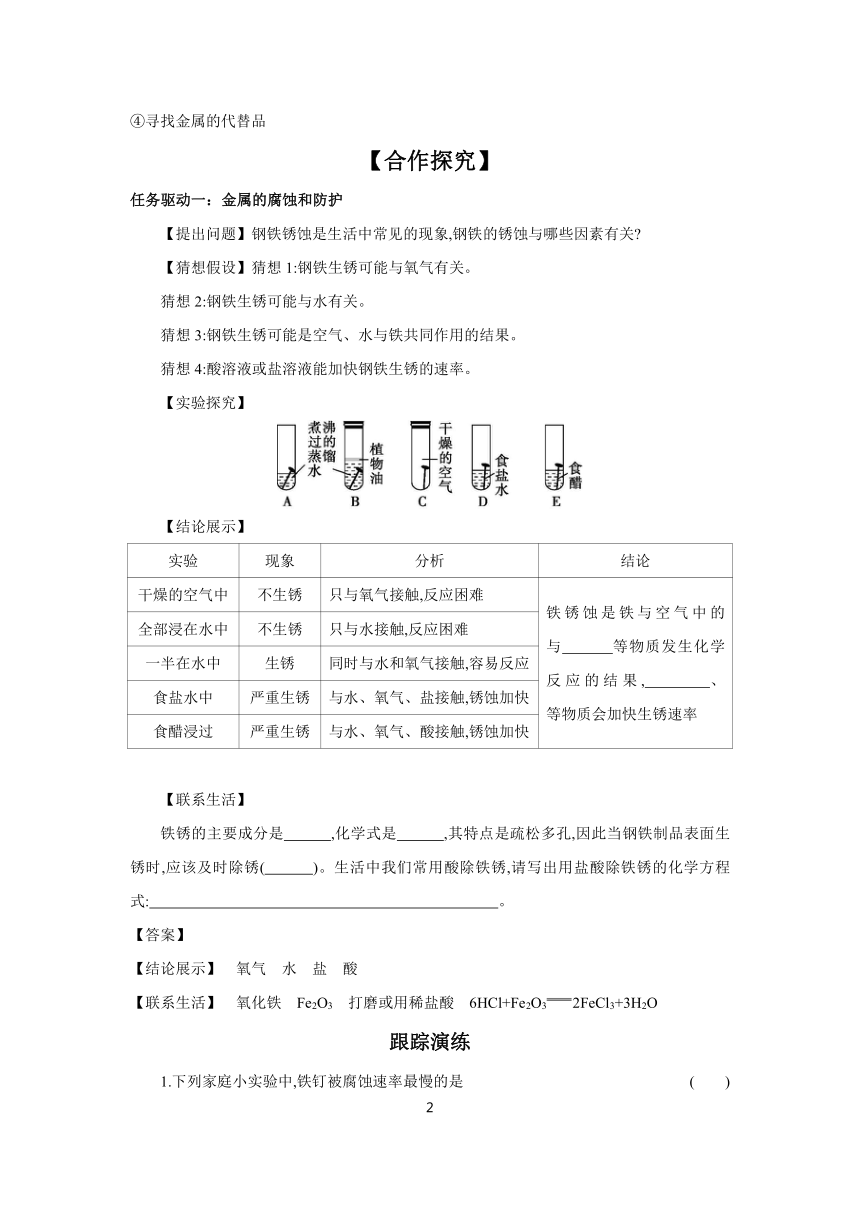
【实验探究】
【结论展示】
实验 现象 分析 结论
干燥的空气中 不生锈 只与氧气接触,反应困难 铁锈蚀是铁与空气中的 与 等物质发生化学反应的结果, 、 等物质会加快生锈速率
全部浸在水中 不生锈 只与水接触,反应困难
一半在水中 生锈 同时与水和氧气接触,容易反应
食盐水中 严重生锈 与水、氧气、盐接触,锈蚀加快
食醋浸过 严重生锈 与水、氧气、酸接触,锈蚀加快
【联系生活】
铁锈的主要成分是 ,化学式是 ,其特点是疏松多孔,因此当钢铁制品表面生锈时,应该及时除锈( )。生活中我们常用酸除铁锈,请写出用盐酸除铁锈的化学方程式: 。
【答案】
【结论展示】 氧气 水 盐 酸
【联系生活】 氧化铁 Fe2O3 打磨或用稀盐酸 6HCl+Fe2O32FeCl3+3H2O
跟踪演练
1.下列家庭小实验中,铁钉被腐蚀速率最慢的是 ( )
【答案】
1.B
任务驱动二:金属资源的保护
金属腐蚀不仅会浪费资源还会给我们带来巨大损失。阅读教材,如何减缓钢铁锈蚀 保护金属资源的有效途径有哪些 你知道哪些废旧金属可对环境造成污染
交流归纳:(一)防止铁生锈的方法:
1. 。
2. 。
3. 。
4. 。
(二)回收金属资源的意义
(1)可节约金属资源。
(2)由于金属冶炼需在高温下进行,废弃金属回收利用可以节约能源。
(3)降低金属制品的生产成本,可方便人们得到物美价廉的金属制品。
(4)可减少金属对环境的污染,保护环境。
(三)保护矿产资源的方法
(1) 。
(2) 。
(3) 。
(4) 。
【答案】
(一)1.保持钢铁制品表面洁净、干燥
2.“穿外衣”——金属表面覆盖保护层(涂刷矿物油、油漆,覆盖搪瓷、塑料)
3.镀上一层不易生锈的金属,例如镀锡、镀锌、镀铬等
4.“增强体质”——改变金属的组成和结构制成合金,如:在钢铁中加入铬、镍等(不锈钢)
(三)(1)防止金属生锈
(2)要对生锈金属回收利用
(3)寻求金属的替代品
(4)合理开采
跟踪演练
2.生活中我们常见到:①汽车;②机器上的齿轮;③金属门把手;④锯条;⑤铁柜;⑥剪刀;⑦盆;⑧铁轴等铁制品。为了防止它们生锈,通常适合采用下面的哪种方法 (填序号)
(1)在表面刷一层油漆: 。
(2)涂上机油: 。
(3)在表面镀上一层其他金属: 。
(4)在表面烧制搪瓷: 。
(5)使其表面氧化成致密的氧化膜: 。
【学习小助手】
本节课我们主要探究学习了钢铁锈蚀的原理和条件,并了解了通过对钢铁的防护、废旧金属的回收利用来节约和保护金属资源的方法。这些知识在我们的实际生活中经常接触和使用,是非常实用的,我们要正确对待和掌握。
【答案】
2.(1)①⑤
(2)②⑧
(3)③⑥
(4)⑦
(5)④
2
学习目标
1.了解导致钢铁锈蚀的因素以及减缓钢铁锈蚀的办法。
2.知道废旧金属对环境的污染,认识回收利用废旧金属对环境及金属资源保护的重要性,树立珍惜资源、爱护环境的意识。
3.通过对钢铁锈蚀条件的探究,进一步加深对科学探究各要素的理解,提高学生的科学素养。
◎素养要求:1.了解防止金属腐蚀的简单方法。
2.认识废弃金属对环境的影响和回收金属的重要性。
【预习导学】
课时线索
铁锈蚀的条件→金属资源的保护
自主学习
阅读教材,回答下列问题:
1.铁在 中容易生锈,钢铁的锈蚀主要是铁与空气中的 、 等物质发生化学反应的结果;铁锈的成分比较复杂,主要成分是 (填化式),铁锈疏松多孔,不仅不能阻止钢铁制品与 和 接触,还会把空气和 保留在钢铁制品的表面,进一步加快钢铁的锈蚀。
2.防止铁生锈的实质就是破坏铁生锈的条件,即让铁与 或 隔绝,可采用的方法有 。
3.废弃金属回收的意义: 。
保护金属资源的途径: ; ;
; 。
【答案】
1.潮湿的空气 氧气 水蒸气 Fe2O3 氧气 水蒸气 水蒸气
2.氧气 水蒸气 ①保持铁制品表面的清洁、干燥;②表面涂保护膜:如涂油、刷漆、电镀、烤蓝等;③制成不锈钢
3.节约金属资源,减少环境污染 ①防止金属腐蚀 ②回收利用废旧金属 ③合理开采矿物 ④寻找金属的代替品
【合作探究】
任务驱动一:金属的腐蚀和防护
【提出问题】钢铁锈蚀是生活中常见的现象,钢铁的锈蚀与哪些因素有关
【猜想假设】猜想1:钢铁生锈可能与氧气有关。
猜想2:钢铁生锈可能与水有关。
猜想3:钢铁生锈可能是空气、水与铁共同作用的结果。
猜想4:酸溶液或盐溶液能加快钢铁生锈的速率。
【实验探究】
【结论展示】
实验 现象 分析 结论
干燥的空气中 不生锈 只与氧气接触,反应困难 铁锈蚀是铁与空气中的 与 等物质发生化学反应的结果, 、 等物质会加快生锈速率
全部浸在水中 不生锈 只与水接触,反应困难
一半在水中 生锈 同时与水和氧气接触,容易反应
食盐水中 严重生锈 与水、氧气、盐接触,锈蚀加快
食醋浸过 严重生锈 与水、氧气、酸接触,锈蚀加快
【联系生活】
铁锈的主要成分是 ,化学式是 ,其特点是疏松多孔,因此当钢铁制品表面生锈时,应该及时除锈( )。生活中我们常用酸除铁锈,请写出用盐酸除铁锈的化学方程式: 。
【答案】
【结论展示】 氧气 水 盐 酸
【联系生活】 氧化铁 Fe2O3 打磨或用稀盐酸 6HCl+Fe2O32FeCl3+3H2O
跟踪演练
1.下列家庭小实验中,铁钉被腐蚀速率最慢的是 ( )
【答案】
1.B
任务驱动二:金属资源的保护
金属腐蚀不仅会浪费资源还会给我们带来巨大损失。阅读教材,如何减缓钢铁锈蚀 保护金属资源的有效途径有哪些 你知道哪些废旧金属可对环境造成污染
交流归纳:(一)防止铁生锈的方法:
1. 。
2. 。
3. 。
4. 。
(二)回收金属资源的意义
(1)可节约金属资源。
(2)由于金属冶炼需在高温下进行,废弃金属回收利用可以节约能源。
(3)降低金属制品的生产成本,可方便人们得到物美价廉的金属制品。
(4)可减少金属对环境的污染,保护环境。
(三)保护矿产资源的方法
(1) 。
(2) 。
(3) 。
(4) 。
【答案】
(一)1.保持钢铁制品表面洁净、干燥
2.“穿外衣”——金属表面覆盖保护层(涂刷矿物油、油漆,覆盖搪瓷、塑料)
3.镀上一层不易生锈的金属,例如镀锡、镀锌、镀铬等
4.“增强体质”——改变金属的组成和结构制成合金,如:在钢铁中加入铬、镍等(不锈钢)
(三)(1)防止金属生锈
(2)要对生锈金属回收利用
(3)寻求金属的替代品
(4)合理开采
跟踪演练
2.生活中我们常见到:①汽车;②机器上的齿轮;③金属门把手;④锯条;⑤铁柜;⑥剪刀;⑦盆;⑧铁轴等铁制品。为了防止它们生锈,通常适合采用下面的哪种方法 (填序号)
(1)在表面刷一层油漆: 。
(2)涂上机油: 。
(3)在表面镀上一层其他金属: 。
(4)在表面烧制搪瓷: 。
(5)使其表面氧化成致密的氧化膜: 。
【学习小助手】
本节课我们主要探究学习了钢铁锈蚀的原理和条件,并了解了通过对钢铁的防护、废旧金属的回收利用来节约和保护金属资源的方法。这些知识在我们的实际生活中经常接触和使用,是非常实用的,我们要正确对待和掌握。
【答案】
2.(1)①⑤
(2)②⑧
(3)③⑥
(4)⑦
(5)④
2
同课章节目录
