1.1 原子结构与元素性质 课件(共64张PPT) 高中化学鲁科版(2019)必修第二册
文档属性
| 名称 | 1.1 原子结构与元素性质 课件(共64张PPT) 高中化学鲁科版(2019)必修第二册 |
|
|
| 格式 | pptx | ||
| 文件大小 | 2.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-04 00:00:00 | ||
图片预览









文档简介
(共64张PPT)
第1章
原子结构与元素周期律
第1节 原子结构
有关原子结构的知识是自然科学的重要基础知识之一。原子是构成物质的一种基本微粒,物质的组成、性质和变化都与原子结构密切相关。
那么,原子的内部结构是怎样的呢
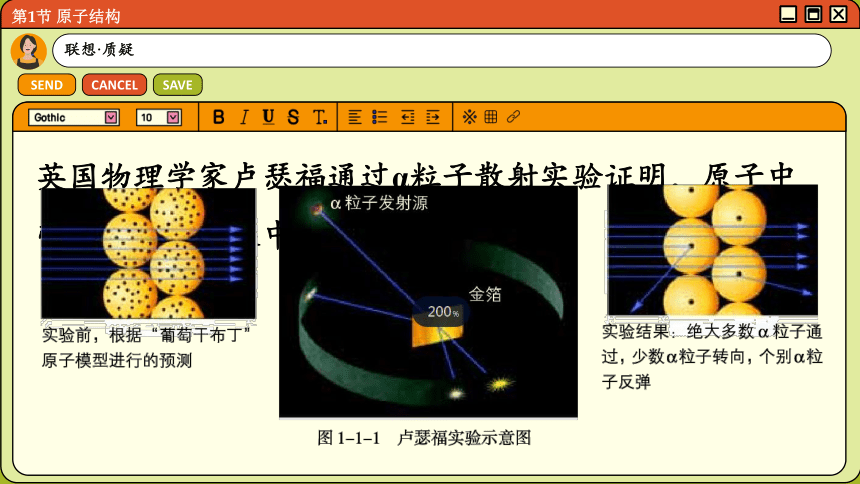
英国物理学家卢瑟福通过α粒子散射实验证明,原子中带正电的部分集中在一起。
联想·质疑
在此实验的基础上,卢瑟福提出了核式原子模型: 原子由原子核和核外电子构成。原子核带正电荷,位于原子的中心; 电子带负电荷,在原子核周围空间做高速运动。
那么,原子核的内部结构是怎样的
电子在核外空间的运动状态又是怎样的呢
原子核,核素
原子是由原子核和核外电子构成的,而原子核又是由更小的微粒——质子( proton)和中子(neutron)构成的。
1.原子核的构成
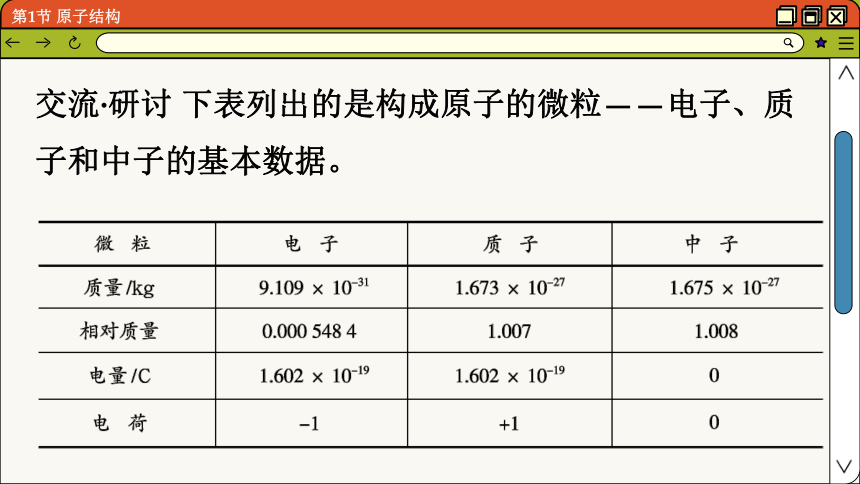
交流·研讨 下表列出的是构成原子的微粒——电子、质子和中子的基本数据。
请根据表中所列数据讨论:
1.在原子中,质子数、核电荷数和核外电子数之间存在着怎样的关系 为什么
2.原子的质量主要由哪些微粒决定
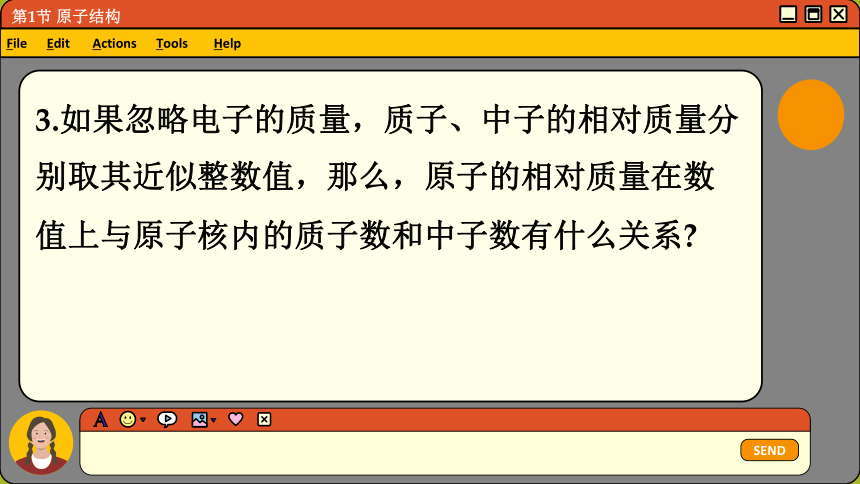
3.如果忽略电子的质量,质子、中子的相对质量分别取其近似整数值,那么,原子的相对质量在数值上与原子核内的质子数和中子数有什么关系
质子带正电荷,中子不带电,质子和中子依靠一种特殊的力一一核力结合在一起。对一个原子来说:
核电荷数 =质子数 =核外电子数
由于电子的质量很小,相对于质子、中子的质量,可以忽略不计,因此原子的质量几乎全部集中在原子核上。也就是说,原子的质量可以看做原子核中质子的质量和中子的质量之和。
人们将原子核中质子数和中子数之和称为质量数。
质子数(Z) + 中子数(N)= 质量数(A)
一般用符号表示一个质量数为 A、质子数为Z的原子,那么,组成原子的有关粒子间的关系可表示为:
1.在科学研究中,人们常用“来表示某种氯原子,请你谈谈其中符号和数字的含义。
2.生物体在生命过程中保留的一种碳原子--会在其死亡后衰变。
迁移·应用
测量在考古遗址中发现的生物遗体里 的数量,可以推断出它的存在年代。请你利用所学知识分析, 与作为相对原子质量标准的在结构上有何异同。
2.核素元素的种类是由原子核内的质子数决定的。
元素 (element)是具有相同质子数(核电荷数)的同一类原子的总称。
同种元素原子的质子数相同,那么,中子数是否也相同呢
观察·思考
这三种氢原子中质子、中子和电子的数量关系如图 1-1-3 所示。
思考
1.氕、氘、氚的原子结构有何异同
2.它们是同一种元素吗
氢元素有氕、氘、氚3种核素,分别用
表示。
除氢外,在天然元素中,还有许多元素具有多种核素,如碳元素有3种核素(C、CHC)氧元素有3种核素(g00)铀元素有3种核素()
氧元素有3种核素()
铀元素有3种核素 () ,
氯元素有2种核素()
有些元素则只有1种核素,如氟()、钠()
例如, ()互为同位素,
其中用做制造氢弹的原料
同位素
其中,是核反应堆的燃料。
同位素分为稳定同位素和放射性同位素两种。放射性同位素最常见的应用是作为放射源和进行同位素示踪。
例如,追踪植物中放射性 发出的射线,能确定磷在植物中的作用部位;
应用放射性同位素发射出的射线,可进行金属制品探伤、食物保鲜和肿瘤治疗等。
放射性同位素与医疗
放射性同位素用于疾病的诊断 用放射性同位素标记的药物进入人体后,医务人员可以利用标记药物的放射性,借助有关仪器从体外观察脏器功能和生化过程的变化。
化学与技术
在疾病的形成过程中,生化变化和功能变化一般要早于组织形态的变化,因此放射性同位素广泛用于肿瘤的早期诊断。例如,用放射性后位素进行诊断可比用X 光法早 3~6个月发现骨癌转移。
放射性同位素用于疾病的治疗 放射性同位素能放射出α、β、γ射线,射线达到一定剂量时有杀死生物细胞的作用。通过长期的实践,科学家们选用不同种类及剂量的放射性同位素,用特殊的方法照射不同部位的肿瘤,杀灭癌细胞或抑制癌细胞的繁殖,并尽量减少对人体正常细胞的损害。
未来的能源核聚变能
核聚变是将轻原子核融合成较重原子核的核反应,它所产生的能量比核裂变反应产生的能量大得多。
例如,1 g (H)全部聚合为氨所放出的热能可使4×108g冰变成水蒸气。
另外,核聚变产生的污染轻,不会造成放射性垃圾。因此,核聚变的和平利用将帮助人类长久地解决能源问题。
要使核聚变作为能源为人类服务,必须使核聚变产生的能量均匀地释放出来,也就是要进行受控核聚变反应。
目前受控核聚变反应的最大技术障碍是难以将核燃料加热到几千万甚至上亿摄氏度的高温。现在,科学家们正在探索在室温下实现受控核聚变的可能性。
核外电子排布
物质在化学反应中的表现与组成该物质的元素的原子结构有着密切的联系,其中核外电子扮演着非常重要的角色。电子在原子内有“广阔”的运动空间。在这“广阔”的空间里核外电子是怎样运动的呢
电子极其微小,即使使用最先进的扫描隧道显微镜(STM),也只能观察到排列有序紧密堆积的原子,而观察不到比原子小得多的电子。一个多世纪以来,科学家们主要采用建立模型的方法对核外电子的运动情况进行研究。
交流·研讨
请你查阅有关原子结构模型的资料,与同学们讨论电子在原子核外是怎样运动的。
现代物质结构理论认为,在含有多个电子的原子里,能量低的电子通常在离核较近的区域内运动,能量高的电子通常在离核较远的区域内运动。据此可以认为,电子是在原子核外距核由近及远、能量由低到高的不同电子层上分层排布的。
把能量最低、离核最近的电子层叫做第一层:能量稍高、离核稍远的电子层叫做第二层;由里往外依次类推,共有7个电子层。
科学研究表明:
每层最多容纳的电子数为 2n2 (n代表电子层数),而最外层电子数则不超过8个(第一层为最外层时,电子数不超过2个)。人们常用原子结构示意图来简明地表示电子在原子核外的分层排布情况。
经过分析发现,元素的性质与原子的最外层电子排布密切相关。
例如,稀有气体元素原子最外层电子数为8(氨除外,它的最外层只有2个电子),结构稳定,既不容易获得电子也不容易失去电子;
金属元素原子最外层电子数一般小于4,较易失去电子形成阳离子;
非金属元素原子最外层电子数一般大于或等于4,有较强的获得电子的倾向,活泼非金属元素的原子则较易获得电子形成阴离子。
化合价是元素的一种重要性质。元素的化合价的数值,与原子的电子层结构特别是最外层电子数有关。
例如,稀有气体元素原子核外电子排布已达稳定结构,既不容易获得电子也不容易失去电子,所以稀有气体元素通常表现为0价。
钠原子最外层只有1个电子,容易失去这个电子形成Nat而达到稳定结构,因此钠元素在化合物中显+1价:氯原子最外层有7个电子,只需获得1个电子形成 CI便可达到稳定结构,因此氯元素在化合物中常显-1价。
1.请你尝试画出钙原子(核电荷数为 20)和钾离子(核电荷数为19)的结构示意图。
交流·研讨
2。通过前面的学习你已经知道,金属钠、金属镁在化学反应中表现出还原性,而氧气、氯气在化学反应中表现出氧化性,你能用原子结构的知识对这一事实进行解释吗
3,你认为原子结构的知识对于理解物质结构和性质的关系有哪些帮助
1913年,玻尔在核式原子模型的基础上指出: 核外电子是处在一定的轨道上绕核运行的,正如太阳系的行星绕太阳运行一样:在核外运行的电子分层排布,按能量高低而距核远近不同。
资料在线
这个模型被称为“玻尔原子模型”。现代物质结构理论在新的实验基础上保留了玻尔原子模型合理的部分,并赋予其新的内容。
核外电子运动的特征
宏观物体的运动都有一定的轨迹,如人造卫星按一定的轨道围绕地球运行,而在原子核外运动的电子并不遵循宏观物体的运动规律。研究表明,电子在核外空间所处的位置及其运动速度不能同时准确地确定。
于是,人们采用统计的方法,对一个电子的多次行为或多个电子的一次行为进行研究,从而统计出电子在核外空间某处单位体积里出现机会的多少,并用电子云形象地进行表示。
概括整合
1.请用图示的方式描述构成原子的各种微粒与元素、核素间的关系,以及元素、核素与同位素间的关系。
2。核外电子排布是有一定规律的。那么,电子在核外是如何排布的 原子的最外层电子排布与元素的化学性质有什么关系
3,你认为研究原子结构有什么意义 请你列举核素在生产和生活中的应用
练习与活动
1,据报道,某些花岗岩会产生氡 ,从而对人体产生伤害。请回答
该原子的质量数是________,质子数是______,中子数是______
(2) 请将以下 Rn 的原子结构示意图补全。
(3)请根据 Rn 的原子结构预测氡气的化学性质
A。非常活泼,容易与氧气等非金属单质反应
B。比较活泼,能与钠等金属反应
C,不太活泼,与氮气性质相似
D,很难与其他物质发生反应
你选择该选项的理由是___________________________
(4)研究发现,镭能蜕变为,故将称为镭射气;钍能蜕变为,故将留称为钍射气;锕能蜕变为,故将称为锕射气。
( )
A.属于同种元素
B.互为同位素
C .属于同种核素
D .属于同种原子
由此可见,决定元素种类,决定核素种类。
2。你知道以下微粒结构示意图表示的各是什么微粒吗
3.请利用原子结构的知识解释下列事实。
(1)在硫化钠中,钠元素显+1价,硫元素显-2价
(2)钠原子和铝原子电子层数相同,但金属钠与氯气的反应要比金属铝与氯气的反应容易而且剧烈。
4,查阅资料并与同学们交流: 放射性同位素在能源、农业、医疗以及考古等方面有哪些应用
第1章
原子结构与元素周期律
第1节 原子结构
有关原子结构的知识是自然科学的重要基础知识之一。原子是构成物质的一种基本微粒,物质的组成、性质和变化都与原子结构密切相关。
那么,原子的内部结构是怎样的呢
英国物理学家卢瑟福通过α粒子散射实验证明,原子中带正电的部分集中在一起。
联想·质疑
在此实验的基础上,卢瑟福提出了核式原子模型: 原子由原子核和核外电子构成。原子核带正电荷,位于原子的中心; 电子带负电荷,在原子核周围空间做高速运动。
那么,原子核的内部结构是怎样的
电子在核外空间的运动状态又是怎样的呢
原子核,核素
原子是由原子核和核外电子构成的,而原子核又是由更小的微粒——质子( proton)和中子(neutron)构成的。
1.原子核的构成
交流·研讨 下表列出的是构成原子的微粒——电子、质子和中子的基本数据。
请根据表中所列数据讨论:
1.在原子中,质子数、核电荷数和核外电子数之间存在着怎样的关系 为什么
2.原子的质量主要由哪些微粒决定
3.如果忽略电子的质量,质子、中子的相对质量分别取其近似整数值,那么,原子的相对质量在数值上与原子核内的质子数和中子数有什么关系
质子带正电荷,中子不带电,质子和中子依靠一种特殊的力一一核力结合在一起。对一个原子来说:
核电荷数 =质子数 =核外电子数
由于电子的质量很小,相对于质子、中子的质量,可以忽略不计,因此原子的质量几乎全部集中在原子核上。也就是说,原子的质量可以看做原子核中质子的质量和中子的质量之和。
人们将原子核中质子数和中子数之和称为质量数。
质子数(Z) + 中子数(N)= 质量数(A)
一般用符号表示一个质量数为 A、质子数为Z的原子,那么,组成原子的有关粒子间的关系可表示为:
1.在科学研究中,人们常用“来表示某种氯原子,请你谈谈其中符号和数字的含义。
2.生物体在生命过程中保留的一种碳原子--会在其死亡后衰变。
迁移·应用
测量在考古遗址中发现的生物遗体里 的数量,可以推断出它的存在年代。请你利用所学知识分析, 与作为相对原子质量标准的在结构上有何异同。
2.核素元素的种类是由原子核内的质子数决定的。
元素 (element)是具有相同质子数(核电荷数)的同一类原子的总称。
同种元素原子的质子数相同,那么,中子数是否也相同呢
观察·思考
这三种氢原子中质子、中子和电子的数量关系如图 1-1-3 所示。
思考
1.氕、氘、氚的原子结构有何异同
2.它们是同一种元素吗
氢元素有氕、氘、氚3种核素,分别用
表示。
除氢外,在天然元素中,还有许多元素具有多种核素,如碳元素有3种核素(C、CHC)氧元素有3种核素(g00)铀元素有3种核素()
氧元素有3种核素()
铀元素有3种核素 () ,
氯元素有2种核素()
有些元素则只有1种核素,如氟()、钠()
例如, ()互为同位素,
其中用做制造氢弹的原料
同位素
其中,是核反应堆的燃料。
同位素分为稳定同位素和放射性同位素两种。放射性同位素最常见的应用是作为放射源和进行同位素示踪。
例如,追踪植物中放射性 发出的射线,能确定磷在植物中的作用部位;
应用放射性同位素发射出的射线,可进行金属制品探伤、食物保鲜和肿瘤治疗等。
放射性同位素与医疗
放射性同位素用于疾病的诊断 用放射性同位素标记的药物进入人体后,医务人员可以利用标记药物的放射性,借助有关仪器从体外观察脏器功能和生化过程的变化。
化学与技术
在疾病的形成过程中,生化变化和功能变化一般要早于组织形态的变化,因此放射性同位素广泛用于肿瘤的早期诊断。例如,用放射性后位素进行诊断可比用X 光法早 3~6个月发现骨癌转移。
放射性同位素用于疾病的治疗 放射性同位素能放射出α、β、γ射线,射线达到一定剂量时有杀死生物细胞的作用。通过长期的实践,科学家们选用不同种类及剂量的放射性同位素,用特殊的方法照射不同部位的肿瘤,杀灭癌细胞或抑制癌细胞的繁殖,并尽量减少对人体正常细胞的损害。
未来的能源核聚变能
核聚变是将轻原子核融合成较重原子核的核反应,它所产生的能量比核裂变反应产生的能量大得多。
例如,1 g (H)全部聚合为氨所放出的热能可使4×108g冰变成水蒸气。
另外,核聚变产生的污染轻,不会造成放射性垃圾。因此,核聚变的和平利用将帮助人类长久地解决能源问题。
要使核聚变作为能源为人类服务,必须使核聚变产生的能量均匀地释放出来,也就是要进行受控核聚变反应。
目前受控核聚变反应的最大技术障碍是难以将核燃料加热到几千万甚至上亿摄氏度的高温。现在,科学家们正在探索在室温下实现受控核聚变的可能性。
核外电子排布
物质在化学反应中的表现与组成该物质的元素的原子结构有着密切的联系,其中核外电子扮演着非常重要的角色。电子在原子内有“广阔”的运动空间。在这“广阔”的空间里核外电子是怎样运动的呢
电子极其微小,即使使用最先进的扫描隧道显微镜(STM),也只能观察到排列有序紧密堆积的原子,而观察不到比原子小得多的电子。一个多世纪以来,科学家们主要采用建立模型的方法对核外电子的运动情况进行研究。
交流·研讨
请你查阅有关原子结构模型的资料,与同学们讨论电子在原子核外是怎样运动的。
现代物质结构理论认为,在含有多个电子的原子里,能量低的电子通常在离核较近的区域内运动,能量高的电子通常在离核较远的区域内运动。据此可以认为,电子是在原子核外距核由近及远、能量由低到高的不同电子层上分层排布的。
把能量最低、离核最近的电子层叫做第一层:能量稍高、离核稍远的电子层叫做第二层;由里往外依次类推,共有7个电子层。
科学研究表明:
每层最多容纳的电子数为 2n2 (n代表电子层数),而最外层电子数则不超过8个(第一层为最外层时,电子数不超过2个)。人们常用原子结构示意图来简明地表示电子在原子核外的分层排布情况。
经过分析发现,元素的性质与原子的最外层电子排布密切相关。
例如,稀有气体元素原子最外层电子数为8(氨除外,它的最外层只有2个电子),结构稳定,既不容易获得电子也不容易失去电子;
金属元素原子最外层电子数一般小于4,较易失去电子形成阳离子;
非金属元素原子最外层电子数一般大于或等于4,有较强的获得电子的倾向,活泼非金属元素的原子则较易获得电子形成阴离子。
化合价是元素的一种重要性质。元素的化合价的数值,与原子的电子层结构特别是最外层电子数有关。
例如,稀有气体元素原子核外电子排布已达稳定结构,既不容易获得电子也不容易失去电子,所以稀有气体元素通常表现为0价。
钠原子最外层只有1个电子,容易失去这个电子形成Nat而达到稳定结构,因此钠元素在化合物中显+1价:氯原子最外层有7个电子,只需获得1个电子形成 CI便可达到稳定结构,因此氯元素在化合物中常显-1价。
1.请你尝试画出钙原子(核电荷数为 20)和钾离子(核电荷数为19)的结构示意图。
交流·研讨
2。通过前面的学习你已经知道,金属钠、金属镁在化学反应中表现出还原性,而氧气、氯气在化学反应中表现出氧化性,你能用原子结构的知识对这一事实进行解释吗
3,你认为原子结构的知识对于理解物质结构和性质的关系有哪些帮助
1913年,玻尔在核式原子模型的基础上指出: 核外电子是处在一定的轨道上绕核运行的,正如太阳系的行星绕太阳运行一样:在核外运行的电子分层排布,按能量高低而距核远近不同。
资料在线
这个模型被称为“玻尔原子模型”。现代物质结构理论在新的实验基础上保留了玻尔原子模型合理的部分,并赋予其新的内容。
核外电子运动的特征
宏观物体的运动都有一定的轨迹,如人造卫星按一定的轨道围绕地球运行,而在原子核外运动的电子并不遵循宏观物体的运动规律。研究表明,电子在核外空间所处的位置及其运动速度不能同时准确地确定。
于是,人们采用统计的方法,对一个电子的多次行为或多个电子的一次行为进行研究,从而统计出电子在核外空间某处单位体积里出现机会的多少,并用电子云形象地进行表示。
概括整合
1.请用图示的方式描述构成原子的各种微粒与元素、核素间的关系,以及元素、核素与同位素间的关系。
2。核外电子排布是有一定规律的。那么,电子在核外是如何排布的 原子的最外层电子排布与元素的化学性质有什么关系
3,你认为研究原子结构有什么意义 请你列举核素在生产和生活中的应用
练习与活动
1,据报道,某些花岗岩会产生氡 ,从而对人体产生伤害。请回答
该原子的质量数是________,质子数是______,中子数是______
(2) 请将以下 Rn 的原子结构示意图补全。
(3)请根据 Rn 的原子结构预测氡气的化学性质
A。非常活泼,容易与氧气等非金属单质反应
B。比较活泼,能与钠等金属反应
C,不太活泼,与氮气性质相似
D,很难与其他物质发生反应
你选择该选项的理由是___________________________
(4)研究发现,镭能蜕变为,故将称为镭射气;钍能蜕变为,故将留称为钍射气;锕能蜕变为,故将称为锕射气。
( )
A.属于同种元素
B.互为同位素
C .属于同种核素
D .属于同种原子
由此可见,决定元素种类,决定核素种类。
2。你知道以下微粒结构示意图表示的各是什么微粒吗
3.请利用原子结构的知识解释下列事实。
(1)在硫化钠中,钠元素显+1价,硫元素显-2价
(2)钠原子和铝原子电子层数相同,但金属钠与氯气的反应要比金属铝与氯气的反应容易而且剧烈。
4,查阅资料并与同学们交流: 放射性同位素在能源、农业、医疗以及考古等方面有哪些应用
