安徽省滁州市定远县一初教育集团2023-2024学年九年级下学期开学检测化学试卷(无答案)
文档属性
| 名称 | 安徽省滁州市定远县一初教育集团2023-2024学年九年级下学期开学检测化学试卷(无答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 556.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-04 00:00:00 | ||
图片预览



文档简介
2023-2024学年九年级下学期开学检测化学试卷
第I卷(选择题)
一、选择题(共12分)
1.下列变化中,发生了化学变化的是( )
A.浓硫酸吸水 B.氢氧化钠潮解 C.生石灰吸水 D.浓盐酸挥发
2.现在我国的某些城市禁止燃放烟花爆竹,主要原因是防止
①空气污染 ②噪声污染 ③发生火灾 ④环境污染
A.①② B.①③ C.②③ D.①②③④
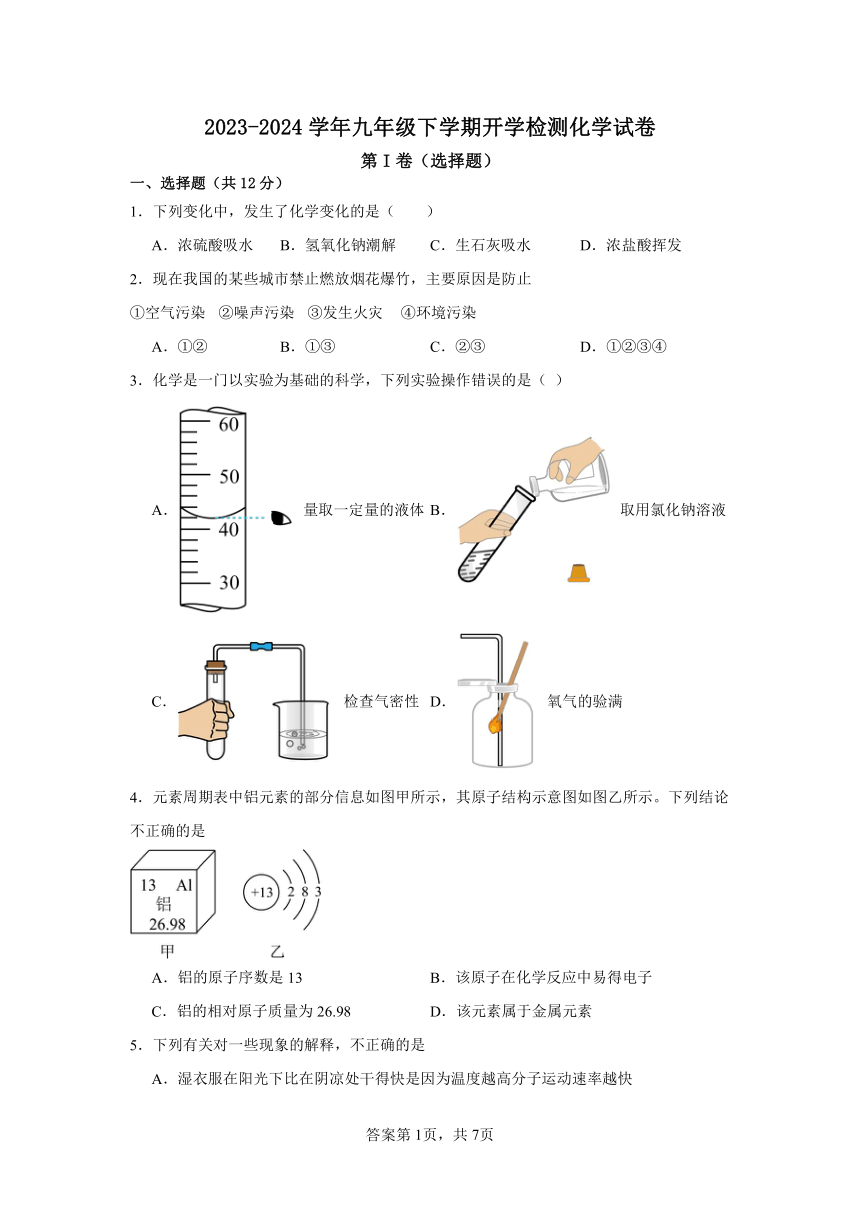
3.化学是一门以实验为基础的科学,下列实验操作错误的是( )
A. 量取一定量的液体 B. 取用氯化钠溶液
C. 检查气密性 D. 氧气的验满
4.元素周期表中铝元素的部分信息如图甲所示,其原子结构示意图如图乙所示。下列结论不正确的是
A.铝的原子序数是13 B.该原子在化学反应中易得电子
C.铝的相对原子质量为26.98 D.该元素属于金属元素
5.下列有关对一些现象的解释,不正确的是
A.湿衣服在阳光下比在阴凉处干得快是因为温度越高分子运动速率越快
B.物质具有热胀冷缩现象是因为分子或原子的大小可随温度的变化而变化
C.糖是甜的,醋是酸的是因为不同的物质分子具有不同的性质
D.水通电后可以产生氢气和氧气说明分子在化学反应中还可以再分
6.“归纳一推理”是重要的化学学习方法。下列选项正确的是
A.原子化学性质由最外层电子数决定,最外层电子数相同的原子化学性质一定相似
B.分子是保持物质化学性质的最小微粒,H2O和H2O2的分子不同则化学性质不同
C.单质是只含一种元素的纯净物,则只含一种元素的物质是单质
D.氧化物一定含氧元素,则含氧元素的物质一定是氧化物
7.如图装置可用于探究空气中氧气含量,若在实验过程中各连接气密性良好,弹簧夹始终打开,活塞可以自由移动,活塞移动位置不超过注射器的刻度范围。下列叙述正确的是
A.实验中过量的白磷、红磷的目的是为了使容器内的空气尽可能完全反应
B.实验过程中注射器活塞始终往内移动
C.反应后冷却至室温,整个装置内气体减少的体积约等于试管内空气体积的1/5
D.分别用过量的白磷、红磷做实验,都可以看到白烟,可得到相同的结论
8.下列有关溶液的叙述中错误的是
A.凡是均一、稳定的液体都是溶液
B.采用增加溶剂、减少溶质、改变温度等方法,可将饱和溶液转化为不饱和溶液
C.在一定温度下,将氯化钠的不饱和溶液转化为饱和溶液,溶液中溶质的质量分数增大
D.配制一定溶质质量分数溶液的实验步骤是计算、称量(量取)、溶解、装瓶
9.A~E是初中化学中的常见物质且都含有一种相同元素,它们之间的一步反应转化关系如图所示(部分反应物、生成物未标出)。其中,A通常为气体,B俗称纯碱,C是大理石的主要成分,E是一种单质。下列说法不正确的是
A.E的化学式为O2
B.D和E可以相互转化
C.A→E可通过光合作用来实现
D.B→C属于中和反应
10.含硫元素的同类物质中硫元素的化合价可能不同,不同类物质中硫元素的化合价可能相同,如表所示。下列判断正确的是
A.X表示碱
B.物质a在空气中燃烧会发出明亮的蓝紫色火焰
C.物质b是二氧化硫,它是空气污染物之一
D.物质d和NaOH溶液发生中和反应生成Na2SO4和H2O
11.二甲醚可以代替氟利昂作制冷剂,对臭氧层没有破坏作用,工业制备二甲醚(CH3OCH3)的化学方程式为,下列有关说法正确的是( )
A.该反应为化合反应
B.X的化学式为CO2
C.二甲醚碳元素的质量分数为26%
D.二甲醚中碳、氢、氧元素的质量比为2:6:1
12.下列实验设计能达到其对应实验目的的是
A.验证分子在不断运动
B.验证质量守恒定律
C.测定空气中氧气的含量
D.比较锌与铁的金属活动性强弱
第II卷(非选择题)
二、填空与简答(共10分)
13.(本题5分)氨气(NH3)的合成是人类科学技术上的重大突破。如图是工业合成氨工艺的主要流程。
(1)氨分离器能将沸点不同的气体分离开来,该过程属于 (填“物理”或“化学”)变化。
(2)流程中能循环使用的物质是 。
(3)合成塔中的反应必须在高温、高压并使用催化剂的条件下进行。该反应的化学方程式为 。
(4)NH3可以进一步制得尿素和碳酸氢铵等化肥。如图是某商店内尿素肥料的标签。
①从标签上看,碳酸氢铵不同于尿素的化学性质是 。
②经计算,尿素【CO(NH2)2】中含氮量为46.7%,则该袋尿素肥料属于 (填“纯净物”或“混合物”)
14.(本题5分)眼镜是人们常用的护眼工具,如图是一款变色眼镜的示意图。请回答下列问题。
(1)图中所标物质属于金属材料的是 (填序号),属于有机合成材料的是 (填序号)。
(2)变色眼镜的玻璃里加入了溴化银(AgBr)。在强光照射下,溴化银分解成单质溴(Br2)和银,玻璃颜色变深,该反应的化学方程式为 。
(3)玻璃镜片与纯铜片互相刻画,纯铜片上留下明显的划痕,说明 。
三、实验题(共6分)
15.(本题6分)下图是初中化学中常见的四个基本实验,请回答下列问题。
(1)图A是利用燃烧法测定空气中氧气含量的实验装置,利用该实验,可以得出有关氧气含量的结论是 ,如果测得的结果偏低,可能的原因之一是 。
(2)图B实验中酒精灯加网罩的作用 。
(3)图C实验中铜片两侧分别放有同样大小的乒乓球碎片和滤纸碎片,观察到乒乓球碎片先燃烧,由此可以得出燃烧的条件之一是 。
(4)图D实验中的错误是 ,称取氯化钠的实际质量为 g。
四、科学探究题(共6分)
16.(本题6分)某化学兴趣小组对用过氧化氢分解生成水和氧气的实验条件进行探究。
【提出问题】哪些因素可能影响该反应的反应速率?
【查阅资料】影响化学反应速率的因素:
①主要因素:反应物本身的性质;
②外界因素:温度,浓度,压强,催化剂,光,激光,反应物颗粒大小,反应物之间的接触面积和反应物状态;
③另外,x射线,γ射线也会影响化学反应速率。
【作出猜想】下面是小组内三位同学所做的猜想,请你完成小丽的猜想。
小红同学:H2O2溶液的浓度可能影响该反应的反应速率。
小明同学:催化剂(MnO2)的用量可能影响该反应的反应速率.
小丽同学:我认为 可能影响该反应的反应速率。
【实验验证】
实验次序 1 2 3 4 5
H2O2溶液浓度 1% 5% 15% 25% 30%
所用时间(秒) 660 205 25 4 3
(1)小红同学的实验是:每次均取10mL30%的H2O2溶液,然后稀释成不同浓度的溶液进行实验,测定各次收集到100mL氧气时所用的时间,记录数据如表:(其他实验条件:温度、催化剂用量等均相同)
请你分析回答:H2O2溶液的浓度对过氧化氢分解制氧气反应速率有什么影响?
(2)小明同学的实验是:每次均用30mL10%的H2O2溶液,采用不同量MnO2粉末做催化剂,测定各次收集到500mL氧气时所用的时间,结果如表:(其他实验条件:过氧化氢溶液浓度、温度等均相同)
实验次序 1 2 3 4 5
MnO2粉末用量(克) 0.2 0.4 0.6 0.8 1.0
所用时间(秒) 8 5 3 2 2
请你分析回答:该反应的化学方程式为 ;催化剂MnO2的用量对过氧化氢分解制氧气反应速率有什么影响?
(3)如果你是小丽同学,在验证你的猜想时,你的实验方案是: 。
【反思与交流】通过该探究实验,你还想探究的问题或还想学习的知识是 。
五、计算题(共6分)
17.(本题6分)鸡蛋壳的主要成分是碳酸钙.某兴趣小组为了测定鸡蛋壳中碳酸钙的含量,现取15g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除碳酸钙外的其他成分不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所有盐酸刚好消耗了加入量的一半.试计算:
(1)生成二氧化碳的质量____.
(2)所用稀盐酸中溶质的质量分数.试卷第6页,共7页
试卷第7页,共7页
答案第2页,共7页
答案第1页,共1页
第I卷(选择题)
一、选择题(共12分)
1.下列变化中,发生了化学变化的是( )
A.浓硫酸吸水 B.氢氧化钠潮解 C.生石灰吸水 D.浓盐酸挥发
2.现在我国的某些城市禁止燃放烟花爆竹,主要原因是防止
①空气污染 ②噪声污染 ③发生火灾 ④环境污染
A.①② B.①③ C.②③ D.①②③④
3.化学是一门以实验为基础的科学,下列实验操作错误的是( )
A. 量取一定量的液体 B. 取用氯化钠溶液
C. 检查气密性 D. 氧气的验满
4.元素周期表中铝元素的部分信息如图甲所示,其原子结构示意图如图乙所示。下列结论不正确的是
A.铝的原子序数是13 B.该原子在化学反应中易得电子
C.铝的相对原子质量为26.98 D.该元素属于金属元素
5.下列有关对一些现象的解释,不正确的是
A.湿衣服在阳光下比在阴凉处干得快是因为温度越高分子运动速率越快
B.物质具有热胀冷缩现象是因为分子或原子的大小可随温度的变化而变化
C.糖是甜的,醋是酸的是因为不同的物质分子具有不同的性质
D.水通电后可以产生氢气和氧气说明分子在化学反应中还可以再分
6.“归纳一推理”是重要的化学学习方法。下列选项正确的是
A.原子化学性质由最外层电子数决定,最外层电子数相同的原子化学性质一定相似
B.分子是保持物质化学性质的最小微粒,H2O和H2O2的分子不同则化学性质不同
C.单质是只含一种元素的纯净物,则只含一种元素的物质是单质
D.氧化物一定含氧元素,则含氧元素的物质一定是氧化物
7.如图装置可用于探究空气中氧气含量,若在实验过程中各连接气密性良好,弹簧夹始终打开,活塞可以自由移动,活塞移动位置不超过注射器的刻度范围。下列叙述正确的是
A.实验中过量的白磷、红磷的目的是为了使容器内的空气尽可能完全反应
B.实验过程中注射器活塞始终往内移动
C.反应后冷却至室温,整个装置内气体减少的体积约等于试管内空气体积的1/5
D.分别用过量的白磷、红磷做实验,都可以看到白烟,可得到相同的结论
8.下列有关溶液的叙述中错误的是
A.凡是均一、稳定的液体都是溶液
B.采用增加溶剂、减少溶质、改变温度等方法,可将饱和溶液转化为不饱和溶液
C.在一定温度下,将氯化钠的不饱和溶液转化为饱和溶液,溶液中溶质的质量分数增大
D.配制一定溶质质量分数溶液的实验步骤是计算、称量(量取)、溶解、装瓶
9.A~E是初中化学中的常见物质且都含有一种相同元素,它们之间的一步反应转化关系如图所示(部分反应物、生成物未标出)。其中,A通常为气体,B俗称纯碱,C是大理石的主要成分,E是一种单质。下列说法不正确的是
A.E的化学式为O2
B.D和E可以相互转化
C.A→E可通过光合作用来实现
D.B→C属于中和反应
10.含硫元素的同类物质中硫元素的化合价可能不同,不同类物质中硫元素的化合价可能相同,如表所示。下列判断正确的是
A.X表示碱
B.物质a在空气中燃烧会发出明亮的蓝紫色火焰
C.物质b是二氧化硫,它是空气污染物之一
D.物质d和NaOH溶液发生中和反应生成Na2SO4和H2O
11.二甲醚可以代替氟利昂作制冷剂,对臭氧层没有破坏作用,工业制备二甲醚(CH3OCH3)的化学方程式为,下列有关说法正确的是( )
A.该反应为化合反应
B.X的化学式为CO2
C.二甲醚碳元素的质量分数为26%
D.二甲醚中碳、氢、氧元素的质量比为2:6:1
12.下列实验设计能达到其对应实验目的的是
A.验证分子在不断运动
B.验证质量守恒定律
C.测定空气中氧气的含量
D.比较锌与铁的金属活动性强弱
第II卷(非选择题)
二、填空与简答(共10分)
13.(本题5分)氨气(NH3)的合成是人类科学技术上的重大突破。如图是工业合成氨工艺的主要流程。
(1)氨分离器能将沸点不同的气体分离开来,该过程属于 (填“物理”或“化学”)变化。
(2)流程中能循环使用的物质是 。
(3)合成塔中的反应必须在高温、高压并使用催化剂的条件下进行。该反应的化学方程式为 。
(4)NH3可以进一步制得尿素和碳酸氢铵等化肥。如图是某商店内尿素肥料的标签。
①从标签上看,碳酸氢铵不同于尿素的化学性质是 。
②经计算,尿素【CO(NH2)2】中含氮量为46.7%,则该袋尿素肥料属于 (填“纯净物”或“混合物”)
14.(本题5分)眼镜是人们常用的护眼工具,如图是一款变色眼镜的示意图。请回答下列问题。
(1)图中所标物质属于金属材料的是 (填序号),属于有机合成材料的是 (填序号)。
(2)变色眼镜的玻璃里加入了溴化银(AgBr)。在强光照射下,溴化银分解成单质溴(Br2)和银,玻璃颜色变深,该反应的化学方程式为 。
(3)玻璃镜片与纯铜片互相刻画,纯铜片上留下明显的划痕,说明 。
三、实验题(共6分)
15.(本题6分)下图是初中化学中常见的四个基本实验,请回答下列问题。
(1)图A是利用燃烧法测定空气中氧气含量的实验装置,利用该实验,可以得出有关氧气含量的结论是 ,如果测得的结果偏低,可能的原因之一是 。
(2)图B实验中酒精灯加网罩的作用 。
(3)图C实验中铜片两侧分别放有同样大小的乒乓球碎片和滤纸碎片,观察到乒乓球碎片先燃烧,由此可以得出燃烧的条件之一是 。
(4)图D实验中的错误是 ,称取氯化钠的实际质量为 g。
四、科学探究题(共6分)
16.(本题6分)某化学兴趣小组对用过氧化氢分解生成水和氧气的实验条件进行探究。
【提出问题】哪些因素可能影响该反应的反应速率?
【查阅资料】影响化学反应速率的因素:
①主要因素:反应物本身的性质;
②外界因素:温度,浓度,压强,催化剂,光,激光,反应物颗粒大小,反应物之间的接触面积和反应物状态;
③另外,x射线,γ射线也会影响化学反应速率。
【作出猜想】下面是小组内三位同学所做的猜想,请你完成小丽的猜想。
小红同学:H2O2溶液的浓度可能影响该反应的反应速率。
小明同学:催化剂(MnO2)的用量可能影响该反应的反应速率.
小丽同学:我认为 可能影响该反应的反应速率。
【实验验证】
实验次序 1 2 3 4 5
H2O2溶液浓度 1% 5% 15% 25% 30%
所用时间(秒) 660 205 25 4 3
(1)小红同学的实验是:每次均取10mL30%的H2O2溶液,然后稀释成不同浓度的溶液进行实验,测定各次收集到100mL氧气时所用的时间,记录数据如表:(其他实验条件:温度、催化剂用量等均相同)
请你分析回答:H2O2溶液的浓度对过氧化氢分解制氧气反应速率有什么影响?
(2)小明同学的实验是:每次均用30mL10%的H2O2溶液,采用不同量MnO2粉末做催化剂,测定各次收集到500mL氧气时所用的时间,结果如表:(其他实验条件:过氧化氢溶液浓度、温度等均相同)
实验次序 1 2 3 4 5
MnO2粉末用量(克) 0.2 0.4 0.6 0.8 1.0
所用时间(秒) 8 5 3 2 2
请你分析回答:该反应的化学方程式为 ;催化剂MnO2的用量对过氧化氢分解制氧气反应速率有什么影响?
(3)如果你是小丽同学,在验证你的猜想时,你的实验方案是: 。
【反思与交流】通过该探究实验,你还想探究的问题或还想学习的知识是 。
五、计算题(共6分)
17.(本题6分)鸡蛋壳的主要成分是碳酸钙.某兴趣小组为了测定鸡蛋壳中碳酸钙的含量,现取15g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除碳酸钙外的其他成分不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所有盐酸刚好消耗了加入量的一半.试计算:
(1)生成二氧化碳的质量____.
(2)所用稀盐酸中溶质的质量分数.试卷第6页,共7页
试卷第7页,共7页
答案第2页,共7页
答案第1页,共1页
同课章节目录
