2023--2024学年九年级化学鲁教版下册第七单元常见的酸和碱分层题(含答案)
文档属性
| 名称 | 2023--2024学年九年级化学鲁教版下册第七单元常见的酸和碱分层题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 513.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-04 00:00:00 | ||
图片预览



文档简介
第七单元 常见的酸和碱 分层题(含答案)2023—2024学年鲁教版化学九年级下册
一、选择题。
1、下列实验现象描述错误的是( )
A.氢气在空气燃烧产生淡蓝色火焰
B.打开盛放浓盐酸的试剂瓶瓶塞,瓶口出现白雾
C.将燃着的木炭伸入氧气中,产生白色火焰,放出热量,生成二氧化碳气体
D.将一氧化碳通过灼热的氧化铜,黑色粉末逐渐变为红色
2、下列物质中,属于碱的是( )
A. B. C. D.
3、“检测土壤浸出液的酸碱性”实验操作示意图如下,其中不正确的是( )
A.土壤加水搅拌 B.过滤
C.检验酸碱性 D.测定pH
4、向石蕊试液中通入二氧化碳气体,再进行加热,溶液颜色变化顺序正确的是( )
A.红色——紫色——红色 B.紫色——红色——紫色
C.红色——紫色——蓝色 D.红色——无色——红色
5、下列检测某溶液pH的操作正确的是( )
A.将pH试纸投入待测液,对照标准比色卡读数
B.用干燥、洁净的玻璃棒蘸取少量待测液,沾在置于洁净表面皿的pH试纸上,半分钟内根据试纸呈现颜色,对照标准比色卡读数
C.用玻璃棒蘸取待测液沾在用蒸馏水润湿的pH试纸上.对照标准比色卡读数
D.用玻璃棒蘸取待测液沾在pH试纸上,3分钟后对照标准比色卡读数
6、对实验现象、过程的描述都正确的是( )
A.硫在空气中点燃发出黄光、放出热量
B.铁粉在空气中加热剧烈燃烧、生成黑色固体
C.浓硫酸敞口放置溶液的颜色、质量不变
D.烧碱固体放入水中迅速溶解、溶液温度升高
7、下列关于盐酸的描述,错误的是( )
A.浓盐酸有刺激性气味
B.盐酸具有强烈的吸水性
C.盐酸是氯化氢气体的水溶液
D.打开装有浓盐酸的试剂瓶,瓶口处有白雾
8、下列物质中能与澄清石灰水反应,但反应若不加指示剂则无明显现象的是( )
A.氯化铜溶液 B.碳酸钠溶液 C.氯化镁溶液 D.稀盐酸
9、用滤纸做成的小花喷洒某无色溶液后放在如图位置,片刻后变成红色。请推测喷洒液和小烧杯中a溶液分别可能是( )
A.酚酞试液和浓氨水 B.酚酞试液和pH<7的溶液
C.石蕊试液和浓硫酸 D.石蕊试液和浓盐酸
10、某电镀厂排出污水的,并含有硫酸铜,要除去有毒的硫酸铜,同时调节至中性,可选用下列物质中的( )
A.生石灰 B.氯化钡 C.硝酸银 D.碳酸钙
11、往KOH溶液中加水,溶液的pH变化正确的是( )
A. B.
C. D.
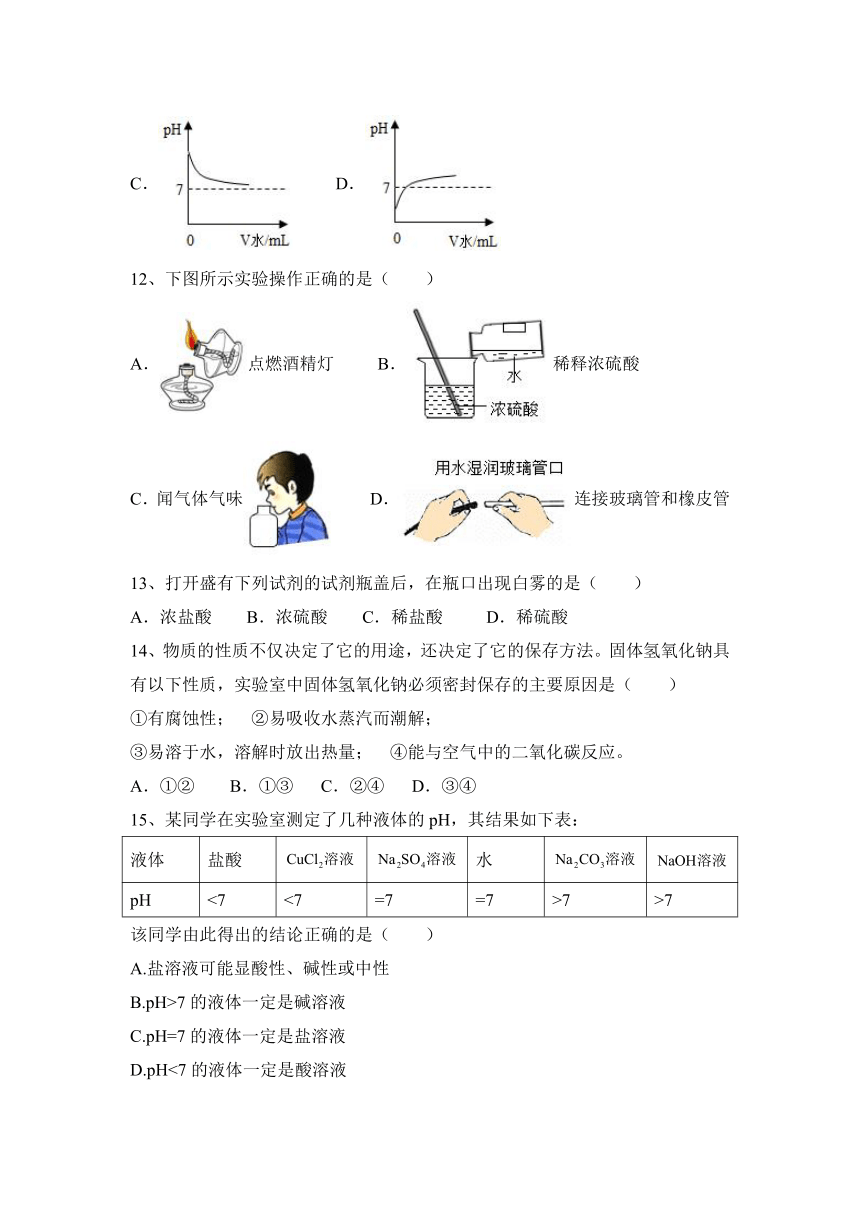
12、下图所示实验操作正确的是( )
A.点燃酒精灯 B.稀释浓硫酸
C.闻气体气味 D.连接玻璃管和橡皮管
13、打开盛有下列试剂的试剂瓶盖后,在瓶口出现白雾的是( )
A.浓盐酸 B.浓硫酸 C.稀盐酸 D.稀硫酸
14、物质的性质不仅决定了它的用途,还决定了它的保存方法。固体氢氧化钠具有以下性质,实验室中固体氢氧化钠必须密封保存的主要原因是( )
①有腐蚀性; ②易吸收水蒸汽而潮解;
③易溶于水,溶解时放出热量; ④能与空气中的二氧化碳反应。
A.①② B.①③ C.②④ D.③④
15、某同学在实验室测定了几种液体的pH,其结果如下表:
液体 盐酸 水
pH <7 <7 =7 =7 >7 >7
该同学由此得出的结论正确的是( )
A.盐溶液可能显酸性、碱性或中性
B.pH>7的液体一定是碱溶液
C.pH=7的液体一定是盐溶液
D.pH<7的液体一定是酸溶液
16、某化工厂发生硫酸泄漏事件,为了减少硫酸对环境的污染,有关部门采取了紧急措施,在泄漏的硫酸上面喷洒了一种化学试剂。你认为这种试剂可能是( )
A.熟石灰 B.硫酸铜 C.食盐 D.干冰
二、填空题。
17、能源和环境与人类的生活和社会发展密切相关。
(1)化石燃料是不可再生能源,包括煤、石油和_________;大量使用煤、石油等化石燃料会产生_________、NO2等污染物,这些污染物在空气中会形成_________,破坏环境。
(2)物质发生化学反应的同时,常伴随着能量的变化,能量的变化通常表现为热量的变化。下列各组物质在一定条件下能够发生化学反应,且放出热量的是_________。(填字母序号)
A 浓硫酸与水 B 镁与盐酸 C 碳与氧气 D 碳与氧化铜
(3)在研究可燃物的燃烧条件时,某同学对教材中的实验做了改进,并用如图所示装置进行实验。
①试判断能够燃烧的是图中的__________(填“a”、“b”或“c”)处,该处燃着的磷会很快熄灭,原因可能是_________ 。
②如图所示的实验与教材中探究燃烧的条件的实验相比,具有的优点是_________ (写一条即可)。
18、“化学是在分子、原子层次上研究物质的性质、组成,结构与变化规律的科学”。请根据你对“化学”这门科学的认识解答以下问题:
(1)通过电解水的实验。可以推断水是由___________(填元素符号)元素组成。
(2)金刚石和石墨组成元素相同,而它们的物理性质却有很大差异,其微观解释是___________ 。
(3)以下物质用途主要是由其物理性质决定的是___________(填序号)。
①氢气填充探空气球 ②氢氧化钠干燥气体
③天然气作燃料 ④用铜制作导线
(4)N2、NH3、HNO3等都是常见的含氮物质,其中氮元素化合价最低的物质是:
___________。
19、有CO2、N2、O2三种气体,能让燃着的木条燃烧更旺的是___。小柯将二氧化碳气体通入滴有紫色石蕊试液的水中,他可能要探究的问题是___,所得溶液的pH___7(选填“<”、“=”或“>”)
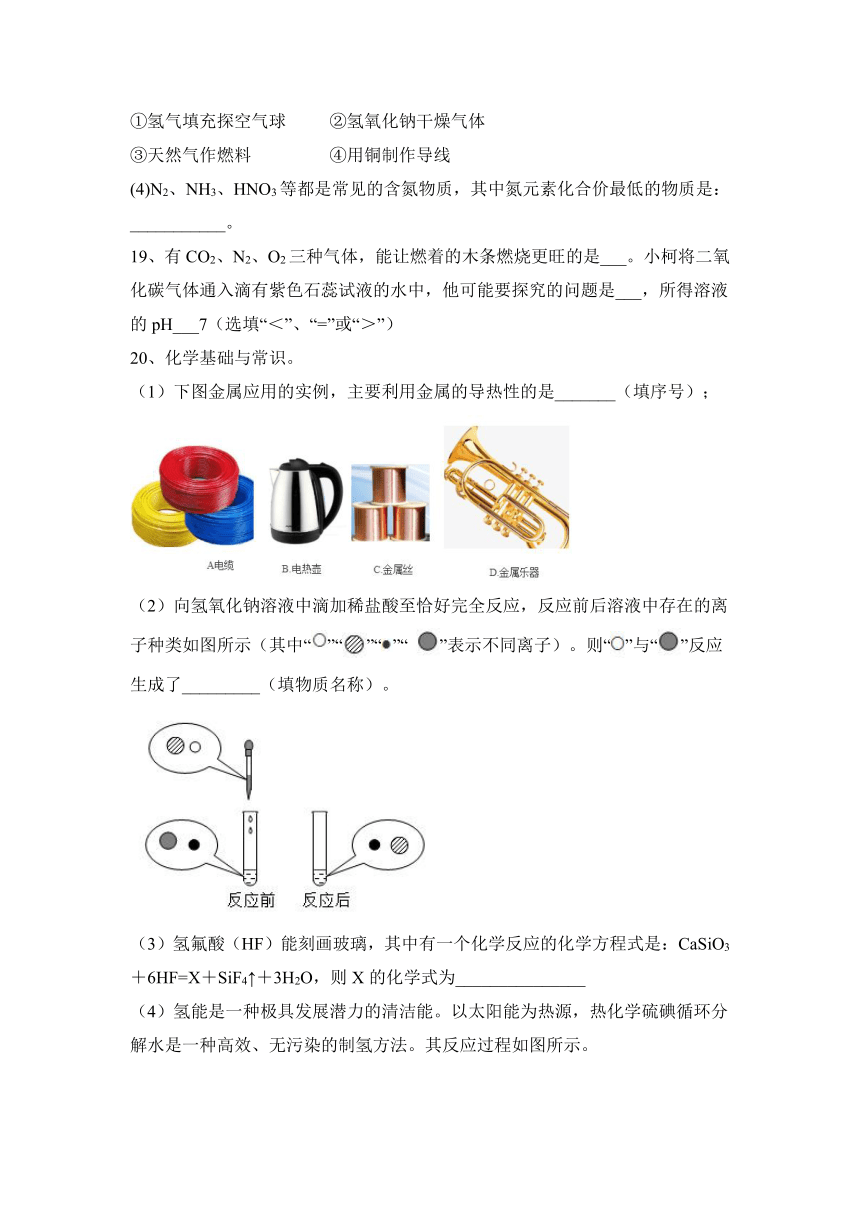
20、化学基础与常识。
(1)下图金属应用的实例,主要利用金属的导热性的是_______(填序号);
(2)向氢氧化钠溶液中滴加稀盐酸至恰好完全反应,反应前后溶液中存在的离子种类如图所示(其中“”“”“”“ ”表示不同离子)。则“”与“”反应生成了_________(填物质名称)。
(3)氢氟酸(HF)能刻画玻璃,其中有一个化学反应的化学方程式是:CaSiO3+6HF=X+SiF4↑+3H2O,则X的化学式为_______________
(4)氢能是一种极具发展潜力的清洁能。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如图所示。
写出反应I中,发生反应的化学方程式:_____________________________。
21、氢氧化钠中混有少量氢氧化钙杂质,用方程式表示除去的方法:_______________ 。
22、某食品包装袋中有一个小纸袋,上面写着“生石灰干燥剂, 请勿食用”。该食品已放置两个月有余。请你对下列问题进行探究。
(1)小纸袋中的物质能否继续作干燥剂?
实验步骤 实验现象 结论
取足量的小纸袋中的固体放入烧杯中,加入适量的水,触摸杯壁 。 可继续作干燥剂
(2)猜想:小纸袋中的物质除含有CaO外,还可能含有Ca(OH)2和 。
(3)请设计实验证明(2)中你所填的物质是否存在。
。
三、实验题。
23、某化学实验小组欲探究盐酸、氢氧化钙的化学性质,取8支试管分别用A-H编号后,做如下实验.
(1)实验中观察到有气泡出现的试管是 ,有沉淀生成的试管是 。
(2)实验后某试管中为红色溶液,当向其中加入过量的NaOH溶液后,溶液变为蓝色.由此推断,该试管中最初盛有的物质是 。
(3)实验后某试管的底部有白色固体,过滤后向滤液中滴加盐酸,一段时间后有气泡冒出,则该滤液中的溶质是 。
24、维生素C又名抗坏血酸,易溶于水,易被氧化,遇热易被破坏。人体缺乏维生素C可能引发多种疾病。甲班化学兴趣小组对它研究如下:
(1)猜想:维生素C可能具有酸性。
(2)设计实验:
实验室提供试剂:维生素C片、蒸馏水、紫色石蕊试液、酚酞试液、稀NaOH溶液和相关仪器。
方案1:将维生素C片研碎、溶于蒸馏水制成溶液,然后向其中滴加紫色石蕊试液。
①实验现象为_____ ,说明维生素C显酸性。
②如果要加速维生素C片在水中的溶解,操作方法是_____ 。
方案2:①将维生素C片溶于蒸馏水制成溶液。
②取少量稀NaOH溶液于试管中,加入两滴酚酞试液,观察溶液呈_____色,然后向其中逐滴加入足量维生素C溶液振荡,直至溶液颜色变为_____色。结论:维生素C显酸性。
(3)继续探究:运用酸的化学性质的知识,你还可用什么实验证明维生素C具有酸性?简述实验方法_____ (要求与上述两种实验方法不相似)。
四、计算题。
25、某纯碱样品中含有杂质NaCl,为测定该样品中Na2CO3的质量分数,称取纯碱样品15 g,向其中逐渐加入稀盐酸,如图是产生的气体质量与加入稀盐酸质量的关系图。
(1)样品中Na2CO3的质量分数是 。
(2)当加入稀盐酸80.0 g时,所得溶液中Na+的质量为 。(结果保留一位小数)
(3)恰好反应后所得溶液中溶质的质量分数。(写出计算过程,结果保留一位小数)
第七单元 常见的酸和碱 分层题(含答案)2023—2024学年鲁教版化学九年级下册
一、选择题。
1、下列实验现象描述错误的是( )
A.氢气在空气燃烧产生淡蓝色火焰
B.打开盛放浓盐酸的试剂瓶瓶塞,瓶口出现白雾
C.将燃着的木炭伸入氧气中,产生白色火焰,放出热量,生成二氧化碳气体
D.将一氧化碳通过灼热的氧化铜,黑色粉末逐渐变为红色
【答案】C
2、下列物质中,属于碱的是( )
A. B. C. D.
【答案】A
3、“检测土壤浸出液的酸碱性”实验操作示意图如下,其中不正确的是( )
A.土壤加水搅拌 B.过滤
C.检验酸碱性 D.测定pH
【答案】C
4、向石蕊试液中通入二氧化碳气体,再进行加热,溶液颜色变化顺序正确的是( )
A.红色——紫色——红色 B.紫色——红色——紫色
C.红色——紫色——蓝色 D.红色——无色——红色
【答案】B
5、下列检测某溶液pH的操作正确的是( )
A.将pH试纸投入待测液,对照标准比色卡读数
B.用干燥、洁净的玻璃棒蘸取少量待测液,沾在置于洁净表面皿的pH试纸上,半分钟内根据试纸呈现颜色,对照标准比色卡读数
C.用玻璃棒蘸取待测液沾在用蒸馏水润湿的pH试纸上.对照标准比色卡读数
D.用玻璃棒蘸取待测液沾在pH试纸上,3分钟后对照标准比色卡读数
【答案】B
6、对实验现象、过程的描述都正确的是( )
A.硫在空气中点燃发出黄光、放出热量
B.铁粉在空气中加热剧烈燃烧、生成黑色固体
C.浓硫酸敞口放置溶液的颜色、质量不变
D.烧碱固体放入水中迅速溶解、溶液温度升高
【答案】D
7、下列关于盐酸的描述,错误的是( )
A.浓盐酸有刺激性气味
B.盐酸具有强烈的吸水性
C.盐酸是氯化氢气体的水溶液
D.打开装有浓盐酸的试剂瓶,瓶口处有白雾
【答案】B
8、下列物质中能与澄清石灰水反应,但反应若不加指示剂则无明显现象的是( )
A.氯化铜溶液 B.碳酸钠溶液 C.氯化镁溶液 D.稀盐酸
【答案】D
9、用滤纸做成的小花喷洒某无色溶液后放在如图位置,片刻后变成红色。请推测喷洒液和小烧杯中a溶液分别可能是( )
A.酚酞试液和浓氨水 B.酚酞试液和pH<7的溶液
C.石蕊试液和浓硫酸 D.石蕊试液和浓盐酸
【答案】A
10、某电镀厂排出污水的,并含有硫酸铜,要除去有毒的硫酸铜,同时调节至中性,可选用下列物质中的( )
A.生石灰 B.氯化钡 C.硝酸银 D.碳酸钙
【答案】A
11、往KOH溶液中加水,溶液的pH变化正确的是( )
A. B.
C. D.
【答案】C
12、下图所示实验操作正确的是( )
A.点燃酒精灯 B.稀释浓硫酸
C.闻气体气味 D.连接玻璃管和橡皮管
【答案】D
13、打开盛有下列试剂的试剂瓶盖后,在瓶口出现白雾的是( )
A.浓盐酸 B.浓硫酸 C.稀盐酸 D.稀硫酸
【答案】A
14、物质的性质不仅决定了它的用途,还决定了它的保存方法。固体氢氧化钠具有以下性质,实验室中固体氢氧化钠必须密封保存的主要原因是( )
①有腐蚀性; ②易吸收水蒸汽而潮解;
③易溶于水,溶解时放出热量; ④能与空气中的二氧化碳反应。
A.①② B.①③ C.②④ D.③④
【答案】C
15、某同学在实验室测定了几种液体的pH,其结果如下表:
液体 盐酸 水
pH <7 <7 =7 =7 >7 >7
该同学由此得出的结论正确的是( )
A.盐溶液可能显酸性、碱性或中性
B.pH>7的液体一定是碱溶液
C.pH=7的液体一定是盐溶液
D.pH<7的液体一定是酸溶液
【答案】A
16、某化工厂发生硫酸泄漏事件,为了减少硫酸对环境的污染,有关部门采取了紧急措施,在泄漏的硫酸上面喷洒了一种化学试剂。你认为这种试剂可能是( )
A.熟石灰 B.硫酸铜 C.食盐 D.干冰
【答案】A
二、填空题。
17、能源和环境与人类的生活和社会发展密切相关。
(1)化石燃料是不可再生能源,包括煤、石油和_________;大量使用煤、石油等化石燃料会产生_________、NO2等污染物,这些污染物在空气中会形成_________,破坏环境。
(2)物质发生化学反应的同时,常伴随着能量的变化,能量的变化通常表现为热量的变化。下列各组物质在一定条件下能够发生化学反应,且放出热量的是_________。(填字母序号)
A 浓硫酸与水 B 镁与盐酸 C 碳与氧气 D 碳与氧化铜
(3)在研究可燃物的燃烧条件时,某同学对教材中的实验做了改进,并用如图所示装置进行实验。
①试判断能够燃烧的是图中的__________(填“a”、“b”或“c”)处,该处燃着的磷会很快熄灭,原因可能是_________ 。
②如图所示的实验与教材中探究燃烧的条件的实验相比,具有的优点是_________ (写一条即可)。
【答案】(1)天然气 SO2 酸雨 (2)BC
(3)a 氧气不足或被耗尽 装置简单(操作方便或污染小等)
18、“化学是在分子、原子层次上研究物质的性质、组成,结构与变化规律的科学”。请根据你对“化学”这门科学的认识解答以下问题:
(1)通过电解水的实验。可以推断水是由___________(填元素符号)元素组成。
(2)金刚石和石墨组成元素相同,而它们的物理性质却有很大差异,其微观解释是___________ 。
(3)以下物质用途主要是由其物理性质决定的是___________(填序号)。
①氢气填充探空气球 ②氢氧化钠干燥气体
③天然气作燃料 ④用铜制作导线
(4)N2、NH3、HNO3等都是常见的含氮物质,其中氮元素化合价最低的物质是:
___________。
【答案】(1)H、O (2)碳原子的排列方式不同 (3)①②④ (4)NH3/氨气
19、有CO2、N2、O2三种气体,能让燃着的木条燃烧更旺的是___。小柯将二氧化碳气体通入滴有紫色石蕊试液的水中,他可能要探究的问题是___,所得溶液的pH___7(选填“<”、“=”或“>”)
【答案】氧气 二氧化碳是否能与水反应 <
20、化学基础与常识。
(1)下图金属应用的实例,主要利用金属的导热性的是_______(填序号);
(2)向氢氧化钠溶液中滴加稀盐酸至恰好完全反应,反应前后溶液中存在的离子种类如图所示(其中“”“”“”“ ”表示不同离子)。则“”与“”反应生成了_________(填物质名称)。
(3)氢氟酸(HF)能刻画玻璃,其中有一个化学反应的化学方程式是:CaSiO3+6HF=X+SiF4↑+3H2O,则X的化学式为_______________
(4)氢能是一种极具发展潜力的清洁能。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如图所示。
写出反应I中,发生反应的化学方程式:_____________________________。
【答案】 (1) B (2)水 (3)CaF2
(4)SO2+I2+2H2O=H2SO4+2HI
21、氢氧化钠中混有少量氢氧化钙杂质,用方程式表示除去的方法:_______________ 。
【答案】NaCO+Ca(OH)=====2NaOH+CaCO↓
22、某食品包装袋中有一个小纸袋,上面写着“生石灰干燥剂, 请勿食用”。该食品已放置两个月有余。请你对下列问题进行探究。
(1)小纸袋中的物质能否继续作干燥剂?
实验步骤 实验现象 结论
取足量的小纸袋中的固体放入烧杯中,加入适量的水,触摸杯壁 。 可继续作干燥剂
(2)猜想:小纸袋中的物质除含有CaO外,还可能含有Ca(OH)2和 。
(3)请设计实验证明(2)中你所填的物质是否存在。
。
【答案】烧杯壁发热 CaCO3
将小纸袋中的固体加入到足量的稀盐酸中,若产生能使澄清石灰水变浑浊的气体,则证明有CaCO3,否则没有。
三、实验题。
23、某化学实验小组欲探究盐酸、氢氧化钙的化学性质,取8支试管分别用A-H编号后,做如下实验.
(1)实验中观察到有气泡出现的试管是 ,有沉淀生成的试管是 。
(2)实验后某试管中为红色溶液,当向其中加入过量的NaOH溶液后,溶液变为蓝色.由此推断,该试管中最初盛有的物质是 。
(3)实验后某试管的底部有白色固体,过滤后向滤液中滴加盐酸,一段时间后有气泡冒出,则该滤液中的溶质是 。
【答案】(1)AC,EH; (2)石蕊试液; (3)NaOH和Na2CO3
24、维生素C又名抗坏血酸,易溶于水,易被氧化,遇热易被破坏。人体缺乏维生素C可能引发多种疾病。甲班化学兴趣小组对它研究如下:
(1)猜想:维生素C可能具有酸性。
(2)设计实验:
实验室提供试剂:维生素C片、蒸馏水、紫色石蕊试液、酚酞试液、稀NaOH溶液和相关仪器。
方案1:将维生素C片研碎、溶于蒸馏水制成溶液,然后向其中滴加紫色石蕊试液。
①实验现象为_____ ,说明维生素C显酸性。
②如果要加速维生素C片在水中的溶解,操作方法是_____ 。
方案2:①将维生素C片溶于蒸馏水制成溶液。
②取少量稀NaOH溶液于试管中,加入两滴酚酞试液,观察溶液呈_____色,然后向其中逐滴加入足量维生素C溶液振荡,直至溶液颜色变为_____色。结论:维生素C显酸性。
(3)继续探究:运用酸的化学性质的知识,你还可用什么实验证明维生素C具有酸性?简述实验方法_____ (要求与上述两种实验方法不相似)。
【答案】(1)显红色 (2)搅拌或振荡 (3)红 无
(4)在维生素C溶液中加入金属镁或Na2CO3有气泡产生
四、计算题。
25、某纯碱样品中含有杂质NaCl,为测定该样品中Na2CO3的质量分数,称取纯碱样品15 g,向其中逐渐加入稀盐酸,如图是产生的气体质量与加入稀盐酸质量的关系图。
(1)样品中Na2CO3的质量分数是 。
(2)当加入稀盐酸80.0 g时,所得溶液中Na+的质量为 。(结果保留一位小数)
(3)恰好反应后所得溶液中溶质的质量分数。(写出计算过程,结果保留一位小数)
【答案】(1)70.7%; (2)6.3 g; (3)22.8%
一、选择题。
1、下列实验现象描述错误的是( )
A.氢气在空气燃烧产生淡蓝色火焰
B.打开盛放浓盐酸的试剂瓶瓶塞,瓶口出现白雾
C.将燃着的木炭伸入氧气中,产生白色火焰,放出热量,生成二氧化碳气体
D.将一氧化碳通过灼热的氧化铜,黑色粉末逐渐变为红色
2、下列物质中,属于碱的是( )
A. B. C. D.
3、“检测土壤浸出液的酸碱性”实验操作示意图如下,其中不正确的是( )
A.土壤加水搅拌 B.过滤
C.检验酸碱性 D.测定pH
4、向石蕊试液中通入二氧化碳气体,再进行加热,溶液颜色变化顺序正确的是( )
A.红色——紫色——红色 B.紫色——红色——紫色
C.红色——紫色——蓝色 D.红色——无色——红色
5、下列检测某溶液pH的操作正确的是( )
A.将pH试纸投入待测液,对照标准比色卡读数
B.用干燥、洁净的玻璃棒蘸取少量待测液,沾在置于洁净表面皿的pH试纸上,半分钟内根据试纸呈现颜色,对照标准比色卡读数
C.用玻璃棒蘸取待测液沾在用蒸馏水润湿的pH试纸上.对照标准比色卡读数
D.用玻璃棒蘸取待测液沾在pH试纸上,3分钟后对照标准比色卡读数
6、对实验现象、过程的描述都正确的是( )
A.硫在空气中点燃发出黄光、放出热量
B.铁粉在空气中加热剧烈燃烧、生成黑色固体
C.浓硫酸敞口放置溶液的颜色、质量不变
D.烧碱固体放入水中迅速溶解、溶液温度升高
7、下列关于盐酸的描述,错误的是( )
A.浓盐酸有刺激性气味
B.盐酸具有强烈的吸水性
C.盐酸是氯化氢气体的水溶液
D.打开装有浓盐酸的试剂瓶,瓶口处有白雾
8、下列物质中能与澄清石灰水反应,但反应若不加指示剂则无明显现象的是( )
A.氯化铜溶液 B.碳酸钠溶液 C.氯化镁溶液 D.稀盐酸
9、用滤纸做成的小花喷洒某无色溶液后放在如图位置,片刻后变成红色。请推测喷洒液和小烧杯中a溶液分别可能是( )
A.酚酞试液和浓氨水 B.酚酞试液和pH<7的溶液
C.石蕊试液和浓硫酸 D.石蕊试液和浓盐酸
10、某电镀厂排出污水的,并含有硫酸铜,要除去有毒的硫酸铜,同时调节至中性,可选用下列物质中的( )
A.生石灰 B.氯化钡 C.硝酸银 D.碳酸钙
11、往KOH溶液中加水,溶液的pH变化正确的是( )
A. B.
C. D.
12、下图所示实验操作正确的是( )
A.点燃酒精灯 B.稀释浓硫酸
C.闻气体气味 D.连接玻璃管和橡皮管
13、打开盛有下列试剂的试剂瓶盖后,在瓶口出现白雾的是( )
A.浓盐酸 B.浓硫酸 C.稀盐酸 D.稀硫酸
14、物质的性质不仅决定了它的用途,还决定了它的保存方法。固体氢氧化钠具有以下性质,实验室中固体氢氧化钠必须密封保存的主要原因是( )
①有腐蚀性; ②易吸收水蒸汽而潮解;
③易溶于水,溶解时放出热量; ④能与空气中的二氧化碳反应。
A.①② B.①③ C.②④ D.③④
15、某同学在实验室测定了几种液体的pH,其结果如下表:
液体 盐酸 水
pH <7 <7 =7 =7 >7 >7
该同学由此得出的结论正确的是( )
A.盐溶液可能显酸性、碱性或中性
B.pH>7的液体一定是碱溶液
C.pH=7的液体一定是盐溶液
D.pH<7的液体一定是酸溶液
16、某化工厂发生硫酸泄漏事件,为了减少硫酸对环境的污染,有关部门采取了紧急措施,在泄漏的硫酸上面喷洒了一种化学试剂。你认为这种试剂可能是( )
A.熟石灰 B.硫酸铜 C.食盐 D.干冰
二、填空题。
17、能源和环境与人类的生活和社会发展密切相关。
(1)化石燃料是不可再生能源,包括煤、石油和_________;大量使用煤、石油等化石燃料会产生_________、NO2等污染物,这些污染物在空气中会形成_________,破坏环境。
(2)物质发生化学反应的同时,常伴随着能量的变化,能量的变化通常表现为热量的变化。下列各组物质在一定条件下能够发生化学反应,且放出热量的是_________。(填字母序号)
A 浓硫酸与水 B 镁与盐酸 C 碳与氧气 D 碳与氧化铜
(3)在研究可燃物的燃烧条件时,某同学对教材中的实验做了改进,并用如图所示装置进行实验。
①试判断能够燃烧的是图中的__________(填“a”、“b”或“c”)处,该处燃着的磷会很快熄灭,原因可能是_________ 。
②如图所示的实验与教材中探究燃烧的条件的实验相比,具有的优点是_________ (写一条即可)。
18、“化学是在分子、原子层次上研究物质的性质、组成,结构与变化规律的科学”。请根据你对“化学”这门科学的认识解答以下问题:
(1)通过电解水的实验。可以推断水是由___________(填元素符号)元素组成。
(2)金刚石和石墨组成元素相同,而它们的物理性质却有很大差异,其微观解释是___________ 。
(3)以下物质用途主要是由其物理性质决定的是___________(填序号)。
①氢气填充探空气球 ②氢氧化钠干燥气体
③天然气作燃料 ④用铜制作导线
(4)N2、NH3、HNO3等都是常见的含氮物质,其中氮元素化合价最低的物质是:
___________。
19、有CO2、N2、O2三种气体,能让燃着的木条燃烧更旺的是___。小柯将二氧化碳气体通入滴有紫色石蕊试液的水中,他可能要探究的问题是___,所得溶液的pH___7(选填“<”、“=”或“>”)
20、化学基础与常识。
(1)下图金属应用的实例,主要利用金属的导热性的是_______(填序号);
(2)向氢氧化钠溶液中滴加稀盐酸至恰好完全反应,反应前后溶液中存在的离子种类如图所示(其中“”“”“”“ ”表示不同离子)。则“”与“”反应生成了_________(填物质名称)。
(3)氢氟酸(HF)能刻画玻璃,其中有一个化学反应的化学方程式是:CaSiO3+6HF=X+SiF4↑+3H2O,则X的化学式为_______________
(4)氢能是一种极具发展潜力的清洁能。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如图所示。
写出反应I中,发生反应的化学方程式:_____________________________。
21、氢氧化钠中混有少量氢氧化钙杂质,用方程式表示除去的方法:_______________ 。
22、某食品包装袋中有一个小纸袋,上面写着“生石灰干燥剂, 请勿食用”。该食品已放置两个月有余。请你对下列问题进行探究。
(1)小纸袋中的物质能否继续作干燥剂?
实验步骤 实验现象 结论
取足量的小纸袋中的固体放入烧杯中,加入适量的水,触摸杯壁 。 可继续作干燥剂
(2)猜想:小纸袋中的物质除含有CaO外,还可能含有Ca(OH)2和 。
(3)请设计实验证明(2)中你所填的物质是否存在。
。
三、实验题。
23、某化学实验小组欲探究盐酸、氢氧化钙的化学性质,取8支试管分别用A-H编号后,做如下实验.
(1)实验中观察到有气泡出现的试管是 ,有沉淀生成的试管是 。
(2)实验后某试管中为红色溶液,当向其中加入过量的NaOH溶液后,溶液变为蓝色.由此推断,该试管中最初盛有的物质是 。
(3)实验后某试管的底部有白色固体,过滤后向滤液中滴加盐酸,一段时间后有气泡冒出,则该滤液中的溶质是 。
24、维生素C又名抗坏血酸,易溶于水,易被氧化,遇热易被破坏。人体缺乏维生素C可能引发多种疾病。甲班化学兴趣小组对它研究如下:
(1)猜想:维生素C可能具有酸性。
(2)设计实验:
实验室提供试剂:维生素C片、蒸馏水、紫色石蕊试液、酚酞试液、稀NaOH溶液和相关仪器。
方案1:将维生素C片研碎、溶于蒸馏水制成溶液,然后向其中滴加紫色石蕊试液。
①实验现象为_____ ,说明维生素C显酸性。
②如果要加速维生素C片在水中的溶解,操作方法是_____ 。
方案2:①将维生素C片溶于蒸馏水制成溶液。
②取少量稀NaOH溶液于试管中,加入两滴酚酞试液,观察溶液呈_____色,然后向其中逐滴加入足量维生素C溶液振荡,直至溶液颜色变为_____色。结论:维生素C显酸性。
(3)继续探究:运用酸的化学性质的知识,你还可用什么实验证明维生素C具有酸性?简述实验方法_____ (要求与上述两种实验方法不相似)。
四、计算题。
25、某纯碱样品中含有杂质NaCl,为测定该样品中Na2CO3的质量分数,称取纯碱样品15 g,向其中逐渐加入稀盐酸,如图是产生的气体质量与加入稀盐酸质量的关系图。
(1)样品中Na2CO3的质量分数是 。
(2)当加入稀盐酸80.0 g时,所得溶液中Na+的质量为 。(结果保留一位小数)
(3)恰好反应后所得溶液中溶质的质量分数。(写出计算过程,结果保留一位小数)
第七单元 常见的酸和碱 分层题(含答案)2023—2024学年鲁教版化学九年级下册
一、选择题。
1、下列实验现象描述错误的是( )
A.氢气在空气燃烧产生淡蓝色火焰
B.打开盛放浓盐酸的试剂瓶瓶塞,瓶口出现白雾
C.将燃着的木炭伸入氧气中,产生白色火焰,放出热量,生成二氧化碳气体
D.将一氧化碳通过灼热的氧化铜,黑色粉末逐渐变为红色
【答案】C
2、下列物质中,属于碱的是( )
A. B. C. D.
【答案】A
3、“检测土壤浸出液的酸碱性”实验操作示意图如下,其中不正确的是( )
A.土壤加水搅拌 B.过滤
C.检验酸碱性 D.测定pH
【答案】C
4、向石蕊试液中通入二氧化碳气体,再进行加热,溶液颜色变化顺序正确的是( )
A.红色——紫色——红色 B.紫色——红色——紫色
C.红色——紫色——蓝色 D.红色——无色——红色
【答案】B
5、下列检测某溶液pH的操作正确的是( )
A.将pH试纸投入待测液,对照标准比色卡读数
B.用干燥、洁净的玻璃棒蘸取少量待测液,沾在置于洁净表面皿的pH试纸上,半分钟内根据试纸呈现颜色,对照标准比色卡读数
C.用玻璃棒蘸取待测液沾在用蒸馏水润湿的pH试纸上.对照标准比色卡读数
D.用玻璃棒蘸取待测液沾在pH试纸上,3分钟后对照标准比色卡读数
【答案】B
6、对实验现象、过程的描述都正确的是( )
A.硫在空气中点燃发出黄光、放出热量
B.铁粉在空气中加热剧烈燃烧、生成黑色固体
C.浓硫酸敞口放置溶液的颜色、质量不变
D.烧碱固体放入水中迅速溶解、溶液温度升高
【答案】D
7、下列关于盐酸的描述,错误的是( )
A.浓盐酸有刺激性气味
B.盐酸具有强烈的吸水性
C.盐酸是氯化氢气体的水溶液
D.打开装有浓盐酸的试剂瓶,瓶口处有白雾
【答案】B
8、下列物质中能与澄清石灰水反应,但反应若不加指示剂则无明显现象的是( )
A.氯化铜溶液 B.碳酸钠溶液 C.氯化镁溶液 D.稀盐酸
【答案】D
9、用滤纸做成的小花喷洒某无色溶液后放在如图位置,片刻后变成红色。请推测喷洒液和小烧杯中a溶液分别可能是( )
A.酚酞试液和浓氨水 B.酚酞试液和pH<7的溶液
C.石蕊试液和浓硫酸 D.石蕊试液和浓盐酸
【答案】A
10、某电镀厂排出污水的,并含有硫酸铜,要除去有毒的硫酸铜,同时调节至中性,可选用下列物质中的( )
A.生石灰 B.氯化钡 C.硝酸银 D.碳酸钙
【答案】A
11、往KOH溶液中加水,溶液的pH变化正确的是( )
A. B.
C. D.
【答案】C
12、下图所示实验操作正确的是( )
A.点燃酒精灯 B.稀释浓硫酸
C.闻气体气味 D.连接玻璃管和橡皮管
【答案】D
13、打开盛有下列试剂的试剂瓶盖后,在瓶口出现白雾的是( )
A.浓盐酸 B.浓硫酸 C.稀盐酸 D.稀硫酸
【答案】A
14、物质的性质不仅决定了它的用途,还决定了它的保存方法。固体氢氧化钠具有以下性质,实验室中固体氢氧化钠必须密封保存的主要原因是( )
①有腐蚀性; ②易吸收水蒸汽而潮解;
③易溶于水,溶解时放出热量; ④能与空气中的二氧化碳反应。
A.①② B.①③ C.②④ D.③④
【答案】C
15、某同学在实验室测定了几种液体的pH,其结果如下表:
液体 盐酸 水
pH <7 <7 =7 =7 >7 >7
该同学由此得出的结论正确的是( )
A.盐溶液可能显酸性、碱性或中性
B.pH>7的液体一定是碱溶液
C.pH=7的液体一定是盐溶液
D.pH<7的液体一定是酸溶液
【答案】A
16、某化工厂发生硫酸泄漏事件,为了减少硫酸对环境的污染,有关部门采取了紧急措施,在泄漏的硫酸上面喷洒了一种化学试剂。你认为这种试剂可能是( )
A.熟石灰 B.硫酸铜 C.食盐 D.干冰
【答案】A
二、填空题。
17、能源和环境与人类的生活和社会发展密切相关。
(1)化石燃料是不可再生能源,包括煤、石油和_________;大量使用煤、石油等化石燃料会产生_________、NO2等污染物,这些污染物在空气中会形成_________,破坏环境。
(2)物质发生化学反应的同时,常伴随着能量的变化,能量的变化通常表现为热量的变化。下列各组物质在一定条件下能够发生化学反应,且放出热量的是_________。(填字母序号)
A 浓硫酸与水 B 镁与盐酸 C 碳与氧气 D 碳与氧化铜
(3)在研究可燃物的燃烧条件时,某同学对教材中的实验做了改进,并用如图所示装置进行实验。
①试判断能够燃烧的是图中的__________(填“a”、“b”或“c”)处,该处燃着的磷会很快熄灭,原因可能是_________ 。
②如图所示的实验与教材中探究燃烧的条件的实验相比,具有的优点是_________ (写一条即可)。
【答案】(1)天然气 SO2 酸雨 (2)BC
(3)a 氧气不足或被耗尽 装置简单(操作方便或污染小等)
18、“化学是在分子、原子层次上研究物质的性质、组成,结构与变化规律的科学”。请根据你对“化学”这门科学的认识解答以下问题:
(1)通过电解水的实验。可以推断水是由___________(填元素符号)元素组成。
(2)金刚石和石墨组成元素相同,而它们的物理性质却有很大差异,其微观解释是___________ 。
(3)以下物质用途主要是由其物理性质决定的是___________(填序号)。
①氢气填充探空气球 ②氢氧化钠干燥气体
③天然气作燃料 ④用铜制作导线
(4)N2、NH3、HNO3等都是常见的含氮物质,其中氮元素化合价最低的物质是:
___________。
【答案】(1)H、O (2)碳原子的排列方式不同 (3)①②④ (4)NH3/氨气
19、有CO2、N2、O2三种气体,能让燃着的木条燃烧更旺的是___。小柯将二氧化碳气体通入滴有紫色石蕊试液的水中,他可能要探究的问题是___,所得溶液的pH___7(选填“<”、“=”或“>”)
【答案】氧气 二氧化碳是否能与水反应 <
20、化学基础与常识。
(1)下图金属应用的实例,主要利用金属的导热性的是_______(填序号);
(2)向氢氧化钠溶液中滴加稀盐酸至恰好完全反应,反应前后溶液中存在的离子种类如图所示(其中“”“”“”“ ”表示不同离子)。则“”与“”反应生成了_________(填物质名称)。
(3)氢氟酸(HF)能刻画玻璃,其中有一个化学反应的化学方程式是:CaSiO3+6HF=X+SiF4↑+3H2O,则X的化学式为_______________
(4)氢能是一种极具发展潜力的清洁能。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如图所示。
写出反应I中,发生反应的化学方程式:_____________________________。
【答案】 (1) B (2)水 (3)CaF2
(4)SO2+I2+2H2O=H2SO4+2HI
21、氢氧化钠中混有少量氢氧化钙杂质,用方程式表示除去的方法:_______________ 。
【答案】NaCO+Ca(OH)=====2NaOH+CaCO↓
22、某食品包装袋中有一个小纸袋,上面写着“生石灰干燥剂, 请勿食用”。该食品已放置两个月有余。请你对下列问题进行探究。
(1)小纸袋中的物质能否继续作干燥剂?
实验步骤 实验现象 结论
取足量的小纸袋中的固体放入烧杯中,加入适量的水,触摸杯壁 。 可继续作干燥剂
(2)猜想:小纸袋中的物质除含有CaO外,还可能含有Ca(OH)2和 。
(3)请设计实验证明(2)中你所填的物质是否存在。
。
【答案】烧杯壁发热 CaCO3
将小纸袋中的固体加入到足量的稀盐酸中,若产生能使澄清石灰水变浑浊的气体,则证明有CaCO3,否则没有。
三、实验题。
23、某化学实验小组欲探究盐酸、氢氧化钙的化学性质,取8支试管分别用A-H编号后,做如下实验.
(1)实验中观察到有气泡出现的试管是 ,有沉淀生成的试管是 。
(2)实验后某试管中为红色溶液,当向其中加入过量的NaOH溶液后,溶液变为蓝色.由此推断,该试管中最初盛有的物质是 。
(3)实验后某试管的底部有白色固体,过滤后向滤液中滴加盐酸,一段时间后有气泡冒出,则该滤液中的溶质是 。
【答案】(1)AC,EH; (2)石蕊试液; (3)NaOH和Na2CO3
24、维生素C又名抗坏血酸,易溶于水,易被氧化,遇热易被破坏。人体缺乏维生素C可能引发多种疾病。甲班化学兴趣小组对它研究如下:
(1)猜想:维生素C可能具有酸性。
(2)设计实验:
实验室提供试剂:维生素C片、蒸馏水、紫色石蕊试液、酚酞试液、稀NaOH溶液和相关仪器。
方案1:将维生素C片研碎、溶于蒸馏水制成溶液,然后向其中滴加紫色石蕊试液。
①实验现象为_____ ,说明维生素C显酸性。
②如果要加速维生素C片在水中的溶解,操作方法是_____ 。
方案2:①将维生素C片溶于蒸馏水制成溶液。
②取少量稀NaOH溶液于试管中,加入两滴酚酞试液,观察溶液呈_____色,然后向其中逐滴加入足量维生素C溶液振荡,直至溶液颜色变为_____色。结论:维生素C显酸性。
(3)继续探究:运用酸的化学性质的知识,你还可用什么实验证明维生素C具有酸性?简述实验方法_____ (要求与上述两种实验方法不相似)。
【答案】(1)显红色 (2)搅拌或振荡 (3)红 无
(4)在维生素C溶液中加入金属镁或Na2CO3有气泡产生
四、计算题。
25、某纯碱样品中含有杂质NaCl,为测定该样品中Na2CO3的质量分数,称取纯碱样品15 g,向其中逐渐加入稀盐酸,如图是产生的气体质量与加入稀盐酸质量的关系图。
(1)样品中Na2CO3的质量分数是 。
(2)当加入稀盐酸80.0 g时,所得溶液中Na+的质量为 。(结果保留一位小数)
(3)恰好反应后所得溶液中溶质的质量分数。(写出计算过程,结果保留一位小数)
【答案】(1)70.7%; (2)6.3 g; (3)22.8%
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
