2023-2024学年人教版九年级化学下册 9.3.2 溶液的浓度(第2课时)课件(共14张PPT)
文档属性
| 名称 | 2023-2024学年人教版九年级化学下册 9.3.2 溶液的浓度(第2课时)课件(共14张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 31.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-05 00:00:00 | ||
图片预览





文档简介
(共14张PPT)
MASS FRACTION OF SOLUTE
课题3 溶液的浓度
第2课时
复习巩固
溶质质量分数
=
m质
ρ溶液V溶液
×100%
ω(溶质)=
m(溶质)
× 100%
m(溶液)
m(溶质)
m(溶质)+m(溶液)
× 100%
=
t℃时,某物质的溶解度为S,
则t℃,该物质饱和溶液中:
ω(溶质)=
S
× 100%
S+100 g
课堂练习
1
蒸干40g氯化钾溶液,得到10g氯化钾,
求该氯化钾溶液中溶质质量分数
根据信息,列出关系式
2
向45g水中加入5g氯化钠搅拌后全部溶解,求该溶液中溶质质量分数
3
一定量的硝酸钾溶于80g水中制成100g硝酸钾溶液,求该溶液的溶质质量分数
10 g
40 g
× 100%
5 g
45 g + 5 g
× 100%
100 g-80 g
100 g
× 100%
课堂练习
18 g + 10 g
90 g + 10g
× 100%
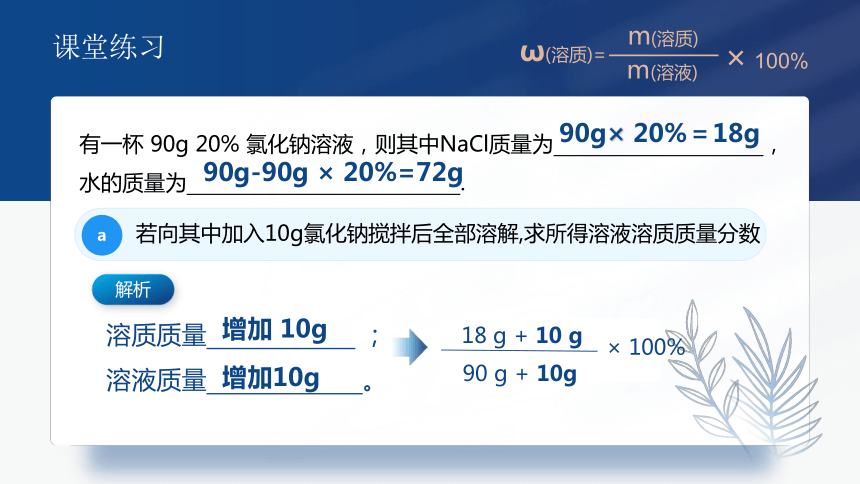
有一杯 90g 20% 氯化钠溶液,则其中NaCl质量为 ,
水的质量为 .
90g× 20%=18g
90g-90g × 20%=72g
a
若向其中加入10g氯化钠搅拌后全部溶解,求所得溶液溶质质量分数
解析
溶质质量 ;
溶液质量 。
增加 10g
增加10g
ω(溶质)=
m(溶质)
× 100%
m(溶液)
课堂练习
ω(溶质)=
m(溶质)
× 100%
m(溶液)
18 g
90 g + 10g
× 100%
有一杯 90g 20% 氯化钠溶液,则其中NaCl质量为 ,
水的质量为 .
90g× 20%=18g
90g-90g × 20%=72g
b
若向其中加入10g水,求所得溶液溶质质量分数为
解析
溶质质量 ;
溶液质量 。
不变
增加10g
总结归纳
溶质质量分数
=
m质
ρ溶液V溶液
×100%
ω(溶质)=
m(溶质)
× 100%
m(溶液)
m(溶质)
m(溶质)+m(溶液)
× 100%
=
公式变形
m(溶质)=m(溶液) × ω
m(溶液)=m(溶液) ÷ ω
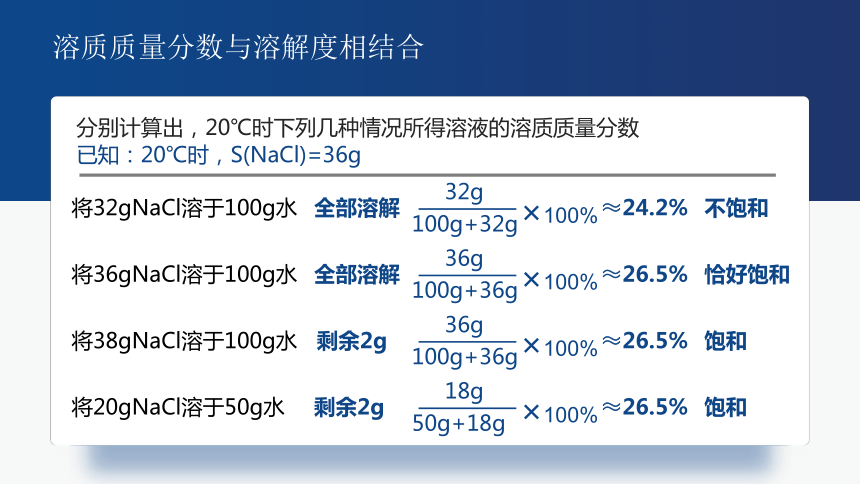
溶质质量分数与溶解度相结合
已知:20℃时,S(NaCl)=36g
分别计算出,20℃时下列几种情况所得溶液的溶质质量分数
将32gNaCl溶于100g水
全部溶解
不饱和
≈24.2%
32g
100g+32g
×100%
将36gNaCl溶于100g水
全部溶解
恰好饱和
≈26.5%
36g
100g+36g
×100%
将38gNaCl溶于100g水
剩余2g
饱和
≈26.5%
36g
100g+36g
×100%
将20gNaCl溶于50g水
剩余2g
饱和
≈26.5%
18g
50g+18g
×100%
例题:A、B、C三种物质的溶解度下图
t2 ℃时,A物质的饱和溶液中溶质的质量分数为 .
(2) t2 ℃时,把15g A物质放到50g水中,充
分溶解后,溶液中溶质的质量分数为 .
20%
溶质质量分数与溶解度相结合
ω(溶质)=
S
× 100%
S+100 g
20%
50 g水中最多溶解12.5 g
解 析
例题:A、B、C三种物质的溶解度下图
(3)t2 ℃时,A、B、C三种物质的饱和溶液中
溶质的质量分数由大到小的顺序为________.
A>B>C
溶质质量分数与溶解度相结合
ω(溶质)=
S
× 100%
S+100 g
饱和溶液,S越大,ω(溶质)越大
解 析
比较溶解度大小即可
溶解度: A>B>C
ω(溶质) :A>B>C
溶液的稀释
100g 质量分数为98%的浓硫酸中溶质质量为多少?
若与100g水混合后溶质质量为多少?求混合后溶质的质量分数?
100 g溶液中溶质的质量为:
100 g × 98%=98 g
与100 g 水混合后溶质质量不变,依然为98 g
解 析
混合后溶质的质量分数
100 g ×98%
× 100%
= 49%
100 g +100g
溶液的稀释
计算依据
m(加水) = m(稀溶液) – m(浓溶液)
m浓ω浓 = m稀ω稀
依据溶液稀释前后,溶质质量不变
计算公式
溶液的稀释
50 g
98%浓硫酸
50g98%的浓硫酸加水稀释成20%的稀硫酸,求稀硫酸的质量为多少?需要加水多少克
m(稀硫酸)20%浓硫酸
加水?
解:
50g × 98% = m稀× 20%
m加水=245g-50g=195g
m稀= 245g
答:稀硫酸的质量为245g,
需要加水的质量为195g
m浓ω浓 = m稀ω稀
溶液的稀释
10 ml
98%浓硫酸
用 98% 的浓硫酸10 mL( 密度 1.84 g·mL-1) 配制 10% 的硫酸溶液,需要水多少毫升?
m(稀硫酸)10%浓硫酸
加水?
解:
能力提升
10ml × 1.84g/ml × 98% = m稀× 10%
m加水 = 180.32g - 10ml × 1.84g/ml
m稀= 180.32g
答:需要加水的体积为161.92 ml
m浓ω浓 = m稀ω稀
= 161.92g
V加水= 161.92 ml
有一瓶未开封的浓盐酸,部分标签如右表所示,则溶液的质量是 g,溶质的质量是 g,溶剂的质量是
g,溶质质量分数是 .
MASS FRACTION OF SOLUTE
课题3 溶液的浓度
第2课时
复习巩固
溶质质量分数
=
m质
ρ溶液V溶液
×100%
ω(溶质)=
m(溶质)
× 100%
m(溶液)
m(溶质)
m(溶质)+m(溶液)
× 100%
=
t℃时,某物质的溶解度为S,
则t℃,该物质饱和溶液中:
ω(溶质)=
S
× 100%
S+100 g
课堂练习
1
蒸干40g氯化钾溶液,得到10g氯化钾,
求该氯化钾溶液中溶质质量分数
根据信息,列出关系式
2
向45g水中加入5g氯化钠搅拌后全部溶解,求该溶液中溶质质量分数
3
一定量的硝酸钾溶于80g水中制成100g硝酸钾溶液,求该溶液的溶质质量分数
10 g
40 g
× 100%
5 g
45 g + 5 g
× 100%
100 g-80 g
100 g
× 100%
课堂练习
18 g + 10 g
90 g + 10g
× 100%
有一杯 90g 20% 氯化钠溶液,则其中NaCl质量为 ,
水的质量为 .
90g× 20%=18g
90g-90g × 20%=72g
a
若向其中加入10g氯化钠搅拌后全部溶解,求所得溶液溶质质量分数
解析
溶质质量 ;
溶液质量 。
增加 10g
增加10g
ω(溶质)=
m(溶质)
× 100%
m(溶液)
课堂练习
ω(溶质)=
m(溶质)
× 100%
m(溶液)
18 g
90 g + 10g
× 100%
有一杯 90g 20% 氯化钠溶液,则其中NaCl质量为 ,
水的质量为 .
90g× 20%=18g
90g-90g × 20%=72g
b
若向其中加入10g水,求所得溶液溶质质量分数为
解析
溶质质量 ;
溶液质量 。
不变
增加10g
总结归纳
溶质质量分数
=
m质
ρ溶液V溶液
×100%
ω(溶质)=
m(溶质)
× 100%
m(溶液)
m(溶质)
m(溶质)+m(溶液)
× 100%
=
公式变形
m(溶质)=m(溶液) × ω
m(溶液)=m(溶液) ÷ ω
溶质质量分数与溶解度相结合
已知:20℃时,S(NaCl)=36g
分别计算出,20℃时下列几种情况所得溶液的溶质质量分数
将32gNaCl溶于100g水
全部溶解
不饱和
≈24.2%
32g
100g+32g
×100%
将36gNaCl溶于100g水
全部溶解
恰好饱和
≈26.5%
36g
100g+36g
×100%
将38gNaCl溶于100g水
剩余2g
饱和
≈26.5%
36g
100g+36g
×100%
将20gNaCl溶于50g水
剩余2g
饱和
≈26.5%
18g
50g+18g
×100%
例题:A、B、C三种物质的溶解度下图
t2 ℃时,A物质的饱和溶液中溶质的质量分数为 .
(2) t2 ℃时,把15g A物质放到50g水中,充
分溶解后,溶液中溶质的质量分数为 .
20%
溶质质量分数与溶解度相结合
ω(溶质)=
S
× 100%
S+100 g
20%
50 g水中最多溶解12.5 g
解 析
例题:A、B、C三种物质的溶解度下图
(3)t2 ℃时,A、B、C三种物质的饱和溶液中
溶质的质量分数由大到小的顺序为________.
A>B>C
溶质质量分数与溶解度相结合
ω(溶质)=
S
× 100%
S+100 g
饱和溶液,S越大,ω(溶质)越大
解 析
比较溶解度大小即可
溶解度: A>B>C
ω(溶质) :A>B>C
溶液的稀释
100g 质量分数为98%的浓硫酸中溶质质量为多少?
若与100g水混合后溶质质量为多少?求混合后溶质的质量分数?
100 g溶液中溶质的质量为:
100 g × 98%=98 g
与100 g 水混合后溶质质量不变,依然为98 g
解 析
混合后溶质的质量分数
100 g ×98%
× 100%
= 49%
100 g +100g
溶液的稀释
计算依据
m(加水) = m(稀溶液) – m(浓溶液)
m浓ω浓 = m稀ω稀
依据溶液稀释前后,溶质质量不变
计算公式
溶液的稀释
50 g
98%浓硫酸
50g98%的浓硫酸加水稀释成20%的稀硫酸,求稀硫酸的质量为多少?需要加水多少克
m(稀硫酸)20%浓硫酸
加水?
解:
50g × 98% = m稀× 20%
m加水=245g-50g=195g
m稀= 245g
答:稀硫酸的质量为245g,
需要加水的质量为195g
m浓ω浓 = m稀ω稀
溶液的稀释
10 ml
98%浓硫酸
用 98% 的浓硫酸10 mL( 密度 1.84 g·mL-1) 配制 10% 的硫酸溶液,需要水多少毫升?
m(稀硫酸)10%浓硫酸
加水?
解:
能力提升
10ml × 1.84g/ml × 98% = m稀× 10%
m加水 = 180.32g - 10ml × 1.84g/ml
m稀= 180.32g
答:需要加水的体积为161.92 ml
m浓ω浓 = m稀ω稀
= 161.92g
V加水= 161.92 ml
有一瓶未开封的浓盐酸,部分标签如右表所示,则溶液的质量是 g,溶质的质量是 g,溶剂的质量是
g,溶质质量分数是 .
同课章节目录
