吉林省长春市榆树市部分学校2023-2024学年九年级下学期开学联考化学试题(含答案)
文档属性
| 名称 | 吉林省长春市榆树市部分学校2023-2024学年九年级下学期开学联考化学试题(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 209.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-06 00:00:00 | ||
图片预览




文档简介
2023-2024学年度第二学期开学部分学校联考九年级化学
一.选择题(共10小题,每题1分,共10分)
1.(1分)下列制作传统工艺品过程中,原料发生化学变化的是( )
A.黏土烧制青花瓷 B.布料缝制香荷包
C.丝线编制中国结 D.玉石雕刻玉如意
2.(1分)航天员在太空中呼吸的“人造空气”与我们身边的空气成分含量基本相同,“人造空气”中氧气含量约为( )
A.78% B.21% C.0.94% D.0.03%
3.(1分)下列事实能用分子或原子间有一定间隔解释的是( )
A.汽油要密封保存
B.电解水生成氢气和氧气
C.用水银温度计测量体温
D.湿衣服在太阳下晾晒干得快
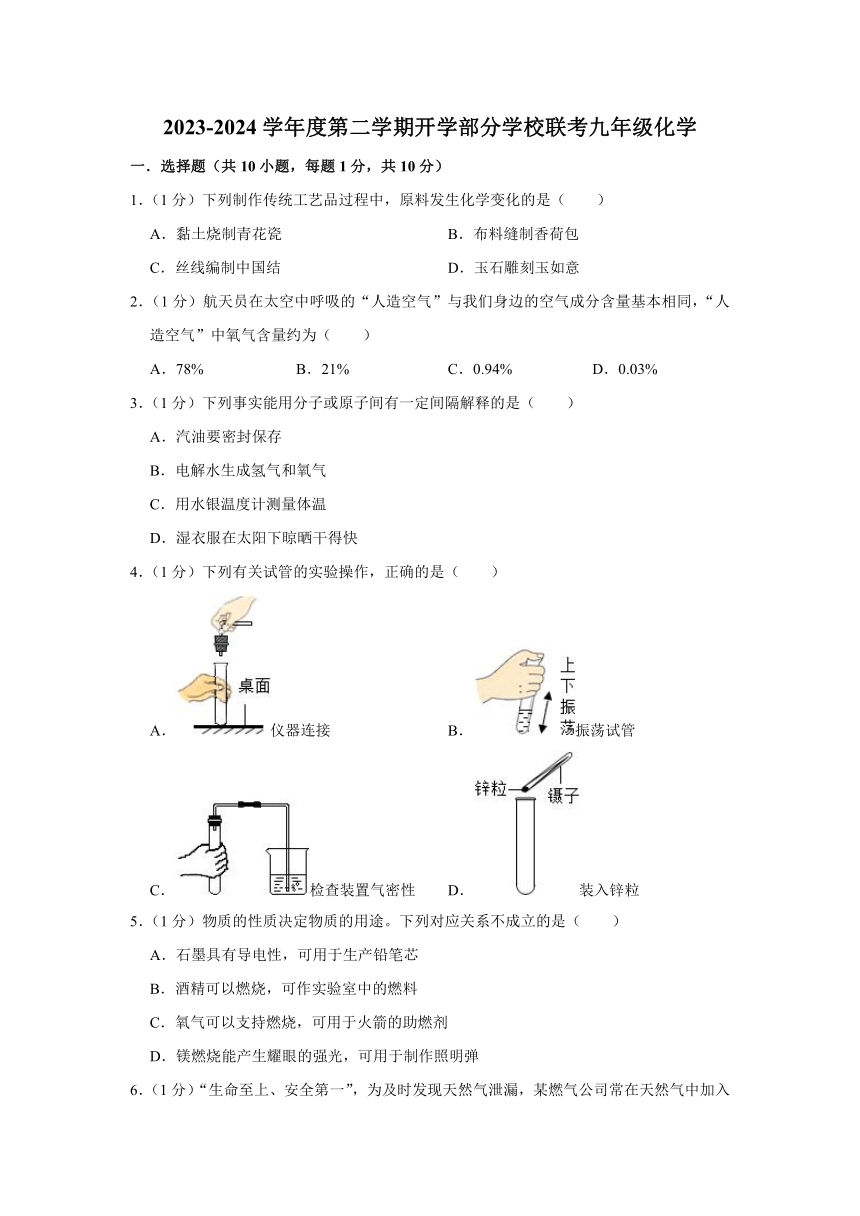
4.(1分)下列有关试管的实验操作,正确的是( )
A.仪器连接 B.振荡试管
C.检查装置气密性 D.装入锌粒
5.(1分)物质的性质决定物质的用途。下列对应关系不成立的是( )
A.石墨具有导电性,可用于生产铅笔芯
B.酒精可以燃烧,可作实验室中的燃料
C.氧气可以支持燃烧,可用于火箭的助燃剂
D.镁燃烧能产生耀眼的强光,可用于制作照明弹
6.(1分)“生命至上、安全第一”,为及时发现天然气泄漏,某燃气公司常在天然气中加入少量具有特殊气味的乙硫醇(C2H5SH)。乙硫醇在空气中也能燃烧,反应的化学方程式为:2C2H5SH+9O24CO2+6H2O+2X。X的化学式为( )
A.H2S B.SO3 C.H2SO4 D.SO2
7.(1分)我国宋代《梦溪笔谈》中有“熬胆矾铁釜久之亦化为铜”的记载,其化学反应原理为Fe+CuSO4═Cu+FeSO4,该反应的基本反应类型是( )
A.化合反应 B.置换反应 C.分解反应 D.氧化反应
8.(1分)下列涉及化学学科观点的说法,错误的是( )
A.微粒观:一氧化碳分子是由碳原子和氧原子构成
B.元素观:由同种元素组成的物质一定是单质
C.分类观:空气和矿泉水都属于混合物
D.守恒观:化学反应前后各原子数目保持不变
9.(1分)推理是一种重要的化学思维方法,下列推理合理的是( )
A.化合物由不同种元素组成,所以由不同种元素组成的纯净物一定是化合物
B.水在通电条件下生成氢气和氧气,所以水是由氢分子和氧分子构成的
C.燃烧需要同时满足三个条件,所以只有同时破坏燃烧的三个条件才能灭火
D.置换反应有单质和化合物生成,所以有单质和化合物生成的反应一定是置换反应
10.(1分)鉴别如表各组物质的方法中,肯定不可行的是( )
A 氧化铜、二氧化锰 取样后分别加等浓度的双氧水,观察产生气泡快慢
B 羊毛纤维、蚕丝纤维 取样后分别灼烧,闻是否产生烧焦羽毛的气味
C 浓硫酸、稀硫酸 取样后分别插入小木条,观察木条颜色变化
D 硫酸钠、硫酸铵 取样后分别加熟石灰研磨,闻是否有刺激性气味
A.A B.B C.C D.D
二、非选择题(共40分)
11.(3分)用化学用语回答下列问题:
(1)氮元素 。
(2)2个硫原子 。
(3)3个镁离子 。
12.(3分)下面是三种粒子的结构示意图,回答下列问题:
(1)写出A粒子的符号 。
(2)A、B、C中具有稳定结构的原子是 。
(3)A、C两种元素组成的化合物中C元素的化合价为 价。
13.(4分)化学在保障人体健康、预防和治疗新冠感染方面贡献巨大。回答下列问题。
(1)医用酒精可通过擦拭或喷洒于物体表面起消毒杀菌作用,酒精的化学式为 。
(2)喷洒酒精消毒时,嗅到酒精的气味,体现了分子具有的性质是 。
(3)过氧乙酸是常用杀毒剂,如图是某品牌过氧乙酸消毒液的标签:
过氧乙酸消毒液 重量:500g 化学式:C2H4O3 含量:40% 使用方法:浸泡、喷雾、熏蒸等方法,与水稀释后使用。 注意事项:密封、避光、避热。 不可与可燃物混合存放。
①过氧乙酸消毒液属于 (填“纯净物”或“混合物”)。
②过氧乙酸中C、H、O三种元素的质量比为 。
14.(5分)“嫦娥五号”月球采样返回,“天问一号”成功抵达火星,标志着我国航天事业取得突破性进展。
(1)月壤含有可作为核聚变燃料的氦﹣3等物质。如图为氦元素在周期表中的部分信息。氦﹣3原子内质子数与中子数之和为3,则其所含中子数为 。
(2)着陆器上的仪器可探测水。若月球上存在大量的水,可利用光催化分解水技术得到氧气,请写出该反应的化学方程式 ;此反应与电解水反应相似,也可证明水由 元素组成。
(3)火星拥有丰富的二氧化碳资源。火星低层大气的主要成分如下表:
气体成分 CO2 N2 Ar O2 其他
体积分数/% 95.32 2.7 1.6 0.13 0.25
①为鉴别一瓶模拟“火星低层大气”组成的气体和一瓶空气,可采用的化学方法是 。
②若为满足人类未来在火星上生活,下列研究设想合理的是 (填代号)。
A.将CO2转化为O2,提高O2含量
B.将CO2分解转化为N2,提高N2含量
C.寻找水的存在和开发水循环技术
15.(3分)如图是元素周期表部分元素的信息,根据所给信息按要求填空。
(1)磷原子的相对原子质量是 。
(2)写出11号元素的离子符号 。
(3)某分子由3个原子构成,且含有10个质子,根据上表的信息分析,其化学符号是 。
16.(4分)现有 A、氮气 B、氯化钠 C、熟石灰 D、盐酸,四种物质,请用合适物质的字母代号填空:
(1)可帮助消化的是 。
(2)可用作保护气的是 。
(3)可用作调味品的是 。
(4)可用作改良酸性土壤的是 。
17.(4分)教材中的下列实验均用到了红磷,请回答下列问题:
(1)甲实验:能否将红磷换成铁丝来进行该实验? (说明理由)。
(2)乙实验:若取用红磷的量不足,对实验的结果是否有影响? 。
(3)丙实验:通过铜片上的白磷燃烧而红磷不燃烧的实验现象,可以得出可燃物燃烧的条件之一是 ;欲使热水中的白磷燃烧,操作方法是 。
18.(4分)在验证“质量守恒定律”的课堂教学中,A、B、C三个实验分别由甲、乙、丙三组同学来完成,他们都进行了规范的操作、准确的称量。回答下列问题:
(1)A实验中小气球的作用是 。
(2)B实验中观察到反应后天平不平衡,其原因是 。
(3)C实验中若硫酸铜溶液的量不足,对实验结论 (填“有”或“没有”)影响。
(4)由质量守恒定律可知,化学反应前后,一定不变的是 (填序号)。
①原子种类
②原子数目
③分子种类
④分子数目
⑤元素种类
⑥物质种类
19.(5分)制取气体是初中化学实验的重要内容,根据要求回答下列问题:
(1)写出标有序号的仪器名称:① 。
(2)实验室加热氯化铵和熟石灰制取氨气(密度约为空气的一半,极易溶于水),选择的发生装置和收集装置分别是 (填字母序号,下同)。
(3)若要得到干燥的氧气,所选择装置的连接顺序为:B→ → 。
(4)某兴趣小组的同学连接B、G、H装置进行实验。若实验时G装置中蜡烛燃烧更剧烈,H装置中溶液变浑浊,则B装置中所装固体、液体药品是 。
20.(5分)同学们在进行课外实验“碎鸡蛋壳与醋酸的反应”时,发现会产生大量气泡。于是同学们一起再实验,对产生的气体成分进行了下列探究。
【查阅资料】①浓硫酸是一种常见的干燥剂;水能使白色无水硫酸铜固体变蓝色。
②鸡蛋壳的主要成分是CaCO3,杂质不与醋酸反应,白醋由醋酸(化学式为CH3COOH)和水组成。
③加热的条件下氢气、一氧化碳都能使氧化铜转化为铜。
【提出猜想】(1)该气体可能含有CO2、O2、CO、H2中的一种或几种。猜想依据是 。
【设计实验】将白醋和鸡蛋壳反应产生的气体缓缓通入如图装置进行实验。
【实验预测】(2)若气体中含有氧气则F中的实验现象为 ;若气体中含有氢气但不含有一氧化碳,则G中的实验现象应为 ,H中的现象应为 。
【进行实验】实验中只观察到D处澄清石灰水变浑浊其余都无明显现象。
【得出结论】(3)CaCO3与CH3COOH反应会产生 ,通过询问老师获知,生成物中有一种物质叫醋酸钙[Ca(CH3COO)2]。
【交流反思】(4)将20.0g的鸡蛋壳与足量的稀醋酸按上图进行实验,D装置增重了5.5g,则生成二氧化碳的质量为 g。
(5)计算该样品中鸡蛋壳的中碳酸钙的质量分数。
设解:设20.0g的鸡蛋壳中的碳酸钙的质量为x。
写出方程式
写出相对分子质量、已知量、未知量
列比例式
求解x=12.5g
该鸡蛋壳中碳酸钙的质量分数为 (列式并计算结果)。
九年级化学参考答案
1. A。2. B。3. C。4. C。5. A。6. D。7. B。8. B。9. A。10. B。
11.
(1)N;
(2)2S;
(3)3Mg2+。
12.
(1)O2﹣;
(2)B;
(3)+3。
13.
(1)C2H5OH;
(2)分子是不断运动的;
(3)①混合物;
②6:1:12;
14.
(1)1;
(2)2H2O2H2↑+O2↑;氢、氧;
(3)①用燃着的木条分别伸入瓶中,木条熄灭的是模拟火星低层的气体,木条无明显变化的是空气;
②AC。
15.
(1)30.97;
(2)Na+;
(3)H2O。
16.
(1)D;
(2)A;
(3)B;
(4)C。
17.
(1)不能,铁丝不能在空气中燃烧;
(2)没有影响;
(3)温度达到着火点;向热水中的白磷通入氧气。
18.
(1)平衡(或调节或缓冲)内外气压;使装置密闭(或形成封闭体系)。
(2)生成的二氧化碳气体逸散到空气中。
(3)没有。
(4)①②⑤。
19.
(1)分液漏斗;
(2)AD;
(3)F;E;
(4)二氧化锰、过氧化氢溶液。
20.
(1)化学反应前后元素的种类不变;
(2)红色固体变黑色;白色固体变蓝色;没有明显变化(或无明显现象);
(3)CO2;
(4)5.5;
(5)CaCO3+CH3COOH=Ca(CH3COO)2+H2O+CO2↑;
CaCO3+CH3COOH=Ca(CH3COO)2+H2O+CO2↑
100 44
x 5.5g
;
。
一.选择题(共10小题,每题1分,共10分)
1.(1分)下列制作传统工艺品过程中,原料发生化学变化的是( )
A.黏土烧制青花瓷 B.布料缝制香荷包
C.丝线编制中国结 D.玉石雕刻玉如意
2.(1分)航天员在太空中呼吸的“人造空气”与我们身边的空气成分含量基本相同,“人造空气”中氧气含量约为( )
A.78% B.21% C.0.94% D.0.03%
3.(1分)下列事实能用分子或原子间有一定间隔解释的是( )
A.汽油要密封保存
B.电解水生成氢气和氧气
C.用水银温度计测量体温
D.湿衣服在太阳下晾晒干得快
4.(1分)下列有关试管的实验操作,正确的是( )
A.仪器连接 B.振荡试管
C.检查装置气密性 D.装入锌粒
5.(1分)物质的性质决定物质的用途。下列对应关系不成立的是( )
A.石墨具有导电性,可用于生产铅笔芯
B.酒精可以燃烧,可作实验室中的燃料
C.氧气可以支持燃烧,可用于火箭的助燃剂
D.镁燃烧能产生耀眼的强光,可用于制作照明弹
6.(1分)“生命至上、安全第一”,为及时发现天然气泄漏,某燃气公司常在天然气中加入少量具有特殊气味的乙硫醇(C2H5SH)。乙硫醇在空气中也能燃烧,反应的化学方程式为:2C2H5SH+9O24CO2+6H2O+2X。X的化学式为( )
A.H2S B.SO3 C.H2SO4 D.SO2
7.(1分)我国宋代《梦溪笔谈》中有“熬胆矾铁釜久之亦化为铜”的记载,其化学反应原理为Fe+CuSO4═Cu+FeSO4,该反应的基本反应类型是( )
A.化合反应 B.置换反应 C.分解反应 D.氧化反应
8.(1分)下列涉及化学学科观点的说法,错误的是( )
A.微粒观:一氧化碳分子是由碳原子和氧原子构成
B.元素观:由同种元素组成的物质一定是单质
C.分类观:空气和矿泉水都属于混合物
D.守恒观:化学反应前后各原子数目保持不变
9.(1分)推理是一种重要的化学思维方法,下列推理合理的是( )
A.化合物由不同种元素组成,所以由不同种元素组成的纯净物一定是化合物
B.水在通电条件下生成氢气和氧气,所以水是由氢分子和氧分子构成的
C.燃烧需要同时满足三个条件,所以只有同时破坏燃烧的三个条件才能灭火
D.置换反应有单质和化合物生成,所以有单质和化合物生成的反应一定是置换反应
10.(1分)鉴别如表各组物质的方法中,肯定不可行的是( )
A 氧化铜、二氧化锰 取样后分别加等浓度的双氧水,观察产生气泡快慢
B 羊毛纤维、蚕丝纤维 取样后分别灼烧,闻是否产生烧焦羽毛的气味
C 浓硫酸、稀硫酸 取样后分别插入小木条,观察木条颜色变化
D 硫酸钠、硫酸铵 取样后分别加熟石灰研磨,闻是否有刺激性气味
A.A B.B C.C D.D
二、非选择题(共40分)
11.(3分)用化学用语回答下列问题:
(1)氮元素 。
(2)2个硫原子 。
(3)3个镁离子 。
12.(3分)下面是三种粒子的结构示意图,回答下列问题:
(1)写出A粒子的符号 。
(2)A、B、C中具有稳定结构的原子是 。
(3)A、C两种元素组成的化合物中C元素的化合价为 价。
13.(4分)化学在保障人体健康、预防和治疗新冠感染方面贡献巨大。回答下列问题。
(1)医用酒精可通过擦拭或喷洒于物体表面起消毒杀菌作用,酒精的化学式为 。
(2)喷洒酒精消毒时,嗅到酒精的气味,体现了分子具有的性质是 。
(3)过氧乙酸是常用杀毒剂,如图是某品牌过氧乙酸消毒液的标签:
过氧乙酸消毒液 重量:500g 化学式:C2H4O3 含量:40% 使用方法:浸泡、喷雾、熏蒸等方法,与水稀释后使用。 注意事项:密封、避光、避热。 不可与可燃物混合存放。
①过氧乙酸消毒液属于 (填“纯净物”或“混合物”)。
②过氧乙酸中C、H、O三种元素的质量比为 。
14.(5分)“嫦娥五号”月球采样返回,“天问一号”成功抵达火星,标志着我国航天事业取得突破性进展。
(1)月壤含有可作为核聚变燃料的氦﹣3等物质。如图为氦元素在周期表中的部分信息。氦﹣3原子内质子数与中子数之和为3,则其所含中子数为 。
(2)着陆器上的仪器可探测水。若月球上存在大量的水,可利用光催化分解水技术得到氧气,请写出该反应的化学方程式 ;此反应与电解水反应相似,也可证明水由 元素组成。
(3)火星拥有丰富的二氧化碳资源。火星低层大气的主要成分如下表:
气体成分 CO2 N2 Ar O2 其他
体积分数/% 95.32 2.7 1.6 0.13 0.25
①为鉴别一瓶模拟“火星低层大气”组成的气体和一瓶空气,可采用的化学方法是 。
②若为满足人类未来在火星上生活,下列研究设想合理的是 (填代号)。
A.将CO2转化为O2,提高O2含量
B.将CO2分解转化为N2,提高N2含量
C.寻找水的存在和开发水循环技术
15.(3分)如图是元素周期表部分元素的信息,根据所给信息按要求填空。
(1)磷原子的相对原子质量是 。
(2)写出11号元素的离子符号 。
(3)某分子由3个原子构成,且含有10个质子,根据上表的信息分析,其化学符号是 。
16.(4分)现有 A、氮气 B、氯化钠 C、熟石灰 D、盐酸,四种物质,请用合适物质的字母代号填空:
(1)可帮助消化的是 。
(2)可用作保护气的是 。
(3)可用作调味品的是 。
(4)可用作改良酸性土壤的是 。
17.(4分)教材中的下列实验均用到了红磷,请回答下列问题:
(1)甲实验:能否将红磷换成铁丝来进行该实验? (说明理由)。
(2)乙实验:若取用红磷的量不足,对实验的结果是否有影响? 。
(3)丙实验:通过铜片上的白磷燃烧而红磷不燃烧的实验现象,可以得出可燃物燃烧的条件之一是 ;欲使热水中的白磷燃烧,操作方法是 。
18.(4分)在验证“质量守恒定律”的课堂教学中,A、B、C三个实验分别由甲、乙、丙三组同学来完成,他们都进行了规范的操作、准确的称量。回答下列问题:
(1)A实验中小气球的作用是 。
(2)B实验中观察到反应后天平不平衡,其原因是 。
(3)C实验中若硫酸铜溶液的量不足,对实验结论 (填“有”或“没有”)影响。
(4)由质量守恒定律可知,化学反应前后,一定不变的是 (填序号)。
①原子种类
②原子数目
③分子种类
④分子数目
⑤元素种类
⑥物质种类
19.(5分)制取气体是初中化学实验的重要内容,根据要求回答下列问题:
(1)写出标有序号的仪器名称:① 。
(2)实验室加热氯化铵和熟石灰制取氨气(密度约为空气的一半,极易溶于水),选择的发生装置和收集装置分别是 (填字母序号,下同)。
(3)若要得到干燥的氧气,所选择装置的连接顺序为:B→ → 。
(4)某兴趣小组的同学连接B、G、H装置进行实验。若实验时G装置中蜡烛燃烧更剧烈,H装置中溶液变浑浊,则B装置中所装固体、液体药品是 。
20.(5分)同学们在进行课外实验“碎鸡蛋壳与醋酸的反应”时,发现会产生大量气泡。于是同学们一起再实验,对产生的气体成分进行了下列探究。
【查阅资料】①浓硫酸是一种常见的干燥剂;水能使白色无水硫酸铜固体变蓝色。
②鸡蛋壳的主要成分是CaCO3,杂质不与醋酸反应,白醋由醋酸(化学式为CH3COOH)和水组成。
③加热的条件下氢气、一氧化碳都能使氧化铜转化为铜。
【提出猜想】(1)该气体可能含有CO2、O2、CO、H2中的一种或几种。猜想依据是 。
【设计实验】将白醋和鸡蛋壳反应产生的气体缓缓通入如图装置进行实验。
【实验预测】(2)若气体中含有氧气则F中的实验现象为 ;若气体中含有氢气但不含有一氧化碳,则G中的实验现象应为 ,H中的现象应为 。
【进行实验】实验中只观察到D处澄清石灰水变浑浊其余都无明显现象。
【得出结论】(3)CaCO3与CH3COOH反应会产生 ,通过询问老师获知,生成物中有一种物质叫醋酸钙[Ca(CH3COO)2]。
【交流反思】(4)将20.0g的鸡蛋壳与足量的稀醋酸按上图进行实验,D装置增重了5.5g,则生成二氧化碳的质量为 g。
(5)计算该样品中鸡蛋壳的中碳酸钙的质量分数。
设解:设20.0g的鸡蛋壳中的碳酸钙的质量为x。
写出方程式
写出相对分子质量、已知量、未知量
列比例式
求解x=12.5g
该鸡蛋壳中碳酸钙的质量分数为 (列式并计算结果)。
九年级化学参考答案
1. A。2. B。3. C。4. C。5. A。6. D。7. B。8. B。9. A。10. B。
11.
(1)N;
(2)2S;
(3)3Mg2+。
12.
(1)O2﹣;
(2)B;
(3)+3。
13.
(1)C2H5OH;
(2)分子是不断运动的;
(3)①混合物;
②6:1:12;
14.
(1)1;
(2)2H2O2H2↑+O2↑;氢、氧;
(3)①用燃着的木条分别伸入瓶中,木条熄灭的是模拟火星低层的气体,木条无明显变化的是空气;
②AC。
15.
(1)30.97;
(2)Na+;
(3)H2O。
16.
(1)D;
(2)A;
(3)B;
(4)C。
17.
(1)不能,铁丝不能在空气中燃烧;
(2)没有影响;
(3)温度达到着火点;向热水中的白磷通入氧气。
18.
(1)平衡(或调节或缓冲)内外气压;使装置密闭(或形成封闭体系)。
(2)生成的二氧化碳气体逸散到空气中。
(3)没有。
(4)①②⑤。
19.
(1)分液漏斗;
(2)AD;
(3)F;E;
(4)二氧化锰、过氧化氢溶液。
20.
(1)化学反应前后元素的种类不变;
(2)红色固体变黑色;白色固体变蓝色;没有明显变化(或无明显现象);
(3)CO2;
(4)5.5;
(5)CaCO3+CH3COOH=Ca(CH3COO)2+H2O+CO2↑;
CaCO3+CH3COOH=Ca(CH3COO)2+H2O+CO2↑
100 44
x 5.5g
;
。
同课章节目录
