化学人教版(2019)选择性必修3 2.2.1烯烃(共23张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 2.2.1烯烃(共23张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 21.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-07 00:00:00 | ||
图片预览





文档简介
(共23张PPT)
第二章 烃
2019人教版选择性必修三
第二节 烯烃 炔烃
第一课时 烯烃
核心素养发展目标
1.理解烯烃的结构与化学性质,培养宏观辨识与微观探析的能力。
2.了解烯烃的顺反异构及二烯烃的加成反应,培养微观探析与变化观念的能力。
乙烯的结构
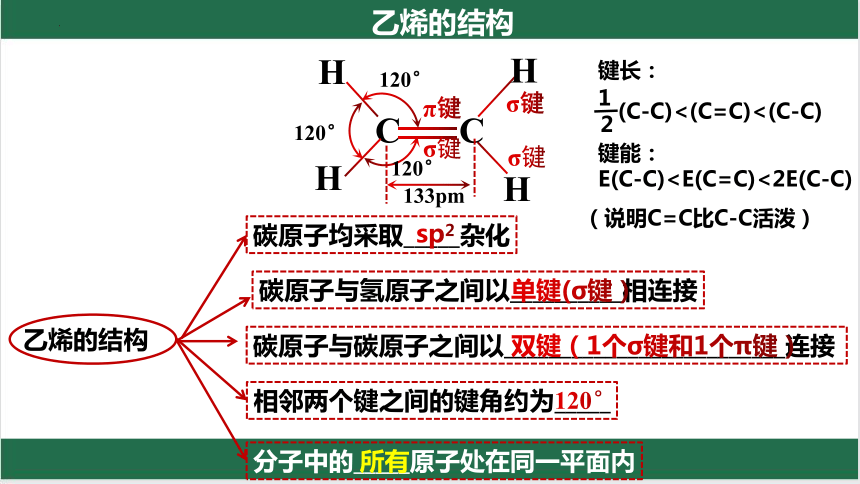
乙烯的结构
碳原子均采取_____杂化
sp2
碳原子与氢原子之间以__________相连接
单键(σ键)
碳原子与碳原子之间以_________________________连接
双键(1个σ键和1个π键)
相邻两个键之间的键角约为_____
分子中的_____原子处在同一平面内
120°
所有
C
C
H
H
H
H
σ键
σ键
π键
σ键
133pm
120°
120°
120°
键长:
(说明C=C比C-C活泼)
(C-C)<(C=C)<(C-C)
1
2
键能:
E(C-C)乙烯的性质
物理性质
化学性质
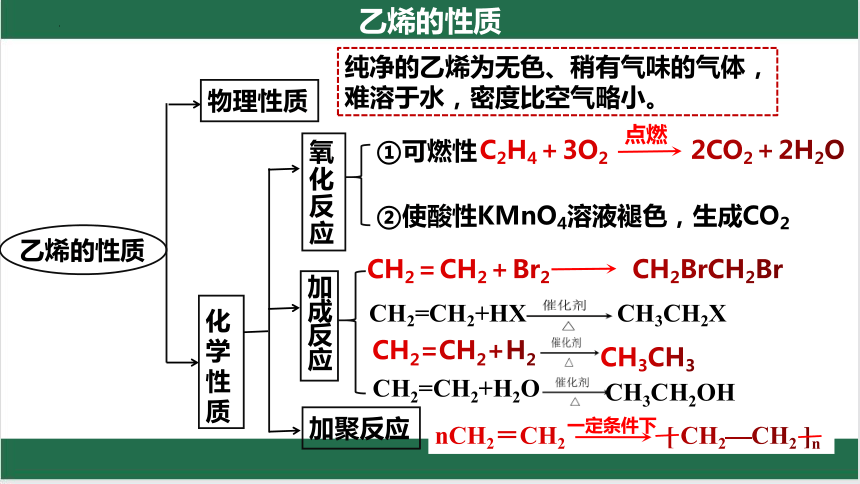
纯净的乙烯为无色、稍有气味的气体,
难溶于水,密度比空气略小。
氧化反应
加成反应
加聚反应
①可燃性
C2H4+3O2 2CO2+2H2O
点燃
②使酸性KMnO4溶液褪色,生成CO2
CH2=CH2+Br2 CH2BrCH2Br
nCH2=CH2 [ CH2—CH2 ]n
一定条件下
CH2=CH2+HX
CH3CH2X
CH2=CH2+H2O
CH3CH2OH
CH2=CH2+H2
CH3CH3
乙烯的性质
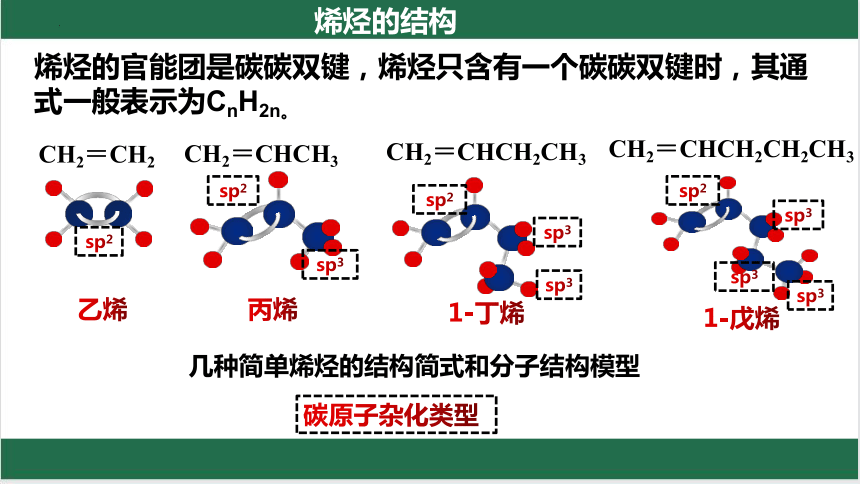
几种简单烯烃的结构简式和分子结构模型
CH2=CH2
乙烯
CH2=CHCH3
丙烯
CH2=CHCH2CH3
1-丁烯
CH2=CHCH2CH2CH3
1-戊烯
烯烃的结构
烯烃的官能团是碳碳双键,烯烃只含有一个碳碳双键时,其通式一般表示为CnH2n。
碳原子杂化类型
sp3
sp3
sp3
sp3
sp3
sp3
sp2
sp2
sp2
sp2
随着碳原子数的增多,沸点依次升高
质量分数:烯烃中的碳和氢的质量分数为恒定值,碳为85.7%,氢为14.3%
烯烃的物理性质
思考与讨论1:结合单烯烃的结构简式及沸点、相对密度,分析烯烃的物理性质,它们有着怎样的递变性? 为什么?
密度依次增大
(密度小于水)
C2-C4为气态
随着分子中碳原子数的递增,
1、相对分子质量越大, 分子间作用力越强, 沸点逐渐升高。
2、密度逐渐增大,都小于水的密度。
3、常温下的状态:气态→液态→固态。
标准状况下 C2—C4呈气态
碳原子数相同时,支链越多,熔沸点越低。
4、溶解性:
不溶于水,易溶于有机溶剂
烯烃的物理性质
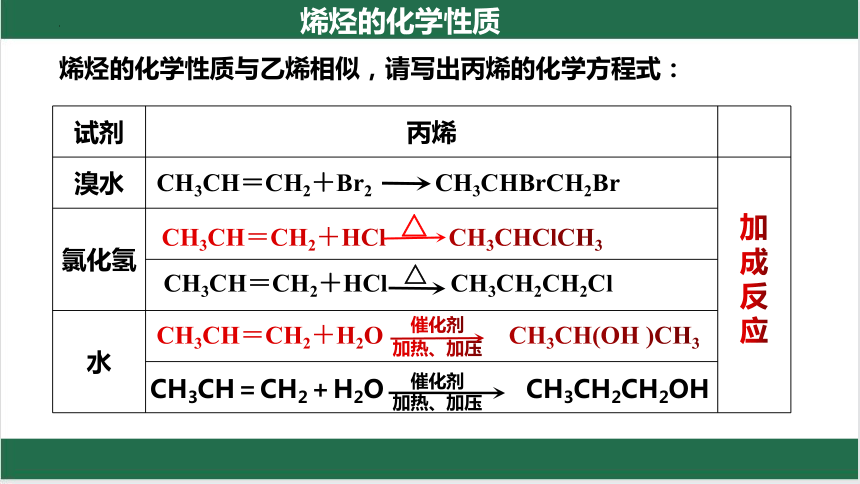
试剂 丙烯
溴水
氯化氢 水 CH3CH=CH2+Br2 CH3CHBrCH2Br
CH3CH=CH2+HCl CH3CH2CH2Cl
△
CH3CH=CH2+HCl CH3CHClCH3
△
CH3CH=CH2+H2O CH3CH2CH2OH
催化剂
加热、加压
CH3CH=CH2+H2O CH3CH(OH )CH3
催化剂
加热、加压
烯烃的化学性质与乙烯相似,请写出丙烯的化学方程式:
烯烃的化学性质
加成反应
烯烃的加聚反应
nCH2=CH2 [ CH2—CH2 ]n
一定条件下
一定条件
一定条件
烯烃的化学性质
单体
链节
聚合度
①可燃性
O2
nCO2+nH2O
CnH2n+
烯烃的氧化反应
②使酸性KMnO4溶液褪色
CH2=
CO2
KMnO4
H+
KMnO4
H+
C=O
R'
R''
C=
R'
R''
酮
R—CH=
R—COOH
KMnO4
H+
羧酸
二氢成气
一氢成酸
无氢成酮
烯烃的化学性质
二烯烃:
分子中含2个碳碳双键的烯烃
CH2=CH—CH=CH2与Cl2的反应方程式:
CH2=CH—CH=CH2+Cl2
CH2—CH—CH=CH2
Cl
Cl
(1)1,2-加成
CH2=CH—CH=CH2+Cl2
CH2—CH=CH—CH2
Cl
Cl
(2)1,4-加成
如最常见的1,3-丁二烯(CH2=CH—CH=CH2)
1,3-丁二烯的1,2-加成和1,4-加成是竞争反应,到底哪一种加成产物占优势取决于反应条件。
二烯烃的化学性质
Diels—Alder成环反应
二烯烃的化学性质
共轭二烯烃的特征反应
1-丁烯与1,3-丁二烯反应
二烯烃的化学性质
2-丁烯与1,3-丁二烯反应
共轭二烯烃的特征反应
烯烃的立体异构
通过碳碳双键连接的原子或原子团不能绕键轴旋转会导致其空间排列方式不同,产生顺反异构现象。
产生顺反异构体的条件:
②组成双键的每个碳原子必须连接两个不同的原子或原子团
有顺反异构的类型
无顺反异构的类型
①具有碳碳双键
顺-2-丁烯
反-2-丁烯
烯烃的立体异构
顺反异构体的化学性质基本相同,物理性质有一定的差异。
熔点:-138.9℃
沸点:3.7℃
密度:0.621g.cm-3
熔点:-105.5℃
沸点:0.9℃
密度:0.604g.cm-3
相同的原子或原子团位于双键同一侧为顺式结构
相同的原子或原子团位于双键两侧为反式结构
化学性质
氧化反应
加成反应
加聚反应
①可燃性
②使酸性KMnO4溶液褪色
O2
nCO2+nH2O
CnH2n+
卤素单质或其溶液
卤代烃
氢气
烷烃
卤化氢
卤代烃
水
醇
生成高分子化合物
小结
(1)通式符合CnH2n的烃都是烯烃( )
(2)乙烯和聚乙烯都能使溴水褪色( )
(3)乙烯能使溴水和酸性高锰酸钾溶液褪色,发生的反应类型相同( )
(4)丁烷有2种同分异构体,故丁烯也有2种同分异构体( )
(5)通入氢气可以除去乙烷中的少量乙烯( )
×
×
1.正误判断
×
×
×
达标检测
2.下列物质不存在顺反立体异构的是( )
B
达标检测
3.下列说法中,错误的是( )
A.无论乙烯的加成,还是乙烯使酸性KMnO4溶液褪色,都与乙烯分子中含有的碳碳双键有关
B.无论使用溴的四氯化碳溶液还是酸性KMnO4溶液都可以鉴别乙烯和乙烷
C.相同质量的乙烯和甲烷完全燃烧后生成的水的质量相同
D.乙烯的化学性质比乙烷的化学性质活泼
C
达标检测
4.某烃的结构用键线式可表示为 ,则该烃与Br2加成时(物质的量之比为1∶1)所得产物有( )
A.3种 B.4种 C.5种 D.6种
C
达标检测
5. 1 mol某气态烃能与1 mol氯化氢发生加成反应,加成后的产物又可与7 mol氯气发生完全的取代反应,则该烃的结构简式为( )
A.CH2=CH2 B.CH3CH=CH2
C.CH3CH2CH=CH2 D.CH3CH2CH2CH=CH2
B
达标检测
B
达标检测
第二章 烃
2019人教版选择性必修三
第二节 烯烃 炔烃
第一课时 烯烃
核心素养发展目标
1.理解烯烃的结构与化学性质,培养宏观辨识与微观探析的能力。
2.了解烯烃的顺反异构及二烯烃的加成反应,培养微观探析与变化观念的能力。
乙烯的结构
乙烯的结构
碳原子均采取_____杂化
sp2
碳原子与氢原子之间以__________相连接
单键(σ键)
碳原子与碳原子之间以_________________________连接
双键(1个σ键和1个π键)
相邻两个键之间的键角约为_____
分子中的_____原子处在同一平面内
120°
所有
C
C
H
H
H
H
σ键
σ键
π键
σ键
133pm
120°
120°
120°
键长:
(说明C=C比C-C活泼)
(C-C)<(C=C)<(C-C)
1
2
键能:
E(C-C)
物理性质
化学性质
纯净的乙烯为无色、稍有气味的气体,
难溶于水,密度比空气略小。
氧化反应
加成反应
加聚反应
①可燃性
C2H4+3O2 2CO2+2H2O
点燃
②使酸性KMnO4溶液褪色,生成CO2
CH2=CH2+Br2 CH2BrCH2Br
nCH2=CH2 [ CH2—CH2 ]n
一定条件下
CH2=CH2+HX
CH3CH2X
CH2=CH2+H2O
CH3CH2OH
CH2=CH2+H2
CH3CH3
乙烯的性质
几种简单烯烃的结构简式和分子结构模型
CH2=CH2
乙烯
CH2=CHCH3
丙烯
CH2=CHCH2CH3
1-丁烯
CH2=CHCH2CH2CH3
1-戊烯
烯烃的结构
烯烃的官能团是碳碳双键,烯烃只含有一个碳碳双键时,其通式一般表示为CnH2n。
碳原子杂化类型
sp3
sp3
sp3
sp3
sp3
sp3
sp2
sp2
sp2
sp2
随着碳原子数的增多,沸点依次升高
质量分数:烯烃中的碳和氢的质量分数为恒定值,碳为85.7%,氢为14.3%
烯烃的物理性质
思考与讨论1:结合单烯烃的结构简式及沸点、相对密度,分析烯烃的物理性质,它们有着怎样的递变性? 为什么?
密度依次增大
(密度小于水)
C2-C4为气态
随着分子中碳原子数的递增,
1、相对分子质量越大, 分子间作用力越强, 沸点逐渐升高。
2、密度逐渐增大,都小于水的密度。
3、常温下的状态:气态→液态→固态。
标准状况下 C2—C4呈气态
碳原子数相同时,支链越多,熔沸点越低。
4、溶解性:
不溶于水,易溶于有机溶剂
烯烃的物理性质
试剂 丙烯
溴水
氯化氢 水 CH3CH=CH2+Br2 CH3CHBrCH2Br
CH3CH=CH2+HCl CH3CH2CH2Cl
△
CH3CH=CH2+HCl CH3CHClCH3
△
CH3CH=CH2+H2O CH3CH2CH2OH
催化剂
加热、加压
CH3CH=CH2+H2O CH3CH(OH )CH3
催化剂
加热、加压
烯烃的化学性质与乙烯相似,请写出丙烯的化学方程式:
烯烃的化学性质
加成反应
烯烃的加聚反应
nCH2=CH2 [ CH2—CH2 ]n
一定条件下
一定条件
一定条件
烯烃的化学性质
单体
链节
聚合度
①可燃性
O2
nCO2+nH2O
CnH2n+
烯烃的氧化反应
②使酸性KMnO4溶液褪色
CH2=
CO2
KMnO4
H+
KMnO4
H+
C=O
R'
R''
C=
R'
R''
酮
R—CH=
R—COOH
KMnO4
H+
羧酸
二氢成气
一氢成酸
无氢成酮
烯烃的化学性质
二烯烃:
分子中含2个碳碳双键的烯烃
CH2=CH—CH=CH2与Cl2的反应方程式:
CH2=CH—CH=CH2+Cl2
CH2—CH—CH=CH2
Cl
Cl
(1)1,2-加成
CH2=CH—CH=CH2+Cl2
CH2—CH=CH—CH2
Cl
Cl
(2)1,4-加成
如最常见的1,3-丁二烯(CH2=CH—CH=CH2)
1,3-丁二烯的1,2-加成和1,4-加成是竞争反应,到底哪一种加成产物占优势取决于反应条件。
二烯烃的化学性质
Diels—Alder成环反应
二烯烃的化学性质
共轭二烯烃的特征反应
1-丁烯与1,3-丁二烯反应
二烯烃的化学性质
2-丁烯与1,3-丁二烯反应
共轭二烯烃的特征反应
烯烃的立体异构
通过碳碳双键连接的原子或原子团不能绕键轴旋转会导致其空间排列方式不同,产生顺反异构现象。
产生顺反异构体的条件:
②组成双键的每个碳原子必须连接两个不同的原子或原子团
有顺反异构的类型
无顺反异构的类型
①具有碳碳双键
顺-2-丁烯
反-2-丁烯
烯烃的立体异构
顺反异构体的化学性质基本相同,物理性质有一定的差异。
熔点:-138.9℃
沸点:3.7℃
密度:0.621g.cm-3
熔点:-105.5℃
沸点:0.9℃
密度:0.604g.cm-3
相同的原子或原子团位于双键同一侧为顺式结构
相同的原子或原子团位于双键两侧为反式结构
化学性质
氧化反应
加成反应
加聚反应
①可燃性
②使酸性KMnO4溶液褪色
O2
nCO2+nH2O
CnH2n+
卤素单质或其溶液
卤代烃
氢气
烷烃
卤化氢
卤代烃
水
醇
生成高分子化合物
小结
(1)通式符合CnH2n的烃都是烯烃( )
(2)乙烯和聚乙烯都能使溴水褪色( )
(3)乙烯能使溴水和酸性高锰酸钾溶液褪色,发生的反应类型相同( )
(4)丁烷有2种同分异构体,故丁烯也有2种同分异构体( )
(5)通入氢气可以除去乙烷中的少量乙烯( )
×
×
1.正误判断
×
×
×
达标检测
2.下列物质不存在顺反立体异构的是( )
B
达标检测
3.下列说法中,错误的是( )
A.无论乙烯的加成,还是乙烯使酸性KMnO4溶液褪色,都与乙烯分子中含有的碳碳双键有关
B.无论使用溴的四氯化碳溶液还是酸性KMnO4溶液都可以鉴别乙烯和乙烷
C.相同质量的乙烯和甲烷完全燃烧后生成的水的质量相同
D.乙烯的化学性质比乙烷的化学性质活泼
C
达标检测
4.某烃的结构用键线式可表示为 ,则该烃与Br2加成时(物质的量之比为1∶1)所得产物有( )
A.3种 B.4种 C.5种 D.6种
C
达标检测
5. 1 mol某气态烃能与1 mol氯化氢发生加成反应,加成后的产物又可与7 mol氯气发生完全的取代反应,则该烃的结构简式为( )
A.CH2=CH2 B.CH3CH=CH2
C.CH3CH2CH=CH2 D.CH3CH2CH2CH=CH2
B
达标检测
B
达标检测
