8.1溶液的酸碱性同步练习科粤版化学九年级下册(含答案)
文档属性
| 名称 | 8.1溶液的酸碱性同步练习科粤版化学九年级下册(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 724.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-09 00:00:00 | ||
图片预览


文档简介
8.1溶液的酸碱性
一、多选题
1.如图为天然气在酸性环境中脱硫过程的原理,说法正确的是
A.整个过程涉及的元素中仅Fe、O元素的化合价发生了变化
B.工业上,每吸收3.4t H2S,需提供约1.6tO2
C.随着反应的进行,整个溶液的pH变大
D.理论上,每消耗1.7t H2S,需向体系内再补充4.9t H2SO4
2.下列图像分别与选项中的操作相对应,合理的是
A.向等质量的水中分别加入相同质量的氢氧化钠固体和硝酸铵固体
B. 在盛有空气的密闭容器中点燃红磷
C.向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉
D.向一定质量的稀盐酸中不断加入氢氧化钠溶液
3.向一定量的稀盐酸中逐滴加入氢氧化钠溶液至过量,测得水的质量、氯化钠的质量随氢氧化钠溶液质量的变化如图所示。说法正确的是
A.乙表示的物质为水 B.a→b,所得溶液的酸性逐渐减弱
C.b→c,所得溶液中氯化钠的质量没有变化 D.0→c,所得溶液中NaOH的质量不断增加
4.某同学做HCl和NaOH的中和反应实验时,测得反应过程中溶液的酸碱度变化如图所示。下列说法中正确的是( )
A.该实验是把稀盐酸加入氢氧化钠溶液中
B.加入溶液a g时,溶液呈酸性
C.当加入溶液10g时,HCl和NaOH恰好完全反应
D.加入溶液b g时,溶液呈碱性
5.下列所示的图像不能反映相对应实验的是
A.向pH=12的Ca(OH)2溶液中不断加水稀释
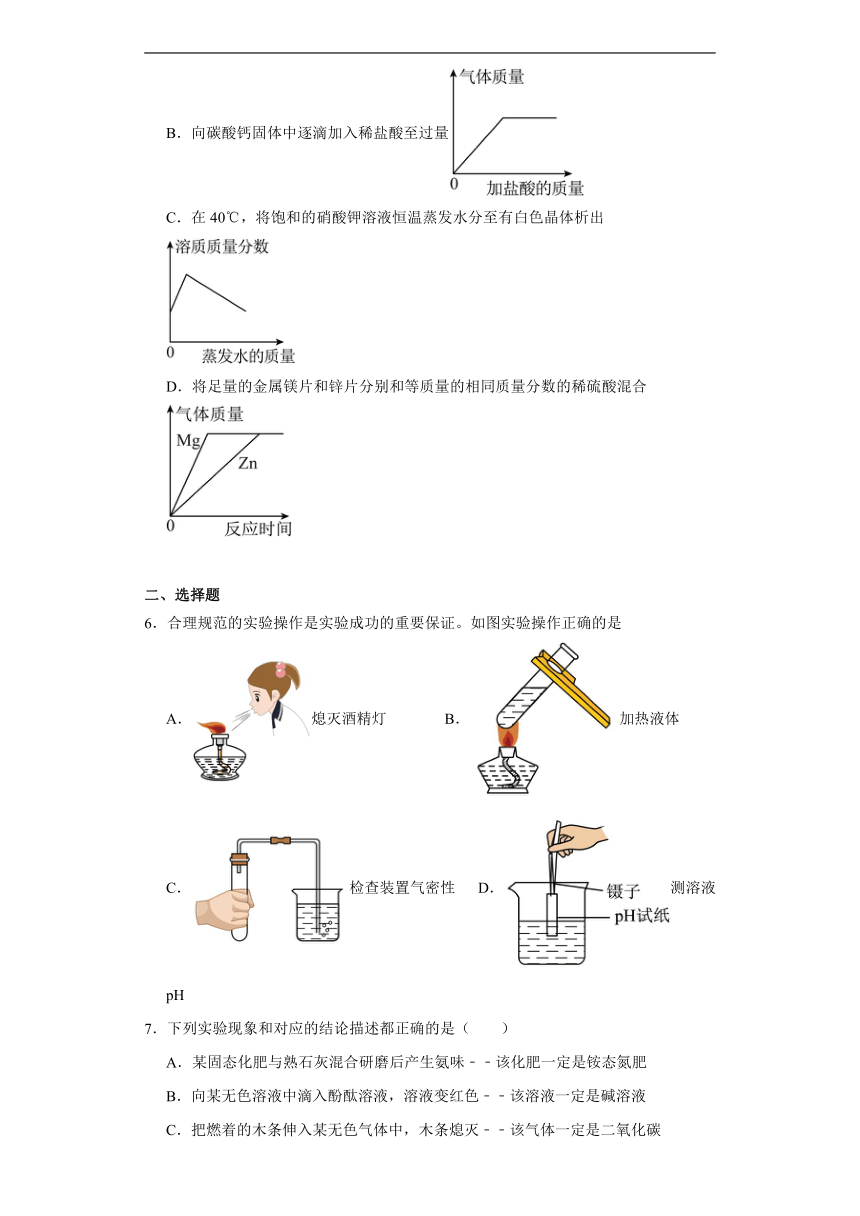
B.向碳酸钙固体中逐滴加入稀盐酸至过量
C.在40℃,将饱和的硝酸钾溶液恒温蒸发水分至有白色晶体析出
D.将足量的金属镁片和锌片分别和等质量的相同质量分数的稀硫酸混合
二、选择题
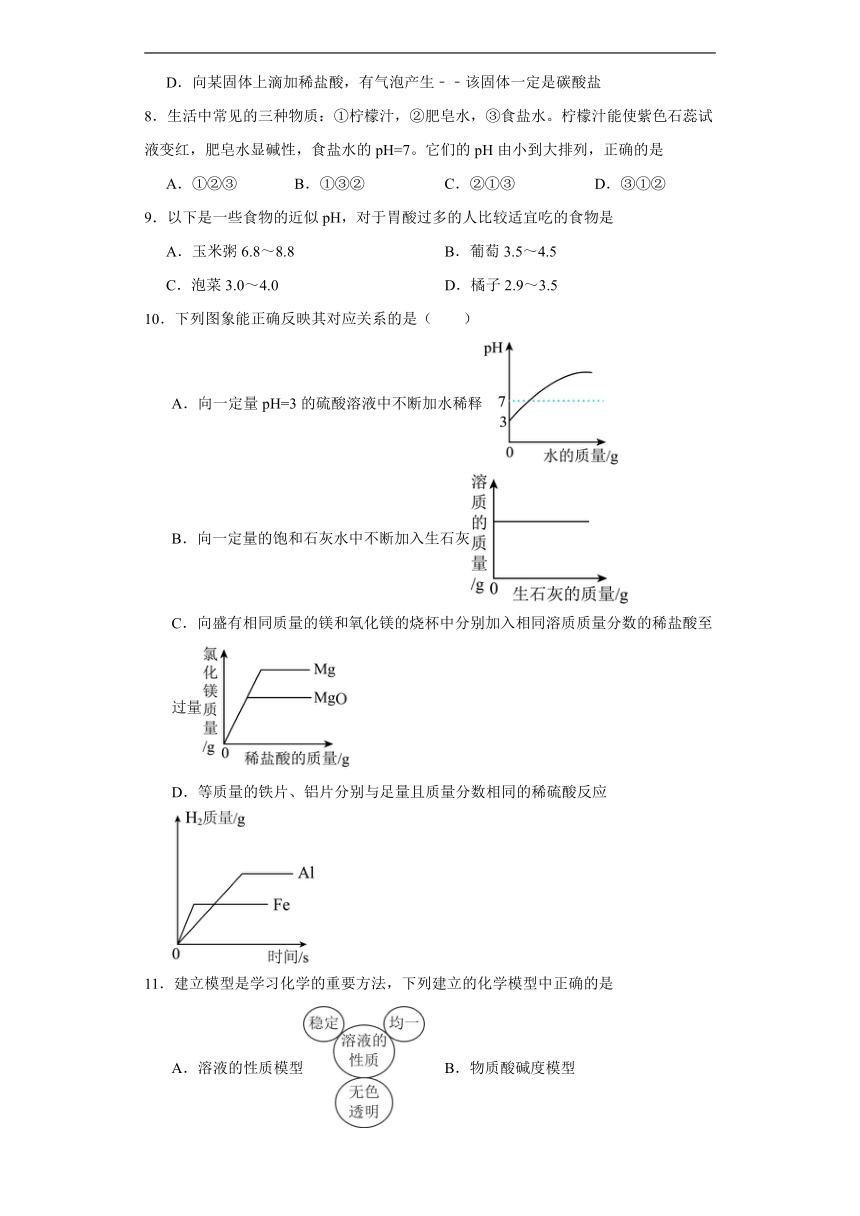
6.合理规范的实验操作是实验成功的重要保证。如图实验操作正确的是
A.熄灭酒精灯 B.加热液体
C.检查装置气密性 D.测溶液pH
7.下列实验现象和对应的结论描述都正确的是( )
A.某固态化肥与熟石灰混合研磨后产生氨味﹣﹣该化肥一定是铵态氮肥
B.向某无色溶液中滴入酚酞溶液,溶液变红色﹣﹣该溶液一定是碱溶液
C.把燃着的木条伸入某无色气体中,木条熄灭﹣﹣该气体一定是二氧化碳
D.向某固体上滴加稀盐酸,有气泡产生﹣﹣该固体一定是碳酸盐
8.生活中常见的三种物质:①柠檬汁,②肥皂水,③食盐水。柠檬汁能使紫色石蕊试液变红,肥皂水显碱性,食盐水的pH=7。它们的pH由小到大排列,正确的是
A.①②③ B.①③② C.②①③ D.③①②
9.以下是一些食物的近似pH,对于胃酸过多的人比较适宜吃的食物是
A.玉米粥6.8~8.8 B.葡萄3.5~4.5
C.泡菜3.0~4.0 D.橘子2.9~3.5
10.下列图象能正确反映其对应关系的是( )
A.向一定量pH=3的硫酸溶液中不断加水稀释
B.向一定量的饱和石灰水中不断加入生石灰
C.向盛有相同质量的镁和氧化镁的烧杯中分别加入相同溶质质量分数的稀盐酸至过量
D.等质量的铁片、铝片分别与足量且质量分数相同的稀硫酸反应
11.建立模型是学习化学的重要方法,下列建立的化学模型中正确的是
A.溶液的性质模型 B.物质酸碱度模型
C.物质的分类模型 D.氧化反应与复分解反应的关系模型
12.下列实验操作,错误的是
A.加热液体 B.熄灭酒精灯
C.检验装置气密性 D.测某溶液pH值
13.常温下向一定量的澄清石灰水中逐渐加入生石灰(忽略挥发)。下列图像正确的是
A.④ B.①④ C.②④ D.①②④
14.学习要善于分析比较,去伪存真。下列说法中正确的一项是
A.不能使酚酞变色的溶液的pH一定等于7
B.已知NaHSO4在溶液中离解出Na+、H+和SO42-,其pH<7,但不是酸
C.上网查资料得知水也能离解出极少量H+和OH-,所以水既可看作酸也可看作碱
D.甲用石蕊试液测知某果汁液变红色;乙改用pH试纸测知pH=8.2
15.将一定质量分数的烧碱溶液加水稀释,下列各图能正确表示加水量与溶液的pH变化的是
A. B. C. D.
三、综合应用题
16.甜瓜珍品——江西梨瓜以“脆、甜、香”而闻名。梨瓜中含有丰富的蛋白质、粗纤维、维生素、钙、磷、铁、镁、钾、硒等人体所需的营养素;
(1)梨瓜贮存时常套一个塑料袋,其作用是阻止梨瓜中水分流失,还能隔绝 防止腐烂;
(2)梨瓜适宜生长在pH为6.0-6.8的土壤中,实验室测定溶液pH的操作方法是 ;
(3)如图为硒元素的某些信息,硒原子核内有 个质子,硒原子的相对原子质量是 ,硒原子在化学反应中易 (填“得到”或“失去”)电子。
17.化学是以实验为基础的科学,科学探究是学习化学的重要手段。
(1)写出图中不能用于直接加热的仪器名称 。
(2)了解溶液的酸碱性,对于生活、生产以及人类的生命活动具有重要的意义。
①测酸碱度常用pH试纸,用pH试纸测定溶液的酸碱度,操作方法是: 。
②下图是绘制的氢氧化钙溶液与稀盐酸反应时的pH值变化图,据图判断横坐标溶液中所含的离子主要有 ,滴入溶液体积为V2mL时,溶液中的溶质为 。
(3)利用下图装置可以用纯净、干燥的CO还原Fe2O3并检验气体产物。已知由一氧化碳发生装置得到的CO中混有杂质CO2和H2O。
①请写出装置C玻璃管发生化学反应的方程式。
②实验中装置D的作用是什么?
③请分析上述反应装置是否合理,如不合理提出改进建议。
(4)为测定某石灰石样品中碳酸钙的质量分数,称取1g石灰石(杂质不参加反应)放入烧杯中,加入18g稀盐酸,二者恰好完全反应,反应后烧杯中剩余物质的总质量为18.67g(气体的溶解忽略不计)。请计算该样品中碳酸钙的质量分数。
18.氯化铜晶体(CuC12·xH2O)是重要的化工原料,可用作催化剂、消毒剂等。用孔雀石【主要成分是Cu2(OH)2CO3,还含少量Fe、Si的化合物】制备氯化铜晶体的方案如图:
已知:I、FeCl3和FeCl2可相互转换:,3
Ⅱ、有关金属氢氧化物沉淀时溶液的pH:
pH Fe(OH)3 Cu(OH)2 Fe(OH)2
开始沉淀的pH 2.7 5.4 8.1
沉淀完全的pH 3.7 6.9 9.6
(1)溶液B中含有金属离子Cu2+、Fe2+、Fe3+,则试剂①应选用______(填字母):
A.Fe B.Cl2 C.NH3·H2O D.NaOH
(2)加入试剂2的目的是调节pH至a,a的范围是 ,由溶液E获得CuC12·xH2O,包含的4个基本操作依次是 →冷却结晶→过滤→无水酒精洗涤滤渣。洗涤时使用无水酒精而不使用水的主要原因是 。
(3)为测定氯化铜晶体【CuC12·xH2O】中x的值,称取ag晶体、加入足量氢氧化钠溶液,过滤、洗涤、加热沉淀至完全转化成氧化铜,称量所得黑色固体质量为bg。则x= (用含a、b的代数式表示)。
参考答案:
1.BC
2.BC
3.BC
4.BCD
5.AC
6.C
7.A
8.B
9.A
10.C
11.B
12.A
13.A
14.B
15.D
16. 氧气 用玻璃棒蘸取待测液,滴到pH试纸上,把试纸显示的颜色与标准比色卡比较,读出溶液的pH 34 78.96 得到
17. 烧杯 用玻璃棒蘸取待测液滴在pH试纸上,将显示的颜色与标准比色卡对比,即可得到溶液的pH值 H+和Cl- 氯化钙和氯化氢(或CaCl2和HCl) 吸收并证明反应后生成有二氧化碳(合理即可) 不合理,应加装反应后尾气收集或点燃装置(合理即可) 75%
18.(1)B
(2) 3.7≤a<5.4/5.4>a≥3.7 蒸发浓缩 防止晶体因溶解而损失
(3)
一、多选题
1.如图为天然气在酸性环境中脱硫过程的原理,说法正确的是
A.整个过程涉及的元素中仅Fe、O元素的化合价发生了变化
B.工业上,每吸收3.4t H2S,需提供约1.6tO2
C.随着反应的进行,整个溶液的pH变大
D.理论上,每消耗1.7t H2S,需向体系内再补充4.9t H2SO4
2.下列图像分别与选项中的操作相对应,合理的是
A.向等质量的水中分别加入相同质量的氢氧化钠固体和硝酸铵固体
B. 在盛有空气的密闭容器中点燃红磷
C.向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉
D.向一定质量的稀盐酸中不断加入氢氧化钠溶液
3.向一定量的稀盐酸中逐滴加入氢氧化钠溶液至过量,测得水的质量、氯化钠的质量随氢氧化钠溶液质量的变化如图所示。说法正确的是
A.乙表示的物质为水 B.a→b,所得溶液的酸性逐渐减弱
C.b→c,所得溶液中氯化钠的质量没有变化 D.0→c,所得溶液中NaOH的质量不断增加
4.某同学做HCl和NaOH的中和反应实验时,测得反应过程中溶液的酸碱度变化如图所示。下列说法中正确的是( )
A.该实验是把稀盐酸加入氢氧化钠溶液中
B.加入溶液a g时,溶液呈酸性
C.当加入溶液10g时,HCl和NaOH恰好完全反应
D.加入溶液b g时,溶液呈碱性
5.下列所示的图像不能反映相对应实验的是
A.向pH=12的Ca(OH)2溶液中不断加水稀释
B.向碳酸钙固体中逐滴加入稀盐酸至过量
C.在40℃,将饱和的硝酸钾溶液恒温蒸发水分至有白色晶体析出
D.将足量的金属镁片和锌片分别和等质量的相同质量分数的稀硫酸混合
二、选择题
6.合理规范的实验操作是实验成功的重要保证。如图实验操作正确的是
A.熄灭酒精灯 B.加热液体
C.检查装置气密性 D.测溶液pH
7.下列实验现象和对应的结论描述都正确的是( )
A.某固态化肥与熟石灰混合研磨后产生氨味﹣﹣该化肥一定是铵态氮肥
B.向某无色溶液中滴入酚酞溶液,溶液变红色﹣﹣该溶液一定是碱溶液
C.把燃着的木条伸入某无色气体中,木条熄灭﹣﹣该气体一定是二氧化碳
D.向某固体上滴加稀盐酸,有气泡产生﹣﹣该固体一定是碳酸盐
8.生活中常见的三种物质:①柠檬汁,②肥皂水,③食盐水。柠檬汁能使紫色石蕊试液变红,肥皂水显碱性,食盐水的pH=7。它们的pH由小到大排列,正确的是
A.①②③ B.①③② C.②①③ D.③①②
9.以下是一些食物的近似pH,对于胃酸过多的人比较适宜吃的食物是
A.玉米粥6.8~8.8 B.葡萄3.5~4.5
C.泡菜3.0~4.0 D.橘子2.9~3.5
10.下列图象能正确反映其对应关系的是( )
A.向一定量pH=3的硫酸溶液中不断加水稀释
B.向一定量的饱和石灰水中不断加入生石灰
C.向盛有相同质量的镁和氧化镁的烧杯中分别加入相同溶质质量分数的稀盐酸至过量
D.等质量的铁片、铝片分别与足量且质量分数相同的稀硫酸反应
11.建立模型是学习化学的重要方法,下列建立的化学模型中正确的是
A.溶液的性质模型 B.物质酸碱度模型
C.物质的分类模型 D.氧化反应与复分解反应的关系模型
12.下列实验操作,错误的是
A.加热液体 B.熄灭酒精灯
C.检验装置气密性 D.测某溶液pH值
13.常温下向一定量的澄清石灰水中逐渐加入生石灰(忽略挥发)。下列图像正确的是
A.④ B.①④ C.②④ D.①②④
14.学习要善于分析比较,去伪存真。下列说法中正确的一项是
A.不能使酚酞变色的溶液的pH一定等于7
B.已知NaHSO4在溶液中离解出Na+、H+和SO42-,其pH<7,但不是酸
C.上网查资料得知水也能离解出极少量H+和OH-,所以水既可看作酸也可看作碱
D.甲用石蕊试液测知某果汁液变红色;乙改用pH试纸测知pH=8.2
15.将一定质量分数的烧碱溶液加水稀释,下列各图能正确表示加水量与溶液的pH变化的是
A. B. C. D.
三、综合应用题
16.甜瓜珍品——江西梨瓜以“脆、甜、香”而闻名。梨瓜中含有丰富的蛋白质、粗纤维、维生素、钙、磷、铁、镁、钾、硒等人体所需的营养素;
(1)梨瓜贮存时常套一个塑料袋,其作用是阻止梨瓜中水分流失,还能隔绝 防止腐烂;
(2)梨瓜适宜生长在pH为6.0-6.8的土壤中,实验室测定溶液pH的操作方法是 ;
(3)如图为硒元素的某些信息,硒原子核内有 个质子,硒原子的相对原子质量是 ,硒原子在化学反应中易 (填“得到”或“失去”)电子。
17.化学是以实验为基础的科学,科学探究是学习化学的重要手段。
(1)写出图中不能用于直接加热的仪器名称 。
(2)了解溶液的酸碱性,对于生活、生产以及人类的生命活动具有重要的意义。
①测酸碱度常用pH试纸,用pH试纸测定溶液的酸碱度,操作方法是: 。
②下图是绘制的氢氧化钙溶液与稀盐酸反应时的pH值变化图,据图判断横坐标溶液中所含的离子主要有 ,滴入溶液体积为V2mL时,溶液中的溶质为 。
(3)利用下图装置可以用纯净、干燥的CO还原Fe2O3并检验气体产物。已知由一氧化碳发生装置得到的CO中混有杂质CO2和H2O。
①请写出装置C玻璃管发生化学反应的方程式。
②实验中装置D的作用是什么?
③请分析上述反应装置是否合理,如不合理提出改进建议。
(4)为测定某石灰石样品中碳酸钙的质量分数,称取1g石灰石(杂质不参加反应)放入烧杯中,加入18g稀盐酸,二者恰好完全反应,反应后烧杯中剩余物质的总质量为18.67g(气体的溶解忽略不计)。请计算该样品中碳酸钙的质量分数。
18.氯化铜晶体(CuC12·xH2O)是重要的化工原料,可用作催化剂、消毒剂等。用孔雀石【主要成分是Cu2(OH)2CO3,还含少量Fe、Si的化合物】制备氯化铜晶体的方案如图:
已知:I、FeCl3和FeCl2可相互转换:,3
Ⅱ、有关金属氢氧化物沉淀时溶液的pH:
pH Fe(OH)3 Cu(OH)2 Fe(OH)2
开始沉淀的pH 2.7 5.4 8.1
沉淀完全的pH 3.7 6.9 9.6
(1)溶液B中含有金属离子Cu2+、Fe2+、Fe3+,则试剂①应选用______(填字母):
A.Fe B.Cl2 C.NH3·H2O D.NaOH
(2)加入试剂2的目的是调节pH至a,a的范围是 ,由溶液E获得CuC12·xH2O,包含的4个基本操作依次是 →冷却结晶→过滤→无水酒精洗涤滤渣。洗涤时使用无水酒精而不使用水的主要原因是 。
(3)为测定氯化铜晶体【CuC12·xH2O】中x的值,称取ag晶体、加入足量氢氧化钠溶液,过滤、洗涤、加热沉淀至完全转化成氧化铜,称量所得黑色固体质量为bg。则x= (用含a、b的代数式表示)。
参考答案:
1.BC
2.BC
3.BC
4.BCD
5.AC
6.C
7.A
8.B
9.A
10.C
11.B
12.A
13.A
14.B
15.D
16. 氧气 用玻璃棒蘸取待测液,滴到pH试纸上,把试纸显示的颜色与标准比色卡比较,读出溶液的pH 34 78.96 得到
17. 烧杯 用玻璃棒蘸取待测液滴在pH试纸上,将显示的颜色与标准比色卡对比,即可得到溶液的pH值 H+和Cl- 氯化钙和氯化氢(或CaCl2和HCl) 吸收并证明反应后生成有二氧化碳(合理即可) 不合理,应加装反应后尾气收集或点燃装置(合理即可) 75%
18.(1)B
(2) 3.7≤a<5.4/5.4>a≥3.7 蒸发浓缩 防止晶体因溶解而损失
(3)
