8.2金属的化学性质同步练习人教版化学九年级下册(含答案)
文档属性
| 名称 | 8.2金属的化学性质同步练习人教版化学九年级下册(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 261.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-10 00:00:00 | ||
图片预览



文档简介
8.2金属的化学性质
一、多选题
1.为探究铝、锌、铜三种金属的活动性顺序,某学习小组做了如甲图所示实验。实验结束后,将试管①、试管②内的物质全部倒入同烧杯中,经过充分反应后烧杯中的红色固体物质比刚混合时明显增多(如乙图所示)。
下列说法正确的是
A.反应后烧杯中的固体一定含有锌
B.甲图试管②中反应后固体一定不含锌
C.反应后烧杯中的溶液不确定是否含有氯化铜
D.烧杯中最后所得固体的质量一定大于 2克
2.化学小组为探究铝、铜、银三种金属的活动性顺序,设计了下图所示实验方案(金属 丝使用时均已用砂纸打磨)。下列说法正确的是
A.由实验甲可知金属活动性:Al>Cu
B.由实验乙可知金属活动性:Ag>Cu
C.实验甲中的CuSO4改为CuCl2,也能完成本实验探究
D.若要探究铝、铜、银活动性顺序,甲、乙、丙实验必须全做
3.两种金属的混合物11克,加入足量的稀硫酸,经实验测得生成的氢气为1克,则这种混合物粉末可能是
A.铝和镁 B.镁和锌 C.锌和铁 D.铝和铜
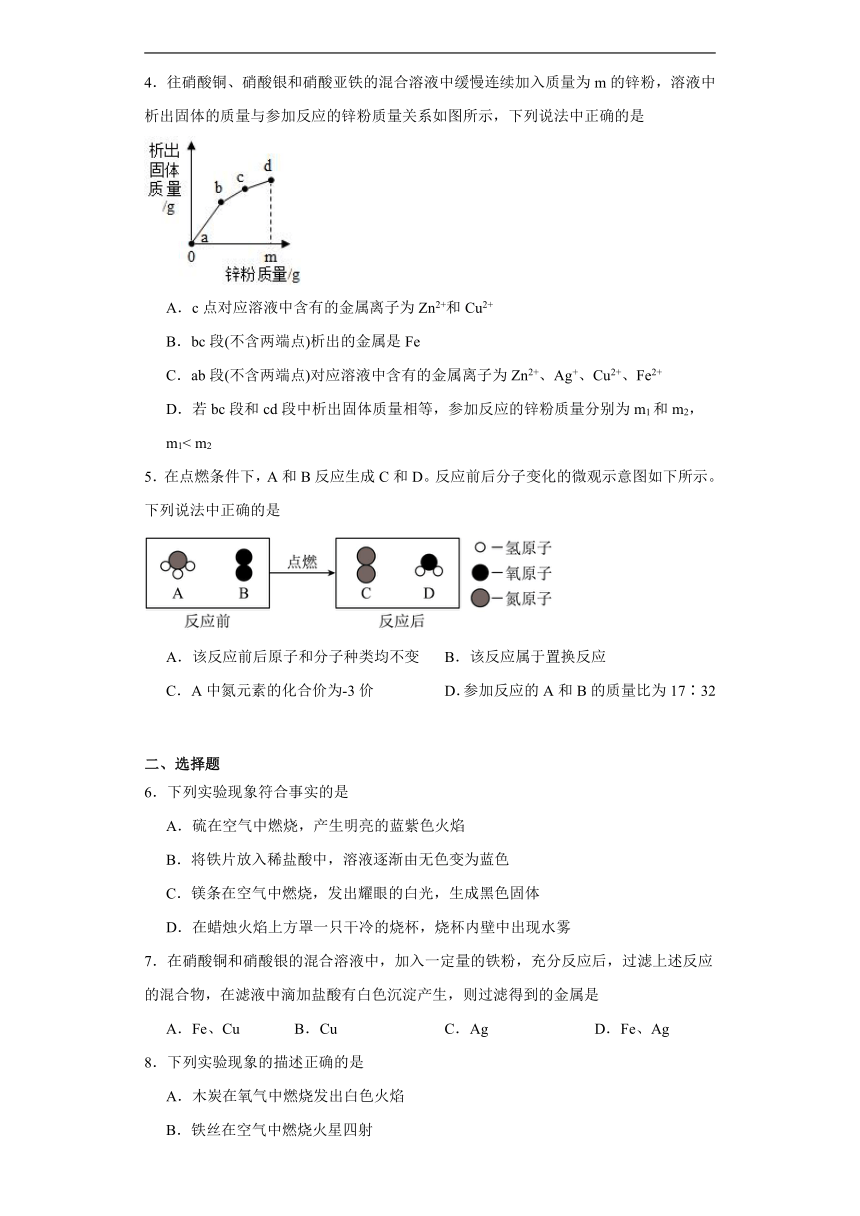
4.往硝酸铜、硝酸银和硝酸亚铁的混合溶液中缓慢连续加入质量为m的锌粉,溶液中析出固体的质量与参加反应的锌粉质量关系如图所示,下列说法中正确的是
A.c点对应溶液中含有的金属离子为Zn2+和Cu2+
B.bc段(不含两端点)析出的金属是Fe
C.ab段(不含两端点)对应溶液中含有的金属离子为Zn2+、Ag+、Cu2+、Fe2+
D.若bc段和cd段中析出固体质量相等,参加反应的锌粉质量分别为m1和m2,m1< m2
5.在点燃条件下,A和B反应生成C和D。反应前后分子变化的微观示意图如下所示。下列说法中正确的是
A.该反应前后原子和分子种类均不变 B.该反应属于置换反应
C.A中氮元素的化合价为-3价 D.参加反应的A和B的质量比为17∶32
二、选择题
6.下列实验现象符合事实的是
A.硫在空气中燃烧,产生明亮的蓝紫色火焰
B.将铁片放入稀盐酸中,溶液逐渐由无色变为蓝色
C.镁条在空气中燃烧,发出耀眼的白光,生成黑色固体
D.在蜡烛火焰上方罩一只干冷的烧杯,烧杯内壁中出现水雾
7.在硝酸铜和硝酸银的混合溶液中,加入一定量的铁粉,充分反应后,过滤上述反应的混合物,在滤液中滴加盐酸有白色沉淀产生,则过滤得到的金属是
A.Fe、Cu B.Cu C.Ag D.Fe、Ag
8.下列实验现象的描述正确的是
A.木炭在氧气中燃烧发出白色火焰
B.铁丝在空气中燃烧火星四射
C.镁条在空气中燃烧发出耀眼白光
D.铁片在稀盐酸中逐渐溶解,有气泡产生,溶液由无色变成蓝色
9.某反应的微观示意图如下,下列说法正确的是
A.图中反应的基本类型是置换反应
B.反应前后元素的种类及化合价均不变
C.反应涉及到的物质中, 属于单质,只有 属于氧化物
D.参加反应的 和 的微粒个数比是4∶3
10.下列排序正确的是
A.地壳中元素含量:
B.空气中体积分数:
C.金属活动性顺序:
D.氯元素的化合价:
11.下列化学方程式及基本反应类型均正确的是
A.H2CO3H2O+CO2分解反应 B.Al+H2SO4=Al2(SO4)3+H2↑ 化合反应
C.2Mg+O22MgO 氧化反应 D.2Na+CuSO4=Na2SO4+Cu 置换反应
12.小明取等质量的铁片和铁粉分别放入两支试管中,分别加入相同体积、相同浓度的足量稀盐酸。下列示意图中,与实验结果相符的是
A. B. C. D.
13.通过下列实验操作和现象能得出相应结论的是
实验操作 现象 结论
A 向收集满 CO2的软塑料瓶中加入约1/3 体积滴有石蕊试液的水,旋紧瓶盖,振荡 塑料瓶变瘪, 溶液变红 CO2能与石蕊反应
B 用课本中的装置做测定空气中氧气含量的实验 进入瓶中的水量超过了瓶内空气体积的1/5 所用的燃烧物可能是硫粉
C 将白磷浸没在热水中,再向热水中的白磷通氧气 通氧气前白磷不燃烧,通氧气后白磷燃烧 氧气是可燃物燃烧的条件之一
D 把质量相同的镁条与锌粒同时放入相同浓度和体积的盐酸中 镁条与盐酸 产生气体更快 镁的金属活动性比锌强
A.A B.B C.C D.D
14.某镁合金 2.4g 与足量的稀硫酸充分反应后生成 0.19g 氢气,该合金中不可能含有
A.Zn B.Fe C.Al D.Cu
15.向AgNO3、Cu(NO3)2、Mg(NO3)2的混合溶液中加入一些锌粉,完全反应后过滤。下列情况可能发生的是( )
A.滤纸上有Cu,滤液中有AgNO3、Cu(NO3)2、Zn(NO3)2、Mg(NO3)2
B.滤纸上有Cu、Ag,滤液中有AgNO3、Zn(NO3)2、Mg(NO3)2
C.滤纸上有Cu、Ag、Zn,滤液中有Zn(NO3)2、Mg(NO3)2
D.滤纸上有Cu、Ag、Zn、Mg,滤液中有Zn(NO3)2
三、综合应用题
16.中国国家文物局 3 月 31 日在公布了 2021 年度中国十大考古新发现之一的四川三星堆遗址,此次新发掘的 6 座“祭祀坑”出土了金面具、鸟形金箔饰等重要文物。
(1)黄金制成金面具、鸟形金箔饰体现了金的 性。
(2)“真金不怕火炼”说明金 。
(3)欲确定金、银、铜三种金属的活动性顺序,涉及的化学方程式为 。
(4)假黄金“黄铜”是铜、锌合金。某同学取 10 克的黄铜放入盛有足量的稀硫酸的锥形瓶中,收集到 0.1 克气体,试计算黄铜中铜的质量?
17.用如图所示的装置做镁与稀盐酸反应的实验。
(1)实验时将注射器中的稀盐酸 (选填“快速”或“缓慢”)推入锥形瓶中,其原因是 。
(2)室温下2.4g镁与100g稀盐酸恰好完全反应,计算产生氢气的质量。
18.铜是与人类关系非常密切的有色金属,被广泛地应用于电气、交通、轻工、机械制造、冶金、能源、高科技、石油化工、建筑工业、国防工业等领域,在中国有色金属材料的消费中仅次于铝。人们以辉铜矿(住要成分为Cu2S)为原料可以冶炼铜。Cu2S在高温下与氧气反应的部分转化关系如下图:
(1)Cu2O中铜元素的质量分数为 (保留一位小数)。
(2)反应2的基本类型是 。
(3)Cu2S在高温下与氧气反应会产生大气污染物SO2,严重时会产生 型酸雨。
(4)从含有CuSO4和H2SO4的混合溶液中加入铁屑可以回收铜:现有100gCuSO4和H2SO4的混合溶液。加入足量铁屑充分反应后回收到32g铜,求混合溶液中CuSO4的质量分数(要求写出详细的计算过程)。
参考答案:
1.BC
2.AC
3.AD
4.CD
5.BC
6.D
7.C
8.C
9.A
10.B
11.D
12.D
13.C
14.C
15.C
16.(1)延展
(2)在高温条件下不与氧气反应
(3)
(4)解:设10g黄铜中锌的质量为 x
铜的质量为10g-3.25g=6.75g
答:10g黄铜中铜的质量为 6.75g。
17.(1) 快速 镁和稀盐酸反应生成氯化镁和氢气,生成了气体,装置内压强增大,缓慢推入,会导致盐酸无法全部推入
(2)解:设产生氢气的质量为x
x=0.2g
答:产生氢气的质量为0.2g
18.(1)88.9%
(2)置换反应
(3)硫酸
(4)解:设CuSO4的质量为。
混合溶液中硫酸铜的质量分数为,
答:混合溶液中硫酸铜的质量分数为8%。
一、多选题
1.为探究铝、锌、铜三种金属的活动性顺序,某学习小组做了如甲图所示实验。实验结束后,将试管①、试管②内的物质全部倒入同烧杯中,经过充分反应后烧杯中的红色固体物质比刚混合时明显增多(如乙图所示)。
下列说法正确的是
A.反应后烧杯中的固体一定含有锌
B.甲图试管②中反应后固体一定不含锌
C.反应后烧杯中的溶液不确定是否含有氯化铜
D.烧杯中最后所得固体的质量一定大于 2克
2.化学小组为探究铝、铜、银三种金属的活动性顺序,设计了下图所示实验方案(金属 丝使用时均已用砂纸打磨)。下列说法正确的是
A.由实验甲可知金属活动性:Al>Cu
B.由实验乙可知金属活动性:Ag>Cu
C.实验甲中的CuSO4改为CuCl2,也能完成本实验探究
D.若要探究铝、铜、银活动性顺序,甲、乙、丙实验必须全做
3.两种金属的混合物11克,加入足量的稀硫酸,经实验测得生成的氢气为1克,则这种混合物粉末可能是
A.铝和镁 B.镁和锌 C.锌和铁 D.铝和铜
4.往硝酸铜、硝酸银和硝酸亚铁的混合溶液中缓慢连续加入质量为m的锌粉,溶液中析出固体的质量与参加反应的锌粉质量关系如图所示,下列说法中正确的是
A.c点对应溶液中含有的金属离子为Zn2+和Cu2+
B.bc段(不含两端点)析出的金属是Fe
C.ab段(不含两端点)对应溶液中含有的金属离子为Zn2+、Ag+、Cu2+、Fe2+
D.若bc段和cd段中析出固体质量相等,参加反应的锌粉质量分别为m1和m2,m1< m2
5.在点燃条件下,A和B反应生成C和D。反应前后分子变化的微观示意图如下所示。下列说法中正确的是
A.该反应前后原子和分子种类均不变 B.该反应属于置换反应
C.A中氮元素的化合价为-3价 D.参加反应的A和B的质量比为17∶32
二、选择题
6.下列实验现象符合事实的是
A.硫在空气中燃烧,产生明亮的蓝紫色火焰
B.将铁片放入稀盐酸中,溶液逐渐由无色变为蓝色
C.镁条在空气中燃烧,发出耀眼的白光,生成黑色固体
D.在蜡烛火焰上方罩一只干冷的烧杯,烧杯内壁中出现水雾
7.在硝酸铜和硝酸银的混合溶液中,加入一定量的铁粉,充分反应后,过滤上述反应的混合物,在滤液中滴加盐酸有白色沉淀产生,则过滤得到的金属是
A.Fe、Cu B.Cu C.Ag D.Fe、Ag
8.下列实验现象的描述正确的是
A.木炭在氧气中燃烧发出白色火焰
B.铁丝在空气中燃烧火星四射
C.镁条在空气中燃烧发出耀眼白光
D.铁片在稀盐酸中逐渐溶解,有气泡产生,溶液由无色变成蓝色
9.某反应的微观示意图如下,下列说法正确的是
A.图中反应的基本类型是置换反应
B.反应前后元素的种类及化合价均不变
C.反应涉及到的物质中, 属于单质,只有 属于氧化物
D.参加反应的 和 的微粒个数比是4∶3
10.下列排序正确的是
A.地壳中元素含量:
B.空气中体积分数:
C.金属活动性顺序:
D.氯元素的化合价:
11.下列化学方程式及基本反应类型均正确的是
A.H2CO3H2O+CO2分解反应 B.Al+H2SO4=Al2(SO4)3+H2↑ 化合反应
C.2Mg+O22MgO 氧化反应 D.2Na+CuSO4=Na2SO4+Cu 置换反应
12.小明取等质量的铁片和铁粉分别放入两支试管中,分别加入相同体积、相同浓度的足量稀盐酸。下列示意图中,与实验结果相符的是
A. B. C. D.
13.通过下列实验操作和现象能得出相应结论的是
实验操作 现象 结论
A 向收集满 CO2的软塑料瓶中加入约1/3 体积滴有石蕊试液的水,旋紧瓶盖,振荡 塑料瓶变瘪, 溶液变红 CO2能与石蕊反应
B 用课本中的装置做测定空气中氧气含量的实验 进入瓶中的水量超过了瓶内空气体积的1/5 所用的燃烧物可能是硫粉
C 将白磷浸没在热水中,再向热水中的白磷通氧气 通氧气前白磷不燃烧,通氧气后白磷燃烧 氧气是可燃物燃烧的条件之一
D 把质量相同的镁条与锌粒同时放入相同浓度和体积的盐酸中 镁条与盐酸 产生气体更快 镁的金属活动性比锌强
A.A B.B C.C D.D
14.某镁合金 2.4g 与足量的稀硫酸充分反应后生成 0.19g 氢气,该合金中不可能含有
A.Zn B.Fe C.Al D.Cu
15.向AgNO3、Cu(NO3)2、Mg(NO3)2的混合溶液中加入一些锌粉,完全反应后过滤。下列情况可能发生的是( )
A.滤纸上有Cu,滤液中有AgNO3、Cu(NO3)2、Zn(NO3)2、Mg(NO3)2
B.滤纸上有Cu、Ag,滤液中有AgNO3、Zn(NO3)2、Mg(NO3)2
C.滤纸上有Cu、Ag、Zn,滤液中有Zn(NO3)2、Mg(NO3)2
D.滤纸上有Cu、Ag、Zn、Mg,滤液中有Zn(NO3)2
三、综合应用题
16.中国国家文物局 3 月 31 日在公布了 2021 年度中国十大考古新发现之一的四川三星堆遗址,此次新发掘的 6 座“祭祀坑”出土了金面具、鸟形金箔饰等重要文物。
(1)黄金制成金面具、鸟形金箔饰体现了金的 性。
(2)“真金不怕火炼”说明金 。
(3)欲确定金、银、铜三种金属的活动性顺序,涉及的化学方程式为 。
(4)假黄金“黄铜”是铜、锌合金。某同学取 10 克的黄铜放入盛有足量的稀硫酸的锥形瓶中,收集到 0.1 克气体,试计算黄铜中铜的质量?
17.用如图所示的装置做镁与稀盐酸反应的实验。
(1)实验时将注射器中的稀盐酸 (选填“快速”或“缓慢”)推入锥形瓶中,其原因是 。
(2)室温下2.4g镁与100g稀盐酸恰好完全反应,计算产生氢气的质量。
18.铜是与人类关系非常密切的有色金属,被广泛地应用于电气、交通、轻工、机械制造、冶金、能源、高科技、石油化工、建筑工业、国防工业等领域,在中国有色金属材料的消费中仅次于铝。人们以辉铜矿(住要成分为Cu2S)为原料可以冶炼铜。Cu2S在高温下与氧气反应的部分转化关系如下图:
(1)Cu2O中铜元素的质量分数为 (保留一位小数)。
(2)反应2的基本类型是 。
(3)Cu2S在高温下与氧气反应会产生大气污染物SO2,严重时会产生 型酸雨。
(4)从含有CuSO4和H2SO4的混合溶液中加入铁屑可以回收铜:现有100gCuSO4和H2SO4的混合溶液。加入足量铁屑充分反应后回收到32g铜,求混合溶液中CuSO4的质量分数(要求写出详细的计算过程)。
参考答案:
1.BC
2.AC
3.AD
4.CD
5.BC
6.D
7.C
8.C
9.A
10.B
11.D
12.D
13.C
14.C
15.C
16.(1)延展
(2)在高温条件下不与氧气反应
(3)
(4)解:设10g黄铜中锌的质量为 x
铜的质量为10g-3.25g=6.75g
答:10g黄铜中铜的质量为 6.75g。
17.(1) 快速 镁和稀盐酸反应生成氯化镁和氢气,生成了气体,装置内压强增大,缓慢推入,会导致盐酸无法全部推入
(2)解:设产生氢气的质量为x
x=0.2g
答:产生氢气的质量为0.2g
18.(1)88.9%
(2)置换反应
(3)硫酸
(4)解:设CuSO4的质量为。
混合溶液中硫酸铜的质量分数为,
答:混合溶液中硫酸铜的质量分数为8%。
同课章节目录
