第二章 专题强化3 气体的等温变化规律的应用 学案(学生版+教师版)—2024年春高中物理人教版选择性必修三
文档属性
| 名称 | 第二章 专题强化3 气体的等温变化规律的应用 学案(学生版+教师版)—2024年春高中物理人教版选择性必修三 | 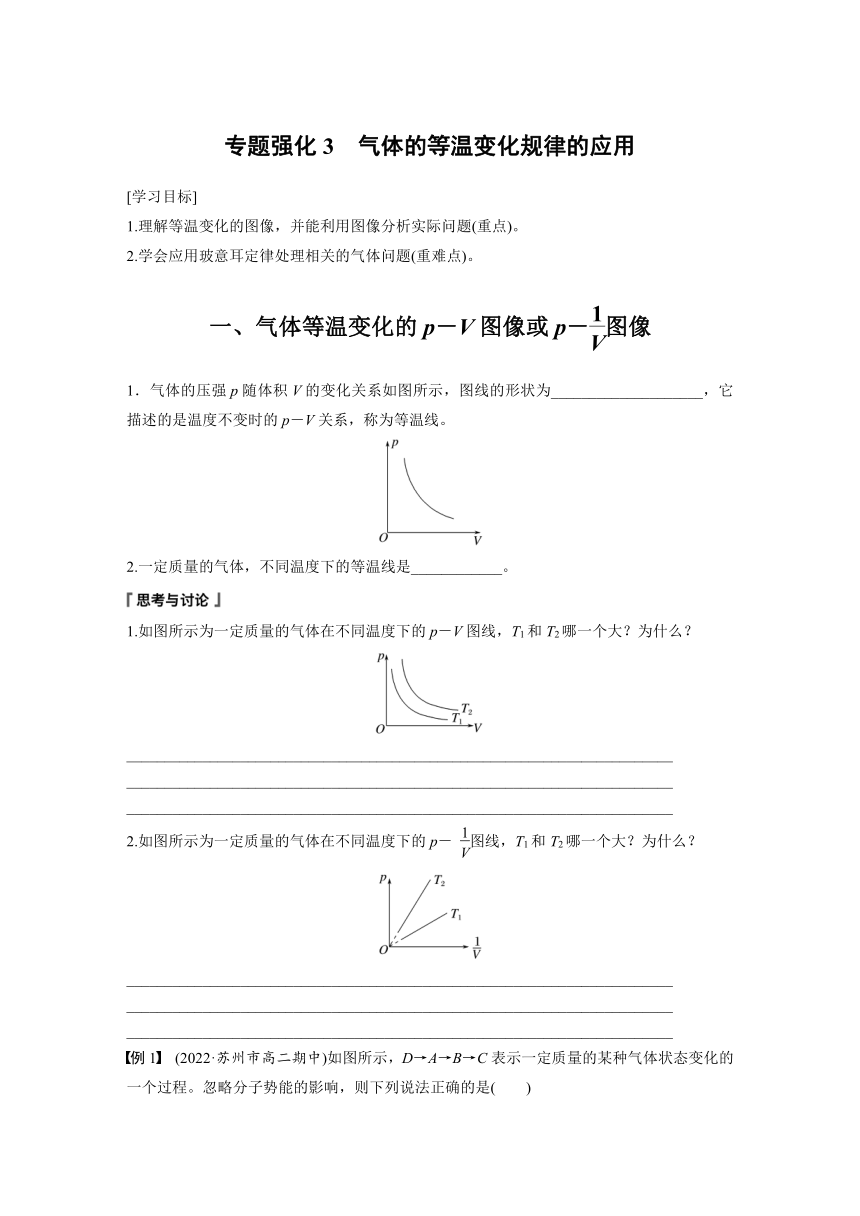 | |
| 格式 | docx | ||
| 文件大小 | 152.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 物理 | ||
| 更新时间 | 2024-03-11 13:57:29 | ||
图片预览



文档简介
专题强化3 气体的等温变化规律的应用
[学习目标]
1.理解等温变化的图像,并能利用图像分析实际问题(重点)。
2.学会应用玻意耳定律处理相关的气体问题(重难点)。
一、气体等温变化的p-V图像或p-图像
1.气体的压强p随体积V的变化关系如图所示,图线的形状为____________________,它描述的是温度不变时的p-V关系,称为等温线。
2.一定质量的气体,不同温度下的等温线是____________。
1.如图所示为一定质量的气体在不同温度下的p-V图线,T1和T2哪一个大?为什么?
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
2.如图所示为一定质量的气体在不同温度下的p- 图线,T1和T2哪一个大?为什么?
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
例1 (2022·苏州市高二期中)如图所示,D→A→B→C表示一定质量的某种气体状态变化的一个过程。忽略分子势能的影响,则下列说法正确的是( )
A.D→A温度升高
B.B→C气体内能不变
C.A→B气体分子平均速率变小
D.A→B体积变大,压强变大,内能不变
例2 如图所示是一定质量的某种气体状态变化的p-V图像,气体由状态A变化到状态B的过程中,关于气体的温度和分子平均速率的变化情况,下列说法正确的是( )
A.都一直保持不变
B.温度先升高后降低
C.温度先降低后升高
D.平均速率先减小后增大
二、玻意耳定律的应用
例3 如图所示,一端封闭、粗细均匀的U形玻璃管开口向上竖直放置,管内用水银将一段气体封闭在管中。当温度为T时,被封闭的气柱长L=22 cm,两边水银柱高度差h=16 cm,已知大气压强p0=76 cmHg。
(1)求此时被封闭的气柱的压强p;
(2)现向开口端缓慢注入水银,设气体温度保持不变,再次稳定后封闭气柱长度变为20 cm,求此时两边水银柱的高度差。
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
例4 (2022·盐城市高二月考)如图所示,在水平地面上放置一个深度h=48 cm、质量M=
30 kg的圆柱形金属容器,通过锁定在容器正中央、质量m=10 kg的薄圆柱形活塞密闭一些气体,此时气体压强与外界大气压相等,活塞与容器内横截面积均为S=50 cm2。解除锁定后,活塞下降直至静止。不考虑气体温度的变化,忽略一切摩擦,大气压强p0=1.0×105 Pa,重力加速度g取10 m/s2。
(1)求活塞静止时距容器底部的高度;
(2)活塞静止后,通过计算分析对活塞施加竖直向上的拉力F能否将金属容器缓缓提离地面。
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
应用玻意耳定律解题的一般步骤
(1)确定研究对象,并判断是否满足玻意耳定律的条件。
(2)确定初、末状态及状态参量(p1、V1;p2、V2)。
(3)根据玻意耳定律列方程求解(注意统一单位)。
(4)注意分析隐含条件,作出必要的判断和说明。
特别提醒 确定气体压强或体积时,只要初、末状态的单位统一即可,没有必要都转换成国际单位制的单位。
例5 用打气筒给自行车打气,设每打一次可打入压强为1 atm的空气0.1 L,自行车内胎的容积为2.0 L,假设胎内原来空气的压强为1 atm,且打气过程温度不变且内胎容积不变,那么打了40次后胎内空气压强为( )
A.5 atm B.4 atm
C.3 atm D.2 atm
温度不变时,向球或轮胎中充气时气体的质量发生变化。只要选择球或轮胎内原有气体和即将打入的气体整体作为研究对象,就可以把变质量气体问题转化为定质量气体的问题。
专题强化3 气体的等温变化规律的应用
[学习目标] 1.理解等温变化的图像,并能利用图像分析实际问题(重点)。2.学会应用玻意耳定律处理相关的气体问题(重难点)。
一、气体等温变化的p-V图像或p-图像
1.气体的压强p随体积V的变化关系如图所示,图线的形状为双曲线,它描述的是温度不变时的p-V关系,称为等温线。
2.一定质量的气体,不同温度下的等温线是不同的。
1.如图所示为一定质量的气体在不同温度下的p-V图线,T1和T2哪一个大?为什么?
答案 T2。一定质量的气体,温度越高,气体压强与体积的乘积必然越大,在p-V图像上的等温线离坐标原点越远。
2.如图所示为一定质量的气体在不同温度下的p-图线,T1和T2哪一个大?为什么?
答案 T2。直线的斜率表示p与V的乘积,斜率越大,p与V乘积越大,温度越高。
例1 (2022·苏州市高二期中)如图所示,D→A→B→C表示一定质量的某种气体状态变化的一个过程。忽略分子势能的影响,则下列说法正确的是( )
A.D→A温度升高
B.B→C气体内能不变
C.A→B气体分子平均速率变小
D.A→B体积变大,压强变大,内能不变
答案 B
解析 根据玻意耳定律可知,当气体经历等温变化时,其p-图像应为延长线过原点的倾斜直线,则由题图可知D→A和B→C均为等温过程,则B→C气体内能不变,A错误,B正确;p-图像斜率越大,所表示的等温线温度越高,所以TB>TA,则A→B气体分子平均速率变大,且气体的压强和内能均变大,气体体积不变,C、D错误。
例2 如图所示是一定质量的某种气体状态变化的p-V图像,气体由状态A变化到状态B的过程中,关于气体的温度和分子平均速率的变化情况,下列说法正确的是( )
A.都一直保持不变
B.温度先升高后降低
C.温度先降低后升高
D.平均速率先减小后增大
答案 B
解析 由题图可知pAVA=pBVB,所以A、B两状态的温度相等,在同一等温线上,可在p-V图上作出等温线,如图所示。由于离原点越远的等温线温度越高,所以从状态A到状态B温度应先升高后降低,分子平均速率先增大后减小,故选B。
二、玻意耳定律的应用
例3 如图所示,一端封闭、粗细均匀的U形玻璃管开口向上竖直放置,管内用水银将一段气体封闭在管中。当温度为T时,被封闭的气柱长L=22 cm,两边水银柱高度差h=16 cm,已知大气压强p0=76 cmHg。
(1)求此时被封闭的气柱的压强p;
(2)现向开口端缓慢注入水银,设气体温度保持不变,再次稳定后封闭气柱长度变为20 cm,求此时两边水银柱的高度差。
答案 (1)60 cmHg (2)10 cm
解析 (1)封闭气柱的压强
p1=p0-ph=76 cmHg-16 cmHg=60 cmHg
(2)因为气体发生等温变化,设玻璃管横截面积为S,此时两边水银柱的高度差为h′,
根据玻意耳定律有p1LS=p1′L′S,
代入数值得p1′=p1=×60 cmHg=66 cmHg
又p1′+ph′=p0,ph′=10 cmHg,
得h′=10 cm。
例4 (2022·盐城市高二月考)如图所示,在水平地面上放置一个深度h=48 cm、质量M=30 kg的圆柱形金属容器,通过锁定在容器正中央、质量m=10 kg的薄圆柱形活塞密闭一些气体,此时气体压强与外界大气压相等,活塞与容器内横截面积均为S=50 cm2。解除锁定后,活塞下降直至静止。不考虑气体温度的变化,忽略一切摩擦,大气压强p0=1.0×105 Pa,重力加速度g取10 m/s2。
(1)求活塞静止时距容器底部的高度;
(2)活塞静止后,通过计算分析对活塞施加竖直向上的拉力F能否将金属容器缓缓提离地面。
答案 (1)20 cm (2)金属容器不能被提离地面
解析 (1)活塞解除锁定前气体的压强为p1=1.0×105 Pa,容器内气体的体积为V1=L1S
其中L1=24 cm,活塞静止时,气体的压强为p2=p0+=1.0×105 Pa+ Pa=1.2×105 Pa
设此时活塞距容器底部的高度为L2,气体体积为V2=L2S,根据玻意耳定律p1V1=p2V2
代入数据得L2== cm=20 cm
(2)活塞静止后,假设活塞能被拉至容器开口端,根据玻意耳定律p1L1S=p3hS
代入数据得p3=5×104 Pa,对活塞受力分析,由平衡条件得F+p3S=p0S+mg
解得F=350 N<(m+M)g=(30+10)×10 N=400 N,所以金属容器不能被提离地面。
应用玻意耳定律解题的一般步骤
(1)确定研究对象,并判断是否满足玻意耳定律的条件。
(2)确定初、末状态及状态参量(p1、V1;p2、V2)。
(3)根据玻意耳定律列方程求解(注意统一单位)。
(4)注意分析隐含条件,作出必要的判断和说明。
特别提醒 确定气体压强或体积时,只要初、末状态的单位统一即可,没有必要都转换成国际单位制的单位。
例5 用打气筒给自行车打气,设每打一次可打入压强为1 atm的空气0.1 L,自行车内胎的容积为2.0 L,假设胎内原来空气的压强为1 atm,且打气过程温度不变且内胎容积不变,那么打了40次后胎内空气压强为( )
A.5 atm B.4 atm C.3 atm D.2 atm
答案 C
解析 每打一次可打入压强为1 atm的空气0.1 L,打了40次,气压为1 atm时总体积为0.1×40 L=4 L,加上胎内原有的气体,压缩前气体总体积V1=4 L+2 L=6 L,压入内胎,体积减小为2 L,根据玻意耳定律得p1V1=p2V2,代入数据解得p2=3 atm,故选C。
温度不变时,向球或轮胎中充气时气体的质量发生变化。只要选择球或轮胎内原有气体和即将打入的气体整体作为研究对象,就可以把变质量气体问题转化为定质量气体的问题。
[学习目标]
1.理解等温变化的图像,并能利用图像分析实际问题(重点)。
2.学会应用玻意耳定律处理相关的气体问题(重难点)。
一、气体等温变化的p-V图像或p-图像
1.气体的压强p随体积V的变化关系如图所示,图线的形状为____________________,它描述的是温度不变时的p-V关系,称为等温线。
2.一定质量的气体,不同温度下的等温线是____________。
1.如图所示为一定质量的气体在不同温度下的p-V图线,T1和T2哪一个大?为什么?
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
2.如图所示为一定质量的气体在不同温度下的p- 图线,T1和T2哪一个大?为什么?
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
例1 (2022·苏州市高二期中)如图所示,D→A→B→C表示一定质量的某种气体状态变化的一个过程。忽略分子势能的影响,则下列说法正确的是( )
A.D→A温度升高
B.B→C气体内能不变
C.A→B气体分子平均速率变小
D.A→B体积变大,压强变大,内能不变
例2 如图所示是一定质量的某种气体状态变化的p-V图像,气体由状态A变化到状态B的过程中,关于气体的温度和分子平均速率的变化情况,下列说法正确的是( )
A.都一直保持不变
B.温度先升高后降低
C.温度先降低后升高
D.平均速率先减小后增大
二、玻意耳定律的应用
例3 如图所示,一端封闭、粗细均匀的U形玻璃管开口向上竖直放置,管内用水银将一段气体封闭在管中。当温度为T时,被封闭的气柱长L=22 cm,两边水银柱高度差h=16 cm,已知大气压强p0=76 cmHg。
(1)求此时被封闭的气柱的压强p;
(2)现向开口端缓慢注入水银,设气体温度保持不变,再次稳定后封闭气柱长度变为20 cm,求此时两边水银柱的高度差。
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
例4 (2022·盐城市高二月考)如图所示,在水平地面上放置一个深度h=48 cm、质量M=
30 kg的圆柱形金属容器,通过锁定在容器正中央、质量m=10 kg的薄圆柱形活塞密闭一些气体,此时气体压强与外界大气压相等,活塞与容器内横截面积均为S=50 cm2。解除锁定后,活塞下降直至静止。不考虑气体温度的变化,忽略一切摩擦,大气压强p0=1.0×105 Pa,重力加速度g取10 m/s2。
(1)求活塞静止时距容器底部的高度;
(2)活塞静止后,通过计算分析对活塞施加竖直向上的拉力F能否将金属容器缓缓提离地面。
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
应用玻意耳定律解题的一般步骤
(1)确定研究对象,并判断是否满足玻意耳定律的条件。
(2)确定初、末状态及状态参量(p1、V1;p2、V2)。
(3)根据玻意耳定律列方程求解(注意统一单位)。
(4)注意分析隐含条件,作出必要的判断和说明。
特别提醒 确定气体压强或体积时,只要初、末状态的单位统一即可,没有必要都转换成国际单位制的单位。
例5 用打气筒给自行车打气,设每打一次可打入压强为1 atm的空气0.1 L,自行车内胎的容积为2.0 L,假设胎内原来空气的压强为1 atm,且打气过程温度不变且内胎容积不变,那么打了40次后胎内空气压强为( )
A.5 atm B.4 atm
C.3 atm D.2 atm
温度不变时,向球或轮胎中充气时气体的质量发生变化。只要选择球或轮胎内原有气体和即将打入的气体整体作为研究对象,就可以把变质量气体问题转化为定质量气体的问题。
专题强化3 气体的等温变化规律的应用
[学习目标] 1.理解等温变化的图像,并能利用图像分析实际问题(重点)。2.学会应用玻意耳定律处理相关的气体问题(重难点)。
一、气体等温变化的p-V图像或p-图像
1.气体的压强p随体积V的变化关系如图所示,图线的形状为双曲线,它描述的是温度不变时的p-V关系,称为等温线。
2.一定质量的气体,不同温度下的等温线是不同的。
1.如图所示为一定质量的气体在不同温度下的p-V图线,T1和T2哪一个大?为什么?
答案 T2。一定质量的气体,温度越高,气体压强与体积的乘积必然越大,在p-V图像上的等温线离坐标原点越远。
2.如图所示为一定质量的气体在不同温度下的p-图线,T1和T2哪一个大?为什么?
答案 T2。直线的斜率表示p与V的乘积,斜率越大,p与V乘积越大,温度越高。
例1 (2022·苏州市高二期中)如图所示,D→A→B→C表示一定质量的某种气体状态变化的一个过程。忽略分子势能的影响,则下列说法正确的是( )
A.D→A温度升高
B.B→C气体内能不变
C.A→B气体分子平均速率变小
D.A→B体积变大,压强变大,内能不变
答案 B
解析 根据玻意耳定律可知,当气体经历等温变化时,其p-图像应为延长线过原点的倾斜直线,则由题图可知D→A和B→C均为等温过程,则B→C气体内能不变,A错误,B正确;p-图像斜率越大,所表示的等温线温度越高,所以TB>TA,则A→B气体分子平均速率变大,且气体的压强和内能均变大,气体体积不变,C、D错误。
例2 如图所示是一定质量的某种气体状态变化的p-V图像,气体由状态A变化到状态B的过程中,关于气体的温度和分子平均速率的变化情况,下列说法正确的是( )
A.都一直保持不变
B.温度先升高后降低
C.温度先降低后升高
D.平均速率先减小后增大
答案 B
解析 由题图可知pAVA=pBVB,所以A、B两状态的温度相等,在同一等温线上,可在p-V图上作出等温线,如图所示。由于离原点越远的等温线温度越高,所以从状态A到状态B温度应先升高后降低,分子平均速率先增大后减小,故选B。
二、玻意耳定律的应用
例3 如图所示,一端封闭、粗细均匀的U形玻璃管开口向上竖直放置,管内用水银将一段气体封闭在管中。当温度为T时,被封闭的气柱长L=22 cm,两边水银柱高度差h=16 cm,已知大气压强p0=76 cmHg。
(1)求此时被封闭的气柱的压强p;
(2)现向开口端缓慢注入水银,设气体温度保持不变,再次稳定后封闭气柱长度变为20 cm,求此时两边水银柱的高度差。
答案 (1)60 cmHg (2)10 cm
解析 (1)封闭气柱的压强
p1=p0-ph=76 cmHg-16 cmHg=60 cmHg
(2)因为气体发生等温变化,设玻璃管横截面积为S,此时两边水银柱的高度差为h′,
根据玻意耳定律有p1LS=p1′L′S,
代入数值得p1′=p1=×60 cmHg=66 cmHg
又p1′+ph′=p0,ph′=10 cmHg,
得h′=10 cm。
例4 (2022·盐城市高二月考)如图所示,在水平地面上放置一个深度h=48 cm、质量M=30 kg的圆柱形金属容器,通过锁定在容器正中央、质量m=10 kg的薄圆柱形活塞密闭一些气体,此时气体压强与外界大气压相等,活塞与容器内横截面积均为S=50 cm2。解除锁定后,活塞下降直至静止。不考虑气体温度的变化,忽略一切摩擦,大气压强p0=1.0×105 Pa,重力加速度g取10 m/s2。
(1)求活塞静止时距容器底部的高度;
(2)活塞静止后,通过计算分析对活塞施加竖直向上的拉力F能否将金属容器缓缓提离地面。
答案 (1)20 cm (2)金属容器不能被提离地面
解析 (1)活塞解除锁定前气体的压强为p1=1.0×105 Pa,容器内气体的体积为V1=L1S
其中L1=24 cm,活塞静止时,气体的压强为p2=p0+=1.0×105 Pa+ Pa=1.2×105 Pa
设此时活塞距容器底部的高度为L2,气体体积为V2=L2S,根据玻意耳定律p1V1=p2V2
代入数据得L2== cm=20 cm
(2)活塞静止后,假设活塞能被拉至容器开口端,根据玻意耳定律p1L1S=p3hS
代入数据得p3=5×104 Pa,对活塞受力分析,由平衡条件得F+p3S=p0S+mg
解得F=350 N<(m+M)g=(30+10)×10 N=400 N,所以金属容器不能被提离地面。
应用玻意耳定律解题的一般步骤
(1)确定研究对象,并判断是否满足玻意耳定律的条件。
(2)确定初、末状态及状态参量(p1、V1;p2、V2)。
(3)根据玻意耳定律列方程求解(注意统一单位)。
(4)注意分析隐含条件,作出必要的判断和说明。
特别提醒 确定气体压强或体积时,只要初、末状态的单位统一即可,没有必要都转换成国际单位制的单位。
例5 用打气筒给自行车打气,设每打一次可打入压强为1 atm的空气0.1 L,自行车内胎的容积为2.0 L,假设胎内原来空气的压强为1 atm,且打气过程温度不变且内胎容积不变,那么打了40次后胎内空气压强为( )
A.5 atm B.4 atm C.3 atm D.2 atm
答案 C
解析 每打一次可打入压强为1 atm的空气0.1 L,打了40次,气压为1 atm时总体积为0.1×40 L=4 L,加上胎内原有的气体,压缩前气体总体积V1=4 L+2 L=6 L,压入内胎,体积减小为2 L,根据玻意耳定律得p1V1=p2V2,代入数据解得p2=3 atm,故选C。
温度不变时,向球或轮胎中充气时气体的质量发生变化。只要选择球或轮胎内原有气体和即将打入的气体整体作为研究对象,就可以把变质量气体问题转化为定质量气体的问题。
同课章节目录
- 第一章 分子动理论
- 1 分子动理论的基本内容
- 2 实验:用油膜法估测油酸分子的大小
- 3 分子运动速率分布规律
- 4 分子动能和分子势能
- 第二章 气体、固体和液体
- 1 温度和温标
- 2 气体的等温变化
- 3 气体的等压变化和等容变化
- 4 固体
- 5 液体
- 第三章 热力学定律
- 1 功、热和内能的改变
- 2 热力学第一定律
- 3 能量守恒定律
- 4 热力学第二定律
- 第四章 原子结构和波粒二象性
- 1 普朗克黑体辐射理论
- 2 光电效应
- 3 原子的核式结构模型
- 4 氢原子光谱和玻尔的原子模型
- 5 粒子的波动性和量子力学的建立
- 第五章 原子核
- 1 原子核的组成
- 2 放射性元素的衰变
- 3 核力与结合能
- 4 核裂变与核聚变
- 5 “基本”粒子
