化学科粤版九下同步课件:7.1 溶解与乳化第一课时(共14张PPT内嵌视频)
文档属性
| 名称 | 化学科粤版九下同步课件:7.1 溶解与乳化第一课时(共14张PPT内嵌视频) |

|
|
| 格式 | pptx | ||
| 文件大小 | 21.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-11 00:00:00 | ||
图片预览






文档简介
(共14张PPT)
溶解与乳化
第七章 溶液
新课导入
交流讨论
海水是纯净物还是混合物?为什么可以用海水晒盐?
海水是混合物,其中溶解有很多的氯化钠
观察活动
认识溶解现象
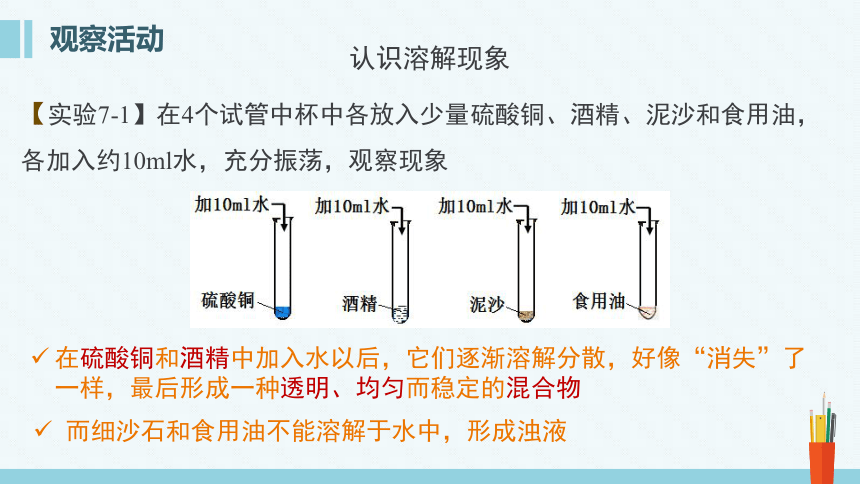
【实验7-1】在4个试管中杯中各放入少量硫酸铜、酒精、泥沙和食用油,各加入约10ml水,充分振荡,观察现象
在硫酸铜和酒精中加入水以后,它们逐渐溶解分散,好像“消失”了一样,最后形成一种透明、均匀而稳定的混合物
而细沙石和食用油不能溶解于水中,形成浊液
一、溶液的定义
定义:一种或几种物质分散到另一种物质中形成均一的、稳定的混合物
均一性:溶液形成以后,溶液任一部分的组成和性质完全相同(指密度、浓度、性质等)
稳定性:溶液在外界条件(包括温度、压强)不改变的情况下,溶质不会从溶剂中分离出来
硫酸铜溶液
蔗糖溶液
二、溶液 的组成
溶剂
溶质
被溶解的物质,如硫酸铜、食盐、酒精等
起溶解作用的物质,如水
可以是固体、气体或液体
①水能溶解很多物质,是一种最常见的溶剂
②溶液的质量=溶质质量+溶剂质量,其中,溶质质量指溶解了 的那部分溶质质量,不包括没有溶解的那部分质量
③溶液的体积≠溶质体积+溶剂体积质
交流讨论
溶液
中的溶质和溶剂怎
么判
断呢
体系 溶质 溶剂
气体+液体
固体+液体
液体+液体 无水
有水
1、通常不指明溶剂的溶液,一般指的是水溶液
2、对于任何一种溶液,溶质可以有多种,但溶剂只有一种
气 体
液 体
固 体
液 体
量 少
量 多
非水物
水
交流讨论
酒精可溶质可溶剂
溶液中可以有多种溶质
溶液 名称 食盐水 石灰水 酒精溶液 碘酒 稀盐酸 稀硫酸 食盐和蔗糖的
水溶液
溶质
溶剂
有些物质(如CO2)能与水反应,此时溶液中的溶质为新生成的物质
氯化钠
氢氧化钙
水
水
氯化氢
水
硫酸
水
酒精
水
碘
酒精
食盐、蔗糖
水
观察活动
知道影响溶质溶解快慢的因素
【实验7-2】比较等量硫酸铜在水中溶解的快慢
﹤
温度越高
溶解越快
观察活动
知道影响溶质溶解快慢的因素
﹥
粉末状溶质比块状溶质溶解快
﹥
搅拌溶剂,溶质溶解的快
三、影响溶解快慢的因素
温度越高
影响因素
颗粒大小
是否搅拌
定义
组成
判断溶质溶剂的方法
影响溶解快慢的因素
溶 液
特点
随堂练习
2.有一杯食盐溶液,实验测得其上部密度为a g/cm3,下部密度为b g/cm3,则a与b的关系是( )
A.a=b B.a<b C.a>b D.无法确定
1.下列关于溶液的说法正确的是( )
①无色 ②混合物 ③化合物 ④均一 ⑤稳定 ⑥各部分性质相同
A.①③④⑤ B.②④⑤⑥
C.①②④⑤ D.①③⑤⑥
B
A
3.下列有关溶液的说法正确的是( )
A.溶液一定是澄清、透明、无色的
B.溶液中的溶剂一定是水
C.外界条件不改变时,溶质、溶剂不分离
D.只有固体可以作溶质
4.把足量的锌放到一定量的稀硫酸中所形成的溶液中溶质是( )
A.硫酸 B.硫酸锌 C.锌 D.水
C
B
随堂练习
溶解与乳化
第七章 溶液
新课导入
交流讨论
海水是纯净物还是混合物?为什么可以用海水晒盐?
海水是混合物,其中溶解有很多的氯化钠
观察活动
认识溶解现象
【实验7-1】在4个试管中杯中各放入少量硫酸铜、酒精、泥沙和食用油,各加入约10ml水,充分振荡,观察现象
在硫酸铜和酒精中加入水以后,它们逐渐溶解分散,好像“消失”了一样,最后形成一种透明、均匀而稳定的混合物
而细沙石和食用油不能溶解于水中,形成浊液
一、溶液的定义
定义:一种或几种物质分散到另一种物质中形成均一的、稳定的混合物
均一性:溶液形成以后,溶液任一部分的组成和性质完全相同(指密度、浓度、性质等)
稳定性:溶液在外界条件(包括温度、压强)不改变的情况下,溶质不会从溶剂中分离出来
硫酸铜溶液
蔗糖溶液
二、溶液 的组成
溶剂
溶质
被溶解的物质,如硫酸铜、食盐、酒精等
起溶解作用的物质,如水
可以是固体、气体或液体
①水能溶解很多物质,是一种最常见的溶剂
②溶液的质量=溶质质量+溶剂质量,其中,溶质质量指溶解了 的那部分溶质质量,不包括没有溶解的那部分质量
③溶液的体积≠溶质体积+溶剂体积质
交流讨论
溶液
中的溶质和溶剂怎
么判
断呢
体系 溶质 溶剂
气体+液体
固体+液体
液体+液体 无水
有水
1、通常不指明溶剂的溶液,一般指的是水溶液
2、对于任何一种溶液,溶质可以有多种,但溶剂只有一种
气 体
液 体
固 体
液 体
量 少
量 多
非水物
水
交流讨论
酒精可溶质可溶剂
溶液中可以有多种溶质
溶液 名称 食盐水 石灰水 酒精溶液 碘酒 稀盐酸 稀硫酸 食盐和蔗糖的
水溶液
溶质
溶剂
有些物质(如CO2)能与水反应,此时溶液中的溶质为新生成的物质
氯化钠
氢氧化钙
水
水
氯化氢
水
硫酸
水
酒精
水
碘
酒精
食盐、蔗糖
水
观察活动
知道影响溶质溶解快慢的因素
【实验7-2】比较等量硫酸铜在水中溶解的快慢
﹤
温度越高
溶解越快
观察活动
知道影响溶质溶解快慢的因素
﹥
粉末状溶质比块状溶质溶解快
﹥
搅拌溶剂,溶质溶解的快
三、影响溶解快慢的因素
温度越高
影响因素
颗粒大小
是否搅拌
定义
组成
判断溶质溶剂的方法
影响溶解快慢的因素
溶 液
特点
随堂练习
2.有一杯食盐溶液,实验测得其上部密度为a g/cm3,下部密度为b g/cm3,则a与b的关系是( )
A.a=b B.a<b C.a>b D.无法确定
1.下列关于溶液的说法正确的是( )
①无色 ②混合物 ③化合物 ④均一 ⑤稳定 ⑥各部分性质相同
A.①③④⑤ B.②④⑤⑥
C.①②④⑤ D.①③⑤⑥
B
A
3.下列有关溶液的说法正确的是( )
A.溶液一定是澄清、透明、无色的
B.溶液中的溶剂一定是水
C.外界条件不改变时,溶质、溶剂不分离
D.只有固体可以作溶质
4.把足量的锌放到一定量的稀硫酸中所形成的溶液中溶质是( )
A.硫酸 B.硫酸锌 C.锌 D.水
C
B
随堂练习
