7.2碱及其性质同步练习鲁教版化学九年级下册(含答案)
文档属性
| 名称 | 7.2碱及其性质同步练习鲁教版化学九年级下册(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 690.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-13 00:00:00 | ||
图片预览



文档简介
7.2碱及其性质 同步练习
一、多选题
1.工业上用石灰石浆吸收废气中的二氧化硫,并制取石膏(主要成分为硫酸钙)的简易流程如图。下列说法正确的是( )
A.石灰石变成石灰石浆发生的是物理变化
B.粉碎和加水制成石灰石浆的目的是增大接触面积,提高SO2的吸收率
C.该流程还可以减少二氧化碳的排放,减缓温室效应
D.吸收塔中参加反应的物质是Ca(OH) 2 SO2 O2
2.分类法是化学学习的重要方法之。下列有关物质的分类正确的是
A.氧化物:氧化铁、五氧化二磷、水 B.混合物:煤、石油、天然气
C.酸:盐酸、硫酸、高锰酸钾 D.碱:火碱、纯碱、消石灰
3.下列选项中物质的俗名和化学名称表示同一物质的是
A.食盐---氯化钠
B.水银---银
C.石灰石---碳酸钙
D.纯碱---碳酸钠
4.如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了。则液体A和气体B组合可能是
液体A 气体B
A NaOH溶液 CO2
B NaOH溶液 O2
C 浓硫酸 H2
D 稀硫酸 NH3
A.A B.B C.C D.D
5.下列选项中物质的名称、俗名、化学式一致的是( )
A.氢氧化钙 熟石灰 Ca(OH)2 B.二氧化碳 冰 CO2
C.乙醇 酒精 C2H6O D.碳酸钠 小苏打 NaHCO3
二、选择题
6.下列实验方案或措施不合理的是
A.除去CaO中混有的CaCO3,高温煅烧
B.除去MnO2粉末中混有的KCl,加足量的水溶解、过滤、洗涤、干燥
C.用无色酚酞溶液检验氢氧化钠溶液是否变质
D.用稀H2SO4区别NaOH、K2CO3、BaCl2三种白色固体
7.下列物质的名称、俗名和化学式均正确的是
A.碳酸钠 纯碱 NaCO3 B.氢氧化钙 生石灰 Ca(OH)2
C.银 水银 Ag D.固态二氧化碳 干冰 CO2
8.物质的性质在很大程度上决定了其用途。下列物质的用途主要体现其物理性质的是
A.干冰用于人工降雨 B.稀有气体用作焊接保护气
C.氧气用于供给呼吸 D.生石灰用作干燥剂
9.下列有关物质性质与用途的说法不正确的是
A.活性炭可用于净水,利用其具有吸附性
B.水可以灭火,利用水可以降低可燃物的着火点
C.石墨可以做电极,利用石墨具有导电性
D.熟石灰可以中和酸性土壤,利用熟石灰呈碱性
10.下列物质久置于敞口容器中,其质量增加且变质的是
A.烧碱固体 B.浓硫酸 C.浓盐酸 D.氯化钠固体
11.推理是学习化学的一种重要方法,但不合理的推理会得出错误的结论。以下推理正确的是
A.含碳元素的物质充分燃烧会生成CO2,燃烧能生成CO2的物质一定含碳元素
B.离子是带电荷的微粒,带电荷的微粒一定是离子
C.碱溶液的pH都大于7,pH大于7的溶液一定是碱溶液
D.分子可以构成物质,物质一定是由分子构成的
12.根据特点对不同物质进行比较、分类是化学学习的重要方法之一。下列物质中,其名称、化学式和属类都正确的是( )
A.干冰﹣H2O﹣氧化物 B.水银﹣Ag﹣金属单质
C.碳酸氢一H2CO3﹣酸 D.苛性钠﹣NaOH﹣碱
13.实验室盛装氢氧化钠的试剂瓶应张贴的安全标志是
A. B. C. D.
14.晓晓同学需配制100 g溶质质量分数为12%的NaOH溶液来制作“叶脉书签”。在配制溶液的过程中,下列做法正确的是
A.在托盘右盘上垫纸称量12 g NaOH固体
B.用100 mL量筒量取88.0 mL水
C.称量时发现指针向右偏转,应调节游码使天平平衡
D.用药匙搅拌,加速NaOH溶解
15.下列物质敞口露置于空气中,质量不变的是
A.氢氧化钠 B.氯化钠
C.浓盐酸 D.浓硫酸
三、综合应用题
16.中国将力争“碳排放”于2030年前达到峰值,争取在2060年前实现“碳中和”。
(1)降低“碳排放”有利于实现“碳中和”。下列措施合理的有 (填字母)。
a. 禁止化石燃料的使用
b. 植树造林,增大植被面积
c. 采用节能技术
d. 利用太阳能、风能
(2)“碳中和”目的是使碳排放与碳吸收达平衡,最终实现零碳排放。结合如图1,提出一种可行的碳吸收方式: 。
(3)“碳捕获”并封存被认为是目前减缓全球变暖最经济可行的方式。小张同学利用化学知识,设计了一个简易CO2捕捉器,其捕捉CO2的流程如图2所示。
①此方法中采用“喷雾”的优点是 。
②流程中可循环利用的物质为丁,请写出丁与水反应的化学方程式: 。
③该流程虽然简单,但从节能减排的角度看,存在的不足是 ,这将是小张同学以后运用化学知识需改进的地方。
(4)“碳”的转化与利用
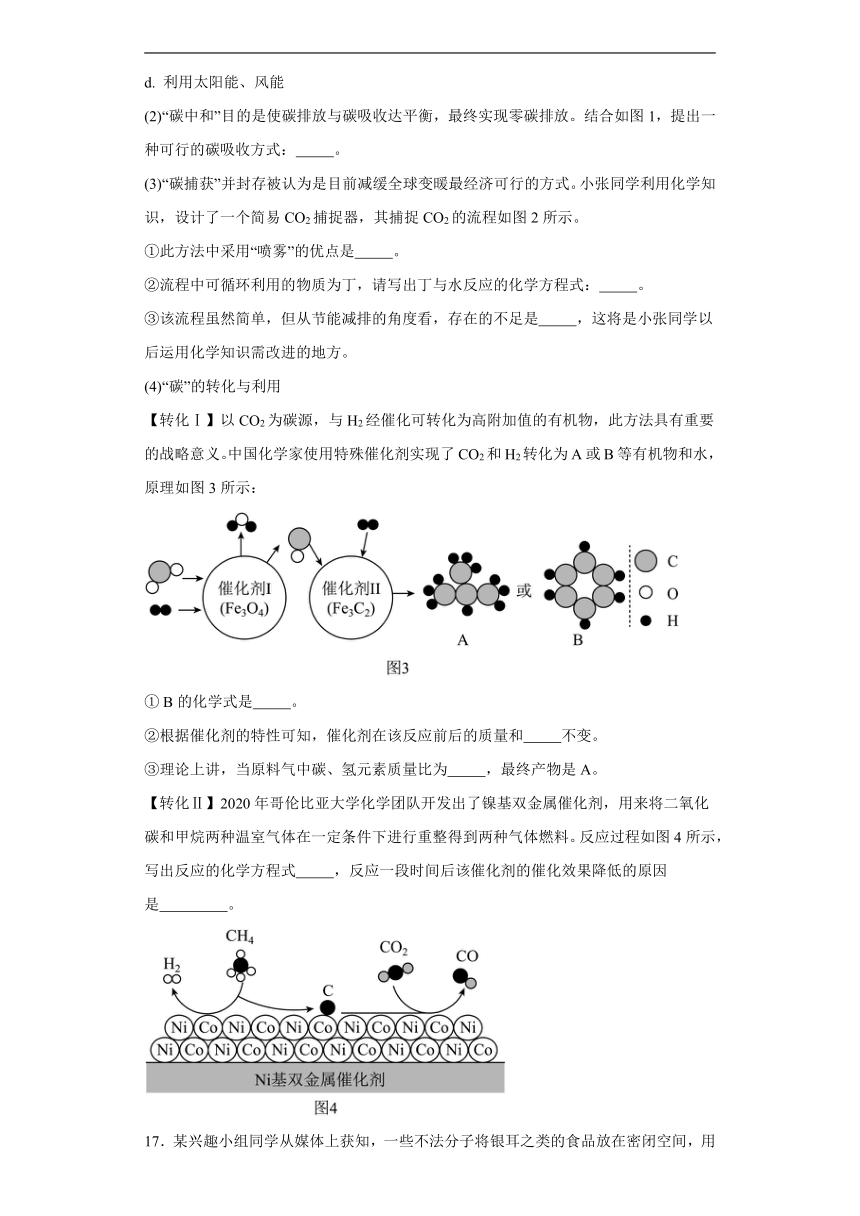
【转化Ⅰ】以CO2为碳源,与H2经催化可转化为高附加值的有机物,此方法具有重要的战略意义。中国化学家使用特殊催化剂实现了CO2和H2转化为A或B等有机物和水,原理如图3所示:
① B的化学式是 。
②根据催化剂的特性可知,催化剂在该反应前后的质量和 不变。
③理论上讲,当原料气中碳、氢元素质量比为 ,最终产物是A。
【转化Ⅱ】2020年哥伦比亚大学化学团队开发出了镍基双金属催化剂,用来将二氧化碳和甲烷两种温室气体在一定条件下进行重整得到两种气体燃料。反应过程如图4所示,写出反应的化学方程式 ,反应一段时间后该催化剂的催化效果降低的原因是 。
17.某兴趣小组同学从媒体上获知,一些不法分子将银耳之类的食品放在密闭空间,用燃烧硫磺产生的二氧化硫熏蒸进行漂白,使得这些食品中残留有一些二氧化硫,小组同学用亚硫酸钠(Na2SO3)与稀硫酸反应制取二氧化硫并对其性质进行如下探究:
(1)实验中需控制产生二氧化硫的速率,可采取的措施是 。
(2)B中溶液变红色,请用化学方程式表示其原因 。
(3)类比二氧化碳的性质,D产生浑浊现象的原因是 。
结合上述实验,某同学设计如下装置证明煤燃烧的产物中既有二氧化碳,也有二氧化硫(二氧化硫能与高锰酸钾溶液反应):
X溶液是 ,Y溶液是 。
(4)实验中观察C中溶液变成无色,D中出现浑浊,E中溶液褪色,F中无明显现象,同学们对F中溶液的溶质产生了兴趣,进而开启了他们的探究之旅。
【查阅资料】亚硫酸钠溶液显碱性;氯化钙和硝酸钙溶液显中性。
【提出问题】实验后F中溶液的溶质是什么?(忽略空气中二氧化碳的影响)
【作出猜想】猜想1:只有亚硫酸钠。
猜想2:只有 。
猜想3:既有氢氧化钠,也有亚硫酸钠。
【设计实验】(1)取F中溶液于试管中,加入氯化钙溶液,溶液 ,证明溶液中含有亚硫酸钠。
(2)往步骤(1)试管中继续加入氯化钙溶液(或硝酸钙溶液)至过量,再滴入无色酚酞溶液,溶液变红色,证明溶液中含有氢氧化钠。
【实验结论】猜想3正确。
【反思交流】若将X和Y中溶液互换, (填“能”或“不能”)得出煤的燃烧产物中既有二氧化碳,也有二氧化硫的结论,理由是 。
18.取久置敞口放置的氢氧化钠溶液于烧杯中,倒入一定量的稀硫酸充分反应。为探究反应后所得溶液X的成分,兴趣小组进行了如图实验(所加试剂均足量)。
(1)产生的无色气体是 。
(2)溶液X的溶质是 。(填写化学式)
(3)计算溶液X中硫酸钠的质量。
(4)设计实验将滤液A变成纯净的氯化钠晶体,请简述你的实验操作步骤 。
参考答案:
1.AB
2.AB
3.AD
4.AD
5.AC
6.C
7.D
8.A
9.B
10.A
11.A
12.D
13.A
14.B
15.B
16.(1)bcd
(2)植树造林
(3) 增大气体与液体的接触面积,使反应快速充分 CaO+H2O=Ca(OH)2 碳酸钙高温煅烧,耗能较多/碳酸钙高温煅烧又释放出了二氧化碳(合理即可)
(4) C6H6 化学性质 24:13 (仅写催化剂也可) 反应过程中有C覆盖在催化剂表面,阻碍了反应的进行
17.(1)调节分液漏斗活塞,控制稀硫酸滴入的速率
(2)H2O+SO2=H2SO3
(3) 二氧化硫与氢氧化钙反应生成难溶于水的物质(或二氧化硫与氢氧化钙反应生成难溶于水的亚硫酸钙) 品红溶液(或高锰酸钾溶液) 澄清石灰水
(4) 氢氧化钠 变浑浊(或有沉淀生成) 不能 二氧化硫和二氧化碳都能使澄清石灰水变浑浊
18.(1)CO2
(2)NaOH、Na2CO3、Na2SO4
(3)设溶液X中硫酸钠的质量为x。
答:溶液X中硫酸钠的质量为2.84g。
(4)加入足量的稀盐酸,再加热浓缩、蒸发结晶
一、多选题
1.工业上用石灰石浆吸收废气中的二氧化硫,并制取石膏(主要成分为硫酸钙)的简易流程如图。下列说法正确的是( )
A.石灰石变成石灰石浆发生的是物理变化
B.粉碎和加水制成石灰石浆的目的是增大接触面积,提高SO2的吸收率
C.该流程还可以减少二氧化碳的排放,减缓温室效应
D.吸收塔中参加反应的物质是Ca(OH) 2 SO2 O2
2.分类法是化学学习的重要方法之。下列有关物质的分类正确的是
A.氧化物:氧化铁、五氧化二磷、水 B.混合物:煤、石油、天然气
C.酸:盐酸、硫酸、高锰酸钾 D.碱:火碱、纯碱、消石灰
3.下列选项中物质的俗名和化学名称表示同一物质的是
A.食盐---氯化钠
B.水银---银
C.石灰石---碳酸钙
D.纯碱---碳酸钠
4.如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了。则液体A和气体B组合可能是
液体A 气体B
A NaOH溶液 CO2
B NaOH溶液 O2
C 浓硫酸 H2
D 稀硫酸 NH3
A.A B.B C.C D.D
5.下列选项中物质的名称、俗名、化学式一致的是( )
A.氢氧化钙 熟石灰 Ca(OH)2 B.二氧化碳 冰 CO2
C.乙醇 酒精 C2H6O D.碳酸钠 小苏打 NaHCO3
二、选择题
6.下列实验方案或措施不合理的是
A.除去CaO中混有的CaCO3,高温煅烧
B.除去MnO2粉末中混有的KCl,加足量的水溶解、过滤、洗涤、干燥
C.用无色酚酞溶液检验氢氧化钠溶液是否变质
D.用稀H2SO4区别NaOH、K2CO3、BaCl2三种白色固体
7.下列物质的名称、俗名和化学式均正确的是
A.碳酸钠 纯碱 NaCO3 B.氢氧化钙 生石灰 Ca(OH)2
C.银 水银 Ag D.固态二氧化碳 干冰 CO2
8.物质的性质在很大程度上决定了其用途。下列物质的用途主要体现其物理性质的是
A.干冰用于人工降雨 B.稀有气体用作焊接保护气
C.氧气用于供给呼吸 D.生石灰用作干燥剂
9.下列有关物质性质与用途的说法不正确的是
A.活性炭可用于净水,利用其具有吸附性
B.水可以灭火,利用水可以降低可燃物的着火点
C.石墨可以做电极,利用石墨具有导电性
D.熟石灰可以中和酸性土壤,利用熟石灰呈碱性
10.下列物质久置于敞口容器中,其质量增加且变质的是
A.烧碱固体 B.浓硫酸 C.浓盐酸 D.氯化钠固体
11.推理是学习化学的一种重要方法,但不合理的推理会得出错误的结论。以下推理正确的是
A.含碳元素的物质充分燃烧会生成CO2,燃烧能生成CO2的物质一定含碳元素
B.离子是带电荷的微粒,带电荷的微粒一定是离子
C.碱溶液的pH都大于7,pH大于7的溶液一定是碱溶液
D.分子可以构成物质,物质一定是由分子构成的
12.根据特点对不同物质进行比较、分类是化学学习的重要方法之一。下列物质中,其名称、化学式和属类都正确的是( )
A.干冰﹣H2O﹣氧化物 B.水银﹣Ag﹣金属单质
C.碳酸氢一H2CO3﹣酸 D.苛性钠﹣NaOH﹣碱
13.实验室盛装氢氧化钠的试剂瓶应张贴的安全标志是
A. B. C. D.
14.晓晓同学需配制100 g溶质质量分数为12%的NaOH溶液来制作“叶脉书签”。在配制溶液的过程中,下列做法正确的是
A.在托盘右盘上垫纸称量12 g NaOH固体
B.用100 mL量筒量取88.0 mL水
C.称量时发现指针向右偏转,应调节游码使天平平衡
D.用药匙搅拌,加速NaOH溶解
15.下列物质敞口露置于空气中,质量不变的是
A.氢氧化钠 B.氯化钠
C.浓盐酸 D.浓硫酸
三、综合应用题
16.中国将力争“碳排放”于2030年前达到峰值,争取在2060年前实现“碳中和”。
(1)降低“碳排放”有利于实现“碳中和”。下列措施合理的有 (填字母)。
a. 禁止化石燃料的使用
b. 植树造林,增大植被面积
c. 采用节能技术
d. 利用太阳能、风能
(2)“碳中和”目的是使碳排放与碳吸收达平衡,最终实现零碳排放。结合如图1,提出一种可行的碳吸收方式: 。
(3)“碳捕获”并封存被认为是目前减缓全球变暖最经济可行的方式。小张同学利用化学知识,设计了一个简易CO2捕捉器,其捕捉CO2的流程如图2所示。
①此方法中采用“喷雾”的优点是 。
②流程中可循环利用的物质为丁,请写出丁与水反应的化学方程式: 。
③该流程虽然简单,但从节能减排的角度看,存在的不足是 ,这将是小张同学以后运用化学知识需改进的地方。
(4)“碳”的转化与利用
【转化Ⅰ】以CO2为碳源,与H2经催化可转化为高附加值的有机物,此方法具有重要的战略意义。中国化学家使用特殊催化剂实现了CO2和H2转化为A或B等有机物和水,原理如图3所示:
① B的化学式是 。
②根据催化剂的特性可知,催化剂在该反应前后的质量和 不变。
③理论上讲,当原料气中碳、氢元素质量比为 ,最终产物是A。
【转化Ⅱ】2020年哥伦比亚大学化学团队开发出了镍基双金属催化剂,用来将二氧化碳和甲烷两种温室气体在一定条件下进行重整得到两种气体燃料。反应过程如图4所示,写出反应的化学方程式 ,反应一段时间后该催化剂的催化效果降低的原因是 。
17.某兴趣小组同学从媒体上获知,一些不法分子将银耳之类的食品放在密闭空间,用燃烧硫磺产生的二氧化硫熏蒸进行漂白,使得这些食品中残留有一些二氧化硫,小组同学用亚硫酸钠(Na2SO3)与稀硫酸反应制取二氧化硫并对其性质进行如下探究:
(1)实验中需控制产生二氧化硫的速率,可采取的措施是 。
(2)B中溶液变红色,请用化学方程式表示其原因 。
(3)类比二氧化碳的性质,D产生浑浊现象的原因是 。
结合上述实验,某同学设计如下装置证明煤燃烧的产物中既有二氧化碳,也有二氧化硫(二氧化硫能与高锰酸钾溶液反应):
X溶液是 ,Y溶液是 。
(4)实验中观察C中溶液变成无色,D中出现浑浊,E中溶液褪色,F中无明显现象,同学们对F中溶液的溶质产生了兴趣,进而开启了他们的探究之旅。
【查阅资料】亚硫酸钠溶液显碱性;氯化钙和硝酸钙溶液显中性。
【提出问题】实验后F中溶液的溶质是什么?(忽略空气中二氧化碳的影响)
【作出猜想】猜想1:只有亚硫酸钠。
猜想2:只有 。
猜想3:既有氢氧化钠,也有亚硫酸钠。
【设计实验】(1)取F中溶液于试管中,加入氯化钙溶液,溶液 ,证明溶液中含有亚硫酸钠。
(2)往步骤(1)试管中继续加入氯化钙溶液(或硝酸钙溶液)至过量,再滴入无色酚酞溶液,溶液变红色,证明溶液中含有氢氧化钠。
【实验结论】猜想3正确。
【反思交流】若将X和Y中溶液互换, (填“能”或“不能”)得出煤的燃烧产物中既有二氧化碳,也有二氧化硫的结论,理由是 。
18.取久置敞口放置的氢氧化钠溶液于烧杯中,倒入一定量的稀硫酸充分反应。为探究反应后所得溶液X的成分,兴趣小组进行了如图实验(所加试剂均足量)。
(1)产生的无色气体是 。
(2)溶液X的溶质是 。(填写化学式)
(3)计算溶液X中硫酸钠的质量。
(4)设计实验将滤液A变成纯净的氯化钠晶体,请简述你的实验操作步骤 。
参考答案:
1.AB
2.AB
3.AD
4.AD
5.AC
6.C
7.D
8.A
9.B
10.A
11.A
12.D
13.A
14.B
15.B
16.(1)bcd
(2)植树造林
(3) 增大气体与液体的接触面积,使反应快速充分 CaO+H2O=Ca(OH)2 碳酸钙高温煅烧,耗能较多/碳酸钙高温煅烧又释放出了二氧化碳(合理即可)
(4) C6H6 化学性质 24:13 (仅写催化剂也可) 反应过程中有C覆盖在催化剂表面,阻碍了反应的进行
17.(1)调节分液漏斗活塞,控制稀硫酸滴入的速率
(2)H2O+SO2=H2SO3
(3) 二氧化硫与氢氧化钙反应生成难溶于水的物质(或二氧化硫与氢氧化钙反应生成难溶于水的亚硫酸钙) 品红溶液(或高锰酸钾溶液) 澄清石灰水
(4) 氢氧化钠 变浑浊(或有沉淀生成) 不能 二氧化硫和二氧化碳都能使澄清石灰水变浑浊
18.(1)CO2
(2)NaOH、Na2CO3、Na2SO4
(3)设溶液X中硫酸钠的质量为x。
答:溶液X中硫酸钠的质量为2.84g。
(4)加入足量的稀盐酸,再加热浓缩、蒸发结晶
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
