9.2金属的化学性质同步练习鲁教版化学九年级下册(含答案)
文档属性
| 名称 | 9.2金属的化学性质同步练习鲁教版化学九年级下册(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 547.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-13 00:00:00 | ||
图片预览


文档简介
9.2金属的化学性质 同步练习
一、多选题
1.取一定质量经粉碎的铜锌合金,先加足量稀硫酸,完全反应(酸溶)后过滤,将滤渣洗净、烘干,再将滤渣在O2中充分灼烧。上述过程中,固体质量(g)与时间的关系如图所示。下列说法正确的是
A.合金中Zn的质量为3.2g B.a~b段反应得蓝色溶液
C.c~d段固体为CuO,d点对应的质量为4g D.在酸溶过程中共收集到气体为0.2g
2.下列实验现象的描述正确的是
A.电解水的实验:电极附近产生气体,一段时间后,正负极气体体积比约为1:2
B.铁钉放在硫酸铜溶液中:银白色固体表面有紫红色固体析出,溶液由蓝色变为浅绿色
C.将生锈的铁钉放入稀硫酸中:开始时溶液由无色变为浅绿色
D.生石灰中加入一定量的水:白色固体变成白色浆液,吸收大量的热
3.某溶液含有Cu(NO3)2和AgNO3,现向其中加入一定量的锌粉,参加反应的锌的质量与溶液中金属离子种类的关系如下图所示,下列说法正确的是
A.a﹣b间(不含两点)的溶液中金属离子为Zn2+、Ag+、Cu2+
B.c﹣d间(不含两点)的溶液中金属离子为Zn2+、Ag+
C.当参加反应的锌的质量为m3时,溶液中固体金属的种类有3种
D.当参加反应的锌的质量分别为m1、m2时,溶液中Cu(NO3)2的质量分数相等
4.将质量相等、溶质质量分数相同的两份稀硫酸分别装在甲、乙两个烧杯中,再称取质量相等的镁和铁,把镁放入甲烧杯中,铁放入乙烧杯中。待反应结束后,发现甲烧杯中镁有剩余,乙烧杯中的铁已全部反应,根据此现象推断,下列结论中,正确的是
A.可能乙烧杯中产生的氢气多
B.可能甲、乙烧杯中产生的气体一样多
C.甲、乙烧杯中消耗金属的质量比可能为3:7
D.甲、乙烧杯中消耗H2SO4质量比不可能为1:1
5.下列除去杂质(少量)的方法中,正确的是
选项 物质 杂质 除杂方法
A Zn Cu 滴加适量AgNO3溶液
B CO2气体 HCl气体 将气体依次通过饱和的NaHCO3溶液、浓硫酸
C Na2SO4溶液 CuSO4 滴加适量NaOH溶液,过滤
D KCl溶液 K2CO3 滴加过量Ba(NO3)2溶液,过滤
A.A B.B C.C D.D
二、选择题
6.白银,全国唯一以贵金属命名的城市。白银的金属矿藏有银、铜、锌等30多种,某同学为验证银、铜、锌三种金属的活动性顺序,以下方案能达到目的的是
A.将Zn片、Cu片分别放入AgNO3溶液中
B.将Zn片、Cu片、Ag片分别放入稀盐酸中
C.将Zn片、Ag片分别放入CuSO4溶液中
D.将Zn片分别放入CuSO4溶液和AgNO3溶液中
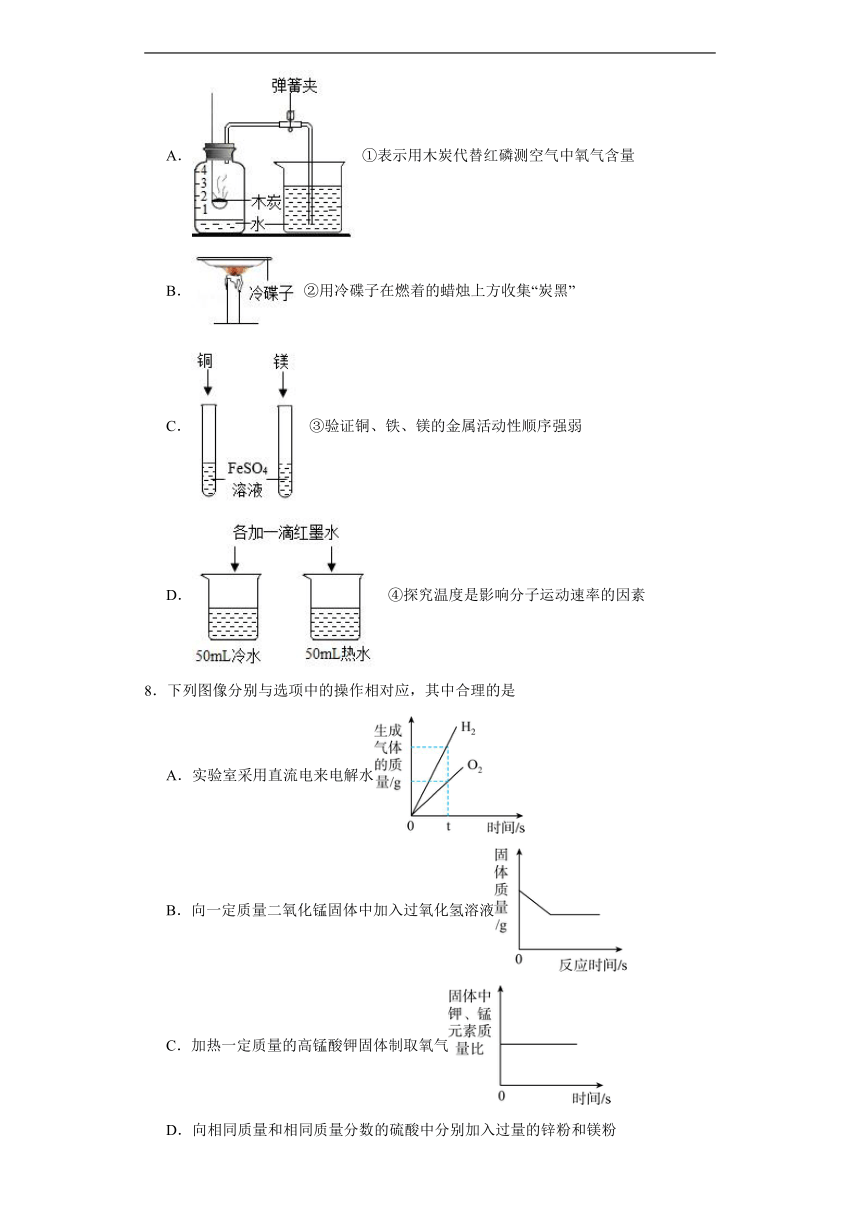
7.下列实验方案,不能达到实验目的的是
A. ①表示用木炭代替红磷测空气中氧气含量
B.②用冷碟子在燃着的蜡烛上方收集“炭黑”
C. ③验证铜、铁、镁的金属活动性顺序强弱
D. ④探究温度是影响分子运动速率的因素
8.下列图像分别与选项中的操作相对应,其中合理的是
A.实验室采用直流电来电解水
B.向一定质量二氧化锰固体中加入过氧化氢溶液
C.加热一定质量的高锰酸钾固体制取氧气
D.向相同质量和相同质量分数的硫酸中分别加入过量的锌粉和镁粉
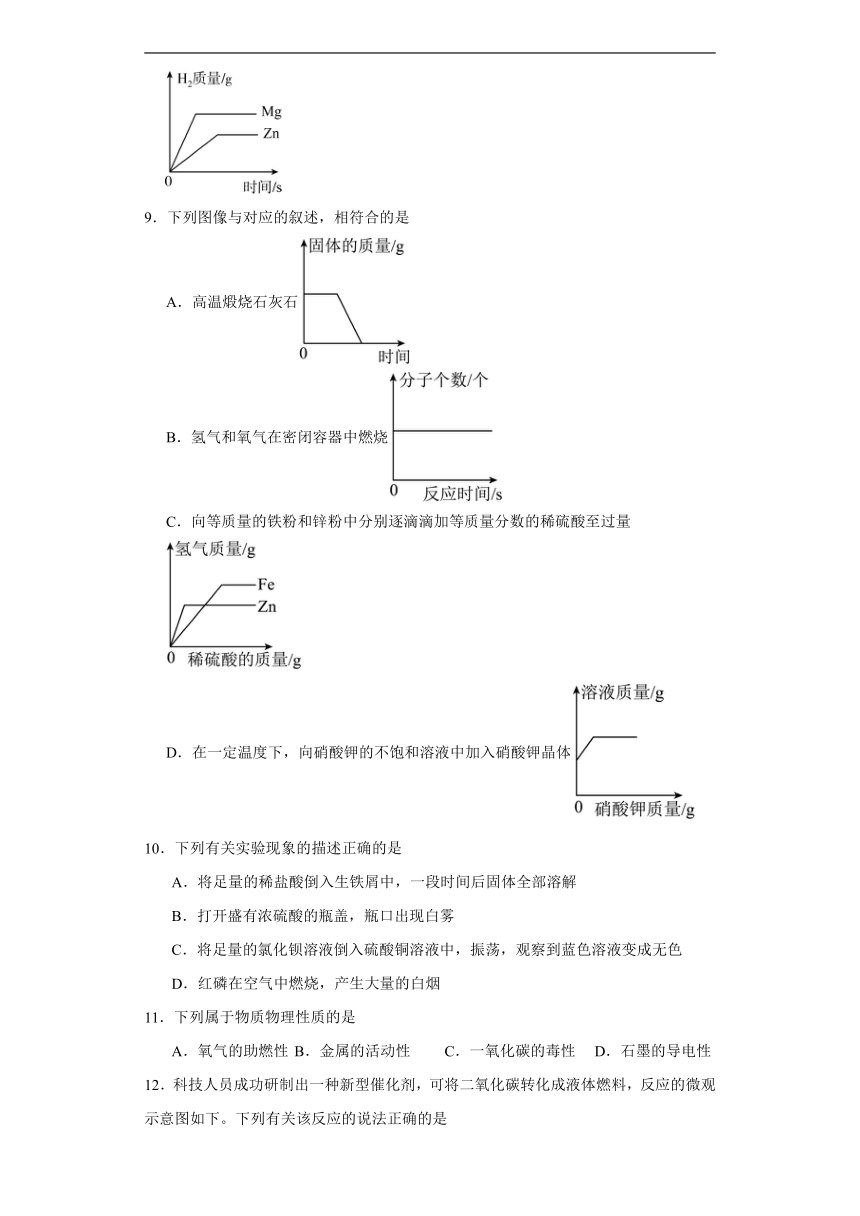
9.下列图像与对应的叙述,相符合的是
A.高温煅烧石灰石
B.氢气和氧气在密闭容器中燃烧
C.向等质量的铁粉和锌粉中分别逐滴滴加等质量分数的稀硫酸至过量
D.在一定温度下,向硝酸钾的不饱和溶液中加入硝酸钾晶体
10.下列有关实验现象的描述正确的是
A.将足量的稀盐酸倒入生铁屑中,一段时间后固体全部溶解
B.打开盛有浓硫酸的瓶盖,瓶口出现白雾
C.将足量的氯化钡溶液倒入硫酸铜溶液中,振荡,观察到蓝色溶液变成无色
D.红磷在空气中燃烧,产生大量的白烟
11.下列属于物质物理性质的是
A.氧气的助燃性 B.金属的活动性 C.一氧化碳的毒性 D.石墨的导电性
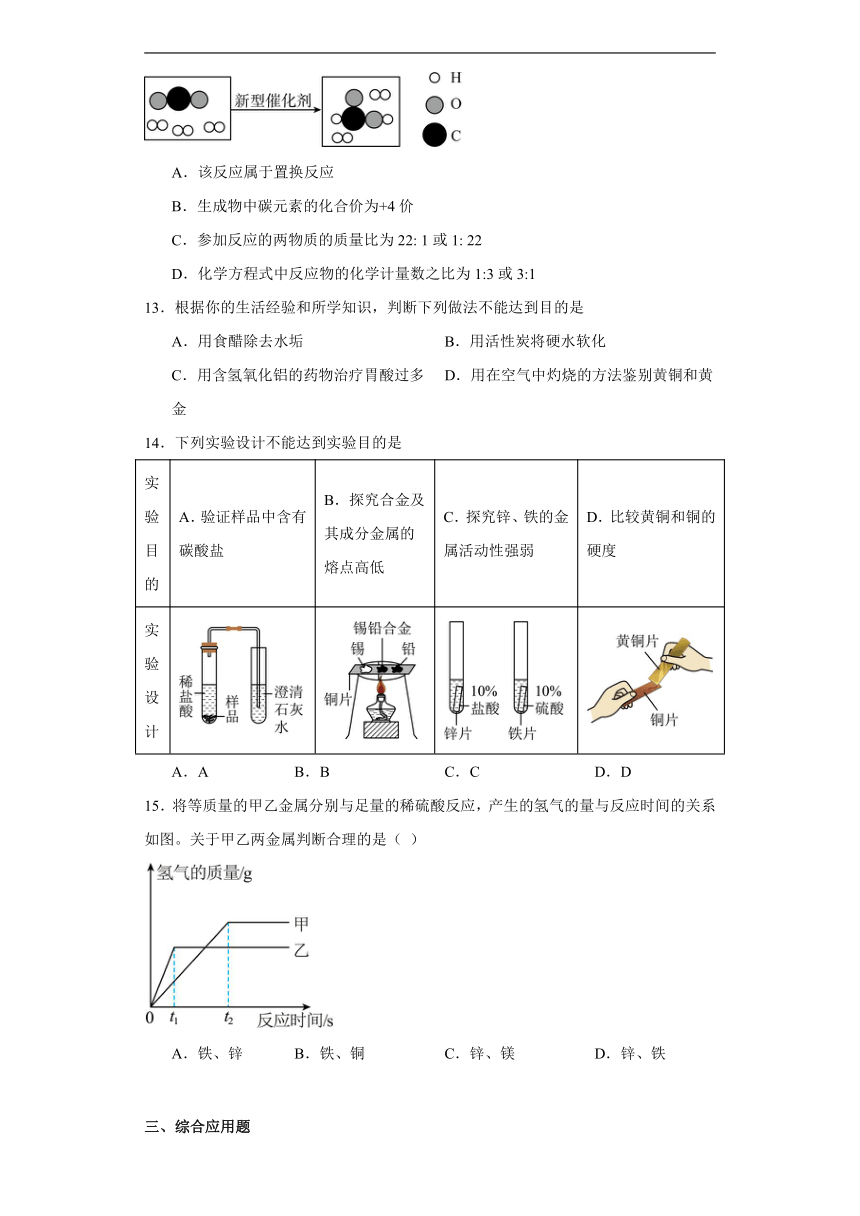
12.科技人员成功研制出一种新型催化剂,可将二氧化碳转化成液体燃料,反应的微观示意图如下。下列有关该反应的说法正确的是
A.该反应属于置换反应
B.生成物中碳元素的化合价为+4价
C.参加反应的两物质的质量比为22: 1或1: 22
D.化学方程式中反应物的化学计量数之比为1:3或3:1
13.根据你的生活经验和所学知识,判断下列做法不能达到目的是
A.用食醋除去水垢 B.用活性炭将硬水软化
C.用含氢氧化铝的药物治疗胃酸过多 D.用在空气中灼烧的方法鉴别黄铜和黄金
14.下列实验设计不能达到实验目的是
实验目的 A.验证样品中含有碳酸盐 B.探究合金及其成分金属的熔点高低 C.探究锌、铁的金属活动性强弱 D.比较黄铜和铜的硬度
实验设计
A.A B.B C.C D.D
15.将等质量的甲乙金属分别与足量的稀硫酸反应,产生的氢气的量与反应时间的关系如图。关于甲乙两金属判断合理的是( )
A.铁、锌 B.铁、铜 C.锌、镁 D.锌、铁
三、综合应用题
16.中国古代炼铜有“湿法炼铜”和“火法炼铜”。
(1)“火法炼铜”是将含氧化铜的铜矿与木炭一起灼烧,写出有金属铜生成过程的化学方程式 ,氧化铜被 (选填“氧化”或“还原”)。
(2)《宋史·食货志》的记载:“以生铁锻成薄片,排置胆水槽中,浸渍数日,铁片乃为胆水所薄,上生赤煤,取括赤煤入炉,三炼成铜。”记载中胆水为硫酸铜溶液,写出“铁片乃为胆水所薄”的反应属于 (填基本反应类型)。
(3)根据化学方程式计算,使用“湿法炼铜”制取12.8g铜,需要含铁量为80%铁合金的质量(其他成分不与硫酸铜反应)。
17.回答下列问题
(1)某化学兴趣小组的同学利用废铜制取硫酸铜,设计了如下甲、乙两个方案:
甲:CuCuO
乙:Cu
[已知:]
①从绿色化学的观点出发,上述两个方案中,你认为比较合理的是 ,简述理由 。
②若取相同质量的单质铜,分别用上述两方案制备硫酸铜,将两者理论上最多制备硫酸铜的质量进行比较,结果为 (填A、B、C序号之一)。
A甲方案较多 B.乙方案较多 C.二者相等
(2)某化学兴趣小组的同学取50g某硫酸铜溶液于一只洁净干燥的烧杯中,然后逐滴加入10%的NaOH溶液,产生沉淀的质量与所滴入NaOH溶液质量的关系曲线如图所示。试回答:
①当滴入NaOH溶液20g时(至图中A点),烧杯中溶液里一定大量存在的溶质是 (写化学式)。
②当滴入10%的NaOH溶液40g时(即B点),试通过计算,求此时所得不饱和溶液的质量(计算结果精确至0.1g)。
18.化学是一门研究物质的科学,我们一般从物质的存在、性质、制备、用途等方面研究一种物质或一类物质。以金属为例,请你参与其中回答相关问题:
(1)认识金属元素存在:自然界中大多数金属都以化合物的形式存在。下列矿石的主要成分属于氧化物的是___________(填字母序号);
A.铝土矿(主要成分Al2O3) B.辉铜矿(主要成分Cu2S)
C.菱铁矿(主要成分FeCO3) D.磁铁矿(主要成分Fe3O4)
(2)探究金属物理性质:下表是A、B、C三种金属的部分物理性质。
金属 导电性(100为标准) 密度(g/cm3) 熔点(℃) 硬度(10为标准)
A 99 8.92 1083 3
B 61 2.70 660 2.9
C 17 7.86 1535 5
①高压输电线不用金属A而选用金属B,主要原因是 。
②C的合金通常可以做菜刀、锤子等,其合金的硬度 5(填“>”“<”或“=”)。
(3)探究金属化学性质及反应规律:在室温条件下进行如图所示实验。若实验中各种条件均相同,观察到甲中的长颈漏斗内红墨水柱比乙高,试解释产生这种现象的原因。
(4)认识金属的制备: 我国西汉时期就有“曾青得铁则化为铜”的记载,其中蕴涵的湿法冶铜原理为: (用化学方程式表示)。
(5)金属在生产生活中应用广泛。如图,向一定量硝酸银溶液中加入铜和锌的混合粉末,充分反应后过滤,得溶液甲和固体乙。
①若乙中含有锌、铜、银三种固体,此时向固体乙中加入稀盐酸,发生反应的化学方程式为 。
②若溶液甲显蓝色,是因为 (用化学反应方程式表示),此时固体乙中一定含有的物质是 。
(6)某炼铁厂用赤铁矿石冶炼生铁。用2000t含氧化铁80%的赤铁矿矿石理论上可以炼出含铁96%生铁多少吨?
参考答案:
1.D
2.AB
3.AC
4.BC
5.BC
6.C
7.A
8.C
9.D
10.D
11.D
12.D
13.B
14.C
15.A
16.(1) C+2CuO2Cu+CO2↑ 还原
(2)置换反应
(3)14g
解:设需要含铁量为80%铁合金的质量为x,
需要含铁量为80%铁合金的质量为14g。
17.(1) 甲 不产生,更环保 C
(2) 、
解:设生成氢氧化铜的质量为x
x=4.9g
此时所得不饱和溶液的质量:50g+40g-4.9g=85.1g
答:此时所得不饱和溶液的质量为85.1g。
18.(1)AD
(2) 金属B的电性较好、密度小 >
(3)反应时镁比铁放出的热量多
(4)Fe+CuSO4=FeSO4+Cu
(5) Zn+2HCl=ZnCl2+H2↑ Cu+2AgNO3=2Ag+Cu(NO3)2 银
(6)设理论上可以炼出含铁96%的生铁的质量为x。
解得:x≈1166.7t
答:理论上可以炼出含铁96%生铁1166.7t。
一、多选题
1.取一定质量经粉碎的铜锌合金,先加足量稀硫酸,完全反应(酸溶)后过滤,将滤渣洗净、烘干,再将滤渣在O2中充分灼烧。上述过程中,固体质量(g)与时间的关系如图所示。下列说法正确的是
A.合金中Zn的质量为3.2g B.a~b段反应得蓝色溶液
C.c~d段固体为CuO,d点对应的质量为4g D.在酸溶过程中共收集到气体为0.2g
2.下列实验现象的描述正确的是
A.电解水的实验:电极附近产生气体,一段时间后,正负极气体体积比约为1:2
B.铁钉放在硫酸铜溶液中:银白色固体表面有紫红色固体析出,溶液由蓝色变为浅绿色
C.将生锈的铁钉放入稀硫酸中:开始时溶液由无色变为浅绿色
D.生石灰中加入一定量的水:白色固体变成白色浆液,吸收大量的热
3.某溶液含有Cu(NO3)2和AgNO3,现向其中加入一定量的锌粉,参加反应的锌的质量与溶液中金属离子种类的关系如下图所示,下列说法正确的是
A.a﹣b间(不含两点)的溶液中金属离子为Zn2+、Ag+、Cu2+
B.c﹣d间(不含两点)的溶液中金属离子为Zn2+、Ag+
C.当参加反应的锌的质量为m3时,溶液中固体金属的种类有3种
D.当参加反应的锌的质量分别为m1、m2时,溶液中Cu(NO3)2的质量分数相等
4.将质量相等、溶质质量分数相同的两份稀硫酸分别装在甲、乙两个烧杯中,再称取质量相等的镁和铁,把镁放入甲烧杯中,铁放入乙烧杯中。待反应结束后,发现甲烧杯中镁有剩余,乙烧杯中的铁已全部反应,根据此现象推断,下列结论中,正确的是
A.可能乙烧杯中产生的氢气多
B.可能甲、乙烧杯中产生的气体一样多
C.甲、乙烧杯中消耗金属的质量比可能为3:7
D.甲、乙烧杯中消耗H2SO4质量比不可能为1:1
5.下列除去杂质(少量)的方法中,正确的是
选项 物质 杂质 除杂方法
A Zn Cu 滴加适量AgNO3溶液
B CO2气体 HCl气体 将气体依次通过饱和的NaHCO3溶液、浓硫酸
C Na2SO4溶液 CuSO4 滴加适量NaOH溶液,过滤
D KCl溶液 K2CO3 滴加过量Ba(NO3)2溶液,过滤
A.A B.B C.C D.D
二、选择题
6.白银,全国唯一以贵金属命名的城市。白银的金属矿藏有银、铜、锌等30多种,某同学为验证银、铜、锌三种金属的活动性顺序,以下方案能达到目的的是
A.将Zn片、Cu片分别放入AgNO3溶液中
B.将Zn片、Cu片、Ag片分别放入稀盐酸中
C.将Zn片、Ag片分别放入CuSO4溶液中
D.将Zn片分别放入CuSO4溶液和AgNO3溶液中
7.下列实验方案,不能达到实验目的的是
A. ①表示用木炭代替红磷测空气中氧气含量
B.②用冷碟子在燃着的蜡烛上方收集“炭黑”
C. ③验证铜、铁、镁的金属活动性顺序强弱
D. ④探究温度是影响分子运动速率的因素
8.下列图像分别与选项中的操作相对应,其中合理的是
A.实验室采用直流电来电解水
B.向一定质量二氧化锰固体中加入过氧化氢溶液
C.加热一定质量的高锰酸钾固体制取氧气
D.向相同质量和相同质量分数的硫酸中分别加入过量的锌粉和镁粉
9.下列图像与对应的叙述,相符合的是
A.高温煅烧石灰石
B.氢气和氧气在密闭容器中燃烧
C.向等质量的铁粉和锌粉中分别逐滴滴加等质量分数的稀硫酸至过量
D.在一定温度下,向硝酸钾的不饱和溶液中加入硝酸钾晶体
10.下列有关实验现象的描述正确的是
A.将足量的稀盐酸倒入生铁屑中,一段时间后固体全部溶解
B.打开盛有浓硫酸的瓶盖,瓶口出现白雾
C.将足量的氯化钡溶液倒入硫酸铜溶液中,振荡,观察到蓝色溶液变成无色
D.红磷在空气中燃烧,产生大量的白烟
11.下列属于物质物理性质的是
A.氧气的助燃性 B.金属的活动性 C.一氧化碳的毒性 D.石墨的导电性
12.科技人员成功研制出一种新型催化剂,可将二氧化碳转化成液体燃料,反应的微观示意图如下。下列有关该反应的说法正确的是
A.该反应属于置换反应
B.生成物中碳元素的化合价为+4价
C.参加反应的两物质的质量比为22: 1或1: 22
D.化学方程式中反应物的化学计量数之比为1:3或3:1
13.根据你的生活经验和所学知识,判断下列做法不能达到目的是
A.用食醋除去水垢 B.用活性炭将硬水软化
C.用含氢氧化铝的药物治疗胃酸过多 D.用在空气中灼烧的方法鉴别黄铜和黄金
14.下列实验设计不能达到实验目的是
实验目的 A.验证样品中含有碳酸盐 B.探究合金及其成分金属的熔点高低 C.探究锌、铁的金属活动性强弱 D.比较黄铜和铜的硬度
实验设计
A.A B.B C.C D.D
15.将等质量的甲乙金属分别与足量的稀硫酸反应,产生的氢气的量与反应时间的关系如图。关于甲乙两金属判断合理的是( )
A.铁、锌 B.铁、铜 C.锌、镁 D.锌、铁
三、综合应用题
16.中国古代炼铜有“湿法炼铜”和“火法炼铜”。
(1)“火法炼铜”是将含氧化铜的铜矿与木炭一起灼烧,写出有金属铜生成过程的化学方程式 ,氧化铜被 (选填“氧化”或“还原”)。
(2)《宋史·食货志》的记载:“以生铁锻成薄片,排置胆水槽中,浸渍数日,铁片乃为胆水所薄,上生赤煤,取括赤煤入炉,三炼成铜。”记载中胆水为硫酸铜溶液,写出“铁片乃为胆水所薄”的反应属于 (填基本反应类型)。
(3)根据化学方程式计算,使用“湿法炼铜”制取12.8g铜,需要含铁量为80%铁合金的质量(其他成分不与硫酸铜反应)。
17.回答下列问题
(1)某化学兴趣小组的同学利用废铜制取硫酸铜,设计了如下甲、乙两个方案:
甲:CuCuO
乙:Cu
[已知:]
①从绿色化学的观点出发,上述两个方案中,你认为比较合理的是 ,简述理由 。
②若取相同质量的单质铜,分别用上述两方案制备硫酸铜,将两者理论上最多制备硫酸铜的质量进行比较,结果为 (填A、B、C序号之一)。
A甲方案较多 B.乙方案较多 C.二者相等
(2)某化学兴趣小组的同学取50g某硫酸铜溶液于一只洁净干燥的烧杯中,然后逐滴加入10%的NaOH溶液,产生沉淀的质量与所滴入NaOH溶液质量的关系曲线如图所示。试回答:
①当滴入NaOH溶液20g时(至图中A点),烧杯中溶液里一定大量存在的溶质是 (写化学式)。
②当滴入10%的NaOH溶液40g时(即B点),试通过计算,求此时所得不饱和溶液的质量(计算结果精确至0.1g)。
18.化学是一门研究物质的科学,我们一般从物质的存在、性质、制备、用途等方面研究一种物质或一类物质。以金属为例,请你参与其中回答相关问题:
(1)认识金属元素存在:自然界中大多数金属都以化合物的形式存在。下列矿石的主要成分属于氧化物的是___________(填字母序号);
A.铝土矿(主要成分Al2O3) B.辉铜矿(主要成分Cu2S)
C.菱铁矿(主要成分FeCO3) D.磁铁矿(主要成分Fe3O4)
(2)探究金属物理性质:下表是A、B、C三种金属的部分物理性质。
金属 导电性(100为标准) 密度(g/cm3) 熔点(℃) 硬度(10为标准)
A 99 8.92 1083 3
B 61 2.70 660 2.9
C 17 7.86 1535 5
①高压输电线不用金属A而选用金属B,主要原因是 。
②C的合金通常可以做菜刀、锤子等,其合金的硬度 5(填“>”“<”或“=”)。
(3)探究金属化学性质及反应规律:在室温条件下进行如图所示实验。若实验中各种条件均相同,观察到甲中的长颈漏斗内红墨水柱比乙高,试解释产生这种现象的原因。
(4)认识金属的制备: 我国西汉时期就有“曾青得铁则化为铜”的记载,其中蕴涵的湿法冶铜原理为: (用化学方程式表示)。
(5)金属在生产生活中应用广泛。如图,向一定量硝酸银溶液中加入铜和锌的混合粉末,充分反应后过滤,得溶液甲和固体乙。
①若乙中含有锌、铜、银三种固体,此时向固体乙中加入稀盐酸,发生反应的化学方程式为 。
②若溶液甲显蓝色,是因为 (用化学反应方程式表示),此时固体乙中一定含有的物质是 。
(6)某炼铁厂用赤铁矿石冶炼生铁。用2000t含氧化铁80%的赤铁矿矿石理论上可以炼出含铁96%生铁多少吨?
参考答案:
1.D
2.AB
3.AC
4.BC
5.BC
6.C
7.A
8.C
9.D
10.D
11.D
12.D
13.B
14.C
15.A
16.(1) C+2CuO2Cu+CO2↑ 还原
(2)置换反应
(3)14g
解:设需要含铁量为80%铁合金的质量为x,
需要含铁量为80%铁合金的质量为14g。
17.(1) 甲 不产生,更环保 C
(2) 、
解:设生成氢氧化铜的质量为x
x=4.9g
此时所得不饱和溶液的质量:50g+40g-4.9g=85.1g
答:此时所得不饱和溶液的质量为85.1g。
18.(1)AD
(2) 金属B的电性较好、密度小 >
(3)反应时镁比铁放出的热量多
(4)Fe+CuSO4=FeSO4+Cu
(5) Zn+2HCl=ZnCl2+H2↑ Cu+2AgNO3=2Ag+Cu(NO3)2 银
(6)设理论上可以炼出含铁96%的生铁的质量为x。
解得:x≈1166.7t
答:理论上可以炼出含铁96%生铁1166.7t。
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
