2024年中考化学总复习考点探究 课件 第三单元 物质构成的奥秘 第2课时(共35张PPT)
文档属性
| 名称 | 2024年中考化学总复习考点探究 课件 第三单元 物质构成的奥秘 第2课时(共35张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 605.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-14 00:00:00 | ||
图片预览










文档简介
(共35张PPT)
第三单元 物质构成的奥秘
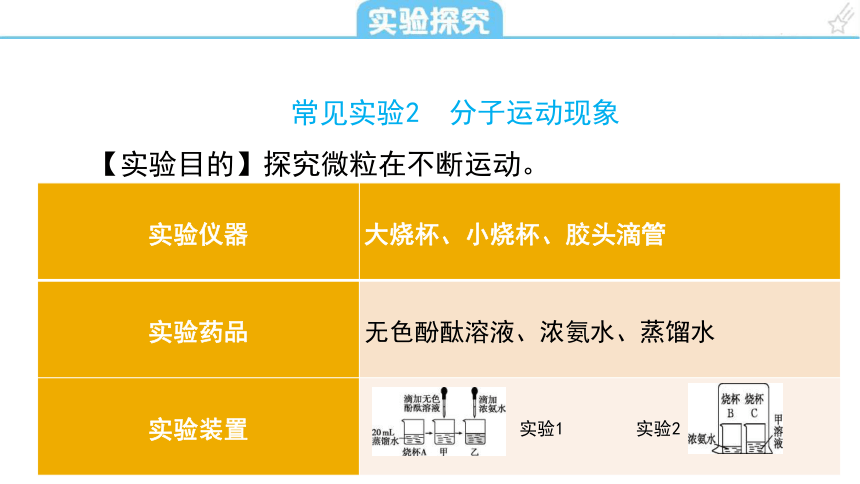
常见实验2 分子运动现象
【实验目的】探究微粒在不断运动。
实验仪器 大烧杯、小烧杯、胶头滴管
实验药品 无色酚酞溶液、浓氨水、蒸馏水
实验装置 实验1 实验2
实验过程 实验现象 实验结论 注意事项
实验1:向烧杯A中加入20 mL蒸馏水,滴入2~3滴无色酚酞溶液,得到溶液甲。向溶液甲中滴加1~2滴浓氨水 溶液 浓氨水显碱性,能使无色酚酞溶液变红 实验2中尽量使大烧杯杯口与桌面不留空隙,防止氨气逸散到空气中
实验2:在烧杯C中重新配制甲溶液。在烧杯B中加入3~5 mL浓氨水,用一个大烧杯把两个烧杯罩在一起 浓氨水中的氨分子不断运动,并进入滴有无色酚酞溶液的蒸馏水中,使溶液变红 由无色变为
红色
烧杯C中的溶液
变红
【实验分析与评价】
1.实验1的作用是
。
2.采用上述实验探究分子运动的优点是 ,不足之处是 。
进行对照,证明浓氨水能使无色酚酞溶液变红
会造成环境污染(或药品使用量大,合理即可)
现象直观
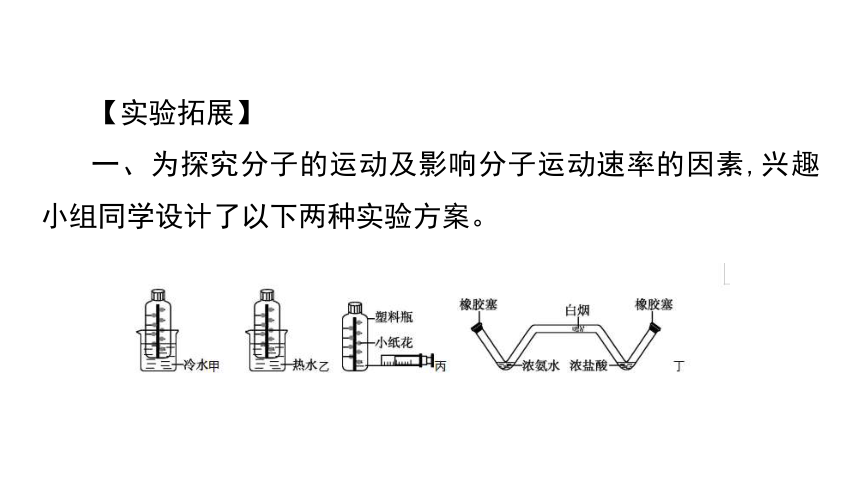
【实验拓展】
一、为探究分子的运动及影响分子运动速率的因素,兴趣小组同学设计了以下两种实验方案。
【实验方案一】
取完全相同的无色透明塑料瓶2只,瓶内分别用细线固定着用滤纸折叠成的大小和形状相同的小纸花,小纸花上均匀喷有无色酚酞溶液,如图甲、乙所示。按照图丙的操作方式分别用注射器向图甲和图乙的塑料瓶底部同时注入8 mL浓氨水,然后将针孔处密封,再将两个塑料瓶分别同时放入等体积的冷水和50 ℃的热水中。瓶甲和瓶乙中可观察到的现象是
两个塑料瓶中的小纸花逐渐变成红色,且小纸花在热水中比在冷水中变红的速度更快 。
与课本中的实验相比,该实验的优点是
可以节约药品,同时也可减少氨气挥发到空气中污染环境 。
【实验方案二】
用图丁所示的玻璃管进行实验,向左、右两端的V形玻璃管口分别滴入等量的浓氨水和浓盐酸,塞紧橡胶塞。一段时间后,玻璃管中可以观察到有白烟(白烟为氯化铵固体颗粒)产生,发生反应的化学方程式为 ;实验中观察到白烟的位置离浓盐酸更近(兴趣小组同学查找资料,得知分子的运动速率与其相对分子质量有关),根据实验现象可得出
。
相对分子质量越小,分子运动速率越快
NH3+HCl NH4Cl
【实验结论】
上述实验证明:分子是不断运动的,且分子的运动速率与
有关。
二、在老师的引导下,同学们设计了以下实验探究分子的运动。
温度、相对分子质量
1.实验过程:
(1)用镊子取两张pH试纸并用水润湿,分别贴于废旧塑料瓶(标上1号)底部的内外壁上。如图所示,另一个废旧塑料瓶做相同处理,并标上2号。观察试纸的颜色。
(2)取出两个一次性杯子,分别放入50 mL食醋,其中一杯再加入50 mL热水。
(3)用1号废旧塑料瓶罩住加入50 mL食醋的杯子,2号废旧塑料瓶罩住加入热水和食醋的杯子,观察试纸的颜色以及颜色变化的快慢。
2.实验现象:贴于1号废旧塑料瓶底部内壁上的试纸变色,变化速度比较慢,贴于1号废旧塑料瓶底部外壁上的试纸
。贴于2号废旧塑料瓶底部内壁上的试纸变色,变化速度比较 ,贴于2号废旧塑料瓶底部外壁上的试纸颜色无明显变化。
3.实验结论:
。
分子在不断运动,且温度越高,分子运动速率越快
无明显变化
快
4.实验评价:改进后实验的优点有
用品简单易得,贴近生活;塑料和一次性杯子重量轻、不易损坏;食醋不会对环境造成污染(合理即可) 。
分子、原子的基本性质
1.(2023·江西节选)茶与咖啡——中国茶清香四溢,西方咖啡醇香浓厚。从微观角度解释闻到香味的原因是
。
【解析】 有香味的分子在不断地运动,向四周扩散,使人们闻到香味。
子、原子的基本性质
分子在不断地运动
2.(2021·江西)“莫道雪融便无迹,雪融成水水成冰”,其中涉及有关物质的说法错误的是 ( )
A.冰和水的化学性质不同
B.冰和水的相对分子质量相同
C.雪和水的分子间隔不同
D.雪融成水是物理变化
A
【解析】 A.由分子构成的物质,分子是保持其化学性质的最小粒子,冰和水都是由水分子构成的,化学性质相同,说法错误;B.冰和水的相对分子质量相同,说法正确;C.雪融化成水后,水分子之间的间隔发生改变,说法正确;D.雪融成水由固态变为液态,只是状态发生改变,没有新物质生成,属于物理变化,说法正确。
3.(2020·江西节选)起床后,测体温。测体温时水银体温计中汞柱会上升的微观原因是汞原子 。
间隔增大
原子的结构
4.(2022·江西)原子中质子数一定等于 ( )
A.中子数
B.核电荷数
C.相对原子质量
D.
核外电子数(或原子序数)
B
【解析】 在原子中,质子数=核外电子数=原子序数=核电荷数,相对原子质量≈质子数+中子数。
5.(2021·江西节选)2021年江西省自主设计的“人造太阳”首次成功放电。
“人造太阳”合理利用了可控核聚变,氘、氚是核聚变的热核材料。
原子种类 质子数 中子数 核外电子数
氘 1 1 1
氚 1 2 x
氘和氚属于 (选填“同种”或“不同种”)元素的原子,上表中x= 。
【解析】 氘和氚的质子数均为1,属于同种元素的原子;原子中,质子数=核外电子数,上表中x=1。
1
同种
6.(2019·江西)考古学家通过测定碳14的含量等方法将人类生活在黄土高原的历史推前至距今212万年。碳14原子的核电荷数为6,相对原子质量为14,则该原子核外电子数为 ( )
A.6 B.8 C.14 D.20
A
原子结构示意图
6.1 下图为铝原子的结构示意图。下列有关铝原子的说法正确的是 ( )
A.图中“+”表示铝原子带正电
B.铝原子的质量主要集中在核外13个电子上
C.铝原子在化学反应中易得到电子
D.铝原子核外有3个电子层
D
【解析】 A.图中“+”表示原子核带正电,不正确;B.铝原子的质量主要集中在原子核上,电子的质量很小,不正确;C.由铝原子的结构示意图可知,铝原子的最外层电子数为3,小于4,在化学反应中易失去电子,不正确;D.弧线表示电子层,由铝原子结构示意图可知,铝原子核外有3个电子层,正确。
元素及离子
7.(2023·江西)镱是量子记忆存储的理想元素,其在元素周期表中的信息如图所示,对图中信息理解正确的是 ( )
A.中子数为70
B.元素符号为yB
C.元素名称为镱
D.相对原子质量为173.1 g
C
【解析】 A.左上角的数字表示原子序数,镱原子的原子序数为70,根据在原子中原子序数=质子数,所以质子数为70,而中子数=相对原子质量-质子数,中子数不是70,错误;B.书写元素符号时应注意:由一个字母表示的元素符号要大写,由两个字母表示的元素符号,第一个字母大写,第二个字母小写,故元素符号表示为Yb,错误;C.该元素的元素名称为镱,正确;D.镱元素的相对原子质量为173.1,相对原子质量的单位是“1”,不是“g”,通常省略,错误。
8.(2023·江西节选)瓷器与玻璃器——瓷器是火与土的结合,玻璃器是火与沙的产融。烧制瓷器所用的黏土中含氧、硅、铝等元素,写出其中一种非金属的元素符号: ;普通玻璃中所含钠离子的符号是 。
Na+
O(或Si)
【解析】 (1)烧制瓷器所用的黏土中含氧、硅、铝等元素,其中氧、硅属于非金属元素,元素符号表示为O、Si;普通玻璃中所含钠离子(1个钠离子带有1个单位的正电荷)的符号是Na+。
9.(2022·江西节选)央视栏目《典籍里的中国》展现了中国智慧,其中有许多古今对比。
如今可将信息存储在芯片上,芯片中含有的某元素在元素周期表中的部分信息如下图,该元素的名称是 。
【解析】 从图中可知,该元素是第14号元素,即硅元素,元素名称为硅。
硅
10.(2021·江西)下列属于非金属元素的是 ( )
A.铝 B.铁 C.钙 D.氧
【解析】 A.铝含有“钅”字旁,属于金属元素;B.铁含有“钅”字旁,属于金属元素;C.钙含有“钅”字旁,属于金属元素;D.氧属于非金属元素。
D
11.(2019·江西节选)联合国确立2019年是“国际化学元素周期表年”,我国姜雪峰教授被选为硫元素代言人,请用表中给定元素完成下列化学用语填空。
(1)硫元素: 。
(2)一种金属离子: 。
Mg2+
S
元素周期表与原子结构示意图的关系
11.1 科学家利用“基因剪刀”技术降低了水稻中砷的含量。下图是砷元素在元素周期表中的部分信息及原子结构示意图。下列说法错误的是 ( )
A.砷属于非金属元素
B.砷的原子序数为33
C.砷原子的相对原子质量为74.92 g
D.x=5,砷与磷元素化学性质相似
C
【解析】 A.砷为“石”字旁,属于固态非金属元素,正确;B.根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为33,正确;C.根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为74.92,相对原子质量单位是“1”,不是“g”,错误;D.根据原子中质子数=核外电子数,所以33=2+8+18+x,x=5,又因为决定元素化学性质的是原子中的最外层电子数,磷原子的最外层电子数为5,而砷原子的最外层电子数也是5,所以砷与磷元素化学性质相似,正确。
第三单元 物质构成的奥秘
常见实验2 分子运动现象
【实验目的】探究微粒在不断运动。
实验仪器 大烧杯、小烧杯、胶头滴管
实验药品 无色酚酞溶液、浓氨水、蒸馏水
实验装置 实验1 实验2
实验过程 实验现象 实验结论 注意事项
实验1:向烧杯A中加入20 mL蒸馏水,滴入2~3滴无色酚酞溶液,得到溶液甲。向溶液甲中滴加1~2滴浓氨水 溶液 浓氨水显碱性,能使无色酚酞溶液变红 实验2中尽量使大烧杯杯口与桌面不留空隙,防止氨气逸散到空气中
实验2:在烧杯C中重新配制甲溶液。在烧杯B中加入3~5 mL浓氨水,用一个大烧杯把两个烧杯罩在一起 浓氨水中的氨分子不断运动,并进入滴有无色酚酞溶液的蒸馏水中,使溶液变红 由无色变为
红色
烧杯C中的溶液
变红
【实验分析与评价】
1.实验1的作用是
。
2.采用上述实验探究分子运动的优点是 ,不足之处是 。
进行对照,证明浓氨水能使无色酚酞溶液变红
会造成环境污染(或药品使用量大,合理即可)
现象直观
【实验拓展】
一、为探究分子的运动及影响分子运动速率的因素,兴趣小组同学设计了以下两种实验方案。
【实验方案一】
取完全相同的无色透明塑料瓶2只,瓶内分别用细线固定着用滤纸折叠成的大小和形状相同的小纸花,小纸花上均匀喷有无色酚酞溶液,如图甲、乙所示。按照图丙的操作方式分别用注射器向图甲和图乙的塑料瓶底部同时注入8 mL浓氨水,然后将针孔处密封,再将两个塑料瓶分别同时放入等体积的冷水和50 ℃的热水中。瓶甲和瓶乙中可观察到的现象是
两个塑料瓶中的小纸花逐渐变成红色,且小纸花在热水中比在冷水中变红的速度更快 。
与课本中的实验相比,该实验的优点是
可以节约药品,同时也可减少氨气挥发到空气中污染环境 。
【实验方案二】
用图丁所示的玻璃管进行实验,向左、右两端的V形玻璃管口分别滴入等量的浓氨水和浓盐酸,塞紧橡胶塞。一段时间后,玻璃管中可以观察到有白烟(白烟为氯化铵固体颗粒)产生,发生反应的化学方程式为 ;实验中观察到白烟的位置离浓盐酸更近(兴趣小组同学查找资料,得知分子的运动速率与其相对分子质量有关),根据实验现象可得出
。
相对分子质量越小,分子运动速率越快
NH3+HCl NH4Cl
【实验结论】
上述实验证明:分子是不断运动的,且分子的运动速率与
有关。
二、在老师的引导下,同学们设计了以下实验探究分子的运动。
温度、相对分子质量
1.实验过程:
(1)用镊子取两张pH试纸并用水润湿,分别贴于废旧塑料瓶(标上1号)底部的内外壁上。如图所示,另一个废旧塑料瓶做相同处理,并标上2号。观察试纸的颜色。
(2)取出两个一次性杯子,分别放入50 mL食醋,其中一杯再加入50 mL热水。
(3)用1号废旧塑料瓶罩住加入50 mL食醋的杯子,2号废旧塑料瓶罩住加入热水和食醋的杯子,观察试纸的颜色以及颜色变化的快慢。
2.实验现象:贴于1号废旧塑料瓶底部内壁上的试纸变色,变化速度比较慢,贴于1号废旧塑料瓶底部外壁上的试纸
。贴于2号废旧塑料瓶底部内壁上的试纸变色,变化速度比较 ,贴于2号废旧塑料瓶底部外壁上的试纸颜色无明显变化。
3.实验结论:
。
分子在不断运动,且温度越高,分子运动速率越快
无明显变化
快
4.实验评价:改进后实验的优点有
用品简单易得,贴近生活;塑料和一次性杯子重量轻、不易损坏;食醋不会对环境造成污染(合理即可) 。
分子、原子的基本性质
1.(2023·江西节选)茶与咖啡——中国茶清香四溢,西方咖啡醇香浓厚。从微观角度解释闻到香味的原因是
。
【解析】 有香味的分子在不断地运动,向四周扩散,使人们闻到香味。
子、原子的基本性质
分子在不断地运动
2.(2021·江西)“莫道雪融便无迹,雪融成水水成冰”,其中涉及有关物质的说法错误的是 ( )
A.冰和水的化学性质不同
B.冰和水的相对分子质量相同
C.雪和水的分子间隔不同
D.雪融成水是物理变化
A
【解析】 A.由分子构成的物质,分子是保持其化学性质的最小粒子,冰和水都是由水分子构成的,化学性质相同,说法错误;B.冰和水的相对分子质量相同,说法正确;C.雪融化成水后,水分子之间的间隔发生改变,说法正确;D.雪融成水由固态变为液态,只是状态发生改变,没有新物质生成,属于物理变化,说法正确。
3.(2020·江西节选)起床后,测体温。测体温时水银体温计中汞柱会上升的微观原因是汞原子 。
间隔增大
原子的结构
4.(2022·江西)原子中质子数一定等于 ( )
A.中子数
B.核电荷数
C.相对原子质量
D.
核外电子数(或原子序数)
B
【解析】 在原子中,质子数=核外电子数=原子序数=核电荷数,相对原子质量≈质子数+中子数。
5.(2021·江西节选)2021年江西省自主设计的“人造太阳”首次成功放电。
“人造太阳”合理利用了可控核聚变,氘、氚是核聚变的热核材料。
原子种类 质子数 中子数 核外电子数
氘 1 1 1
氚 1 2 x
氘和氚属于 (选填“同种”或“不同种”)元素的原子,上表中x= 。
【解析】 氘和氚的质子数均为1,属于同种元素的原子;原子中,质子数=核外电子数,上表中x=1。
1
同种
6.(2019·江西)考古学家通过测定碳14的含量等方法将人类生活在黄土高原的历史推前至距今212万年。碳14原子的核电荷数为6,相对原子质量为14,则该原子核外电子数为 ( )
A.6 B.8 C.14 D.20
A
原子结构示意图
6.1 下图为铝原子的结构示意图。下列有关铝原子的说法正确的是 ( )
A.图中“+”表示铝原子带正电
B.铝原子的质量主要集中在核外13个电子上
C.铝原子在化学反应中易得到电子
D.铝原子核外有3个电子层
D
【解析】 A.图中“+”表示原子核带正电,不正确;B.铝原子的质量主要集中在原子核上,电子的质量很小,不正确;C.由铝原子的结构示意图可知,铝原子的最外层电子数为3,小于4,在化学反应中易失去电子,不正确;D.弧线表示电子层,由铝原子结构示意图可知,铝原子核外有3个电子层,正确。
元素及离子
7.(2023·江西)镱是量子记忆存储的理想元素,其在元素周期表中的信息如图所示,对图中信息理解正确的是 ( )
A.中子数为70
B.元素符号为yB
C.元素名称为镱
D.相对原子质量为173.1 g
C
【解析】 A.左上角的数字表示原子序数,镱原子的原子序数为70,根据在原子中原子序数=质子数,所以质子数为70,而中子数=相对原子质量-质子数,中子数不是70,错误;B.书写元素符号时应注意:由一个字母表示的元素符号要大写,由两个字母表示的元素符号,第一个字母大写,第二个字母小写,故元素符号表示为Yb,错误;C.该元素的元素名称为镱,正确;D.镱元素的相对原子质量为173.1,相对原子质量的单位是“1”,不是“g”,通常省略,错误。
8.(2023·江西节选)瓷器与玻璃器——瓷器是火与土的结合,玻璃器是火与沙的产融。烧制瓷器所用的黏土中含氧、硅、铝等元素,写出其中一种非金属的元素符号: ;普通玻璃中所含钠离子的符号是 。
Na+
O(或Si)
【解析】 (1)烧制瓷器所用的黏土中含氧、硅、铝等元素,其中氧、硅属于非金属元素,元素符号表示为O、Si;普通玻璃中所含钠离子(1个钠离子带有1个单位的正电荷)的符号是Na+。
9.(2022·江西节选)央视栏目《典籍里的中国》展现了中国智慧,其中有许多古今对比。
如今可将信息存储在芯片上,芯片中含有的某元素在元素周期表中的部分信息如下图,该元素的名称是 。
【解析】 从图中可知,该元素是第14号元素,即硅元素,元素名称为硅。
硅
10.(2021·江西)下列属于非金属元素的是 ( )
A.铝 B.铁 C.钙 D.氧
【解析】 A.铝含有“钅”字旁,属于金属元素;B.铁含有“钅”字旁,属于金属元素;C.钙含有“钅”字旁,属于金属元素;D.氧属于非金属元素。
D
11.(2019·江西节选)联合国确立2019年是“国际化学元素周期表年”,我国姜雪峰教授被选为硫元素代言人,请用表中给定元素完成下列化学用语填空。
(1)硫元素: 。
(2)一种金属离子: 。
Mg2+
S
元素周期表与原子结构示意图的关系
11.1 科学家利用“基因剪刀”技术降低了水稻中砷的含量。下图是砷元素在元素周期表中的部分信息及原子结构示意图。下列说法错误的是 ( )
A.砷属于非金属元素
B.砷的原子序数为33
C.砷原子的相对原子质量为74.92 g
D.x=5,砷与磷元素化学性质相似
C
【解析】 A.砷为“石”字旁,属于固态非金属元素,正确;B.根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为33,正确;C.根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为74.92,相对原子质量单位是“1”,不是“g”,错误;D.根据原子中质子数=核外电子数,所以33=2+8+18+x,x=5,又因为决定元素化学性质的是原子中的最外层电子数,磷原子的最外层电子数为5,而砷原子的最外层电子数也是5,所以砷与磷元素化学性质相似,正确。
同课章节目录
