1.3.1氧化还原 课件(共21张PPT) 2023-2024学年高一上学期化学人教版(2019)必修第一册
文档属性
| 名称 | 1.3.1氧化还原 课件(共21张PPT) 2023-2024学年高一上学期化学人教版(2019)必修第一册 |  | |
| 格式 | pptx | ||
| 文件大小 | 27.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-14 00:39:37 | ||
图片预览








文档简介
(共21张PPT)
一价钾钠银氢铵,二价钙镁锌钡氧。
三铝四硅五氮磷,二三铁二四碳。
二四六硫都齐全,铜汞二价最常见。
负一氢氧硝酸根,正一价的是铵根。
单质零价永不忘。
第一章 物质及其变化
第三节 氧化还原反应
第1课时
学习目标
1.能够从多角度认识氧化还原反应。
2.理解氧化还原反应与四种基本反应类型的关系。
新课导入
为什么苹果削皮后颜色很快会变暗?
1
从不同角度认识氧化还原反应
CuO、Fe2O3
C、CO
还原反应
氧化反应
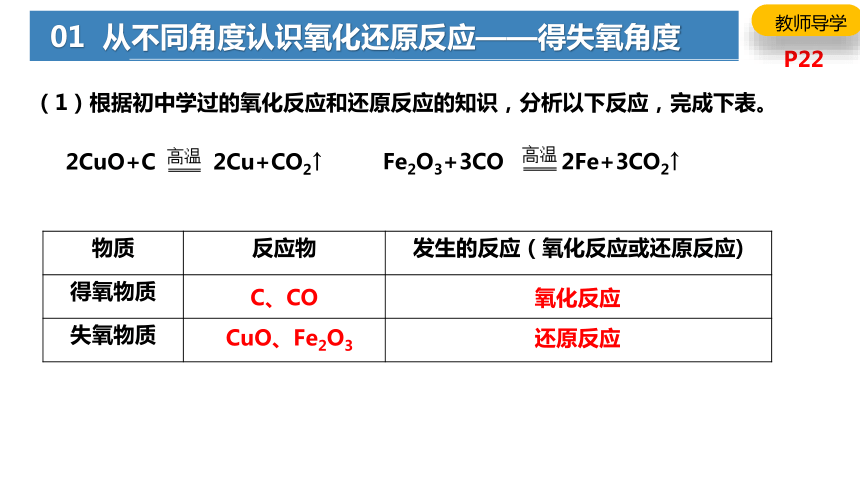
(1)根据初中学过的氧化反应和还原反应的知识,分析以下反应,完成下表。
2CuO+C 2Cu+CO2↑
Fe2O3+3CO 2Fe+3CO2↑
物质 反应物 发生的反应(氧化反应或还原反应)
得氧物质
失氧物质
01 从不同角度认识氧化还原反应——得失氧角度
P22
教师导学
在所列下面的两个反应中是否只发生了氧化反应或还原反应?
CuO+H2 Cu+ H2O
3CO+Fe2O3 2Fe+3CO2
氧化反应
发生了还原反应
Fe2O3
Fe
得到O
CO
失去O
CO2
CuO
得到O
失去O
Cu
H2
H2O
还原反应
氧化反应
可见,有得必有失,有物质得到氧,必定有另一物质失去氧。
01 从不同角度认识氧化还原反应——得失氧角度
氧化反应和还原反应同时发生,相互依存,把这样的反应称为氧化还原反应。
教师导学
以上反应在得氧失氧的同时,元素的化合价是否发生了变化?
同伴助学
碳元素化合价_____,发生_____反应。
碳元素化合价_____,发生_____反应。
高温
Fe2O3
+
3CO
2Fe
+
3CO2
-2
+4
-2
+2
-2
0
+3
高温
2CuO
+
C
2Cu
+
CO2↑
+2
-2
0
0
+4
-2
化合价降低
化合价升高
铜元素化合价_____,发生_____反应。
降低
还原
升高
氧化
铁元素化合价_____,发生_____反应。
降低
还原
升高
氧化
化合价降低
化合价升高
(失氧)
(得氧)
(失氧)
(得氧)
从元素化合价升降的角度认识氧化还原反应
元素化合价升高 → 氧化反应
元素化合价降低 → 还原反应
01 从不同角度认识氧化还原反应——化合价角度
教师导学
氧化还原反应是否一定要有氧的参与?
并非只有得氧、失氧的反应才是氧化还原反应。得氧和失氧的反应只是氧化还原反应中的一部分。
氧化还原反应的特征现象:
Fe+CuSO4 Cu+FeSO4
反应前后元素化合价发生变化。
——判断依据
问题1
不对,可以是同一种元素既被氧化、又还原。
在氧化还原反应中一种元素被氧化,则一定有另一种元素被还原,对吗?
问题2
Cl2 + 2NaOH = NaCl + NaClO + H2O
如:
同伴助学
那么,是什么原因导致元素的化合价发生变化的呢?
教师导学
01 从不同角度认识氧化还原反应——电子转移角度
Cl
Na
钠离子带正电荷
静电作用
氯离子带负电荷
氯化钠
2Na+Cl2 2NaCl
教师导学
结论:氧化还原反应的本质是-----电子的得失
+1
+17
Cl
H
共用电子对
氯化氢的形成,是不是跟氯化钠一样,也是电子的得失呢?
偏向
偏离
01 从不同角度认识氧化还原反应——电子转移角度
教师导学
结论:氧化还原反应的本质是-----共用电子对的偏移
教师导学
氧化还原反应的表观特征是
——化合价的升降变化
判断氧化还原反应
分析氧化还原反应
氧化还原反应的本质是
——电子的转移(得失/共用电子对偏移)
宏观
微观
分别从四大基本反应类型的角度和氧化还原反应的角度对下列反应进行分类
化学反应 基本类型 是否氧化还原反应
分解反应
置换反应
复分解反应
分解反应
复分解反应
置换反应
化合反应
化合反应
是
不是
不是
不是
是
是
是
不是
同伴助学
置换反应
复分解反应
氧化还原反应
反应
反应
分解
化合
化合反应、分解反应 氧化还原反应;
置换反应 氧化还原反应;
复分解反应 氧化还原反应;
不一定是
一定是
一定不是
教师导学
02 氧化还原反应与四种基本反应类型之间的关系
总结:
1.氧化还原反应的特征:有元素化合价的升降
(判断依据)
2.氧化还原反应的本质:有电子的转移
(包括电子的得失或共用电子对的偏移)
元素被还原,发生还原反应
元素失电子/电子对偏离
化合价升高
元素被氧化,发生氧化反应
元素得电子/电子对偏向
化合价降低
失升氧,得降还
教师导学
1.氧化还原反应中一定有氧元素的得失( )
2.氧化还原反应中得电子的物质发生还原反应( )
3.氧化还原反应中所有元素的化合价都一定发生变化( )
4.一个反应中可以只有元素化合价升高,而无元素化合价降低( )
5.有单质参加的反应一定是氧化还原反应( )
×
√
×
×
×
【例1】请同学们认真思考并判断正误:
训练验学
失升氧,得降还
【例2】化学反应按照不同的分类方法可以分为化合反应、分解反应、置换反应、复分解反应,也可以分为氧化还原反应和非氧化还原反应。回答下列问题:
A.既是氧化还原反应又是化合反应的为______(填序号,下同)。
B.属于非氧化还原反应的为_____。
C.不属于四种基本反应类型的为_____。
D.属于置换反应的为_____。
①②
⑤
⑥
③
①CO2+C 2CO
高温
②2Fe+3Cl2 2FeCl3
点燃
③C+H2O(g) CO+H2
高温
④2H2O 2H2↑+O2↑
高温
⑤Na2SO4+BaCl2===2NaCl+BaSO4↓
⑥H2O2+H2S===S↓+2H2O
训练验学
THANKS
谢谢聆听
一价钾钠银氢铵,二价钙镁锌钡氧。
三铝四硅五氮磷,二三铁二四碳。
二四六硫都齐全,铜汞二价最常见。
负一氢氧硝酸根,正一价的是铵根。
单质零价永不忘。
第一章 物质及其变化
第三节 氧化还原反应
第1课时
学习目标
1.能够从多角度认识氧化还原反应。
2.理解氧化还原反应与四种基本反应类型的关系。
新课导入
为什么苹果削皮后颜色很快会变暗?
1
从不同角度认识氧化还原反应
CuO、Fe2O3
C、CO
还原反应
氧化反应
(1)根据初中学过的氧化反应和还原反应的知识,分析以下反应,完成下表。
2CuO+C 2Cu+CO2↑
Fe2O3+3CO 2Fe+3CO2↑
物质 反应物 发生的反应(氧化反应或还原反应)
得氧物质
失氧物质
01 从不同角度认识氧化还原反应——得失氧角度
P22
教师导学
在所列下面的两个反应中是否只发生了氧化反应或还原反应?
CuO+H2 Cu+ H2O
3CO+Fe2O3 2Fe+3CO2
氧化反应
发生了还原反应
Fe2O3
Fe
得到O
CO
失去O
CO2
CuO
得到O
失去O
Cu
H2
H2O
还原反应
氧化反应
可见,有得必有失,有物质得到氧,必定有另一物质失去氧。
01 从不同角度认识氧化还原反应——得失氧角度
氧化反应和还原反应同时发生,相互依存,把这样的反应称为氧化还原反应。
教师导学
以上反应在得氧失氧的同时,元素的化合价是否发生了变化?
同伴助学
碳元素化合价_____,发生_____反应。
碳元素化合价_____,发生_____反应。
高温
Fe2O3
+
3CO
2Fe
+
3CO2
-2
+4
-2
+2
-2
0
+3
高温
2CuO
+
C
2Cu
+
CO2↑
+2
-2
0
0
+4
-2
化合价降低
化合价升高
铜元素化合价_____,发生_____反应。
降低
还原
升高
氧化
铁元素化合价_____,发生_____反应。
降低
还原
升高
氧化
化合价降低
化合价升高
(失氧)
(得氧)
(失氧)
(得氧)
从元素化合价升降的角度认识氧化还原反应
元素化合价升高 → 氧化反应
元素化合价降低 → 还原反应
01 从不同角度认识氧化还原反应——化合价角度
教师导学
氧化还原反应是否一定要有氧的参与?
并非只有得氧、失氧的反应才是氧化还原反应。得氧和失氧的反应只是氧化还原反应中的一部分。
氧化还原反应的特征现象:
Fe+CuSO4 Cu+FeSO4
反应前后元素化合价发生变化。
——判断依据
问题1
不对,可以是同一种元素既被氧化、又还原。
在氧化还原反应中一种元素被氧化,则一定有另一种元素被还原,对吗?
问题2
Cl2 + 2NaOH = NaCl + NaClO + H2O
如:
同伴助学
那么,是什么原因导致元素的化合价发生变化的呢?
教师导学
01 从不同角度认识氧化还原反应——电子转移角度
Cl
Na
钠离子带正电荷
静电作用
氯离子带负电荷
氯化钠
2Na+Cl2 2NaCl
教师导学
结论:氧化还原反应的本质是-----电子的得失
+1
+17
Cl
H
共用电子对
氯化氢的形成,是不是跟氯化钠一样,也是电子的得失呢?
偏向
偏离
01 从不同角度认识氧化还原反应——电子转移角度
教师导学
结论:氧化还原反应的本质是-----共用电子对的偏移
教师导学
氧化还原反应的表观特征是
——化合价的升降变化
判断氧化还原反应
分析氧化还原反应
氧化还原反应的本质是
——电子的转移(得失/共用电子对偏移)
宏观
微观
分别从四大基本反应类型的角度和氧化还原反应的角度对下列反应进行分类
化学反应 基本类型 是否氧化还原反应
分解反应
置换反应
复分解反应
分解反应
复分解反应
置换反应
化合反应
化合反应
是
不是
不是
不是
是
是
是
不是
同伴助学
置换反应
复分解反应
氧化还原反应
反应
反应
分解
化合
化合反应、分解反应 氧化还原反应;
置换反应 氧化还原反应;
复分解反应 氧化还原反应;
不一定是
一定是
一定不是
教师导学
02 氧化还原反应与四种基本反应类型之间的关系
总结:
1.氧化还原反应的特征:有元素化合价的升降
(判断依据)
2.氧化还原反应的本质:有电子的转移
(包括电子的得失或共用电子对的偏移)
元素被还原,发生还原反应
元素失电子/电子对偏离
化合价升高
元素被氧化,发生氧化反应
元素得电子/电子对偏向
化合价降低
失升氧,得降还
教师导学
1.氧化还原反应中一定有氧元素的得失( )
2.氧化还原反应中得电子的物质发生还原反应( )
3.氧化还原反应中所有元素的化合价都一定发生变化( )
4.一个反应中可以只有元素化合价升高,而无元素化合价降低( )
5.有单质参加的反应一定是氧化还原反应( )
×
√
×
×
×
【例1】请同学们认真思考并判断正误:
训练验学
失升氧,得降还
【例2】化学反应按照不同的分类方法可以分为化合反应、分解反应、置换反应、复分解反应,也可以分为氧化还原反应和非氧化还原反应。回答下列问题:
A.既是氧化还原反应又是化合反应的为______(填序号,下同)。
B.属于非氧化还原反应的为_____。
C.不属于四种基本反应类型的为_____。
D.属于置换反应的为_____。
①②
⑤
⑥
③
①CO2+C 2CO
高温
②2Fe+3Cl2 2FeCl3
点燃
③C+H2O(g) CO+H2
高温
④2H2O 2H2↑+O2↑
高温
⑤Na2SO4+BaCl2===2NaCl+BaSO4↓
⑥H2O2+H2S===S↓+2H2O
训练验学
THANKS
谢谢聆听
