8.1金属材料同步练习人教版化学九年级下册(含答案)
文档属性
| 名称 | 8.1金属材料同步练习人教版化学九年级下册(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 657.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-14 00:00:00 | ||
图片预览



文档简介
8.1金属材料 同步练习
一、多选题
1.下列说法正确的是( )
A.原子通过得失电子形成离子,离子一定不能形成原子
B.化合物含有多种元素,含有多种元素的物质一定是化合物
C.CO2能灭火,能使燃着的木条熄灭的无色气体不一定是CO2
D.合金的硬度一般比各成分金属大,多数合金的熔点低于各成分金属
2.制取合金常用的方法是将两种或多种金属(或非金属)加热到某一定温度,使其全部熔化,再冷却成为合金.根据下表中的数据判断(其他条件均满足),下列合金不宜采用上述方法制取的是
金属
熔点
沸点
A.合金 B.合金 C.合金 D.合金
3.下列有关物质的提纯、分离、鉴别以及检验的做法,错误的是
A.除去MnO2中少量KMnO4——加热固体混合物
B.分离铁粉与铜粉——用磁铁吸引
C.鉴别氮气和二氧化碳——伸入燃烧的木条,看木条是否熄灭
D.检验蜡烛中是否含有碳元素——点燃蜡烛,将内壁沾有澄清石灰水的烧杯罩在火焰上方
4.下列推理结果正确的是
A.因铜具有良好的导电性,故用铜来制作导线
B.O2和O3组成元素相同,故化学性质也相同
C.斜面是一种省力的简单机械,故使用斜面一定省力
D.合金的硬度一般比各成分金属大,故熔点也高于成分金属
5.区分下列各组物质的两种方法都正确的是
需区分物质 方法一 方法二
A 空气和氧气 用带火星木条检验 闻气味
B 硬水和软水 加肥皂水,搅拌 观察颜色
C 铜丝和铁丝 用磁铁吸引 观察颜色
D 二氧化碳和一氧化碳 澄清石灰水 点燃
A.A B.B C.C D.D
二、选择题
6.下列金属中常温下为液体的是
A.汞 B.铜 C.锌 D.铅
7.《天工开物》中记述:“凡金箔,每金七厘造方寸金一千片……金性又柔,可屈折如枝柳”。黄金可制成金箔,说明金具有良好的
A.金属光泽 B.导电性 C.延展性 D.导热性
8.化学学习过程中,老师常指导我们用分类法进行学习。分类法有助于我们更好地认识物质,依据分类法下列物质属于单质的是
A.生铁 B.金刚石 C.蒸馏水 D.空气
9.下列各组中的物质按混合物、纯净物、单质、化合物顺序排列的是
A.生铁、水、金刚石、硝酸钾
B.空气、冰水混合物、铁粉、铁锈
C.高锰酸钾、干冰、氢气、稀盐酸
D.水银、液氧、红磷、甲烷
10.文物是宝贵的历史文化遗产。下列文物的主要制作材料属于合金的是
文物
选项 A.青铜亚长牛尊 B.虎形玉佩 C.甲骨片 D.竖线划纹黑陶尊
A.A B.B C.C D.D
11.某合金与铁的物理性质比较如下,熔点:某合金为2500℃,铁为1535℃;密度:某合金为3.00g/cm3, 铁为7.86 g/cm3;硬度(以金刚石硬度为10作为标准):某合金为7.4,铁为4.5;导电性(以银的导电性为100作为标准):某合金为2.3,铁为17。还已知某合金耐腐蚀、强度大。根据以上信息,你认为该合金适合用作
A.导线 B.保险丝 C.飞机外壳 D.炊具
12.通过化学知识的学习,你认为下列说法错误的是( )
A.水银不含水 B.铅笔中不含铅
C.金刚石中不含金 D.干冰是干的冰
13.下列生活实例与其蕴含的化学知识不相符的是
A.用扇子扇煤炉让火更旺—提供更多的氧气,支持燃烧
B.用干冰作制冷剂—干冰升华吸热
C.铝合金用于制作飞机外壳—铝化学性质不活泼
D.用铅笔芯制作简易电池的电极材料—铅笔芯中的石墨具有导电性
14.分类是化学学习的重要方法,下列分类完全正确的是
A.可燃性气体:氢气、氮气、甲烷 B.混合物:生铁、硫酸铜溶液、空气
C.氧化物:水、一氧化碳、氧气 D.金属材料:青铜器、生铁、氧化铜
15.下列有关说法中正确的是( )
A.钛合金材料的密度比较小 B.钛合金的机械强度很低
C.钛合金在海底易发生锈蚀 D.二氧化钛属于合金材料
三、综合应用题
16.请回答下列问题。
(1)石墨常用于制作高铁上的电刷,利用了它良好的 性和润滑性。
(2)工业上经常用“铝热反应”来焊接钢轨,其原理是8Al+3Fe3O4 4Al2O3+9Fe,该反应发生后,不需要再持续加热就可保持高温继续进行,该反应属于 (填“放热”或“吸热”)反应。
(3)水通电分解,其中不发生变化的粒子有 (用化学符号表示)。
(4)除去CO2中混有的少量CO气体,下列方法可行的是______(填字母)。
A.点燃混合气体 B.通入澄清的石灰水中 C.通过灼热的CuO固体
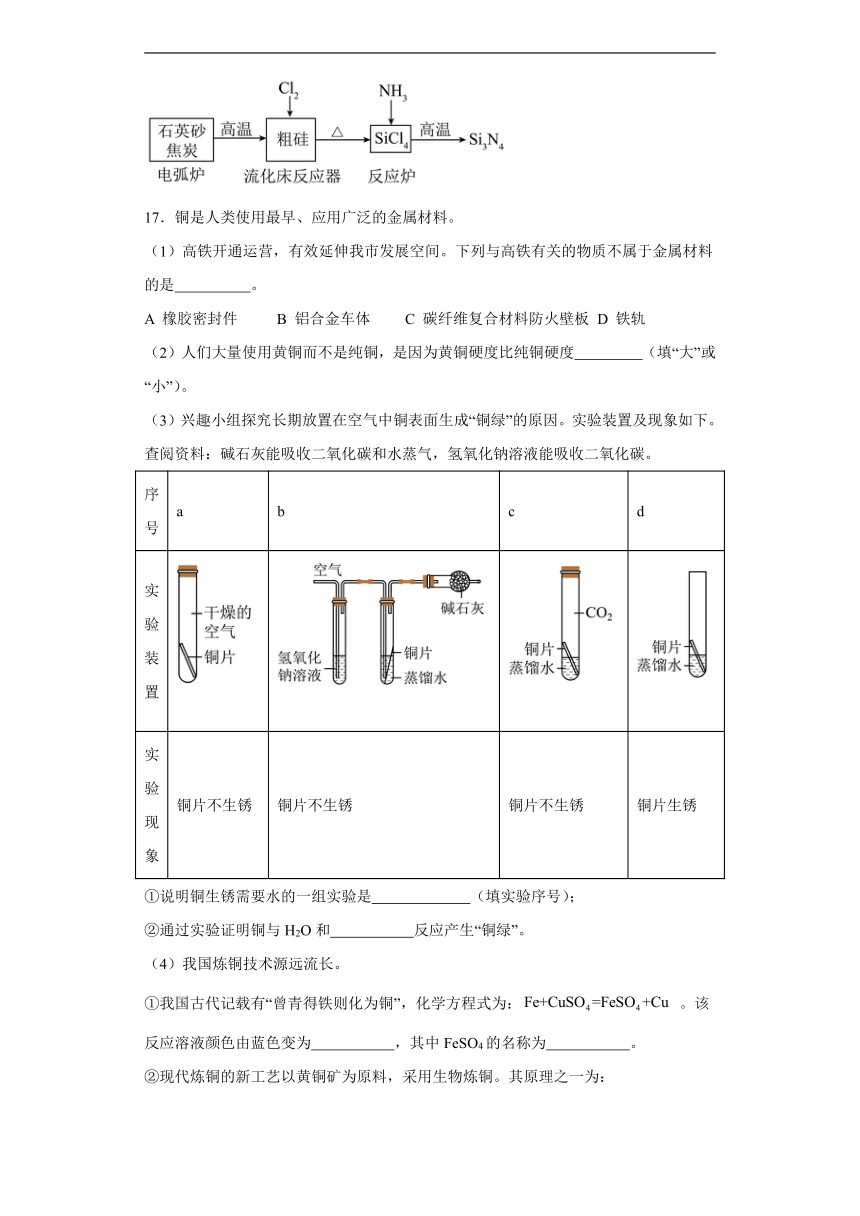
(5)新型陶瓷Si3N4的熔点高,硬度大,化学性质稳定,工业上可以采用化学气相沉积法,在H2的保护下,使SiCl4与N2反应生成Si3N4,沉积在石墨表面,同时生成HCl,请写出图示反应炉中发生的化学方程式: 。
17.铜是人类使用最早、应用广泛的金属材料。
(1)高铁开通运营,有效延伸我市发展空间。下列与高铁有关的物质不属于金属材料的是 。
A 橡胶密封件 B 铝合金车体 C 碳纤维复合材料防火壁板 D 铁轨
(2)人们大量使用黄铜而不是纯铜,是因为黄铜硬度比纯铜硬度 (填“大”或“小”)。
(3)兴趣小组探究长期放置在空气中铜表面生成“铜绿”的原因。实验装置及现象如下。
查阅资料:碱石灰能吸收二氧化碳和水蒸气,氢氧化钠溶液能吸收二氧化碳。
序号 a b c d
实验装置
实验现象 铜片不生锈 铜片不生锈 铜片不生锈 铜片生锈
①说明铜生锈需要水的一组实验是 (填实验序号);
②通过实验证明铜与H2O和 反应产生“铜绿”。
(4)我国炼铜技术源远流长。
①我国古代记载有“曾青得铁则化为铜”,化学方程式为: 。该反应溶液颜色由蓝色变为 ,其中FeSO4的名称为 。
②现代炼铜的新工艺以黄铜矿为原料,采用生物炼铜。其原理之一为: 。R的化学式为 。
(5)兴趣小组取32.0gCuO粉末,按下图装置进行实验。
①实验时,应先 (填“加热样品”或“通一段时间CO”)。
②从环境保护角度,该装置缺少 。
③若加热一段时间后,测得装置B增重11.0g,此时固体中铜元素与氧元素的质量比为 ,若缺少C装置测得数据将 (填“偏大”、“偏小”或“不变”)。
④若32.0gCuO完全被还原成Cu,装置B增重多少克?(写计算过程)
18.铜有重要的用途,铜的化合物广泛存在于自然界。
(1)金属铜性能良好,性质稳定,用途广泛,下列有关铜的说法中,错误的是_______(填字母)。
A.铜有良好的导电性可制成电线 B.纯铜的硬度比黄铜的硬度大
C.铜的发现和利用比铝更早 D.铜在空气加热时表面会变黑
(2)工业上可利用CO还原赤铜矿(Cu2O)“干法”炼铜,实验室可用如图所示装置进行实验:
①在高温条件下,CO还原Cu2O生成单质铜,且“澄清石灰水”变浑浊,请写出“干法”炼铜的化学方程式: 。
②在实验装置的右侧导管口气球的作用是 。
(3)铜锈的化学式为。某实验小组根据其组成推测,铜生锈可能与CO2、H2O和O2均有关,并利用单一控制变量法设计了如下实验:
编号 甲 乙 丙 丁
实验方案
实验现象 铜丝表面有绿色物质(铜锈)生成 铜丝表面无明显现象 现铜丝表面无明显现象 铜丝表面无明显现象
①实验甲和实验丁进行对比,实验丁集气瓶中除了铜丝,还需要添加的物质有 (填化学式)。
②实验甲和实验 进行对比,可得出结论:铜生锈需要O2。
③为了测定某铜丝上铜锈的含量,取100g样品,加入足量的稀硫酸充分反应,化学方程式为:Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑,产生的CO2的质量与时间关系如图所示,求该样品中铜锈的质量 (写出计算过程)。
参考答案:
1.CD
2.BD
3.AC
4.AC
5.CD
6.A
7.C
8.B
9.A
10.A
11.C
12.D
13.C
14.B
15.A
16.(1)导电
(2)放热
(3)H、O
(4)C
(5)
17. AC 大 a d O2和CO2 浅绿色 硫酸亚铁 H2O 通一段时间CO 尾气处理装置(尾气处理方法也得分) 32:3 偏大 设反应生成CO2的质量为x,则
解得:x=17.6g。
答:装置B增重的质量等于生成CO2的质量为17.6g。
18.(1)B
(2) CO+Cu2O2Cu+CO2 尾气处理,防止CO污染空气
(3) CO2,O2 丙 设样品中Cu2(OH)2CO3质量为x,则
x=11.1g
答:样品中Cu2(OH)2CO3质量为11.1g。
一、多选题
1.下列说法正确的是( )
A.原子通过得失电子形成离子,离子一定不能形成原子
B.化合物含有多种元素,含有多种元素的物质一定是化合物
C.CO2能灭火,能使燃着的木条熄灭的无色气体不一定是CO2
D.合金的硬度一般比各成分金属大,多数合金的熔点低于各成分金属
2.制取合金常用的方法是将两种或多种金属(或非金属)加热到某一定温度,使其全部熔化,再冷却成为合金.根据下表中的数据判断(其他条件均满足),下列合金不宜采用上述方法制取的是
金属
熔点
沸点
A.合金 B.合金 C.合金 D.合金
3.下列有关物质的提纯、分离、鉴别以及检验的做法,错误的是
A.除去MnO2中少量KMnO4——加热固体混合物
B.分离铁粉与铜粉——用磁铁吸引
C.鉴别氮气和二氧化碳——伸入燃烧的木条,看木条是否熄灭
D.检验蜡烛中是否含有碳元素——点燃蜡烛,将内壁沾有澄清石灰水的烧杯罩在火焰上方
4.下列推理结果正确的是
A.因铜具有良好的导电性,故用铜来制作导线
B.O2和O3组成元素相同,故化学性质也相同
C.斜面是一种省力的简单机械,故使用斜面一定省力
D.合金的硬度一般比各成分金属大,故熔点也高于成分金属
5.区分下列各组物质的两种方法都正确的是
需区分物质 方法一 方法二
A 空气和氧气 用带火星木条检验 闻气味
B 硬水和软水 加肥皂水,搅拌 观察颜色
C 铜丝和铁丝 用磁铁吸引 观察颜色
D 二氧化碳和一氧化碳 澄清石灰水 点燃
A.A B.B C.C D.D
二、选择题
6.下列金属中常温下为液体的是
A.汞 B.铜 C.锌 D.铅
7.《天工开物》中记述:“凡金箔,每金七厘造方寸金一千片……金性又柔,可屈折如枝柳”。黄金可制成金箔,说明金具有良好的
A.金属光泽 B.导电性 C.延展性 D.导热性
8.化学学习过程中,老师常指导我们用分类法进行学习。分类法有助于我们更好地认识物质,依据分类法下列物质属于单质的是
A.生铁 B.金刚石 C.蒸馏水 D.空气
9.下列各组中的物质按混合物、纯净物、单质、化合物顺序排列的是
A.生铁、水、金刚石、硝酸钾
B.空气、冰水混合物、铁粉、铁锈
C.高锰酸钾、干冰、氢气、稀盐酸
D.水银、液氧、红磷、甲烷
10.文物是宝贵的历史文化遗产。下列文物的主要制作材料属于合金的是
文物
选项 A.青铜亚长牛尊 B.虎形玉佩 C.甲骨片 D.竖线划纹黑陶尊
A.A B.B C.C D.D
11.某合金与铁的物理性质比较如下,熔点:某合金为2500℃,铁为1535℃;密度:某合金为3.00g/cm3, 铁为7.86 g/cm3;硬度(以金刚石硬度为10作为标准):某合金为7.4,铁为4.5;导电性(以银的导电性为100作为标准):某合金为2.3,铁为17。还已知某合金耐腐蚀、强度大。根据以上信息,你认为该合金适合用作
A.导线 B.保险丝 C.飞机外壳 D.炊具
12.通过化学知识的学习,你认为下列说法错误的是( )
A.水银不含水 B.铅笔中不含铅
C.金刚石中不含金 D.干冰是干的冰
13.下列生活实例与其蕴含的化学知识不相符的是
A.用扇子扇煤炉让火更旺—提供更多的氧气,支持燃烧
B.用干冰作制冷剂—干冰升华吸热
C.铝合金用于制作飞机外壳—铝化学性质不活泼
D.用铅笔芯制作简易电池的电极材料—铅笔芯中的石墨具有导电性
14.分类是化学学习的重要方法,下列分类完全正确的是
A.可燃性气体:氢气、氮气、甲烷 B.混合物:生铁、硫酸铜溶液、空气
C.氧化物:水、一氧化碳、氧气 D.金属材料:青铜器、生铁、氧化铜
15.下列有关说法中正确的是( )
A.钛合金材料的密度比较小 B.钛合金的机械强度很低
C.钛合金在海底易发生锈蚀 D.二氧化钛属于合金材料
三、综合应用题
16.请回答下列问题。
(1)石墨常用于制作高铁上的电刷,利用了它良好的 性和润滑性。
(2)工业上经常用“铝热反应”来焊接钢轨,其原理是8Al+3Fe3O4 4Al2O3+9Fe,该反应发生后,不需要再持续加热就可保持高温继续进行,该反应属于 (填“放热”或“吸热”)反应。
(3)水通电分解,其中不发生变化的粒子有 (用化学符号表示)。
(4)除去CO2中混有的少量CO气体,下列方法可行的是______(填字母)。
A.点燃混合气体 B.通入澄清的石灰水中 C.通过灼热的CuO固体
(5)新型陶瓷Si3N4的熔点高,硬度大,化学性质稳定,工业上可以采用化学气相沉积法,在H2的保护下,使SiCl4与N2反应生成Si3N4,沉积在石墨表面,同时生成HCl,请写出图示反应炉中发生的化学方程式: 。
17.铜是人类使用最早、应用广泛的金属材料。
(1)高铁开通运营,有效延伸我市发展空间。下列与高铁有关的物质不属于金属材料的是 。
A 橡胶密封件 B 铝合金车体 C 碳纤维复合材料防火壁板 D 铁轨
(2)人们大量使用黄铜而不是纯铜,是因为黄铜硬度比纯铜硬度 (填“大”或“小”)。
(3)兴趣小组探究长期放置在空气中铜表面生成“铜绿”的原因。实验装置及现象如下。
查阅资料:碱石灰能吸收二氧化碳和水蒸气,氢氧化钠溶液能吸收二氧化碳。
序号 a b c d
实验装置
实验现象 铜片不生锈 铜片不生锈 铜片不生锈 铜片生锈
①说明铜生锈需要水的一组实验是 (填实验序号);
②通过实验证明铜与H2O和 反应产生“铜绿”。
(4)我国炼铜技术源远流长。
①我国古代记载有“曾青得铁则化为铜”,化学方程式为: 。该反应溶液颜色由蓝色变为 ,其中FeSO4的名称为 。
②现代炼铜的新工艺以黄铜矿为原料,采用生物炼铜。其原理之一为: 。R的化学式为 。
(5)兴趣小组取32.0gCuO粉末,按下图装置进行实验。
①实验时,应先 (填“加热样品”或“通一段时间CO”)。
②从环境保护角度,该装置缺少 。
③若加热一段时间后,测得装置B增重11.0g,此时固体中铜元素与氧元素的质量比为 ,若缺少C装置测得数据将 (填“偏大”、“偏小”或“不变”)。
④若32.0gCuO完全被还原成Cu,装置B增重多少克?(写计算过程)
18.铜有重要的用途,铜的化合物广泛存在于自然界。
(1)金属铜性能良好,性质稳定,用途广泛,下列有关铜的说法中,错误的是_______(填字母)。
A.铜有良好的导电性可制成电线 B.纯铜的硬度比黄铜的硬度大
C.铜的发现和利用比铝更早 D.铜在空气加热时表面会变黑
(2)工业上可利用CO还原赤铜矿(Cu2O)“干法”炼铜,实验室可用如图所示装置进行实验:
①在高温条件下,CO还原Cu2O生成单质铜,且“澄清石灰水”变浑浊,请写出“干法”炼铜的化学方程式: 。
②在实验装置的右侧导管口气球的作用是 。
(3)铜锈的化学式为。某实验小组根据其组成推测,铜生锈可能与CO2、H2O和O2均有关,并利用单一控制变量法设计了如下实验:
编号 甲 乙 丙 丁
实验方案
实验现象 铜丝表面有绿色物质(铜锈)生成 铜丝表面无明显现象 现铜丝表面无明显现象 铜丝表面无明显现象
①实验甲和实验丁进行对比,实验丁集气瓶中除了铜丝,还需要添加的物质有 (填化学式)。
②实验甲和实验 进行对比,可得出结论:铜生锈需要O2。
③为了测定某铜丝上铜锈的含量,取100g样品,加入足量的稀硫酸充分反应,化学方程式为:Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑,产生的CO2的质量与时间关系如图所示,求该样品中铜锈的质量 (写出计算过程)。
参考答案:
1.CD
2.BD
3.AC
4.AC
5.CD
6.A
7.C
8.B
9.A
10.A
11.C
12.D
13.C
14.B
15.A
16.(1)导电
(2)放热
(3)H、O
(4)C
(5)
17. AC 大 a d O2和CO2 浅绿色 硫酸亚铁 H2O 通一段时间CO 尾气处理装置(尾气处理方法也得分) 32:3 偏大 设反应生成CO2的质量为x,则
解得:x=17.6g。
答:装置B增重的质量等于生成CO2的质量为17.6g。
18.(1)B
(2) CO+Cu2O2Cu+CO2 尾气处理,防止CO污染空气
(3) CO2,O2 丙 设样品中Cu2(OH)2CO3质量为x,则
x=11.1g
答:样品中Cu2(OH)2CO3质量为11.1g。
同课章节目录
