贵州省贵阳市清镇市博雅实验学校2023-2024学年高三上学期12月月考化学试题(无答案)
文档属性
| 名称 | 贵州省贵阳市清镇市博雅实验学校2023-2024学年高三上学期12月月考化学试题(无答案) | 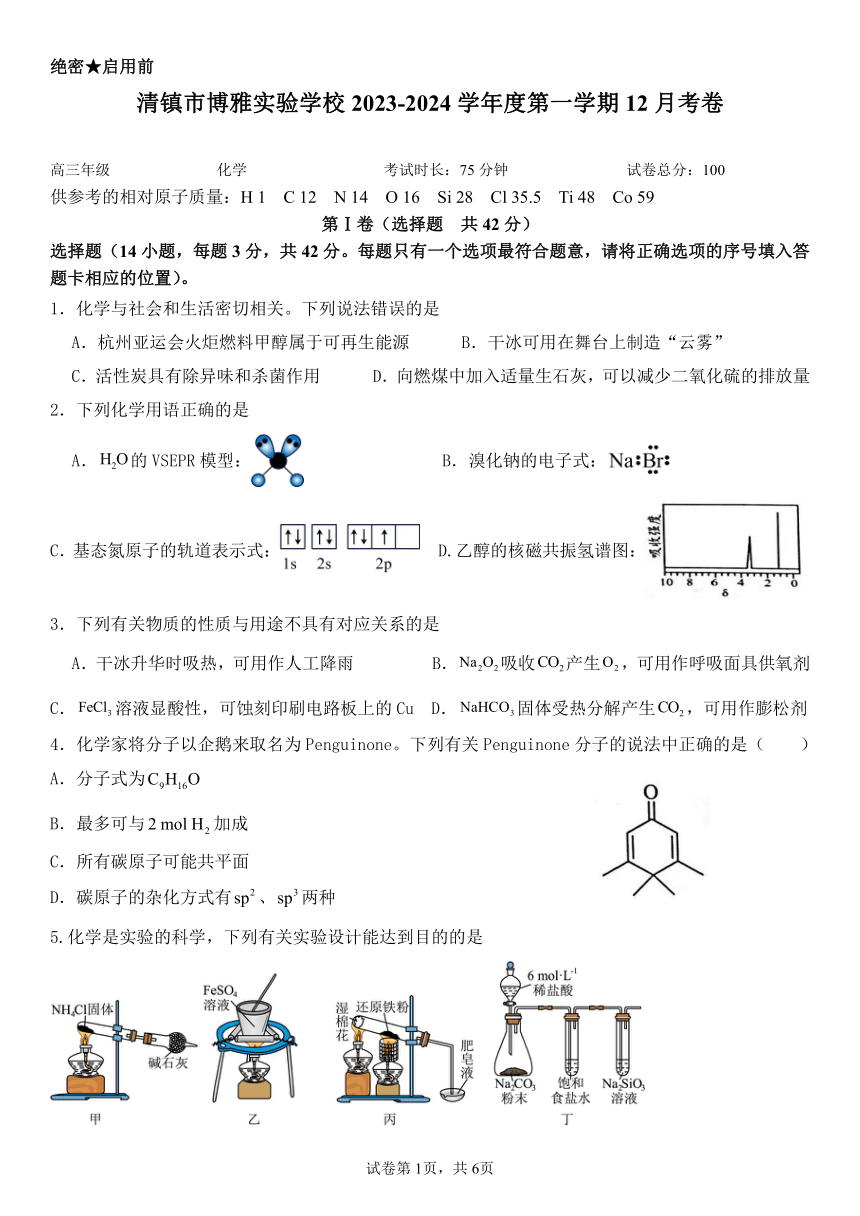 | |
| 格式 | docx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-17 15:17:17 | ||
图片预览


文档简介
绝密★启用前
清镇市博雅实验学校2023-2024学年度第一学期12月考卷
高三年级 化学 考试时长:75分钟 试卷总分:100
供参考的相对原子质量:H 1 C 12 N 14 O 16 Si 28 Cl 35.5 Ti 48 Co 59
第Ⅰ卷(选择题 共42分)
选择题(14小题,每题3分,共42分。每题只有一个选项最符合题意,请将正确选项的序号填入答题卡相应的位置)。
1.化学与社会和生活密切相关。下列说法错误的是
A.杭州亚运会火炬燃料甲醇属于可再生能源 B.干冰可用在舞台上制造“云雾”
C.活性炭具有除异味和杀菌作用 D.向燃煤中加入适量生石灰,可以减少二氧化硫的排放量
2.下列化学用语正确的是
A.的VSEPR模型: B.溴化钠的电子式:
C.基态氮原子的轨道表示式: D.乙醇的核磁共振氢谱图:
3.下列有关物质的性质与用途不具有对应关系的是
A.干冰升华时吸热,可用作人工降雨 B.吸收产生,可用作呼吸面具供氧剂
C.溶液显酸性,可蚀刻印刷电路板上的Cu D.固体受热分解产生,可用作膨松剂
4.化学家将分子以企鹅来取名为Penguinone。下列有关Penguinone分子的说法中正确的是( )
分子式为
B.最多可与加成
C.所有碳原子可能共平面
D.碳原子的杂化方式有、两种
5.化学是实验的科学,下列有关实验设计能达到目的的是
甲用于制备NH3 B. 乙用于蒸发结晶获得FeSO4·7H2O
C. 丙用于探究铁与水蒸气的反应,点燃肥皂泡检验氢气 D. 丁用于验证非金属性:Cl>C>Si
6..X、Y、Z、W是原子序数依次增大的前四周期元素,其中X的电子只有一种自旋方向;Y是地壳中含量最高的元素,Z与Y可形成和两种离子化合物,W原子的核外电子数比Z原子的多4。下列说法正确的是( )
A.X2Y2是极性分子 B.原子半径:Y<Z<W
C.简单氢化物沸点:Y<W D.分子中键角为
7.为阿伏加德罗常数的值。下列说法正确的是
A.28g单晶硅中所含的Si-Si键的数目为
B.溶液中含有的数目为
C.标准状况下,过氧化钠与水反应生成2.24L氧气,转移的电子数为0.2
D.标准状况下,22.4LHF中含有的氟原子数目为
8.下列原理对应离子方程式书写正确的是
A. 泡沫灭火器反应原理:
B.“84”消毒液和洁厕灵不能混用:
C.用食醋处理保温瓶中的水垢:
D.明矾溶液与过量氨水混合:
9.神舟十七号飞船的天线用钛镍记忆合金制造,工业上用钛酸亚铁()冶炼钛(Ti)过程发生反应:(未配平)。下列说法正确的是( )
A.C是氧化剂 B.是氧化产物
C.生成3 mol CO时反应转移6 mol电子 D.配平后C和的化学计量数之比为
10.反应的总能量变化如图所示。下列说法正确的是
过程1释放能量
过程2吸收能量
该反应是放热反应
过程1的能量变化大于过程2
11. CH4与CO2反应得到合成气的原理为 。向容积为2L的恒容密闭容器中充入与,反应过程中CO的体积分数与温度及压强的关系如图所示。下列说法正确的是
A. 该反应焓变:
B. 压强大小关系:
C. M、N状态下平衡常数:
D. N点CH4的平衡转化率与M点的不相同
12.下列关于物质的结构或性质及解释都正确的是( )
选项 物质的结构或性质 解释
A 稳定性: 水分子间存在氢键
B 键角: 中N的孤电子对数比中B的孤电子对数多
C 酸性: 烃基(R-)越长推电子效应越大,使羧基中羟基的极性越小,羧酸的酸性越弱
D 与分子极性相同 二者都是由非极性键构成的分子
13.电解催化还原为乙烯能缓解碳排放引发的温室效应,还将成为获得重要化工原料的补充形式,原理如图所示(a、b均为惰性电极)。下列说法正确的是
A.B为电源负极
B.从左边透过阳离子交换膜到右边
C.电解一段时间后,阳极区溶液的增大
D.阴极反应为
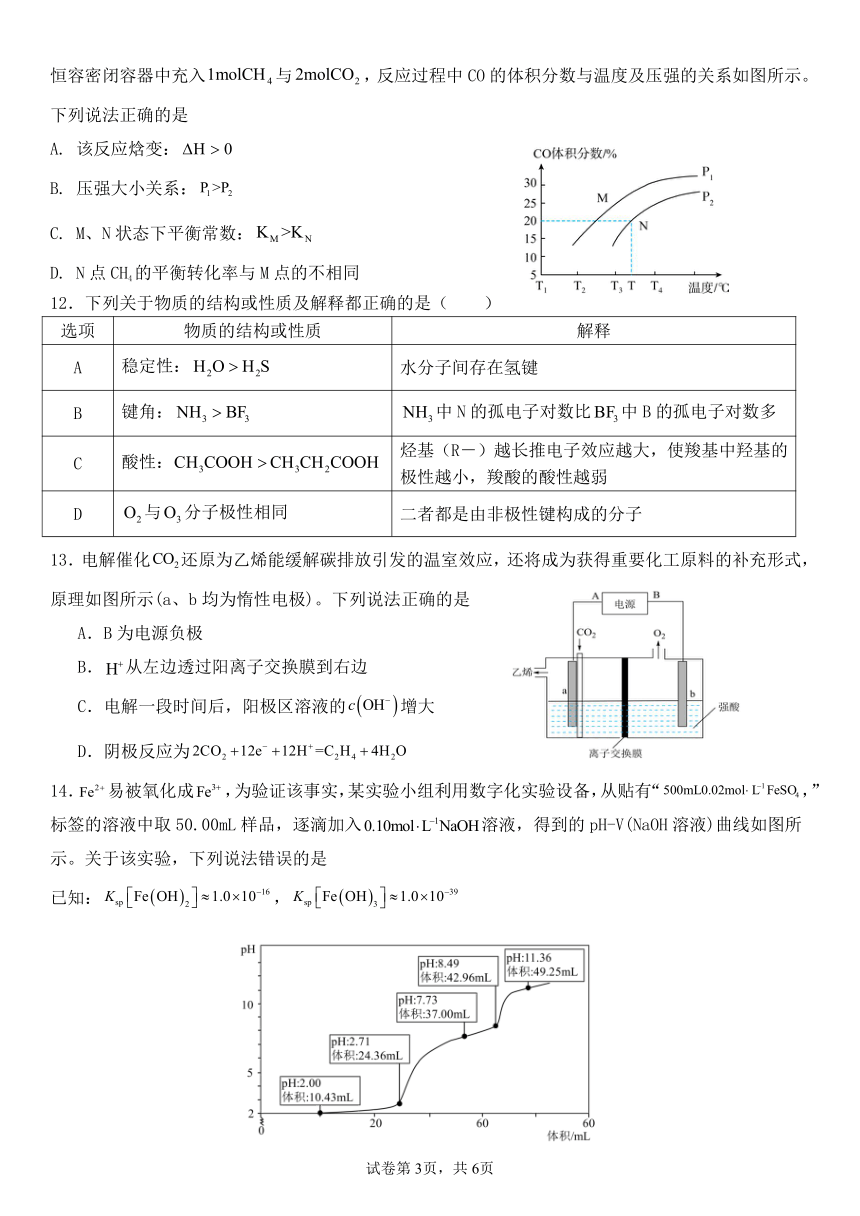
14.易被氧化成,为验证该事实,某实验小组利用数字化实验设备,从贴有“,”标签的溶液中取50.00mL样品,逐滴加入溶液,得到的pH-V(NaOH溶液)曲线如图所示。关于该实验,下列说法错误的是
已知:,
A.使产生沉淀的pH范围为7.73--8.49
B.pH=2.00--2.71时,产生红褐色沉淀现象
C.pH=8.00时,溶液中
D.pH=2.50时,溶液
第Ⅱ卷(非选择题 共58分)
15.(15分)氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备KClO3和NaClO,探究其氧化还原性质。
回答下列问题:
盛放浓盐酸的仪器名称是________,a的作用为________。
d中可选用试剂________(填字母)。
A.Na2S B.NaCl C.Ca(OH)2 D.H2SO4
(3)浓盐酸与二氧化锰反应的离子方程式是__________________________
(4)b中采用的加热方式是________,化学反应的离子方程式是______________,
(5)c中采用冰水浴冷却的目的是________________。
(6)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显________色。可知该条件下KClO3的氧化能力________(填“大于”或“小于”)NaClO。
16.(14分)废旧钴酸锂电池的正极材料主要含有难溶于水的及少量Al、Fe、炭黑等,常用如图所示的一种工艺分离并回收其中的金属钴和锂。
已知:①;
②相关金属离子形成氢氧化物沉淀的pH如下表:
金属阳离子
开始沉淀的pH 4.2 2.7 7.6
沉淀完全的pH 5.2 3.7 9.6
回答下列问题:
(1)中元素Co的化合价为 。
(2)为提高碱浸率,可采取的措施有 (任写一种)。
(3)在浸出液中通入过量发生反应生成Al(OH)3的离子方程式是 。
(4)除杂时,加入空气的主要目的是 ;废渣的主要成分是 。
(5)加氨水控制沉钴的pH,当a≥ 时,此时溶液中c(Co2+)≤10-5mol/L,即认为“沉钴”完全。
(6)钴的氢氧化物加热至290℃时可以完全脱水,所得产物可用于合成钛酸钴。钛酸钴的晶胞结构如图所示,则该晶体化学式为 ;该晶体的密度为 (用代表阿伏加德罗常数)。
17.(14分)雾霾主要成分为灰尘、、和有机碳氢化合物等粒子。烟气脱硝是治理雾霾的方法之一。
(1)以氨气为脱硝剂时,可将还原为。①
②
③
______(用含a、b的代数式表示)。
(2)以臭氧为烟气脱硝剂时,脱硝过程涉及的反应之一为:。不同温度下,控制其它条件一定,在两个恒容容器中发生该反应,相关信息如下表及图所示:
容器 甲 乙
温度/K
容积/L 2
起始充入量 和
①______(填“<”、“>”或“无法确定”),该反应的______0(填“<”或“>”)。
②0~25 min内乙容器中反应的平均速率:V(O2)______.
③温度下,混合气体的起始总压为p,则达到平衡时,的转化率为______,平衡常数K______
(3)乙烯也可用于烟气脱硝。为研究温度、催化剂中负载量对NO去除率的影响,控制其它条件一定,实验结果如图所示。为达到最高的NO去除率,应选择的反应温度约为______,催化剂中负载量为______。
18.(15分)小分子药物高分子化是改进现有药物的重要方法之一,下图是一种制备中间体M对药物进行高分子化改进的路线:
已知:气态烃A是石油裂解的产物,;
回答下列问题:
(1)B的结构简式是 ;E的名称是 。
(2)D→E时,苯环侧链上碳原子的杂化轨道类型由 变为 ;并写出其对应的方程式
(3)F中含有的官能团名称是 。
(4)将布洛芬嫁接到高分子基体M上(M→缓释布洛芬)的反应类型是 。
(5)化合物N是G的的同分异构体,满足下列条件的N共有 种(不考虑立体异构);其中核磁共振氢谱图有五组吸收峰,且峰面积比为2:2:2:1:1的化合物的结构简式为
①含有碳碳双键;②可与新制的共热生成红色沉淀试卷第1页,共3页
试卷第5页,共6页
(北京)股份有限公司
清镇市博雅实验学校2023-2024学年度第一学期12月考卷
高三年级 化学 考试时长:75分钟 试卷总分:100
供参考的相对原子质量:H 1 C 12 N 14 O 16 Si 28 Cl 35.5 Ti 48 Co 59
第Ⅰ卷(选择题 共42分)
选择题(14小题,每题3分,共42分。每题只有一个选项最符合题意,请将正确选项的序号填入答题卡相应的位置)。
1.化学与社会和生活密切相关。下列说法错误的是
A.杭州亚运会火炬燃料甲醇属于可再生能源 B.干冰可用在舞台上制造“云雾”
C.活性炭具有除异味和杀菌作用 D.向燃煤中加入适量生石灰,可以减少二氧化硫的排放量
2.下列化学用语正确的是
A.的VSEPR模型: B.溴化钠的电子式:
C.基态氮原子的轨道表示式: D.乙醇的核磁共振氢谱图:
3.下列有关物质的性质与用途不具有对应关系的是
A.干冰升华时吸热,可用作人工降雨 B.吸收产生,可用作呼吸面具供氧剂
C.溶液显酸性,可蚀刻印刷电路板上的Cu D.固体受热分解产生,可用作膨松剂
4.化学家将分子以企鹅来取名为Penguinone。下列有关Penguinone分子的说法中正确的是( )
分子式为
B.最多可与加成
C.所有碳原子可能共平面
D.碳原子的杂化方式有、两种
5.化学是实验的科学,下列有关实验设计能达到目的的是
甲用于制备NH3 B. 乙用于蒸发结晶获得FeSO4·7H2O
C. 丙用于探究铁与水蒸气的反应,点燃肥皂泡检验氢气 D. 丁用于验证非金属性:Cl>C>Si
6..X、Y、Z、W是原子序数依次增大的前四周期元素,其中X的电子只有一种自旋方向;Y是地壳中含量最高的元素,Z与Y可形成和两种离子化合物,W原子的核外电子数比Z原子的多4。下列说法正确的是( )
A.X2Y2是极性分子 B.原子半径:Y<Z<W
C.简单氢化物沸点:Y<W D.分子中键角为
7.为阿伏加德罗常数的值。下列说法正确的是
A.28g单晶硅中所含的Si-Si键的数目为
B.溶液中含有的数目为
C.标准状况下,过氧化钠与水反应生成2.24L氧气,转移的电子数为0.2
D.标准状况下,22.4LHF中含有的氟原子数目为
8.下列原理对应离子方程式书写正确的是
A. 泡沫灭火器反应原理:
B.“84”消毒液和洁厕灵不能混用:
C.用食醋处理保温瓶中的水垢:
D.明矾溶液与过量氨水混合:
9.神舟十七号飞船的天线用钛镍记忆合金制造,工业上用钛酸亚铁()冶炼钛(Ti)过程发生反应:(未配平)。下列说法正确的是( )
A.C是氧化剂 B.是氧化产物
C.生成3 mol CO时反应转移6 mol电子 D.配平后C和的化学计量数之比为
10.反应的总能量变化如图所示。下列说法正确的是
过程1释放能量
过程2吸收能量
该反应是放热反应
过程1的能量变化大于过程2
11. CH4与CO2反应得到合成气的原理为 。向容积为2L的恒容密闭容器中充入与,反应过程中CO的体积分数与温度及压强的关系如图所示。下列说法正确的是
A. 该反应焓变:
B. 压强大小关系:
C. M、N状态下平衡常数:
D. N点CH4的平衡转化率与M点的不相同
12.下列关于物质的结构或性质及解释都正确的是( )
选项 物质的结构或性质 解释
A 稳定性: 水分子间存在氢键
B 键角: 中N的孤电子对数比中B的孤电子对数多
C 酸性: 烃基(R-)越长推电子效应越大,使羧基中羟基的极性越小,羧酸的酸性越弱
D 与分子极性相同 二者都是由非极性键构成的分子
13.电解催化还原为乙烯能缓解碳排放引发的温室效应,还将成为获得重要化工原料的补充形式,原理如图所示(a、b均为惰性电极)。下列说法正确的是
A.B为电源负极
B.从左边透过阳离子交换膜到右边
C.电解一段时间后,阳极区溶液的增大
D.阴极反应为
14.易被氧化成,为验证该事实,某实验小组利用数字化实验设备,从贴有“,”标签的溶液中取50.00mL样品,逐滴加入溶液,得到的pH-V(NaOH溶液)曲线如图所示。关于该实验,下列说法错误的是
已知:,
A.使产生沉淀的pH范围为7.73--8.49
B.pH=2.00--2.71时,产生红褐色沉淀现象
C.pH=8.00时,溶液中
D.pH=2.50时,溶液
第Ⅱ卷(非选择题 共58分)
15.(15分)氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备KClO3和NaClO,探究其氧化还原性质。
回答下列问题:
盛放浓盐酸的仪器名称是________,a的作用为________。
d中可选用试剂________(填字母)。
A.Na2S B.NaCl C.Ca(OH)2 D.H2SO4
(3)浓盐酸与二氧化锰反应的离子方程式是__________________________
(4)b中采用的加热方式是________,化学反应的离子方程式是______________,
(5)c中采用冰水浴冷却的目的是________________。
(6)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显________色。可知该条件下KClO3的氧化能力________(填“大于”或“小于”)NaClO。
16.(14分)废旧钴酸锂电池的正极材料主要含有难溶于水的及少量Al、Fe、炭黑等,常用如图所示的一种工艺分离并回收其中的金属钴和锂。
已知:①;
②相关金属离子形成氢氧化物沉淀的pH如下表:
金属阳离子
开始沉淀的pH 4.2 2.7 7.6
沉淀完全的pH 5.2 3.7 9.6
回答下列问题:
(1)中元素Co的化合价为 。
(2)为提高碱浸率,可采取的措施有 (任写一种)。
(3)在浸出液中通入过量发生反应生成Al(OH)3的离子方程式是 。
(4)除杂时,加入空气的主要目的是 ;废渣的主要成分是 。
(5)加氨水控制沉钴的pH,当a≥ 时,此时溶液中c(Co2+)≤10-5mol/L,即认为“沉钴”完全。
(6)钴的氢氧化物加热至290℃时可以完全脱水,所得产物可用于合成钛酸钴。钛酸钴的晶胞结构如图所示,则该晶体化学式为 ;该晶体的密度为 (用代表阿伏加德罗常数)。
17.(14分)雾霾主要成分为灰尘、、和有机碳氢化合物等粒子。烟气脱硝是治理雾霾的方法之一。
(1)以氨气为脱硝剂时,可将还原为。①
②
③
______(用含a、b的代数式表示)。
(2)以臭氧为烟气脱硝剂时,脱硝过程涉及的反应之一为:。不同温度下,控制其它条件一定,在两个恒容容器中发生该反应,相关信息如下表及图所示:
容器 甲 乙
温度/K
容积/L 2
起始充入量 和
①______(填“<”、“>”或“无法确定”),该反应的______0(填“<”或“>”)。
②0~25 min内乙容器中反应的平均速率:V(O2)______.
③温度下,混合气体的起始总压为p,则达到平衡时,的转化率为______,平衡常数K______
(3)乙烯也可用于烟气脱硝。为研究温度、催化剂中负载量对NO去除率的影响,控制其它条件一定,实验结果如图所示。为达到最高的NO去除率,应选择的反应温度约为______,催化剂中负载量为______。
18.(15分)小分子药物高分子化是改进现有药物的重要方法之一,下图是一种制备中间体M对药物进行高分子化改进的路线:
已知:气态烃A是石油裂解的产物,;
回答下列问题:
(1)B的结构简式是 ;E的名称是 。
(2)D→E时,苯环侧链上碳原子的杂化轨道类型由 变为 ;并写出其对应的方程式
(3)F中含有的官能团名称是 。
(4)将布洛芬嫁接到高分子基体M上(M→缓释布洛芬)的反应类型是 。
(5)化合物N是G的的同分异构体,满足下列条件的N共有 种(不考虑立体异构);其中核磁共振氢谱图有五组吸收峰,且峰面积比为2:2:2:1:1的化合物的结构简式为
①含有碳碳双键;②可与新制的共热生成红色沉淀试卷第1页,共3页
试卷第5页,共6页
(北京)股份有限公司
同课章节目录
