化学鲁科版(2019)必修第二册综合素养训练三(含解析)
文档属性
| 名称 | 化学鲁科版(2019)必修第二册综合素养训练三(含解析) |  | |
| 格式 | doc | ||
| 文件大小 | 519.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-10-30 16:05:33 | ||
图片预览




文档简介
综合素养训练三
(满分:100分 时间:90分钟)
一、选择题(本题共10小题,每小题2分,共20分,每小题只有一个选项符合题意)
1.生物燃料是以玉米、大豆等为原料生产的燃料,例如乙醇和生物柴油。下列有关说法不正确的是( )
A.生物燃料是可再生能源
B.生物燃料的组成元素与汽油等矿物燃料完全相同
C.发展生物燃料有利于保护生态环境
D.发展生物燃料有利于调整产业结构,提高农民收入
2.下列有关化学用语的说法不正确的是( )
A.中子数为7的碳原子:C
B.氯乙烯的结构简式:CH2===CHCl
C.羟基的电子式:∶H
D.乙酸分子的空间填充模型:
3.下列能用分液漏斗分离的是( )
A.植物油和乙醇 B.乙酸乙酯和水
C.乙酸和乙醇 D.汽油和煤油
4.海葵毒素是从海葵中分离出的一种剧毒物质,分子式为C129H223N3O54。哈佛大学的某研究小组经过8年努力,于1989年完成了海葵毒素的全合成。下列说法正确的是( )
A.海葵毒素是一种高分子化合物
B.海葵毒素是一种无机化合物
C.海葵毒素的成功合成预示着有机合成必将步入新的辉煌
D.海葵毒素的成功合成说明人类是无所不能的,能够合成任何有机物
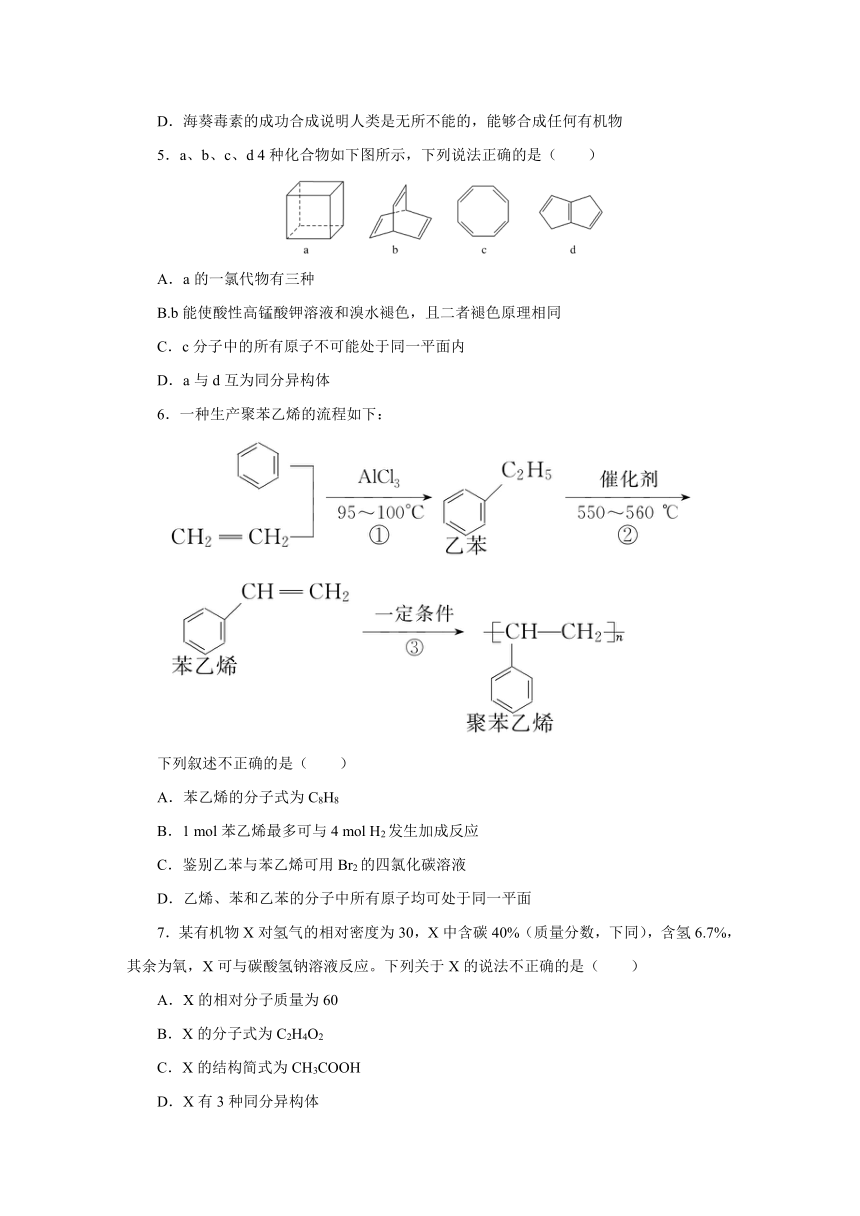
5.a、b、c、d 4种化合物如下图所示,下列说法正确的是( )
A.a的一氯代物有三种
B.b能使酸性高锰酸钾溶液和溴水褪色,且二者褪色原理相同
C.c分子中的所有原子不可能处于同一平面内
D.a与d互为同分异构体
6.一种生产聚苯乙烯的流程如下:
下列叙述不正确的是( )
A.苯乙烯的分子式为C8H8
B.1 mol苯乙烯最多可与4 mol H2发生加成反应
C.鉴别乙苯与苯乙烯可用Br2的四氯化碳溶液
D.乙烯、苯和乙苯的分子中所有原子均可处于同一平面
7.某有机物X对氢气的相对密度为30,X中含碳40%(质量分数,下同),含氢6.7%,其余为氧,X可与碳酸氢钠溶液反应。下列关于X的说法不正确的是( )
A.X的相对分子质量为60
B.X的分子式为C2H4O2
C.X的结构简式为CH3COOH
D.X有3种同分异构体
8.苹果酸的结构简式为,下列说法不正确的是( )
A.苹果酸中能发生酯化反应的官能团有2种
B.1 mol苹果酸可与2 mol NaOH发生中和反应
C.1 mol苹果酸与足量金属Na反应生成3 mol H2
D.HCOO—CH2—CH(OH)—OOCH与苹果酸互为同分异构体
9.合成导电高分子材料PPV的反应如下:
下列说法正确的是( )
A.该反应为缩聚反应
B.PPV是聚苯乙炔
C.PPV与聚苯乙烯的最小结构单元组成相同
D.1 mol 最多可与2 mol H2发生反应
10.某有机物的结构简式为CHOHCH2COOH,在下列各反应的类型中:
①取代 ②加成 ③加聚 ④水解 ⑤酯化 ⑥中和 ⑦氧化 ⑧置换
它能发生的反应有( )
A.①②③⑤⑥⑦ B.②③④⑥⑧
C.①②⑤⑥⑦⑧ D.③④⑤⑥⑦⑧
二、选择题(本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题意,全部选对得4分,选对但不全的得2分,有选错的得0分)
11.下列说法中正确的是( )
A.可用溴水检验甲烷中混有的乙烯
B.聚乙烯(PE)和聚氯乙烯(PVC)都是食品级塑料制品的主要成分
C.分馏、干馏都是物理变化,裂化、裂解都是化学变化
D.常用75%(体积分数)的酒精溶液杀菌、消毒
12.某有机物的结构简式为,它在一定条件下可发生的反应为( )
①酯化反应 ②氧化反应 ③水解反应 ④加聚反应 ⑤取代反应
A.②③④ B.①②③
C.①②⑤ D.③④⑤
13.从石油中分离得到的烃C8H18可以实现如图所示的转化(B、D是生活中常见的两种有机物),下列说法不正确的是( )
A.反应①是裂解反应
B.1 mol B或1 mol D可以与足量Na反应生成0.5 mol H2
C.B、D、E三种物质可以用饱和Na2CO3溶液鉴别
D.反应④的氧化剂只能是氧气
14.105 ℃、101 kPa时,甲烷、乙烷和乙烯组成的混合烃80 mL与过量O2混合并完全燃烧,恢复到原来的温度和压强,混合气体总体积增加了20 mL。原混合烃中乙烷的体积分数为( )
A.12.5% B.25%
C.50% D.75%
15.某课外活动小组设计如图所示装置制取乙酸乙酯。
已知:
①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH。
②有关有机物的沸点:
试剂 乙醚 乙醇 乙酸 乙酸乙酯
沸点(℃) 34.7 78.5 117.9 77.1
下列说法正确的是( )
A.装置中球形干燥管既能冷凝蒸气又能防止倒吸
B.反应结束后大试管中的现象是液体分层,下层为无色油状液体,上层溶液颜色变浅
C.从大试管中分离出的乙酸乙酯中还含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,过滤分离出乙醇
D.最后加入无水硫酸钠,进行蒸馏,收集117.9 ℃左右的馏分,以得到较纯净的乙酸乙酯
三、非选择题(本题共5小题,共60分)
16.(12分)(1)下列各图均能表示甲烷的分子结构,按要求回答下列问题:
①以上哪一种结构更能反映其真实存在状况 (填字母,下同)。
a.Ⅰ b.Ⅱ
c.Ⅲ d.Ⅳ
②下列事实能证明甲烷分子是正四面体结构的是 。
a.CH3Cl只代表一种物质
b.CH2Cl2只代表一种物质
c.CHCl3只代表一种物质
d.CCl4只代表一种物质
(2)烃分子中的碳原子与氢原子结合的方式是 。
a.形成4对共用电子 b.通过1个共价键
c.通过2个共价键 d.通过离子键和共价键
(3)乙烷的电子式为 ,分子式为CmH20的烷烃中m为 ,分子式为C8Hx的烷烃中x为 ,与CO2密度(同温同压且均为气体时)相同的烷烃的分子式为 ,若上述四种烃各为1 mol,在足量O2中燃烧,消耗O2最多的是 。
(4)若CH4、C2H6、C3H8、C4H10四种烃的质量均为1 g,在足量O2中燃烧,消耗O2最多的是 。
17.(12分)已知:A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工发展水平。现以A为主要原料合成乙酸乙酯,其合成路线如图(反应条件略):
回答下列问题:
(1)分别写出A、C的名称: 、 。
(2)B、D分子中的官能团分别是 、 。
(3)写出下列反应的反应类型:① ,④ 。
(4)写出下列反应的化学方程式:
①________________________________________________________________________;
②________________________________________________________________________;
③________________________________________________________________________。
18.(12分)某校学生用如图所示装置进行实验(夹持装置略),以探究苯与液溴发生反应的原理并分离、提纯反应的产物。
请回答下列问题:
(1)冷凝管所起的作用为 ,冷凝水从 (填“a”或“b”)口进入。
(2)实验开始时,关闭K2、打开K1和分液漏斗活塞,滴加苯和液溴的混合物,三颈烧瓶中发生反应的化学方程式为
________________________________________________________________________
________________________________________________________________________。
(3)Ⅲ中小试管内苯的作用是
________________________________________________________________________。
(4)能说明苯与液溴发生了取代反应的现象是
________________________________________________________________________
________________________________________________________________________。
(5)生成的溴苯因溶有未反应的溴而显橙黄色,提纯的方法是
________________________________________________________________________
________________________________________________________________________。
(6)Ⅳ中球形干燥管的作用是 。
19.(12分)某化学兴趣小组设计“乙醇催化氧化实验”来探究催化剂的催化机理并对反应后的产物进行分析,装置(夹持装置已省略)如图所示:
试回答以下问题:
(1)C中热水的作用是 ;在装入实验药品之前,应进行的操作是 。
(2)装入实验药品后,关闭a、b、c,在铜丝的中间部分加热片刻,M处铜丝由红变黑,反应的化学方程式为 ,然后打开a、b、c,通过控制a和b,间歇性地通入气体,即可在M处观察到受热部分的铜丝交替出现变红、变黑的现象。铜丝由黑变红时,发生反应的化学方程式为 。通过实验,可以得出结论:该实验过程中催化剂 (填“参加”或“不参加”)化学反应。
(3)反应进行一段时间后,烧杯F中能收集到的有机物主要有 、 。
(4)若烧杯F中收集到的液体用蓝色石蕊试纸检验,试纸显红色,说明液体中含有 。要除去该物质,可先在混合液中加入 (填字母),然后通过 (填操作名称)即可。
A.氯化钠溶液 B.苯
C.碳酸氢钠溶液 D.四氯化碳
20.(12分)Ⅰ .已知某气态烃X在标准状况下的密度为1.16 g·L-1,A能发生银镜反应,E具有水果香味,有关物质的转化关系如图甲所示。
请回答:
(1)C中含有的官能团名称是 。
(2)化合物M是A的同系物,比A少一个碳原子,请写出M的结构式: 。
(3)下列说法正确的是 (填序号)。
A.有机化合物D在加热条件下可以使黑色的氧化铜变红
B.有机化合物C分子中的所有原子在同一平面上
C.反应③为还原反应,反应④为氧化反应
D.有机化合物B、D、E均能与NaOH溶液反应
Ⅱ .某同学用如图乙所示的实验装置制取少量乙酸乙酯,实验结束后,试管A中上层为透明的、难溶于水的油状液体。
(1)实验开始时,试管A中的导管不伸入液面下的原因是 ;当观察到试管A中 时,认为反应基本完成。
(2)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,如图丙是分离操作步骤流程图。
试剂b是 ;分离方法①是 ;分离方法③是 。
(3)在得到的A中加入无水碳酸钠粉末,振荡,目的是 。
综合素养训练三
1.解析:由题给信息知生物燃料为可再生能源,故A正确;生物燃料的组成元素主要为碳、氢、氧,汽油等矿物燃料的组成元素主要是碳、氢,组成元素不完全相同,故B不正确;发展生物燃料,可减少化石燃料的使用,有利于保护生态环境,故C正确;发展生物柴油有利于调整产业结构,提高农民收入,故D正确。
答案:B
2.解析:中子数为7的碳原子的质量数为13,故A错误;氯乙烯的结构简式为CH2===CHCl,故B正确;羟基的电子式为∶H,故C正确;题图为乙酸分子的空间填充模型,故D正确。
答案:A
3.解析:A项,植物油和乙醇互溶,不能使用分液漏斗分离;B项,乙酸乙酯难溶于水,密度比水小,二者互不相溶,因此可以使用分液漏斗分离;C项,乙酸与乙醇互溶,不能使用分液漏斗分离;D项,汽油和煤油互溶,两者沸点范围不同,应用蒸馏的方法分离,不能使用分液漏斗分离;故选B。
答案:B
4.解析:海葵毒素不是高分子化合物,故A错误;该物质中含有C、H、N、O元素,属于有机物,不属于无机物,故B错误;海葵毒素的成功合成预示着有机合成必将步入新的辉煌,故C正确;海葵毒素的成功合成不能说明人类能合成任何有机物,有些有机物目前还不能人工合成,故D错误。
答案:C
5.解析:a是正方体结构,8个顶点的氢原子位置相同,所以a的一氯代物有一种,A错误;b中含碳碳双键,b使酸性高锰酸钾溶液褪色的原因是发生氧化反应,b与溴水中的溴发生加成反应而使溴水褪色,二者褪色原理不同,故B错误;c中含有碳碳双键,c分子中的所有原子可能处于同一平面内,故C错误;a与d的分子式都是C8H8,结构不同,二者互为同分异构体,故D正确。
答案:D
6.解析:每个苯乙烯分子中含8个C、8个H,可知其分子式为C8H8,故A正确;苯乙烯中苯环、碳碳双键均能与氢气发生加成反应,则1 mol苯乙烯最多可与4 mol H2发生加成反应,故B正确;苯乙烯含碳碳双键,而乙苯不含,苯乙烯能使Br2的四氯化碳溶液褪色,而乙苯不能,可鉴别,故C正确;乙烯分子、苯分子为平面结构,乙苯分子中的所有原子不可能共面,故D错误。
答案:D
7.解析:有机物X对氢气的相对密度为30,则该有机物的相对分子质量为60,故A正确;X中含碳40%,含氢6.7%,其余为氧,所以每个X分子中C的个数为=2,H的个数为≈4,O的个数为=2,X的分子式为C2H4O2,故B正确;X的分子式为C2H4O2,且X可以和NaHCO3溶液反应,则X中含有—COOH,X的结构简式为CH3COOH,故C正确;X的同分异构体有HOCH2CHO、HCOOCH3,共2种,故D不正确。
答案:D
8.答案:C
9.解析:合成导电高分子材料PPV的反应中,有小分子物质HI生成,属于缩聚反应;PPV含有I,而聚苯乙炔为烃类物质,则PPV不是聚苯乙炔;聚苯乙烯的重复结构单元为,不含碳碳双键,而该高聚物的结构单元中含有碳碳双键,所以最小结构单元组成不相同;中苯环和碳碳双键都可与氢气反应,则1 mol 最多可与5 mol H2发生反应。
答案:A
10.解析:中含有羟基,能够发生酯化反应和取代反应,能够与钠发生置换反应,能够被强氧化剂氧化;含有苯环,能够发生加成反应和取代反应;含有羧基,能够发生中和反应和酯化反应;不能发生加聚反应和水解反应。
答案:C
11.解析:乙烯分子中含有碳碳双键,可与溴发生加成反应而使溴水褪色,而甲烷不能使溴水褪色,故A正确;聚氯乙烯中含有氯元素,加热可产生有害物质,不是食品级塑料制品的主要成分,故B错误;干馏为化学变化,故C错误;75%(体积分数)的酒精溶液可使蛋白质变性,起到杀菌、消毒的作用,故D正确。
答案:AD
12.解析:羧基和羟基能发生酯化反应,①正确;醛基和羟基能发生氧化反应,②正确;不能发生水解反应,③错误;不能发生加聚反应,④错误;羧基和羟基都能发生酯化反应,也属于取代反应,⑤正确;故选C。
答案:C
13.解析:根据题目信息,推知B是乙醇、A是乙烯、C是乙醛、D是乙酸、E是乙酸乙酯。由C8H18得到乙烯是石油的裂解,A正确;1 mol CH3CH2OH或1 mol CH3COOH与足量Na反应可生成0.5 mol H2,B正确;乙酸与碳酸钠溶液反应可生成二氧化碳,有气体生成,乙醇与碳酸钠溶液互溶,混合后不分层,而乙酸乙酯与碳酸钠溶液不互溶,混合后分层,现象各不相同,可以鉴别,故C正确;反应④是乙醛被氧化为乙酸,氧化剂可以是氧气,也可以是银氨溶液,D错误。
答案:D
14.解析:CH4+2O2CO2+2H2O,C2H4+3O22CO2+2H2O,2C2H6+7O24CO2+6H2O,恢复到原来的温度和压强,水为气体,由化学方程式可知甲烷、乙烯燃烧前后气体体积不变,乙烷燃烧后气体体积增大,设乙烷的体积为V mL,则:
2C2H6+7O24CO2+6H2O ΔV(体积增大)
2 4+6-2-7=1
V mL 20 mL
2∶1=V mL∶20 mL 解得V=40
所以原混合烃中乙烷的体积分数=×100%=50%,选C。
答案:C
15.解析:球形干燥管可以防止倒吸,同时起冷凝作用,故A正确;乙酸乙酯不溶于饱和碳酸钠溶液,密度比水小,所以液体分层,上层是无色油状液体,乙酸和饱和碳酸钠溶液反应而使下层溶液红色变浅,故B错误;乙醇能与无水氯化钙生成难溶于水的CaCl2·6C2H5OH,可先加入无水氯化钙,过滤分离出乙醇,故C正确;收集的117.9 ℃左右的馏分主要是乙酸,不是较纯净的乙酸乙酯,乙酸乙酯的沸点为77.1 ℃,应该收集77.1 ℃左右的馏分,故D错误。
答案:AC
16.解析:(1)①空间填充模型可以表示原子的相对大小及空间结构,甲烷的空间填充模型更接近分子的真实结构,则Ⅳ最符合。②甲烷为正四面体结构,任意2个H均相邻,CH2Cl2只代表一种物质可证明甲烷分子为正四面体结构。(2)烃中碳原子与氢原子以共价键结合,且C与H之间只能形成1个共价键。(3)烷烃的通式为CnH2n+2,等物质的量时n越大消耗氧气越多。乙烷的电子式为;分子式为CmH20的烷烃中,2m+2=20,则m为9;分子式为C8Hx的烷烃中,x为2×8+2=18;与CO2密度(同温同压且均为气体时)相同的烷烃CnH2n+2满足12n+2n+2=44,解得n=3,分子式为C3H8。若题述四种烃各为1 mol,在足量O2中燃烧,消耗O2最多的是C9H20。(4)等质量时烃中氢元素的质量分数越大,完全燃烧消耗的氧气越多,质量均为1 g的CH4、C2H6、C3H8、C4H10在足量O2中燃烧,消耗O2最多的是CH4。
答案:(1)①d ②b (2)b (3) 9 18 C3H8 C9H20 (4)CH4
17.解析:A是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工发展水平,所以A是CH2===CH2,乙烯和水发生加成反应生成的B为CH3CH2OH,乙醇发生催化氧化反应生成的C为CH3CHO,乙醛发生催化氧化反应生成的D为CH3COOH,乙酸与乙醇发生酯化反应生成乙酸乙酯。(1)由以上分析可知,A为乙烯,C为乙醛。(2)B为CH3CH2OH,含有的官能团为—OH,D为CH3COOH,含有的官能团为—COOH。(3)反应①属于加成反应,反应④属于酯化反应或取代反应。(4)反应①的化学方程式为CH2===CH2+H2OCH3CH2OH;反应②的化学方程式为2CH3CH2OH+O22CH3CHO+2H2O;反应③的化学方程式为2CH3CHO+O22CH3COOH。
答案:(1)乙烯 乙醛
(2)—OH(或羟基) —COOH(或羧基)
(3)加成反应 取代(酯化)反应
(4)CH2===CH2+H2OCH3CH2OH 2CH3CH2OH+O22CH3CHO+2H2O 2CH3CHO+O22CH3COOH
18.解析:(1)冷凝管的作用是冷凝、回流和导气,从a口进水,使水充满冷凝管,冷凝效果好。(2)实验开始时,关闭K2、打开K1和分液漏斗活塞,滴加苯和液溴的混合物,此时三颈烧瓶中发生的反应为2Fe+3Br2===2FeBr3、
(3)Ⅲ中小试管内苯的作用是除去溴化氢中的溴蒸气,避免干扰溴离子检验。(4)从冷凝管出来的气体主要为溴化氢,溴化氢不溶于苯,溴化氢能与硝酸银溶液反应生成浅黄色的溴化银沉淀。(5)生成的溴苯因含有溴而呈橙黄色,常用氢氧化钠溶液将溴苯中的溴除去,其方法是将含有溴的溴苯倒入氢氧化钠溶液中充分混合,静置、分层后,用分液漏斗分离出下层液体,即得到溴苯。(6)Ⅳ中球形干燥管的作用是防止倒吸。
答案:(1)冷凝、回流和导气 a
(2)2Fe+3Br2===2FeBr3、
(3)吸收溴蒸气
(4)Ⅲ中硝酸银溶液内有浅黄色沉淀生成
(5)将含有溴的溴苯倒入氢氧化钠溶液中充分混合,静置、分层后,用分液漏斗分离出下层液体,即得到溴苯
(6)防止倒吸
19.解析:(1)C中热水能使沸点较低的乙醇转化为乙醇蒸气,从而进入M装置中发生反应;在装入实验药品之前,应进行的操作是检查装置的气密性。(2)M处铜丝由红变黑,是因为铜在加热条件下与氧气发生反应,其反应的化学方程式为2Cu+O22CuO;铜丝由黑变红,是因为乙醇与氧化铜在加热条件下发生了反应,其反应的化学方程式为CH3CH2OH+CuOCH3CHO+Cu+H2O,由上述实验过程和现象可知,首先铜转化为氧化铜,然后氧化铜又转化为铜,则催化剂参加了化学反应。(3)因为乙醇和乙醛的沸点都比较低,易挥发,且能溶于水,则反应进行一段时间后,烧杯F中能收集到的有机物主要是乙醛和乙醇。(4)用蓝色石蕊试纸检验,试纸显红色,说明液体显酸性,则可知烧杯F中收集到的液体中含有乙酸,氯化钠溶液、苯、四氯化碳均与乙酸不发生反应,乙酸能与碳酸氢钠溶液发生反应转化为乙酸钠,因此可先在混合液中加入碳酸氢钠溶液,再用蒸馏的方法将乙酸除去。
答案:(1)使D中无水乙醇变为蒸气进入M中 检查装置的气密性
(2)2Cu+O22CuO CH3CH2OH+CuOCH3CHO+Cu+H2O 参加
(3)乙醛(或CH3CHO) 乙醇(或CH3CH2OH)
(4)乙酸(或CH3COOH) C 蒸馏
20.解析:Ⅰ.某气态烃X在标准状况下的密度为1.16 g·L-1,X的摩尔质量是1.16 g·L-1×22.4 L·mol-1≈26 g·mol-1,则X的分子式是C2H2,X是乙炔;A能发生银镜反应,由X与H2O反应生成,A是乙醛;乙醛催化氧化为乙酸,B是乙酸;乙酸和D反应生成具有水果香味的E,E是酯,则D是醇,由X是乙炔及X→C,C→D的反应条件可知,D分子中有2个碳原子,D是乙醇;E是乙酸乙酯;C和水反应生成乙醇,C是乙烯。
(1)C是乙烯,含有的官能团名称是碳碳双键。
(2)A是乙醛,化合物M是A的同系物,比A少一个碳原子,则M是甲醛,M的结构式为。
(3)有机化合物D是乙醇,乙醇在加热条件下和黑色的氧化铜反应生成乙醛、铜和水,所以黑色氧化铜变红,故A正确;有机化合物C是乙烯,乙烯分子中的所有原子在同一平面上,故B正确;反应③为乙炔和氢气反应生成乙烯,反应类型为还原反应(加成反应),反应④是乙烯和水反应生成乙醇,反应类型是加成反应,故C错误;有机化合物B是乙酸,乙酸和氢氧化钠溶液发生中和反应生成乙酸钠和水,E是乙酸乙酯,乙酸乙酯和氢氧化钠溶液发生水解反应生成乙酸钠和乙醇,D是乙醇,乙醇和NaOH不反应,故D错误。
Ⅱ.(1)由于生成的乙酸乙酯中混有的乙酸和乙醇蒸气易溶于水,为了防止倒吸,实验开始时,试管A中的导管不伸入液面下;由于乙酸乙酯难溶于水,因此当观察到试管A中的导管中不再有油状液体滴下时,认为反应基本完成。
(2)乙酸乙酯中含有水、乙酸和乙醇,加入饱和碳酸钠溶液后分液得到A和B,根据流程图丙可知A主要是乙酸乙酯,由于其中还含有少量水,则加入无水碳酸钠粉末可以吸收剩余的水分;B中含有乙酸钠、碳酸钠和乙醇,蒸馏得到乙醇(E),C中含有乙酸钠和碳酸钠,加入稀硫酸得到乙酸和硫酸钠,然后再蒸馏得到乙酸。根据以上分析可知试剂b是稀硫酸;分离方法①是分液;分离方法③是蒸馏。
(3)在得到的A中加入无水碳酸钠粉末,振荡,目的是除去乙酸乙酯中的水分。
答案:Ⅰ.(1)碳碳双键
(2)
(3)AB
Ⅱ.(1)乙酸乙酯中混有的乙酸和乙醇蒸气易溶于水,防倒吸 导管中不再有油状液体滴下
(2)稀硫酸 分液 蒸馏
(3)除去乙酸乙酯中的水分
(满分:100分 时间:90分钟)
一、选择题(本题共10小题,每小题2分,共20分,每小题只有一个选项符合题意)
1.生物燃料是以玉米、大豆等为原料生产的燃料,例如乙醇和生物柴油。下列有关说法不正确的是( )
A.生物燃料是可再生能源
B.生物燃料的组成元素与汽油等矿物燃料完全相同
C.发展生物燃料有利于保护生态环境
D.发展生物燃料有利于调整产业结构,提高农民收入
2.下列有关化学用语的说法不正确的是( )
A.中子数为7的碳原子:C
B.氯乙烯的结构简式:CH2===CHCl
C.羟基的电子式:∶H
D.乙酸分子的空间填充模型:
3.下列能用分液漏斗分离的是( )
A.植物油和乙醇 B.乙酸乙酯和水
C.乙酸和乙醇 D.汽油和煤油
4.海葵毒素是从海葵中分离出的一种剧毒物质,分子式为C129H223N3O54。哈佛大学的某研究小组经过8年努力,于1989年完成了海葵毒素的全合成。下列说法正确的是( )
A.海葵毒素是一种高分子化合物
B.海葵毒素是一种无机化合物
C.海葵毒素的成功合成预示着有机合成必将步入新的辉煌
D.海葵毒素的成功合成说明人类是无所不能的,能够合成任何有机物
5.a、b、c、d 4种化合物如下图所示,下列说法正确的是( )
A.a的一氯代物有三种
B.b能使酸性高锰酸钾溶液和溴水褪色,且二者褪色原理相同
C.c分子中的所有原子不可能处于同一平面内
D.a与d互为同分异构体
6.一种生产聚苯乙烯的流程如下:
下列叙述不正确的是( )
A.苯乙烯的分子式为C8H8
B.1 mol苯乙烯最多可与4 mol H2发生加成反应
C.鉴别乙苯与苯乙烯可用Br2的四氯化碳溶液
D.乙烯、苯和乙苯的分子中所有原子均可处于同一平面
7.某有机物X对氢气的相对密度为30,X中含碳40%(质量分数,下同),含氢6.7%,其余为氧,X可与碳酸氢钠溶液反应。下列关于X的说法不正确的是( )
A.X的相对分子质量为60
B.X的分子式为C2H4O2
C.X的结构简式为CH3COOH
D.X有3种同分异构体
8.苹果酸的结构简式为,下列说法不正确的是( )
A.苹果酸中能发生酯化反应的官能团有2种
B.1 mol苹果酸可与2 mol NaOH发生中和反应
C.1 mol苹果酸与足量金属Na反应生成3 mol H2
D.HCOO—CH2—CH(OH)—OOCH与苹果酸互为同分异构体
9.合成导电高分子材料PPV的反应如下:
下列说法正确的是( )
A.该反应为缩聚反应
B.PPV是聚苯乙炔
C.PPV与聚苯乙烯的最小结构单元组成相同
D.1 mol 最多可与2 mol H2发生反应
10.某有机物的结构简式为CHOHCH2COOH,在下列各反应的类型中:
①取代 ②加成 ③加聚 ④水解 ⑤酯化 ⑥中和 ⑦氧化 ⑧置换
它能发生的反应有( )
A.①②③⑤⑥⑦ B.②③④⑥⑧
C.①②⑤⑥⑦⑧ D.③④⑤⑥⑦⑧
二、选择题(本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题意,全部选对得4分,选对但不全的得2分,有选错的得0分)
11.下列说法中正确的是( )
A.可用溴水检验甲烷中混有的乙烯
B.聚乙烯(PE)和聚氯乙烯(PVC)都是食品级塑料制品的主要成分
C.分馏、干馏都是物理变化,裂化、裂解都是化学变化
D.常用75%(体积分数)的酒精溶液杀菌、消毒
12.某有机物的结构简式为,它在一定条件下可发生的反应为( )
①酯化反应 ②氧化反应 ③水解反应 ④加聚反应 ⑤取代反应
A.②③④ B.①②③
C.①②⑤ D.③④⑤
13.从石油中分离得到的烃C8H18可以实现如图所示的转化(B、D是生活中常见的两种有机物),下列说法不正确的是( )
A.反应①是裂解反应
B.1 mol B或1 mol D可以与足量Na反应生成0.5 mol H2
C.B、D、E三种物质可以用饱和Na2CO3溶液鉴别
D.反应④的氧化剂只能是氧气
14.105 ℃、101 kPa时,甲烷、乙烷和乙烯组成的混合烃80 mL与过量O2混合并完全燃烧,恢复到原来的温度和压强,混合气体总体积增加了20 mL。原混合烃中乙烷的体积分数为( )
A.12.5% B.25%
C.50% D.75%
15.某课外活动小组设计如图所示装置制取乙酸乙酯。
已知:
①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH。
②有关有机物的沸点:
试剂 乙醚 乙醇 乙酸 乙酸乙酯
沸点(℃) 34.7 78.5 117.9 77.1
下列说法正确的是( )
A.装置中球形干燥管既能冷凝蒸气又能防止倒吸
B.反应结束后大试管中的现象是液体分层,下层为无色油状液体,上层溶液颜色变浅
C.从大试管中分离出的乙酸乙酯中还含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,过滤分离出乙醇
D.最后加入无水硫酸钠,进行蒸馏,收集117.9 ℃左右的馏分,以得到较纯净的乙酸乙酯
三、非选择题(本题共5小题,共60分)
16.(12分)(1)下列各图均能表示甲烷的分子结构,按要求回答下列问题:
①以上哪一种结构更能反映其真实存在状况 (填字母,下同)。
a.Ⅰ b.Ⅱ
c.Ⅲ d.Ⅳ
②下列事实能证明甲烷分子是正四面体结构的是 。
a.CH3Cl只代表一种物质
b.CH2Cl2只代表一种物质
c.CHCl3只代表一种物质
d.CCl4只代表一种物质
(2)烃分子中的碳原子与氢原子结合的方式是 。
a.形成4对共用电子 b.通过1个共价键
c.通过2个共价键 d.通过离子键和共价键
(3)乙烷的电子式为 ,分子式为CmH20的烷烃中m为 ,分子式为C8Hx的烷烃中x为 ,与CO2密度(同温同压且均为气体时)相同的烷烃的分子式为 ,若上述四种烃各为1 mol,在足量O2中燃烧,消耗O2最多的是 。
(4)若CH4、C2H6、C3H8、C4H10四种烃的质量均为1 g,在足量O2中燃烧,消耗O2最多的是 。
17.(12分)已知:A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工发展水平。现以A为主要原料合成乙酸乙酯,其合成路线如图(反应条件略):
回答下列问题:
(1)分别写出A、C的名称: 、 。
(2)B、D分子中的官能团分别是 、 。
(3)写出下列反应的反应类型:① ,④ 。
(4)写出下列反应的化学方程式:
①________________________________________________________________________;
②________________________________________________________________________;
③________________________________________________________________________。
18.(12分)某校学生用如图所示装置进行实验(夹持装置略),以探究苯与液溴发生反应的原理并分离、提纯反应的产物。
请回答下列问题:
(1)冷凝管所起的作用为 ,冷凝水从 (填“a”或“b”)口进入。
(2)实验开始时,关闭K2、打开K1和分液漏斗活塞,滴加苯和液溴的混合物,三颈烧瓶中发生反应的化学方程式为
________________________________________________________________________
________________________________________________________________________。
(3)Ⅲ中小试管内苯的作用是
________________________________________________________________________。
(4)能说明苯与液溴发生了取代反应的现象是
________________________________________________________________________
________________________________________________________________________。
(5)生成的溴苯因溶有未反应的溴而显橙黄色,提纯的方法是
________________________________________________________________________
________________________________________________________________________。
(6)Ⅳ中球形干燥管的作用是 。
19.(12分)某化学兴趣小组设计“乙醇催化氧化实验”来探究催化剂的催化机理并对反应后的产物进行分析,装置(夹持装置已省略)如图所示:
试回答以下问题:
(1)C中热水的作用是 ;在装入实验药品之前,应进行的操作是 。
(2)装入实验药品后,关闭a、b、c,在铜丝的中间部分加热片刻,M处铜丝由红变黑,反应的化学方程式为 ,然后打开a、b、c,通过控制a和b,间歇性地通入气体,即可在M处观察到受热部分的铜丝交替出现变红、变黑的现象。铜丝由黑变红时,发生反应的化学方程式为 。通过实验,可以得出结论:该实验过程中催化剂 (填“参加”或“不参加”)化学反应。
(3)反应进行一段时间后,烧杯F中能收集到的有机物主要有 、 。
(4)若烧杯F中收集到的液体用蓝色石蕊试纸检验,试纸显红色,说明液体中含有 。要除去该物质,可先在混合液中加入 (填字母),然后通过 (填操作名称)即可。
A.氯化钠溶液 B.苯
C.碳酸氢钠溶液 D.四氯化碳
20.(12分)Ⅰ .已知某气态烃X在标准状况下的密度为1.16 g·L-1,A能发生银镜反应,E具有水果香味,有关物质的转化关系如图甲所示。
请回答:
(1)C中含有的官能团名称是 。
(2)化合物M是A的同系物,比A少一个碳原子,请写出M的结构式: 。
(3)下列说法正确的是 (填序号)。
A.有机化合物D在加热条件下可以使黑色的氧化铜变红
B.有机化合物C分子中的所有原子在同一平面上
C.反应③为还原反应,反应④为氧化反应
D.有机化合物B、D、E均能与NaOH溶液反应
Ⅱ .某同学用如图乙所示的实验装置制取少量乙酸乙酯,实验结束后,试管A中上层为透明的、难溶于水的油状液体。
(1)实验开始时,试管A中的导管不伸入液面下的原因是 ;当观察到试管A中 时,认为反应基本完成。
(2)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,如图丙是分离操作步骤流程图。
试剂b是 ;分离方法①是 ;分离方法③是 。
(3)在得到的A中加入无水碳酸钠粉末,振荡,目的是 。
综合素养训练三
1.解析:由题给信息知生物燃料为可再生能源,故A正确;生物燃料的组成元素主要为碳、氢、氧,汽油等矿物燃料的组成元素主要是碳、氢,组成元素不完全相同,故B不正确;发展生物燃料,可减少化石燃料的使用,有利于保护生态环境,故C正确;发展生物柴油有利于调整产业结构,提高农民收入,故D正确。
答案:B
2.解析:中子数为7的碳原子的质量数为13,故A错误;氯乙烯的结构简式为CH2===CHCl,故B正确;羟基的电子式为∶H,故C正确;题图为乙酸分子的空间填充模型,故D正确。
答案:A
3.解析:A项,植物油和乙醇互溶,不能使用分液漏斗分离;B项,乙酸乙酯难溶于水,密度比水小,二者互不相溶,因此可以使用分液漏斗分离;C项,乙酸与乙醇互溶,不能使用分液漏斗分离;D项,汽油和煤油互溶,两者沸点范围不同,应用蒸馏的方法分离,不能使用分液漏斗分离;故选B。
答案:B
4.解析:海葵毒素不是高分子化合物,故A错误;该物质中含有C、H、N、O元素,属于有机物,不属于无机物,故B错误;海葵毒素的成功合成预示着有机合成必将步入新的辉煌,故C正确;海葵毒素的成功合成不能说明人类能合成任何有机物,有些有机物目前还不能人工合成,故D错误。
答案:C
5.解析:a是正方体结构,8个顶点的氢原子位置相同,所以a的一氯代物有一种,A错误;b中含碳碳双键,b使酸性高锰酸钾溶液褪色的原因是发生氧化反应,b与溴水中的溴发生加成反应而使溴水褪色,二者褪色原理不同,故B错误;c中含有碳碳双键,c分子中的所有原子可能处于同一平面内,故C错误;a与d的分子式都是C8H8,结构不同,二者互为同分异构体,故D正确。
答案:D
6.解析:每个苯乙烯分子中含8个C、8个H,可知其分子式为C8H8,故A正确;苯乙烯中苯环、碳碳双键均能与氢气发生加成反应,则1 mol苯乙烯最多可与4 mol H2发生加成反应,故B正确;苯乙烯含碳碳双键,而乙苯不含,苯乙烯能使Br2的四氯化碳溶液褪色,而乙苯不能,可鉴别,故C正确;乙烯分子、苯分子为平面结构,乙苯分子中的所有原子不可能共面,故D错误。
答案:D
7.解析:有机物X对氢气的相对密度为30,则该有机物的相对分子质量为60,故A正确;X中含碳40%,含氢6.7%,其余为氧,所以每个X分子中C的个数为=2,H的个数为≈4,O的个数为=2,X的分子式为C2H4O2,故B正确;X的分子式为C2H4O2,且X可以和NaHCO3溶液反应,则X中含有—COOH,X的结构简式为CH3COOH,故C正确;X的同分异构体有HOCH2CHO、HCOOCH3,共2种,故D不正确。
答案:D
8.答案:C
9.解析:合成导电高分子材料PPV的反应中,有小分子物质HI生成,属于缩聚反应;PPV含有I,而聚苯乙炔为烃类物质,则PPV不是聚苯乙炔;聚苯乙烯的重复结构单元为,不含碳碳双键,而该高聚物的结构单元中含有碳碳双键,所以最小结构单元组成不相同;中苯环和碳碳双键都可与氢气反应,则1 mol 最多可与5 mol H2发生反应。
答案:A
10.解析:中含有羟基,能够发生酯化反应和取代反应,能够与钠发生置换反应,能够被强氧化剂氧化;含有苯环,能够发生加成反应和取代反应;含有羧基,能够发生中和反应和酯化反应;不能发生加聚反应和水解反应。
答案:C
11.解析:乙烯分子中含有碳碳双键,可与溴发生加成反应而使溴水褪色,而甲烷不能使溴水褪色,故A正确;聚氯乙烯中含有氯元素,加热可产生有害物质,不是食品级塑料制品的主要成分,故B错误;干馏为化学变化,故C错误;75%(体积分数)的酒精溶液可使蛋白质变性,起到杀菌、消毒的作用,故D正确。
答案:AD
12.解析:羧基和羟基能发生酯化反应,①正确;醛基和羟基能发生氧化反应,②正确;不能发生水解反应,③错误;不能发生加聚反应,④错误;羧基和羟基都能发生酯化反应,也属于取代反应,⑤正确;故选C。
答案:C
13.解析:根据题目信息,推知B是乙醇、A是乙烯、C是乙醛、D是乙酸、E是乙酸乙酯。由C8H18得到乙烯是石油的裂解,A正确;1 mol CH3CH2OH或1 mol CH3COOH与足量Na反应可生成0.5 mol H2,B正确;乙酸与碳酸钠溶液反应可生成二氧化碳,有气体生成,乙醇与碳酸钠溶液互溶,混合后不分层,而乙酸乙酯与碳酸钠溶液不互溶,混合后分层,现象各不相同,可以鉴别,故C正确;反应④是乙醛被氧化为乙酸,氧化剂可以是氧气,也可以是银氨溶液,D错误。
答案:D
14.解析:CH4+2O2CO2+2H2O,C2H4+3O22CO2+2H2O,2C2H6+7O24CO2+6H2O,恢复到原来的温度和压强,水为气体,由化学方程式可知甲烷、乙烯燃烧前后气体体积不变,乙烷燃烧后气体体积增大,设乙烷的体积为V mL,则:
2C2H6+7O24CO2+6H2O ΔV(体积增大)
2 4+6-2-7=1
V mL 20 mL
2∶1=V mL∶20 mL 解得V=40
所以原混合烃中乙烷的体积分数=×100%=50%,选C。
答案:C
15.解析:球形干燥管可以防止倒吸,同时起冷凝作用,故A正确;乙酸乙酯不溶于饱和碳酸钠溶液,密度比水小,所以液体分层,上层是无色油状液体,乙酸和饱和碳酸钠溶液反应而使下层溶液红色变浅,故B错误;乙醇能与无水氯化钙生成难溶于水的CaCl2·6C2H5OH,可先加入无水氯化钙,过滤分离出乙醇,故C正确;收集的117.9 ℃左右的馏分主要是乙酸,不是较纯净的乙酸乙酯,乙酸乙酯的沸点为77.1 ℃,应该收集77.1 ℃左右的馏分,故D错误。
答案:AC
16.解析:(1)①空间填充模型可以表示原子的相对大小及空间结构,甲烷的空间填充模型更接近分子的真实结构,则Ⅳ最符合。②甲烷为正四面体结构,任意2个H均相邻,CH2Cl2只代表一种物质可证明甲烷分子为正四面体结构。(2)烃中碳原子与氢原子以共价键结合,且C与H之间只能形成1个共价键。(3)烷烃的通式为CnH2n+2,等物质的量时n越大消耗氧气越多。乙烷的电子式为;分子式为CmH20的烷烃中,2m+2=20,则m为9;分子式为C8Hx的烷烃中,x为2×8+2=18;与CO2密度(同温同压且均为气体时)相同的烷烃CnH2n+2满足12n+2n+2=44,解得n=3,分子式为C3H8。若题述四种烃各为1 mol,在足量O2中燃烧,消耗O2最多的是C9H20。(4)等质量时烃中氢元素的质量分数越大,完全燃烧消耗的氧气越多,质量均为1 g的CH4、C2H6、C3H8、C4H10在足量O2中燃烧,消耗O2最多的是CH4。
答案:(1)①d ②b (2)b (3) 9 18 C3H8 C9H20 (4)CH4
17.解析:A是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工发展水平,所以A是CH2===CH2,乙烯和水发生加成反应生成的B为CH3CH2OH,乙醇发生催化氧化反应生成的C为CH3CHO,乙醛发生催化氧化反应生成的D为CH3COOH,乙酸与乙醇发生酯化反应生成乙酸乙酯。(1)由以上分析可知,A为乙烯,C为乙醛。(2)B为CH3CH2OH,含有的官能团为—OH,D为CH3COOH,含有的官能团为—COOH。(3)反应①属于加成反应,反应④属于酯化反应或取代反应。(4)反应①的化学方程式为CH2===CH2+H2OCH3CH2OH;反应②的化学方程式为2CH3CH2OH+O22CH3CHO+2H2O;反应③的化学方程式为2CH3CHO+O22CH3COOH。
答案:(1)乙烯 乙醛
(2)—OH(或羟基) —COOH(或羧基)
(3)加成反应 取代(酯化)反应
(4)CH2===CH2+H2OCH3CH2OH 2CH3CH2OH+O22CH3CHO+2H2O 2CH3CHO+O22CH3COOH
18.解析:(1)冷凝管的作用是冷凝、回流和导气,从a口进水,使水充满冷凝管,冷凝效果好。(2)实验开始时,关闭K2、打开K1和分液漏斗活塞,滴加苯和液溴的混合物,此时三颈烧瓶中发生的反应为2Fe+3Br2===2FeBr3、
(3)Ⅲ中小试管内苯的作用是除去溴化氢中的溴蒸气,避免干扰溴离子检验。(4)从冷凝管出来的气体主要为溴化氢,溴化氢不溶于苯,溴化氢能与硝酸银溶液反应生成浅黄色的溴化银沉淀。(5)生成的溴苯因含有溴而呈橙黄色,常用氢氧化钠溶液将溴苯中的溴除去,其方法是将含有溴的溴苯倒入氢氧化钠溶液中充分混合,静置、分层后,用分液漏斗分离出下层液体,即得到溴苯。(6)Ⅳ中球形干燥管的作用是防止倒吸。
答案:(1)冷凝、回流和导气 a
(2)2Fe+3Br2===2FeBr3、
(3)吸收溴蒸气
(4)Ⅲ中硝酸银溶液内有浅黄色沉淀生成
(5)将含有溴的溴苯倒入氢氧化钠溶液中充分混合,静置、分层后,用分液漏斗分离出下层液体,即得到溴苯
(6)防止倒吸
19.解析:(1)C中热水能使沸点较低的乙醇转化为乙醇蒸气,从而进入M装置中发生反应;在装入实验药品之前,应进行的操作是检查装置的气密性。(2)M处铜丝由红变黑,是因为铜在加热条件下与氧气发生反应,其反应的化学方程式为2Cu+O22CuO;铜丝由黑变红,是因为乙醇与氧化铜在加热条件下发生了反应,其反应的化学方程式为CH3CH2OH+CuOCH3CHO+Cu+H2O,由上述实验过程和现象可知,首先铜转化为氧化铜,然后氧化铜又转化为铜,则催化剂参加了化学反应。(3)因为乙醇和乙醛的沸点都比较低,易挥发,且能溶于水,则反应进行一段时间后,烧杯F中能收集到的有机物主要是乙醛和乙醇。(4)用蓝色石蕊试纸检验,试纸显红色,说明液体显酸性,则可知烧杯F中收集到的液体中含有乙酸,氯化钠溶液、苯、四氯化碳均与乙酸不发生反应,乙酸能与碳酸氢钠溶液发生反应转化为乙酸钠,因此可先在混合液中加入碳酸氢钠溶液,再用蒸馏的方法将乙酸除去。
答案:(1)使D中无水乙醇变为蒸气进入M中 检查装置的气密性
(2)2Cu+O22CuO CH3CH2OH+CuOCH3CHO+Cu+H2O 参加
(3)乙醛(或CH3CHO) 乙醇(或CH3CH2OH)
(4)乙酸(或CH3COOH) C 蒸馏
20.解析:Ⅰ.某气态烃X在标准状况下的密度为1.16 g·L-1,X的摩尔质量是1.16 g·L-1×22.4 L·mol-1≈26 g·mol-1,则X的分子式是C2H2,X是乙炔;A能发生银镜反应,由X与H2O反应生成,A是乙醛;乙醛催化氧化为乙酸,B是乙酸;乙酸和D反应生成具有水果香味的E,E是酯,则D是醇,由X是乙炔及X→C,C→D的反应条件可知,D分子中有2个碳原子,D是乙醇;E是乙酸乙酯;C和水反应生成乙醇,C是乙烯。
(1)C是乙烯,含有的官能团名称是碳碳双键。
(2)A是乙醛,化合物M是A的同系物,比A少一个碳原子,则M是甲醛,M的结构式为。
(3)有机化合物D是乙醇,乙醇在加热条件下和黑色的氧化铜反应生成乙醛、铜和水,所以黑色氧化铜变红,故A正确;有机化合物C是乙烯,乙烯分子中的所有原子在同一平面上,故B正确;反应③为乙炔和氢气反应生成乙烯,反应类型为还原反应(加成反应),反应④是乙烯和水反应生成乙醇,反应类型是加成反应,故C错误;有机化合物B是乙酸,乙酸和氢氧化钠溶液发生中和反应生成乙酸钠和水,E是乙酸乙酯,乙酸乙酯和氢氧化钠溶液发生水解反应生成乙酸钠和乙醇,D是乙醇,乙醇和NaOH不反应,故D错误。
Ⅱ.(1)由于生成的乙酸乙酯中混有的乙酸和乙醇蒸气易溶于水,为了防止倒吸,实验开始时,试管A中的导管不伸入液面下;由于乙酸乙酯难溶于水,因此当观察到试管A中的导管中不再有油状液体滴下时,认为反应基本完成。
(2)乙酸乙酯中含有水、乙酸和乙醇,加入饱和碳酸钠溶液后分液得到A和B,根据流程图丙可知A主要是乙酸乙酯,由于其中还含有少量水,则加入无水碳酸钠粉末可以吸收剩余的水分;B中含有乙酸钠、碳酸钠和乙醇,蒸馏得到乙醇(E),C中含有乙酸钠和碳酸钠,加入稀硫酸得到乙酸和硫酸钠,然后再蒸馏得到乙酸。根据以上分析可知试剂b是稀硫酸;分离方法①是分液;分离方法③是蒸馏。
(3)在得到的A中加入无水碳酸钠粉末,振荡,目的是除去乙酸乙酯中的水分。
答案:Ⅰ.(1)碳碳双键
(2)
(3)AB
Ⅱ.(1)乙酸乙酯中混有的乙酸和乙醇蒸气易溶于水,防倒吸 导管中不再有油状液体滴下
(2)稀硫酸 分液 蒸馏
(3)除去乙酸乙酯中的水分
