2023-2024学年高中化学必修第二册第五章化工生产中的重要非金属元素检测卷(含答案)
文档属性
| 名称 | 2023-2024学年高中化学必修第二册第五章化工生产中的重要非金属元素检测卷(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 608.0KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-17 00:00:00 | ||
图片预览


文档简介
中小学教育资源及组卷应用平台
2023-2024学年高中化学必修第二册第五章化工生产中的重要非金属元素检测卷
一、选择题
1.某溶液中含有大量的下列离子:Mg2+、NO3-、K+和M离子,经测定Mg2+、NO3-、K+和M离子的物质的量之比为2∶4∶1∶1,则M离子可能是( )
A.Cl- B.SO42- C.OH- D.Na+
2.陈述I和II均正确且具有因果关系的是( )
选项 陈述I 陈述II
A 金属钠在点燃产生 可在潜水艇中作为的来源
B 碳酸钠受热分解产生 用碳酸钠作膨松剂制作面包
C 浓硫酸与不反应 可用钢瓶运输浓硫酸
D 的金属性比强 船身焊接锌块可减缓船体腐蚀
A.A B.B C.C D.D
3.能正确表示下列反应的离子方程式的是( )
A.铝溶解在NaOH溶液中:
B.的水解:
C.溶于硝酸反应:
D.向氢氧化镁固体中滴加硫酸铁溶液:
4.下列各组离子中能在水溶液中大量共存的是( )
A.、、、 B.、、、
C.、、、 D.、、、
5.硫及其化合物的转化具有重要应用。下列说法正确的是( )
A.硫元素在自然界中均以化合态形式存在
B.空气中排放过量SO2会形成酸雨,且酸雨的pH会随时间增长而降低
C.常温下浓H2SO4能使铁片钝化是因为浓硫酸具有脱水性
D.质量分数为49%、密度为1.4g·cm-3的硫酸,其物质的量浓度为2.8 mol·L-1
6.反应中,氧化产物与还原产物的物质的量之比为( )
A.2:3 B.3:2 C.3:4 D.8:3
7.在指定条件下,下列选项所示的物质间转化能实现的是( )
A.S CuS B.稀H2SO4(aq) SO2(g)
C.浓H2SO4 SO2(g) D.SO2(g)(NH4)2SO3(aq)
8.已知硫酸和氯磺酸结构关系如图:。下列说法错误的是( )
A.氯磺酸是一元酸
B.氯磺酸中硫元素化合价为+6价
C.氯磺酸遇水会发生反应:
D.氯磺酸在HCl作用下可得
9.硫及其化合物的分类与相应硫元素的化合价关系如图所示。下列说法正确的是( )
A.葡萄酒中添加适量c可以起到杀菌和抗氧化的作用
B.工业制备f的最后一步是用水吸收d
C.将c通入紫色石蕊试液中,溶液先变红后褪色
D.可用f的浓溶液干燥a
二、非选择题
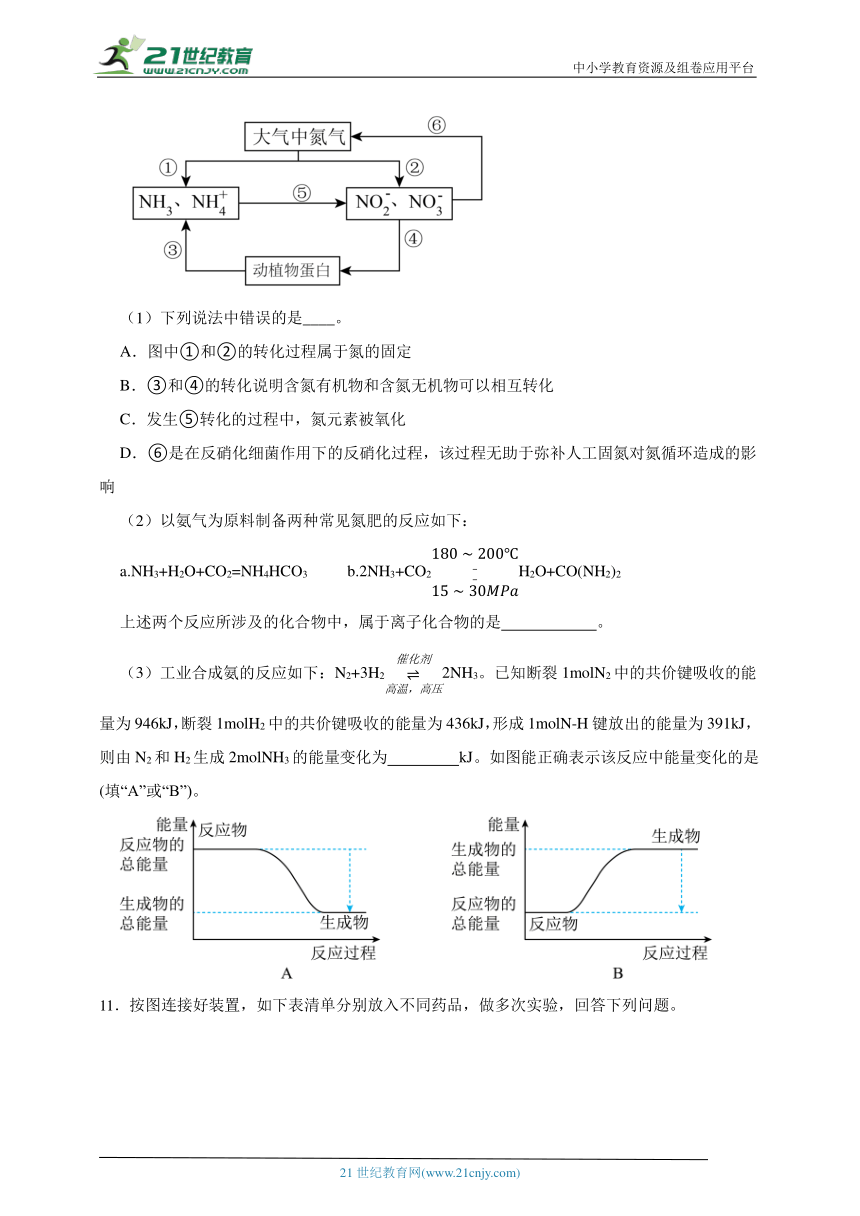
10.氮的循环对人类的生产和生活具有重要意义,如图所示的氮循环是生态系统物质循环的重要组成部分。
(1)下列说法中错误的是____。
A.图中①和②的转化过程属于氮的固定
B.③和④的转化说明含氮有机物和含氮无机物可以相互转化
C.发生⑤转化的过程中,氮元素被氧化
D.⑥是在反硝化细菌作用下的反硝化过程,该过程无助于弥补人工固氮对氮循环造成的影响
(2)以氨气为原料制备两种常见氮肥的反应如下:
a.NH3+H2O+CO2=NH4HCO3 b.2NH3+CO2H2O+CO(NH2)2
上述两个反应所涉及的化合物中,属于离子化合物的是 。
(3)工业合成氨的反应如下:N2+3H22NH3。已知断裂1molN2中的共价键吸收的能量为946kJ,断裂1molH2中的共价键吸收的能量为436kJ,形成1molN-H键放出的能量为391kJ,则由N2和H2生成2molNH3的能量变化为 kJ。如图能正确表示该反应中能量变化的是 (填“A”或“B”)。
11.按图连接好装置,如下表清单分别放入不同药品,做多次实验,回答下列问题。
A B C D E
实验1 70%的溶液 固体 的溶液 溶液 碱石灰
实验2 浓盐酸 浓 淀粉—KI溶液 碱石灰
实验3 ? ? 和混合溶液 碱石灰
实验4 浓氨水 的溶液 水 ——
(1)实验1中,试管内的现象为:溶液C褪色,溶液D中出现白色沉淀 (写化学式)。
(2)实验2中,试管内的现象为: 。
(3)实验3中,溶液D变为红色,则A和B分别为: 。
(4)实验4中,溶液C褪色,并出现白色沉淀,请写出在溶液C中发生的化学反应方程式: 。
(5)在实验1、2、4中,溶液C还有一个共同的作用: 。
12.某化学兴趣小组对含某些离子(如表)的工业废水进行研究,废水中各离子的物质的量浓度相等,均为。
阳离子 、、、
阴离子 、、、、
(1)该溶液为无色溶液,则一定不存在的离子是 。
(2)向废水中加入过量KOH溶液微热,有白色沉淀和无色气体产生,则沉淀是 (填化学式,下同),气体是 。
(3)若向废水中加入过量盐酸,会生成遇空气变为红棕色的无色气体和,写出生成该无色气体和的离子方程式: 。一定条件下红棕色气体与(2)中产生的气体能反应生成无污染的气体,该反应的化学方程式为 。
(4)向(3)中最后所得的溶液中加入过量的溶液,充分反应后观察到有白色沉淀产生。
①白色沉淀是 。
② (填“能”或“不能”)仅依据该现象判断废水中存在白色沉淀中的阴离子,理由是 。
(5)结合(1)(2)(3),该废水中一定存在的离子是 。
13.某无色溶液Y可能含有中的几种,且阳离子数目相同。为确定其组成,某同学进行了如下实验(假设气体均全部逸出,忽略的分解)
已知:①;②。
(1)溶液Y中肯定不存在的阴、阳离子分别是 、 (填离子符号);生成气体1的离子方程式 。
(2)溶液Y中的物质的量是 ;若溶液Y中存在Na+和Cl-,则数目 (填“大于”、“等于”、“小于”)。
(3)若使溶液Y中的完全沉淀,需至少向溶液Y中加入 g NaOH。
答案解析部分
1.【答案】A
2.【答案】D
3.【答案】D
4.【答案】D
5.【答案】B
6.【答案】B
7.【答案】D
8.【答案】C
9.【答案】A
10.【答案】(1)D
(2)NH4HCO3
(3)92;A
11.【答案】(1)
(2)没有明显现象,C中有气泡,D中气泡消失
(3)浓和/和/和/浓和等
(4)
(5)防止倒吸
12.【答案】(1)、
(2);
(3);
(4)AgCl;不能;因为(3)加入了盐酸,引入了氯离子,所以不能根据产生白色沉淀判断含有氯离子
(5)、、、、
13.【答案】(1);Fe3+;
(2)0.015mol;小于
(3)0.4
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2023-2024学年高中化学必修第二册第五章化工生产中的重要非金属元素检测卷
一、选择题
1.某溶液中含有大量的下列离子:Mg2+、NO3-、K+和M离子,经测定Mg2+、NO3-、K+和M离子的物质的量之比为2∶4∶1∶1,则M离子可能是( )
A.Cl- B.SO42- C.OH- D.Na+
2.陈述I和II均正确且具有因果关系的是( )
选项 陈述I 陈述II
A 金属钠在点燃产生 可在潜水艇中作为的来源
B 碳酸钠受热分解产生 用碳酸钠作膨松剂制作面包
C 浓硫酸与不反应 可用钢瓶运输浓硫酸
D 的金属性比强 船身焊接锌块可减缓船体腐蚀
A.A B.B C.C D.D
3.能正确表示下列反应的离子方程式的是( )
A.铝溶解在NaOH溶液中:
B.的水解:
C.溶于硝酸反应:
D.向氢氧化镁固体中滴加硫酸铁溶液:
4.下列各组离子中能在水溶液中大量共存的是( )
A.、、、 B.、、、
C.、、、 D.、、、
5.硫及其化合物的转化具有重要应用。下列说法正确的是( )
A.硫元素在自然界中均以化合态形式存在
B.空气中排放过量SO2会形成酸雨,且酸雨的pH会随时间增长而降低
C.常温下浓H2SO4能使铁片钝化是因为浓硫酸具有脱水性
D.质量分数为49%、密度为1.4g·cm-3的硫酸,其物质的量浓度为2.8 mol·L-1
6.反应中,氧化产物与还原产物的物质的量之比为( )
A.2:3 B.3:2 C.3:4 D.8:3
7.在指定条件下,下列选项所示的物质间转化能实现的是( )
A.S CuS B.稀H2SO4(aq) SO2(g)
C.浓H2SO4 SO2(g) D.SO2(g)(NH4)2SO3(aq)
8.已知硫酸和氯磺酸结构关系如图:。下列说法错误的是( )
A.氯磺酸是一元酸
B.氯磺酸中硫元素化合价为+6价
C.氯磺酸遇水会发生反应:
D.氯磺酸在HCl作用下可得
9.硫及其化合物的分类与相应硫元素的化合价关系如图所示。下列说法正确的是( )
A.葡萄酒中添加适量c可以起到杀菌和抗氧化的作用
B.工业制备f的最后一步是用水吸收d
C.将c通入紫色石蕊试液中,溶液先变红后褪色
D.可用f的浓溶液干燥a
二、非选择题
10.氮的循环对人类的生产和生活具有重要意义,如图所示的氮循环是生态系统物质循环的重要组成部分。
(1)下列说法中错误的是____。
A.图中①和②的转化过程属于氮的固定
B.③和④的转化说明含氮有机物和含氮无机物可以相互转化
C.发生⑤转化的过程中,氮元素被氧化
D.⑥是在反硝化细菌作用下的反硝化过程,该过程无助于弥补人工固氮对氮循环造成的影响
(2)以氨气为原料制备两种常见氮肥的反应如下:
a.NH3+H2O+CO2=NH4HCO3 b.2NH3+CO2H2O+CO(NH2)2
上述两个反应所涉及的化合物中,属于离子化合物的是 。
(3)工业合成氨的反应如下:N2+3H22NH3。已知断裂1molN2中的共价键吸收的能量为946kJ,断裂1molH2中的共价键吸收的能量为436kJ,形成1molN-H键放出的能量为391kJ,则由N2和H2生成2molNH3的能量变化为 kJ。如图能正确表示该反应中能量变化的是 (填“A”或“B”)。
11.按图连接好装置,如下表清单分别放入不同药品,做多次实验,回答下列问题。
A B C D E
实验1 70%的溶液 固体 的溶液 溶液 碱石灰
实验2 浓盐酸 浓 淀粉—KI溶液 碱石灰
实验3 ? ? 和混合溶液 碱石灰
实验4 浓氨水 的溶液 水 ——
(1)实验1中,试管内的现象为:溶液C褪色,溶液D中出现白色沉淀 (写化学式)。
(2)实验2中,试管内的现象为: 。
(3)实验3中,溶液D变为红色,则A和B分别为: 。
(4)实验4中,溶液C褪色,并出现白色沉淀,请写出在溶液C中发生的化学反应方程式: 。
(5)在实验1、2、4中,溶液C还有一个共同的作用: 。
12.某化学兴趣小组对含某些离子(如表)的工业废水进行研究,废水中各离子的物质的量浓度相等,均为。
阳离子 、、、
阴离子 、、、、
(1)该溶液为无色溶液,则一定不存在的离子是 。
(2)向废水中加入过量KOH溶液微热,有白色沉淀和无色气体产生,则沉淀是 (填化学式,下同),气体是 。
(3)若向废水中加入过量盐酸,会生成遇空气变为红棕色的无色气体和,写出生成该无色气体和的离子方程式: 。一定条件下红棕色气体与(2)中产生的气体能反应生成无污染的气体,该反应的化学方程式为 。
(4)向(3)中最后所得的溶液中加入过量的溶液,充分反应后观察到有白色沉淀产生。
①白色沉淀是 。
② (填“能”或“不能”)仅依据该现象判断废水中存在白色沉淀中的阴离子,理由是 。
(5)结合(1)(2)(3),该废水中一定存在的离子是 。
13.某无色溶液Y可能含有中的几种,且阳离子数目相同。为确定其组成,某同学进行了如下实验(假设气体均全部逸出,忽略的分解)
已知:①;②。
(1)溶液Y中肯定不存在的阴、阳离子分别是 、 (填离子符号);生成气体1的离子方程式 。
(2)溶液Y中的物质的量是 ;若溶液Y中存在Na+和Cl-,则数目 (填“大于”、“等于”、“小于”)。
(3)若使溶液Y中的完全沉淀,需至少向溶液Y中加入 g NaOH。
答案解析部分
1.【答案】A
2.【答案】D
3.【答案】D
4.【答案】D
5.【答案】B
6.【答案】B
7.【答案】D
8.【答案】C
9.【答案】A
10.【答案】(1)D
(2)NH4HCO3
(3)92;A
11.【答案】(1)
(2)没有明显现象,C中有气泡,D中气泡消失
(3)浓和/和/和/浓和等
(4)
(5)防止倒吸
12.【答案】(1)、
(2);
(3);
(4)AgCl;不能;因为(3)加入了盐酸,引入了氯离子,所以不能根据产生白色沉淀判断含有氯离子
(5)、、、、
13.【答案】(1);Fe3+;
(2)0.015mol;小于
(3)0.4
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
