浙江省宁波市北仑区2023-2024学年九年级上学期期末科学试题(含解析)
文档属性
| 名称 | 浙江省宁波市北仑区2023-2024学年九年级上学期期末科学试题(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 718.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 华东师大版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2024-03-16 00:00:00 | ||
图片预览


文档简介
2023-2024学年浙江省宁波市北仑区九年级(上)期末科学试卷
一、选择题(本题共20小题,每小题3分,共60分。请选出每小题中一个符合题意的选项,不选、错选均不给分)
1.(3分)习近平总书记在党的二十大报告中提出:积极稳妥推进碳达峰、碳中和践行绿色发展理念,保护城市之肺为共建天蓝、地绿、水清的美丽家园,下列措施不可取的是( )
A.生活垃圾分类回收,垃圾资源化
B.加大空气质量检测,改善环境状况
C.大力开展五水共治,保护水资源
D.大量使用化肥农药,提高粮食产量
2.(3分)《易经》记载:“泽中有火”“上火下泽”。这是对甲烷气体在湖泊池沼水面上起火现象的描述。下列有关甲烷的叙述,正确的是( )
A.从分类上看:属于无机物
B.从变化上看:燃烧只生成一种物质
C.从性质上看:具有助燃性
D.从使用上看:点燃前要检验气体的纯度
3.(3分)科学实验要规范操作,下列初中科学实验操作你认为不正确的是( )
A.二氧化碳的验满 B.倾倒液体
C.检验气密性 D.用纸槽取用粉末
4.(3分)“灰汁团”是浙江传统小吃,制作过程中要用到大米和“灰汁”。“灰汁”制取方法如资料卡所示。下列说法错误的是( )
资料卡 传统方法:稻草烧灰一加水溶解→静置沉淀→过滤取汁
现代方法:将食用碱(纯碱和小苏打的混合物)与水按一定比例混合成汁
A.大米中含有的淀粉属于有机物
B.稻草燃烧属于化学变化
C.传统方法制得的“灰汁”是混合物
D.现代方法制得的“灰汁”不能使酚酞试液变红色
5.(3分)节约用电,从我做起。下列用电器正常工作时,在相同时间内消耗电能最多的是( )
A.台灯 B.液晶电视
C.笔记本电脑 D.空调
6.(3分)继麒鳞芯片后,华为发布业界最高性能处理器鲲鹏920,摆脱了对国外产品的依赖。芯片主要以高纯度的单质硅(Si),在半导体硅元件生产中,常用氢氟酸(HF),反应原理为SiO2+6HF=H2SiF6+2X。下列说法错误的是( )
A.生成物X的化学式是H2O
B.H2SiF6中硅元素显+4价
C.该反应是复分解反应
D.地壳中硅元素含量仅次于氧元素
7.(3分)下列事例中,改变物体内能的途径与其他三项不同的是( )
A.柴火烧水 B.压缩空气发热
C.冬天搓手取暖 D.钻木取火
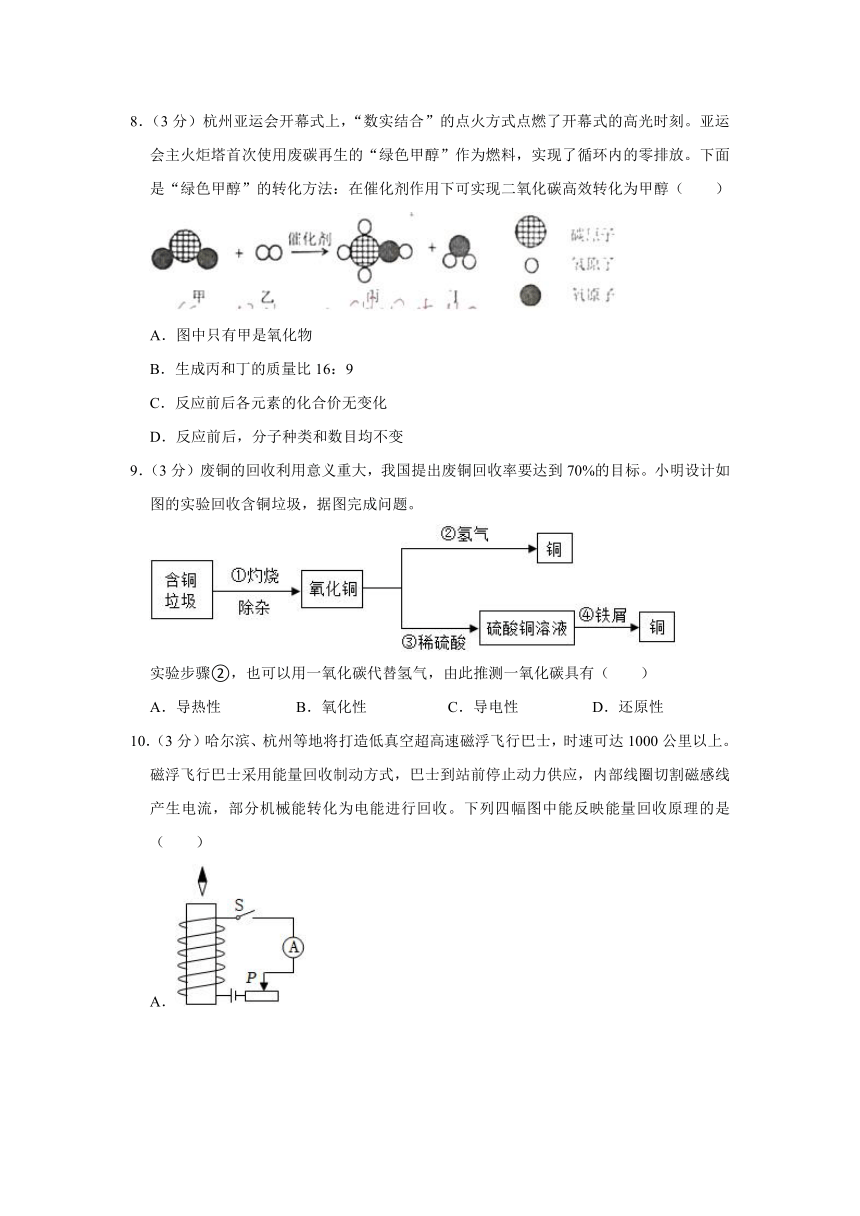
8.(3分)杭州亚运会开幕式上,“数实结合”的点火方式点燃了开幕式的高光时刻。亚运会主火炬塔首次使用废碳再生的“绿色甲醇”作为燃料,实现了循环内的零排放。下面是“绿色甲醇”的转化方法:在催化剂作用下可实现二氧化碳高效转化为甲醇( )
A.图中只有甲是氧化物
B.生成丙和丁的质量比16:9
C.反应前后各元素的化合价无变化
D.反应前后,分子种类和数目均不变
9.(3分)废铜的回收利用意义重大,我国提出废铜回收率要达到70%的目标。小明设计如图的实验回收含铜垃圾,据图完成问题。
实验步骤②,也可以用一氧化碳代替氢气,由此推测一氧化碳具有( )
A.导热性 B.氧化性 C.导电性 D.还原性
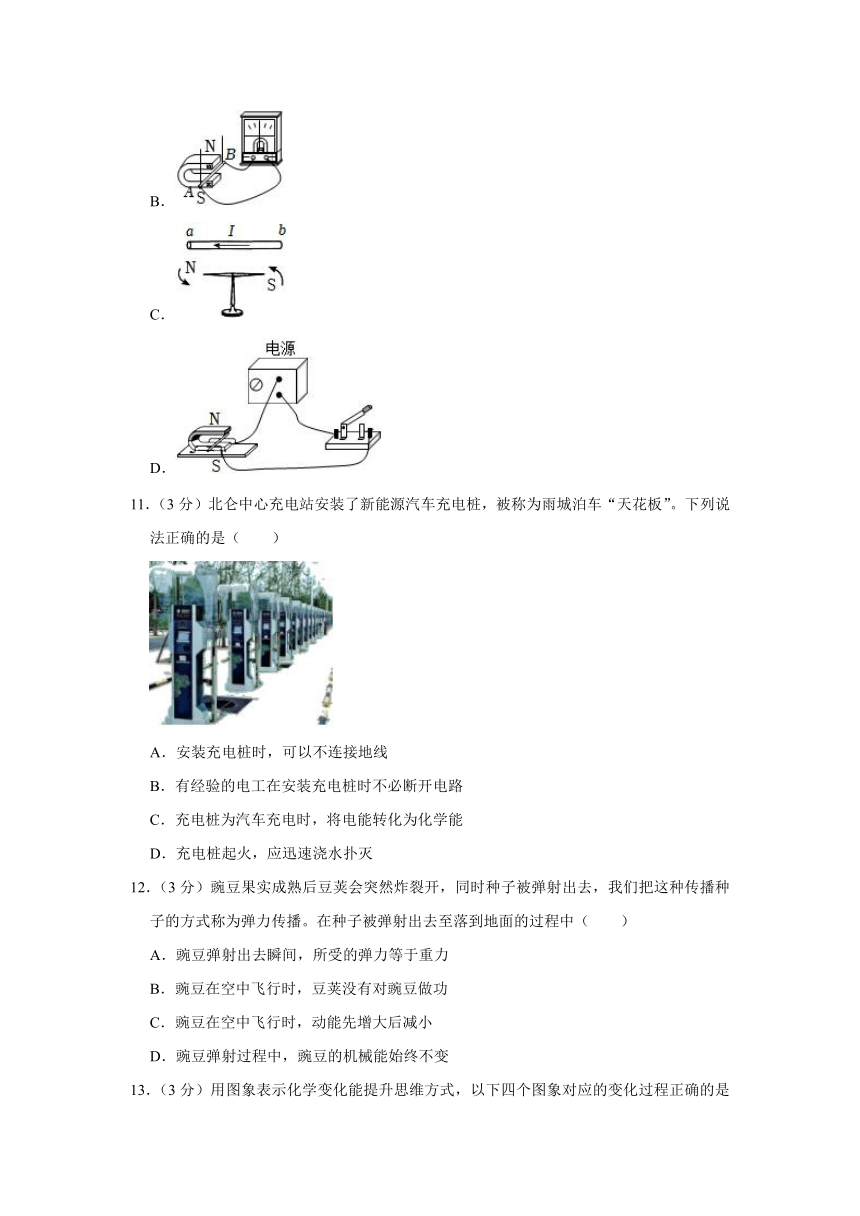
10.(3分)哈尔滨、杭州等地将打造低真空超高速磁浮飞行巴士,时速可达1000公里以上。磁浮飞行巴士采用能量回收制动方式,巴士到站前停止动力供应,内部线圈切割磁感线产生电流,部分机械能转化为电能进行回收。下列四幅图中能反映能量回收原理的是( )
A.
B.
C.
D.
11.(3分)北仑中心充电站安装了新能源汽车充电桩,被称为雨城泊车“天花板”。下列说法正确的是( )
A.安装充电桩时,可以不连接地线
B.有经验的电工在安装充电桩时不必断开电路
C.充电桩为汽车充电时,将电能转化为化学能
D.充电桩起火,应迅速浇水扑灭
12.(3分)豌豆果实成熟后豆荚会突然炸裂开,同时种子被弹射出去,我们把这种传播种子的方式称为弹力传播。在种子被弹射出去至落到地面的过程中( )
A.豌豆弹射出去瞬间,所受的弹力等于重力
B.豌豆在空中飞行时,豆荚没有对豌豆做功
C.豌豆在空中飞行时,动能先增大后减小
D.豌豆弹射过程中,豌豆的机械能始终不变
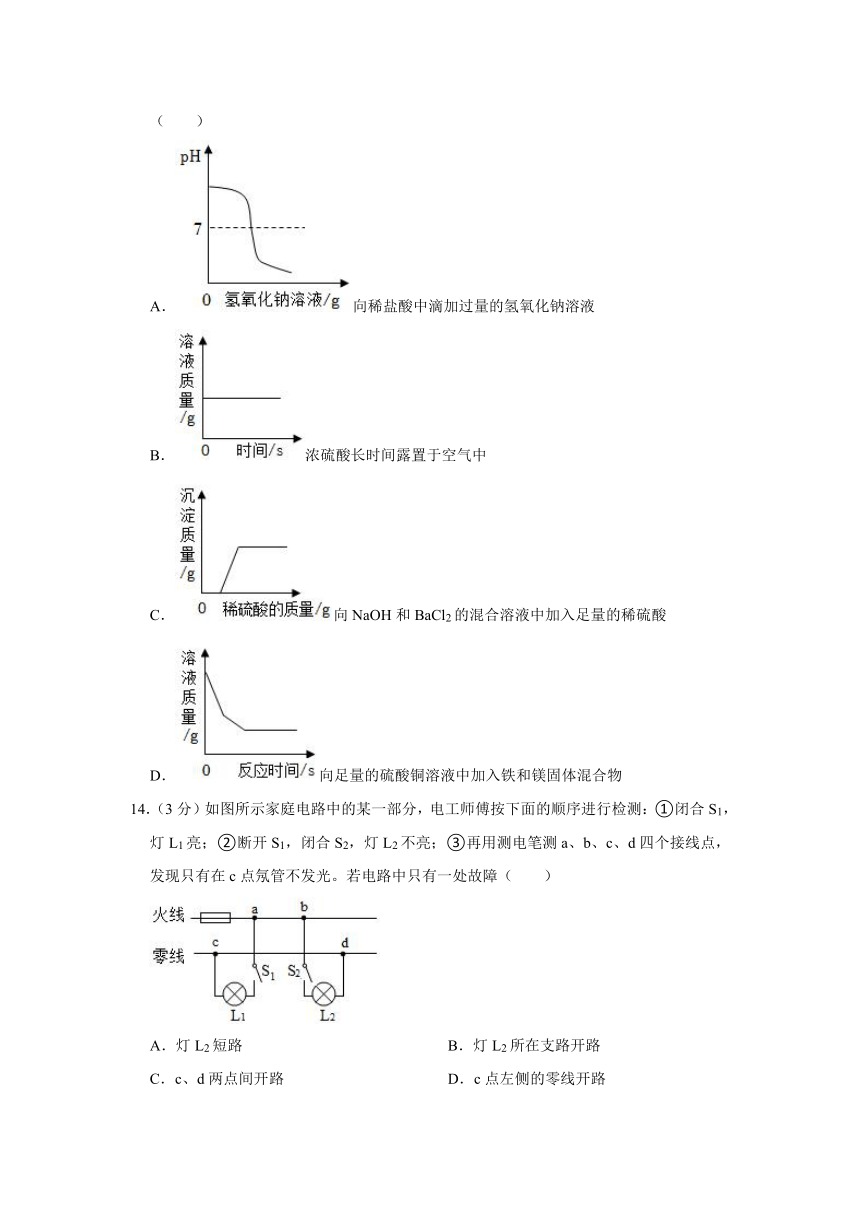
13.(3分)用图象表示化学变化能提升思维方式,以下四个图象对应的变化过程正确的是( )
A.向稀盐酸中滴加过量的氢氧化钠溶液
B.浓硫酸长时间露置于空气中
C.向NaOH和BaCl2的混合溶液中加入足量的稀硫酸
D.向足量的硫酸铜溶液中加入铁和镁固体混合物
14.(3分)如图所示家庭电路中的某一部分,电工师傅按下面的顺序进行检测:①闭合S1,灯L1亮;②断开S1,闭合S2,灯L2不亮;③再用测电笔测a、b、c、d四个接线点,发现只有在c点氖管不发光。若电路中只有一处故障( )
A.灯L2短路 B.灯L2所在支路开路
C.c、d两点间开路 D.c点左侧的零线开路
15.(3分)体育中考测试时,小科选择了引体向上的项目,如图所示。他想要测量自己做“引体向上”时的功率,不需要测量的是( )
A.自身的质量
B.每次身体上升的高度
C.单杠的高度
D.完成“引体向上”的时间
16.(3分)如图所示,两只灯泡L1和L2上分别标有“6V4W”和“3V 1W”字样,将它们串联后接在电压可在3~6V之间调节的电源上,闭合开关S,则下列说法正确的是( )
A.通过灯L1的电流大于通过灯L2的电流
B.当电源电压调节到6V时,灯L1正常发光
C.在调节电源电压的过程中,灯L1始终比灯L2亮
D.在调节电源电压的过程中,两灯的功率变化量相等
17.(3分)小科按图示操作进行酸和碱反应的实验,下列有关分析正确的是( )
A.①中盛放NaOH溶液的试剂瓶瓶塞甲是玻璃塞
B.③反应过程中溶液由红色变为无色
C.⑤中稀释浓硫酸时,倒入的乙物质是水
D.⑥中酚酞试液用完后,滴管及时清洗
18.(3分)某科学兴趣小组在课余时间做了“开门大吉”的游戏,其规则是:每把钥匙代表一种试剂,每扇门代表需要鉴别的两种溶液,钥匙就能把门打开(每把钥匙只能使用一次),下列能够依次将四扇门打开的钥匙顺序是( )
A.①②③④ B.④②③① C.④③②① D.①③②④
19.(3分)如图是探究“电流通过导体时产生热量的多少跟什么因素有关”的实验装置。两个相同的透明容器中密封着等量且初温相同的空气,甲、乙两U形管中液面初始状态是等高相平,通电一段时间后液面的高度如图所示。以下说法错误的是( )
A.通电后电阻丝的内能增大是通过电流做功实现的
B.实验可以得出电流通过电阻产生的热量多少与电流大小有关
C.本实验利用U形管内液面的高度差反映产生热量的多少,这种方法是转换法
D.如果将乙图上方5Ω的电阻也放在右边的容器内,重复上述实验,一段时间后,乙管内液面的高度差比甲更大
20.(3分)模型能够直观反映化学变化的结果。将一定质量的镁条放入某一溶液(如图),其溶质硫酸锌和硫酸亚铁的质量相同,充分反应后烧杯内固体的组成和质量大小关系不可能的是( )
A. B.
C. D.
二、填空题(本题共5题,每空2分,共26分)
21.(6分)现有盐酸、浓硫酸、熟石灰、氯化钠、蛋白质和塑料六种物质,请回答下列问题:
(1)溶于水会放出大量热的是 。
(2)属于天然高分子化合物的是 。
(3)常用来改良酸性土壤的是 。
22.(4分)向稀盐酸中加入足量的金属镁至反应完全,反应的微观模型如图所示。
(1)写出该反应的化学方程式 。
(2)图中的“”“”“”表示溶液中由溶质电离产生的不同离子,则“”表示 。(填写离子符号)
23.(6分)如图甲所示为我国古代发明的取火器的模型图,把木制推杆迅速推入牛角套筒时,杆前端的艾绒立刻燃烧起来 的方式,使筒内空气内能 ,温度升高,达到艾绒的着火点。如图乙所示为单缸四冲程汽油机工作过程中的四个冲程,其中 (选填字母)与上述套筒内空气温度升高过程中能量的转化是一致的。
24.(4分)电脑的中央处理器(CPU),工作时发热显著,常采用铝合金散热片与风扇组合冷却。某笔记本电脑CPU正常工作功率为45W,CPU消耗电能 J。该散热片工作时利用了金属良好的 性。
25.(6分)每年校运动会中都会有跳远、实心球等传统项目。
(1)如图甲,小科在跳远比赛中助跑是为了增大 (选填“惯性”或“动能”),在最高点处 (选填“有”或“没有”)动能。
(2)如图乙是小科同学在投掷实心球的场景,若不计空气阻力,实心球刚脱离手时(A处) C处的动能(选填“大于”“小于”或“等于”)。
三、实验探究题(本题共6小题,每空2分,共42分)
26.(6分)小科利用铁架台、杠杆、钩码和弹簧测力计等器材探究杠杆的平衡条件,实验使用的钩码质量均相等,杠杆上每格长度均相等。
(1)当杠杆静止时如图甲所示,为了方便测量力臂,需要调节杠杆在水平位置平衡 (选填“左”或“右”)调节。
(2)在图乙所示的A、B位置各增加一个钩码,杠杆将会 (选填“仍然平衡”、“左端下沉”或“右端下沉”)。
(3)如图丙所示,用弹簧测力计先后在a、b位置拉杠杆上同一点C,杠杆都在水平位置平衡a,在b位置斜向上的拉力为Fb,则Fa Fb(选填“大于”、“等于”或“小于”)。
27.(8分)在学习了质量守恒定律后,某同学设计了以下几组实验:
(1)上述实验可以用来验证质量守恒定律的有 。(可多选)
(2)实验A中硫酸铜溶液与烧杯中铁粉混合后充分反应,过滤,往滤渣中加入足量的稀盐酸 。
(3)实验D中,若将稀盐酸逐滴滴入烧杯中时,混合物中4种离子(分别用a、b、c、d表示),当滴入稀盐酸的质量在哪个点(选填“甲、乙、丙”)时恰好完全反应 。
28.(6分)图甲是小科的哥哥测定小灯泡额定功率的电路,小灯泡上标有“2.5V”字样。
(1)测小灯泡电压的电压表有“0﹣3V”、“0﹣15V”两个量程,小科的哥哥正确选用了“ ”量程。
(2)闭合开关,移动滑动变阻器滑片,使电压表的示数为2.5V 。
(3)小科发现,与我们教材中测小灯泡电功率的电路相比,哥哥的实验电路多了一根导线 。(用图甲中导线旁的字母表示)
29.(8分)小科利用以下“认识物质性质“的思维模型,在老师的指导下学习未知气体X的性质。
(1)变化→性质:小科用图甲装置进行实验,向左侧塑料瓶里倒入足量的气体X,观察到试纸A不变红
(2)性质→变化:通过学习知道,气体能与氢氧化钠反应,且不产生其他气体。如图乙,反应结束后打开止水夹。预测将出现的现象 ,并写出对应的原因: 。
(3)性质→应用:根据以上性质,若要收集一瓶干燥的气体X,将气体X干燥后 (选填字母)进行收集。
30.(6分)某固体物质可能含有Na2SO4、Na2CO3、CaCl2、KCl和KOH中的一种或几种。为探究其组成,流程和现象记录如图:
(1)根据实验现象可知,固体物质中一定含有 ,一定不含有 。
(2)取无色溶液B,依次滴加AgNO3溶液和稀HNO3,有白色沉淀产生,通过该实验现象能否说明原固体中含有KCl,并说明理由 。
31.(8分)为了比较水和食用油的吸热能力,小科用两个相同的装置做了如图所示的实验。
物质 质量/g 初始温度/℃ 加热时间/min 最后温度/℃
水 60 20 6 42
食用油 60 20 6 62
实验数据记录如表。
(1)实验中,加热相同的时间,水吸收的热量 食用油吸收的热量(选填“大于”、“小于”或“等于”)。
(2)加热结束时,若不考虑蒸发,则水的内能比加热前 (选填“大”或“小”)。
(3)实验表明, (选填“水”或“食用油”)吸热的能力更强。
(4)若水的比热容为4.2×103J/(kg ℃),则食用油的比热容为 J/(kg ℃)。
四、解答题(本题共5小题,第32题4分,第33题6分,第34、35题各7分,第36题8分,共32分)
32.(4分)汽泡爽是一种冲调饮料。其主要原料为柠檬酸(C6H8O7)和小苏打(NaHCO3);使用时将一包汽泡爽粉末倒入玻璃杯中,加入200mL冷水,待粉末完全溶解,就得到一杯果味饮料。
(1)小苏打(NaHCO3)从组成上看,它属于一种 。
A.酸
B.碱
C.盐
D.氧化物
(2)一个柠檬酸分子(C6H8O7)由 个原子构成。
33.(6分)2022年北京冬奥会成功举办。使用的高科技场馆设施环保又节能,如:部分场馆采用地暖供热;氢能大巴首次上岗服务。开幕式上中国式浪漫惊艳世界;中国运动员的拼搏精神激励世人。
(1)地暖工作时水从热源吸热后,顺着管路流动,将热传至室内各个房间。地暖利用了水比热容大的性质 (填序号)选项也利用了该性质。
A.用水洗去衣服上的脏东西
B.将水用作汽车发动机的冷却液
C.用水扑灭大火
D.电解水产生氢气和氧气
(2)氢气的热值是1.4×108J/kg,氢能大巴在某次服务中消耗了2kg的氢气,则2kg氢气完全燃烧时释放的热量为 J(已知Q热量=mq热值)
(3)冰立方雪花台中的LED灯的电功率仅为同等亮度白炽灯的,请从能量转化效率的角度分析,使用LED灯照明比使用白炽灯更节能是因为 。
34.(7分)如图甲所示的装置,A是重12N的空吊篮,小科将A提升到高处,A上升的速度v随时间t变化关系如图丙所示。忽略绳重及摩擦,求:
(1)1~2s内拉力F的功率。
(2)动滑轮所受的重力。
(3)用此装置匀速提升34N重物时的机械效率(重物放在空吊篮内)。
35.(7分)某滚桶洗衣机自带加热功能,其洗衣过程分“加热水”、“保温洗涤”“脱水”三种状态,如图是其简化电路图1、R2的阻值分别为24.2Ω和242Ω。
(1)当开关置于2位置时,R2与电动机并联,此时洗衣机的工作状态是 (选填“加热水”、“保温洗涤”或“脱水”)。
(2)关闭其他用电器,只有洗衣机处于“脱水”状态,脱水一段时间后(kW h)的电能表转盘转过150转,则在这段时间内 焦耳。
(3)洗衣机处于“加热水”状态时(R1与R2并联),正常工作的功率为多少?
36.(8分)在探究酸、碱性质时,小科的操作过程如图甲所示,烧杯中固体质量与加入溶液的质量关系如图乙所示。请回答下列问题:
(1)根据图像分析,开始加入氢氧化钠溶液直到过量的过程,烧杯内的现象是 。
(2)求实验所用稀盐酸的溶质质量分数。
(3)当反应进行到图乙中A点时,求加入的氢氧化钠溶液的质量。
2023-2024学年浙江省宁波市北仑区九年级(上)期末科学试卷
参考答案与试题解析
一、选择题(本题共20小题,每小题3分,共60分。请选出每小题中一个符合题意的选项,不选、错选均不给分)
1.(3分)习近平总书记在党的二十大报告中提出:积极稳妥推进碳达峰、碳中和践行绿色发展理念,保护城市之肺为共建天蓝、地绿、水清的美丽家园,下列措施不可取的是( )
A.生活垃圾分类回收,垃圾资源化
B.加大空气质量检测,改善环境状况
C.大力开展五水共治,保护水资源
D.大量使用化肥农药,提高粮食产量
【答案】D
【解答】解:习近平总书记在党的二十大报告中提出:积极稳妥推进碳达峰、碳中和践行绿色发展理念、地绿,应该将生活垃圾分类回收;加大空气质量检测;大力开展五水共治;化肥和农药的使用,但是会造成水体和土壤污染,应合理使用。
故选:D。
2.(3分)《易经》记载:“泽中有火”“上火下泽”。这是对甲烷气体在湖泊池沼水面上起火现象的描述。下列有关甲烷的叙述,正确的是( )
A.从分类上看:属于无机物
B.从变化上看:燃烧只生成一种物质
C.从性质上看:具有助燃性
D.从使用上看:点燃前要检验气体的纯度
【答案】D
【解答】解:A、甲烷是一种含碳元素的化合物,说法错误;
B、甲烷燃烧生成二氧化碳和水,故不合题意;
C、甲烷具有可燃性,说法错误;
D、甲烷具有可燃性,因此点燃前要检验气体的纯度,故符合题意。
故选:D。
3.(3分)科学实验要规范操作,下列初中科学实验操作你认为不正确的是( )
A.二氧化碳的验满 B.倾倒液体
C.检验气密性 D.用纸槽取用粉末
【答案】A
【解答】解:A、二氧化碳验满时,故本选项操作错误;
B、取用液体时:①试剂瓶瓶口要紧挨试管口;②标签向着手心;③瓶塞倒放桌面上,从而污染药品;
C、检查装置的气密性时,然后用手握住试管外壁,故本选项操作正确;
D、固体粉末放入试管内时,然后放入平置的试管内,故本选项操作正确。
故选:A。
4.(3分)“灰汁团”是浙江传统小吃,制作过程中要用到大米和“灰汁”。“灰汁”制取方法如资料卡所示。下列说法错误的是( )
资料卡 传统方法:稻草烧灰一加水溶解→静置沉淀→过滤取汁
现代方法:将食用碱(纯碱和小苏打的混合物)与水按一定比例混合成汁
A.大米中含有的淀粉属于有机物
B.稻草燃烧属于化学变化
C.传统方法制得的“灰汁”是混合物
D.现代方法制得的“灰汁”不能使酚酞试液变红色
【答案】D
【解答】解:A、大米中含有的淀粉是一种含碳元素的化合物,说法正确;
B、稻草燃烧过程中有新物质生成,说法正确;
C、传统方法制得的“灰汁”中含有多种物质,说法正确;
D、现代方法制得的“灰汁”中含有碳酸钠和碳酸氢钠,能使酚酞试液变红色。
故选:D。
5.(3分)节约用电,从我做起。下列用电器正常工作时,在相同时间内消耗电能最多的是( )
A.台灯 B.液晶电视
C.笔记本电脑 D.空调
【答案】D
【解答】解:这四个用电器工作时,空调机的功率是最大的,由W=Pt可知。
故选:D。
6.(3分)继麒鳞芯片后,华为发布业界最高性能处理器鲲鹏920,摆脱了对国外产品的依赖。芯片主要以高纯度的单质硅(Si),在半导体硅元件生产中,常用氢氟酸(HF),反应原理为SiO2+6HF=H2SiF6+2X。下列说法错误的是( )
A.生成物X的化学式是H2O
B.H2SiF6中硅元素显+4价
C.该反应是复分解反应
D.地壳中硅元素含量仅次于氧元素
【答案】C
【解答】解:A、由SiO2+6HF═H3SiF6+2X可知,反应前后硅原子都是4个,反应后应该是2个,反应前氢原子是6个,其中8个包含在2X中,因此生成物X的化学式是H2O,该选项说法正确;
B、H3SiF6中氢元素化合价是+1,氟元素化合价是﹣3,硅元素显+4价;
C、该反应不是两种化合物相互交换成分生成新的两种化合物,该选项说法不正确;
D、地壳中硅元素含量仅次于氧元素;
故选:C。
7.(3分)下列事例中,改变物体内能的途径与其他三项不同的是( )
A.柴火烧水 B.压缩空气发热
C.冬天搓手取暖 D.钻木取火
【答案】A
【解答】解:
A、柴火烧水是通过热传递的方式改变内能的;
BCD、压缩空气发热、钻木取火都是做功使物体的内能增加的;
显然A选项与其它三个选项改变物体内能的方式不同。
故选:A。
8.(3分)杭州亚运会开幕式上,“数实结合”的点火方式点燃了开幕式的高光时刻。亚运会主火炬塔首次使用废碳再生的“绿色甲醇”作为燃料,实现了循环内的零排放。下面是“绿色甲醇”的转化方法:在催化剂作用下可实现二氧化碳高效转化为甲醇( )
A.图中只有甲是氧化物
B.生成丙和丁的质量比16:9
C.反应前后各元素的化合价无变化
D.反应前后,分子种类和数目均不变
【答案】B
【解答】解:由微观反应示意图可知,在催化剂的催化作用下,该反应的化学方程式是:CO2+3H8CH3OH+H2O;
A、氧化物是由两种元素组成,该反应中的二氧化碳和水均属于氧化物;
B、由化学方程式可知,故B说法正确;
C、反应物中的氢气是一种单质,反应后,氢元素的化合价不为零,氢元素的化合价一定发生改变;
D、由化学方程式可知,分子种类和数目均发生改变。
故选:B。
9.(3分)废铜的回收利用意义重大,我国提出废铜回收率要达到70%的目标。小明设计如图的实验回收含铜垃圾,据图完成问题。
实验步骤②,也可以用一氧化碳代替氢气,由此推测一氧化碳具有( )
A.导热性 B.氧化性 C.导电性 D.还原性
【答案】D
【解答】解:在实验步骤②中氢气与氧化铜反应生成铜和水,氢气夺取氧化铜中的氧,具有还原性,由此推测一氧化碳具有还原性,D正确。
故选:D。
10.(3分)哈尔滨、杭州等地将打造低真空超高速磁浮飞行巴士,时速可达1000公里以上。磁浮飞行巴士采用能量回收制动方式,巴士到站前停止动力供应,内部线圈切割磁感线产生电流,部分机械能转化为电能进行回收。下列四幅图中能反映能量回收原理的是( )
A.
B.
C.
D.
【答案】B
【解答】解:线圈随车轮转动并在磁场中切割磁感线产生感应电流,将机械能转化为电能;
A、该装置是电磁铁,故A不符合题意;
B、闭合电路的部分导体在磁场中做切割磁感线运动时,这种现象叫电磁感应现象,故B符合题意;
C、这是奥斯特实验,故C不符合题意;
D、通电导体在磁场中要受到力的作用,故D不符合题意。
故选:B。
11.(3分)北仑中心充电站安装了新能源汽车充电桩,被称为雨城泊车“天花板”。下列说法正确的是( )
A.安装充电桩时,可以不连接地线
B.有经验的电工在安装充电桩时不必断开电路
C.充电桩为汽车充电时,将电能转化为化学能
D.充电桩起火,应迅速浇水扑灭
【答案】C
【解答】解:A、安装充电桩时,要接地线;
B、安装充电桩时必须断开电源。
C、充电桩为汽车充电时,故C正确。
D、万一有充电桩起火,故B不符合安全用电要求;
故选:C。
12.(3分)豌豆果实成熟后豆荚会突然炸裂开,同时种子被弹射出去,我们把这种传播种子的方式称为弹力传播。在种子被弹射出去至落到地面的过程中( )
A.豌豆弹射出去瞬间,所受的弹力等于重力
B.豌豆在空中飞行时,豆荚没有对豌豆做功
C.豌豆在空中飞行时,动能先增大后减小
D.豌豆弹射过程中,豌豆的机械能始终不变
【答案】B
【解答】解:A.豌豆弹射出去瞬间,受力不平衡,故A错误;
B.豌豆在空中飞行时,没有对豌豆做功;
C.豌豆在空中飞行时,动能先变小后变大,动能一直增大;
D.豌豆弹射过程中,豌豆的机械能增大。
故选:B。
13.(3分)用图象表示化学变化能提升思维方式,以下四个图象对应的变化过程正确的是( )
A.向稀盐酸中滴加过量的氢氧化钠溶液
B.浓硫酸长时间露置于空气中
C.向NaOH和BaCl2的混合溶液中加入足量的稀硫酸
D.向足量的硫酸铜溶液中加入铁和镁固体混合物
【答案】D
【解答】解:A、向稀盐酸中滴加过量的氢氧化钠溶液,pH小于7,酸性越来越弱,溶液呈中性,酸反应完了,溶液呈碱性;故A图像错误;
B、浓硫酸具有吸水性,溶液质量越会增大;
C、向NaOH和BaCl2的混合溶液中加入足量的稀硫酸,硫酸根离子能与钡离子反应生成不溶于酸的硫酸钡沉淀,故C图错误;
D、镁、铁、铜的活动性顺序为:镁>铁>铜,镁先与硫酸铜溶液反应生成铜和硫酸镁2=Cu+MgSO4 可知,每24份质量的镁参加反应生成64份质量的铜;当镁完全反应后,由化学方程式Fe+CuSO4=Cu+FeSO8可知,每56份质量的铁参加反应生成64份质量的铜,但减少的幅度变小,溶液的质量不再减少;
故选:D。
14.(3分)如图所示家庭电路中的某一部分,电工师傅按下面的顺序进行检测:①闭合S1,灯L1亮;②断开S1,闭合S2,灯L2不亮;③再用测电笔测a、b、c、d四个接线点,发现只有在c点氖管不发光。若电路中只有一处故障( )
A.灯L2短路 B.灯L2所在支路开路
C.c、d两点间开路 D.c点左侧的零线开路
【答案】C
【解答】解:闭合S1,灯L1亮,电路中有电流,从保险丝→a→S8→L1→c以及c点左侧的零线都没有断路,故D错误;
断开S1,闭合S8,灯L2不亮,灯L2不亮的原因有两个:一个是断路、一个是短路,
若灯L7短路时,电路的电流会很大,灯泡L1也不会发光,a、b两个接线点上,故A错误;
若灯L2所在支路开路,d点氖管不发光;
若c、d两点间开路5与零线不能构成闭合电路,电路中没有电流,但d点会通过灯泡L2与火线间接相连,试电笔的氖管会发光。
故选:C。
15.(3分)体育中考测试时,小科选择了引体向上的项目,如图所示。他想要测量自己做“引体向上”时的功率,不需要测量的是( )
A.自身的质量
B.每次身体上升的高度
C.单杠的高度
D.完成“引体向上”的时间
【答案】C
【解答】解:做引体向上的功率P===需要测量的物理量是小科的质量、小科做引体向上的时间,故C符合题意。
故选:C。
16.(3分)如图所示,两只灯泡L1和L2上分别标有“6V4W”和“3V 1W”字样,将它们串联后接在电压可在3~6V之间调节的电源上,闭合开关S,则下列说法正确的是( )
A.通过灯L1的电流大于通过灯L2的电流
B.当电源电压调节到6V时,灯L1正常发光
C.在调节电源电压的过程中,灯L1始终比灯L2亮
D.在调节电源电压的过程中,两灯的功率变化量相等
【答案】D
【解答】解:由P=可得
R1===6Ω,R2===9Ω;
A、两灯泡串联2的电流等于通过灯L2的电流,故A错误;
BC、在调节电源电压的过程中2R可知,两灯泡的实际功率相等,故BC错误;
D、两灯泡串联,通过两灯泡的电流变化相同,由P=I4R可知,灯泡功率的变化相同。
故选:D。
17.(3分)小科按图示操作进行酸和碱反应的实验,下列有关分析正确的是( )
A.①中盛放NaOH溶液的试剂瓶瓶塞甲是玻璃塞
B.③反应过程中溶液由红色变为无色
C.⑤中稀释浓硫酸时,倒入的乙物质是水
D.⑥中酚酞试液用完后,滴管及时清洗
【答案】B
【解答】解:A、氢氧化钠溶液能与玻璃的主要成分反应,不能使用玻璃塞。
B、滴有酚酞溶液的氢氧化钠溶液显红色,至恰好完全反应,③反应过程中溶液由红色变为无色。
C、稀释浓硫酸时,同时用玻璃棒不断搅拌;一定不能把水注入浓硫酸中,倒入的乙物质是浓硫酸。
D、滴瓶上的滴管使用后直接插回原瓶,否则试剂瓶中的溶液将被稀释。
故选:B。
18.(3分)某科学兴趣小组在课余时间做了“开门大吉”的游戏,其规则是:每把钥匙代表一种试剂,每扇门代表需要鉴别的两种溶液,钥匙就能把门打开(每把钥匙只能使用一次),下列能够依次将四扇门打开的钥匙顺序是( )
A.①②③④ B.④②③① C.④③②① D.①③②④
【答案】B
【解答】解:由于碳酸钠溶液显碱性,鉴别碳酸钠和氢氧化钠时,检验碳酸根的存在,与氢氧化钠不反应)或④稀盐酸(与碳酸钠反应有气泡生成;鉴别氢氧化钠与氢氧化钙溶液,与氢氧化钠不反应)或③二氧化碳(与氢氧化钙反应有沉淀生成;鉴别氢氧化钙和氯化钙,与氯化钙不反应),与盐酸不反应),顺序为④②③①。
故选:B。
19.(3分)如图是探究“电流通过导体时产生热量的多少跟什么因素有关”的实验装置。两个相同的透明容器中密封着等量且初温相同的空气,甲、乙两U形管中液面初始状态是等高相平,通电一段时间后液面的高度如图所示。以下说法错误的是( )
A.通电后电阻丝的内能增大是通过电流做功实现的
B.实验可以得出电流通过电阻产生的热量多少与电流大小有关
C.本实验利用U形管内液面的高度差反映产生热量的多少,这种方法是转换法
D.如果将乙图上方5Ω的电阻也放在右边的容器内,重复上述实验,一段时间后,乙管内液面的高度差比甲更大
【答案】D
【解答】解:A、电流做功的过程就是电能转化为其它形式能的过程,电阻丝的内能增大是通过电流做功实现的;
B、上图中,容器内两电阻大小相等,通过左侧容器中电阻的电流大于通过右侧容器中电阻的电流,故可以研究电流产生的热量与电流的关系;
C、本实验利用U形管内液面的高度差反映产生热量的多少,故C正确;
D、如果将乙图上方5Ω的电阻也放在右边的容器内,容器内的总电阻小于5欧姆,根据Q=I3Rt可生可知,左侧电阻产生热量多,故D错误。
故选:D。
20.(3分)模型能够直观反映化学变化的结果。将一定质量的镁条放入某一溶液(如图),其溶质硫酸锌和硫酸亚铁的质量相同,充分反应后烧杯内固体的组成和质量大小关系不可能的是( )
A. B.
C. D.
【答案】C
【解答】解:在金属活动性顺序表中镁锌铁的活动性为:镁>锌>铁,将镁条加入硫酸锌和硫酸亚铁的溶液中,反应方程式为Mg+FeSO4=MgSO4+Fe,即每24份质量的镁能置换出56份质量的铁,若镁还有剩余,反应方程式为Mg+ZnSO4=MgSO4+Zn,即每24份质量的镁能置换出65份质量的锌,设等质量为m=0.5mg=0.37mg.
A、由图A知,可能硫酸亚铁完全反应完,则生成的铁和锌的质量可能相等;
B、由图B知,可能硫酸亚铁完全反应完,则生成的铁的质量可能大于生成的锌的质量;
C、由图C知,硫酸亚铁和硫酸锌均反应完全,生成铁的质量一定小于生成锌的质量,故C错误;
D、由图D知,硫酸亚铁和硫酸锌均反应完全,生成铁的质量一定小于生成锌的质量。
故选:C。
二、填空题(本题共5题,每空2分,共26分)
21.(6分)现有盐酸、浓硫酸、熟石灰、氯化钠、蛋白质和塑料六种物质,请回答下列问题:
(1)溶于水会放出大量热的是 浓硫酸 。
(2)属于天然高分子化合物的是 蛋白质 。
(3)常用来改良酸性土壤的是 熟石灰 。
【答案】(1)浓硫酸;
(2)蛋白质;
(3)熟石灰。
【解答】解:(1)浓硫酸溶于水会放出大量热;故答案为:浓硫酸;
(2)蛋白质属于天然高分子化合物;故答案为:蛋白质;
(3)熟石灰是氢氧化钙的俗称,是一种碱,因此常用来改良酸性土壤。
22.(4分)向稀盐酸中加入足量的金属镁至反应完全,反应的微观模型如图所示。
(1)写出该反应的化学方程式 Mg+2HCl=MgCl2+H2↑ 。
(2)图中的“”“”“”表示溶液中由溶质电离产生的不同离子,则“”表示 Mg2+ 。(填写离子符号)
【答案】(1)Mg+2HCl=MgCl2+H2↑;
(2)Mg2+。
【解答】解:(1)向稀盐酸中加入足量的金属镁至反应完全,镁和稀盐酸反应生成氯化镁和氢气2+H2↑。
(2)图中的“”“〇”“”表示溶液中由溶质电离产生的不同离子,由反应的化学方程式可知,反应后溶液中有镁离子和氯离子”表示镁离子,离子符号为:Mg2+。
故答案为:
(1)Mg+2HCl=MgCl2+H6↑;
(2)Mg2+。
23.(6分)如图甲所示为我国古代发明的取火器的模型图,把木制推杆迅速推入牛角套筒时,杆前端的艾绒立刻燃烧起来 做功 的方式,使筒内空气内能 增大 ,温度升高,达到艾绒的着火点。如图乙所示为单缸四冲程汽油机工作过程中的四个冲程,其中 D (选填字母)与上述套筒内空气温度升高过程中能量的转化是一致的。
【答案】做功;增大;D。
【解答】解:(1)把木制推杆迅速推入牛角套筒时,杆前端的艾绒立刻燃烧起来,使筒内空气内能增大,达到艾绒的着火点;
(2)此过程中压缩套筒内空气做功,使套筒内气体的内能增加。在该实验中,与汽油机的压缩冲程的能量转化相同,活塞向上运动,与上述实验过程的能量转化一致。
故答案为:做功;增大;D。
24.(4分)电脑的中央处理器(CPU),工作时发热显著,常采用铝合金散热片与风扇组合冷却。某笔记本电脑CPU正常工作功率为45W,CPU消耗电能 1.62×105 J。该散热片工作时利用了金属良好的 导热 性。
【答案】1.62×105;导热。
【解答】解:正常工作1小时,CPU消耗电能W=Pt=45W×1×3600s=7.62×105J;
该散热片工作时利用了金属良好的导热性。
故答案为:1.62×105;导热。
25.(6分)每年校运动会中都会有跳远、实心球等传统项目。
(1)如图甲,小科在跳远比赛中助跑是为了增大 动能 (选填“惯性”或“动能”),在最高点处 有 (选填“有”或“没有”)动能。
(2)如图乙是小科同学在投掷实心球的场景,若不计空气阻力,实心球刚脱离手时(A处) 小于 C处的动能(选填“大于”“小于”或“等于”)。
【答案】(1)动能;有;(2)小于。
【解答】解:(1)惯性是物体的性质,只与物体的质量有关,则人的惯性不变;经过最高点时人的速度不为零,若动能为零;
(2)若不计空气阻力,实心球的机械能守恒,重力势能较大,C的动能大。
故答案为:(1)动能;有;(2)小于。
三、实验探究题(本题共6小题,每空2分,共42分)
26.(6分)小科利用铁架台、杠杆、钩码和弹簧测力计等器材探究杠杆的平衡条件,实验使用的钩码质量均相等,杠杆上每格长度均相等。
(1)当杠杆静止时如图甲所示,为了方便测量力臂,需要调节杠杆在水平位置平衡 右 (选填“左”或“右”)调节。
(2)在图乙所示的A、B位置各增加一个钩码,杠杆将会 左端下沉 (选填“仍然平衡”、“左端下沉”或“右端下沉”)。
(3)如图丙所示,用弹簧测力计先后在a、b位置拉杠杆上同一点C,杠杆都在水平位置平衡a,在b位置斜向上的拉力为Fb,则Fa 小于 Fb(选填“大于”、“等于”或“小于”)。
【答案】(1)右;(2)左端下沉;(3)小于。
【解答】解:(1)当杠杆静止时,发现左端下沉,此时,直至杠杆在水平位置平衡;
(2)设钩码的重力为G,每一格的长度为L,A,
左侧=3G×3L=8GL,右侧=4G×2L=6GL,
所以左端下沉;
(3)根据杠杆的平衡条件分析,将测力计绕C点从a位置转动到b位置过程中,其阻力臂不变,而动力臂在从a到b的过程逐渐减小,即Fa<Fb。
故答案为:(1)右;(2)左端下沉。
27.(8分)在学习了质量守恒定律后,某同学设计了以下几组实验:
(1)上述实验可以用来验证质量守恒定律的有 ACD 。(可多选)
(2)实验A中硫酸铜溶液与烧杯中铁粉混合后充分反应,过滤,往滤渣中加入足量的稀盐酸 硫酸亚铁,硫酸亚铁、硫酸铜 。
(3)实验D中,若将稀盐酸逐滴滴入烧杯中时,混合物中4种离子(分别用a、b、c、d表示),当滴入稀盐酸的质量在哪个点(选填“甲、乙、丙”)时恰好完全反应 丙,这是因为c表示氢氧根离子数量,随着反应进行,氢离子和氢氧根离子结合生成水分子,当当滴入稀盐酸的质量在丙点时,氢氧根离子数量减小到0,说明氢氧化钠恰好和盐酸完全反应 。
【答案】见试题解答内容
【解答】解:(1)上述实验可以用来验证质量守恒定律的有ACD,B不能。
故填:ACD。
(2)实验A中硫酸铜溶液与烧杯中铁粉混合后充分反应,过滤,没有产生气泡,滤液中溶质的可能组成:硫酸亚铁(铁和硫酸铜恰好完全反应)。
故填:硫酸亚铁,硫酸亚铁。
(3)当滴入稀盐酸的质量在丙点时恰好完全反应,理由:c表示氢氧根离子数量,氢离子和氢氧根离子结合生成水分子,氢氧根离子数量减小到0。
故填:丙,这是因为c表示氢氧根离子数量,氢离子和氢氧根离子结合生成水分子,氢氧根离子数量减小到0。
28.(6分)图甲是小科的哥哥测定小灯泡额定功率的电路,小灯泡上标有“2.5V”字样。
(1)测小灯泡电压的电压表有“0﹣3V”、“0﹣15V”两个量程,小科的哥哥正确选用了“ 0﹣3V ”量程。
(2)闭合开关,移动滑动变阻器滑片,使电压表的示数为2.5V 0.75W 。
(3)小科发现,与我们教材中测小灯泡电功率的电路相比,哥哥的实验电路多了一根导线 b 。(用图甲中导线旁的字母表示)
【答案】(1)0﹣3V;(2)0.75W;(3)b。
【解答】解:(1)小灯泡上标有“2.5V”字样,故电压表选用“2﹣3V”量程;
(2)闭合开关,移动滑动变阻器滑片,此时电流表的示数如图乙所示,分度值0.02A,则小灯泡额定功率为:
P=UI=7.5V×0.2A=0.75W;
(3)原电路图中,滑动变阻器和灯泡并联是错误的,灯泡,电压表并联在灯泡两端,这根导线是b。
故答案为:(1)0﹣4V;(2)0.75W。
29.(8分)小科利用以下“认识物质性质“的思维模型,在老师的指导下学习未知气体X的性质。
(1)变化→性质:小科用图甲装置进行实验,向左侧塑料瓶里倒入足量的气体X,观察到试纸A不变红
(2)性质→变化:通过学习知道,气体能与氢氧化钠反应,且不产生其他气体。如图乙,反应结束后打开止水夹。预测将出现的现象 烧杯中的水倒吸进入烧瓶 ,并写出对应的原因: 气体X与氢氧化钠反应导致瓶内气压减小,大气压将水压入烧瓶 。
(3)性质→应用:根据以上性质,若要收集一瓶干燥的气体X,将气体X干燥后 B或E (选填字母)进行收集。
【答案】(1)气体X的密度比空气大,且能与水反应生成酸性物质;
(2)烧杯中的水倒吸进入烧瓶;气体X与氢氧化钠反应导致瓶内气压减小,大气压将水压入烧瓶;
(3)B或E。
【解答】解:(1)小科用图甲装置进行实验,向左侧塑料瓶里倒入足量的气体X,试纸B(湿润的紫色石蕊试纸)比C(湿润的紫色石蕊试纸)先变红(C在高处,据此推测气体X的性质有密度比空气大;
(2)气体X能与氢氧化钠反应,且不产生其他气体,小科向充满气体X的烧瓶中注入10mL氢氧化钠溶液,造成装置内的压强减小,在外界大气压的作用下;
(3)由上述实验可知,气体X的密度比空气大,可采用向上排空气法。
故答案为:
(1)气体X的密度比空气大,且能与水反应生成酸性物质;
(2)烧杯中的水倒吸进入烧瓶;气体X与氢氧化钠反应导致瓶内气压减小;
(3)B或E。
30.(6分)某固体物质可能含有Na2SO4、Na2CO3、CaCl2、KCl和KOH中的一种或几种。为探究其组成,流程和现象记录如图:
(1)根据实验现象可知,固体物质中一定含有 Na2SO4、Na2CO3 ,一定不含有 CaCl2、KOH 。
(2)取无色溶液B,依次滴加AgNO3溶液和稀HNO3,有白色沉淀产生,通过该实验现象能否说明原固体中含有KCl,并说明理由 步骤②中加入了氯化钡溶液引入了氯离子 。
【答案】见试题解答内容
【解答】解:固体物质溶于水得无色溶液,而碳酸钠和氯化钙反应能够生成沉淀,硫酸钠和氯化钡会生成不溶于酸的硫酸钡沉淀,氢氧化钾。
无色溶液A中加入氯化钡会生成白色沉淀和pH=7的溶液B,所以固体物质中一定不含氢氧化钾,白色沉淀溶于酸会生成气体,所以混合物中一定含有碳酸钠,一定不含氯化钙;
(1)由以上分析可知固体物质中一定含有Na2SO8、Na2CO3,一定没有CaCl7、KOH,可能含有KCl。
(2)取无色溶液B,依次滴加AgNO3和稀HNO3不能检验原固体中是否含有KCl,理由是:步骤②中加入了氯化钡溶液引入了氯离子。
故答案为:(1)Na4SO4、Na2CO2;CaCl2、KOH。
(2)步骤②中加入了氯化钡溶液引入了氯离子。
31.(8分)为了比较水和食用油的吸热能力,小科用两个相同的装置做了如图所示的实验。
物质 质量/g 初始温度/℃ 加热时间/min 最后温度/℃
水 60 20 6 42
食用油 60 20 6 62
实验数据记录如表。
(1)实验中,加热相同的时间,水吸收的热量 等于 食用油吸收的热量(选填“大于”、“小于”或“等于”)。
(2)加热结束时,若不考虑蒸发,则水的内能比加热前 大 (选填“大”或“小”)。
(3)实验表明, 水 (选填“水”或“食用油”)吸热的能力更强。
(4)若水的比热容为4.2×103J/(kg ℃),则食用油的比热容为 2.2×103 J/(kg ℃)。
【答案】(1)等于;(2)大;(3)水;(4)2.2×103。
【解答】解:(1)实验中,加热相同的时间,水吸收的热量等于食用油吸收的热量;
(2)加热结束时,水吸热温度升高,则水的内能比加热前大;
(3)根据表中数据可知,加热6分钟(吸热相同)
42℃﹣20℃=22℃
食用油升高的温度为
62℃﹣20℃=42℃
根据比较吸热能力的方法,水的吸热能力强。
根据Q=cmΔt可知,在质量和升高的温度相同的情况下,则食用油的比热容为
c=×4.3×103J/(kg ℃)=2.8×103J/(kg ℃)。
故答案为:(1)等于;(2)大;(4)2.7×103。
四、解答题(本题共5小题,第32题4分,第33题6分,第34、35题各7分,第36题8分,共32分)
32.(4分)汽泡爽是一种冲调饮料。其主要原料为柠檬酸(C6H8O7)和小苏打(NaHCO3);使用时将一包汽泡爽粉末倒入玻璃杯中,加入200mL冷水,待粉末完全溶解,就得到一杯果味饮料。
(1)小苏打(NaHCO3)从组成上看,它属于一种 C 。
A.酸
B.碱
C.盐
D.氧化物
(2)一个柠檬酸分子(C6H8O7)由 21 个原子构成。
【答案】(1)C;
(2)21。
【解答】解:(1)小苏打(NaHCO3)是由金属离子与酸根离子构成的化合物,属于盐;
(2)一个柠檬酸分子(C6H8O7)是由6个碳原子、8个氢原子和7个氧原子构成的;
故答案为:
(1)C;
(2)21。
33.(6分)2022年北京冬奥会成功举办。使用的高科技场馆设施环保又节能,如:部分场馆采用地暖供热;氢能大巴首次上岗服务。开幕式上中国式浪漫惊艳世界;中国运动员的拼搏精神激励世人。
(1)地暖工作时水从热源吸热后,顺着管路流动,将热传至室内各个房间。地暖利用了水比热容大的性质 B (填序号)选项也利用了该性质。
A.用水洗去衣服上的脏东西
B.将水用作汽车发动机的冷却液
C.用水扑灭大火
D.电解水产生氢气和氧气
(2)氢气的热值是1.4×108J/kg,氢能大巴在某次服务中消耗了2kg的氢气,则2kg氢气完全燃烧时释放的热量为 2.8×108 J(已知Q热量=mq热值)
(3)冰立方雪花台中的LED灯的电功率仅为同等亮度白炽灯的,请从能量转化效率的角度分析,使用LED灯照明比使用白炽灯更节能是因为 LED灯将电能转化为光能的效率更高 。
【答案】(1)B;(2)2.8×108;(3)LED灯将电能转化为光能的效率更高。
【解答】解:(1)地暖利用了水的比热容较大的性质,因此选项B也体现的是这个性质;
(2)2kg氢气完全燃烧时释放的热量Q放=mq=2kg×4.4×108J/kg=7.8×108J;
(3)白炽灯会将电能转化为热能用来发热,而LED灯主要将电能转化为光能。
故答案为:(1)B;(2)3.8×108;(3)LED灯将电能转化为光能的效率更高。
34.(7分)如图甲所示的装置,A是重12N的空吊篮,小科将A提升到高处,A上升的速度v随时间t变化关系如图丙所示。忽略绳重及摩擦,求:
(1)1~2s内拉力F的功率。
(2)动滑轮所受的重力。
(3)用此装置匀速提升34N重物时的机械效率(重物放在空吊篮内)。
【答案】(1)1~2s内拉力F的功率为40W;
(2)动滑轮所受的重力为4N;
(3)用此装置匀速提升34N重物时的机械效率为68%。
【解答】解:(1)由图丙可知1~2s内A的速度vA=8.5m/s,由图甲可知,拉力端移动速度v=nvA=2×4.5m/s=5m/s,由图乙可知3~2s内拉力F=8N,
因此5~2s内拉力F的功率:
P===Fv=8N×2m/s=40W;
(2)因为忽略绳重及摩擦,拉力F=A+G动),
所以动滑轮所受的重力:
G动=nF﹣GA=2×5N﹣12N=4N;
(3)因为忽略绳重及摩擦,C处绳子拉力FC=(G物+GA+G动)=×(34N+12N+4N)=25N,
用此装置匀速提升重物34N时的机械效率:
η=====×100%=68%。
答:(1)1~2s内拉力F的功率为40W;
(2)动滑轮所受的重力为6N;
(3)用此装置匀速提升34N重物时的机械效率为68%。
35.(7分)某滚桶洗衣机自带加热功能,其洗衣过程分“加热水”、“保温洗涤”“脱水”三种状态,如图是其简化电路图1、R2的阻值分别为24.2Ω和242Ω。
(1)当开关置于2位置时,R2与电动机并联,此时洗衣机的工作状态是 保温洗涤 (选填“加热水”、“保温洗涤”或“脱水”)。
(2)关闭其他用电器,只有洗衣机处于“脱水”状态,脱水一段时间后(kW h)的电能表转盘转过150转,则在这段时间内 1.8×105 焦耳。
(3)洗衣机处于“加热水”状态时(R1与R2并联),正常工作的功率为多少?
【答案】(1)保温洗涤;
(2)1.8×105;
(3)洗衣机处于“加热水”状态(R1与R2并联)正常工作的功率为2200W。
【解答】解:(1)由电路图可知,开关置于1位置时,R1与R7并联,电路的总电阻最小,洗衣机处于“加热水”状态,电动机与R2并联,洗衣机处于“保温洗涤”状态,电路中只有电动机工作;
(2)标有3000r/(kW h)的电能表转盘转过150转,消耗的电能:
W==0.05kW h=5.05×3.6×104J=1.8×103J;
(3)开关应置于1位置时,R1与R4并联,电路的总电阻最小,洗衣机处于“加热水”状态,
因并联电路中各支路两端的电压相等,所以
P加热=+=+=2200W。
答:(1)保温洗涤;
(2)1.6×105;
(3)洗衣机处于“加热水”状态(R1与R2并联)正常工作的功率为2200W。
36.(8分)在探究酸、碱性质时,小科的操作过程如图甲所示,烧杯中固体质量与加入溶液的质量关系如图乙所示。请回答下列问题:
(1)根据图像分析,开始加入氢氧化钠溶液直到过量的过程,烧杯内的现象是 产生蓝色沉淀 。
(2)求实验所用稀盐酸的溶质质量分数。
(3)当反应进行到图乙中A点时,求加入的氢氧化钠溶液的质量。
【答案】(1)产生蓝色沉淀。
(2)7.3%。
(3)162.5g。
【解答】解:(1)氢氧化钠和氯化铜反应生成蓝色沉淀氢氧化铜和氯化钠,烧杯内的现象是产生蓝色沉淀。
故答案为:产生蓝色沉淀。
(2)设与18g氧化铜反应的氯化氢质量是x,反应生成氯化铜质量是y。
CuO+2HCl═CuCl2+H7O
80 73
18g x y
= =
x=16.425g y=30.375g
所用稀盐酸的溶质质量分数是×100%=7.3%
答:所用稀盐酸的溶质质量分数是4.3%。
(3)设过量的100g稀盐酸消耗氢氧化钠质量为z。
NaOH+HCl═NaCl+H2O
40 36.5
z 100g×7.3%
=
z=3g
设30.375g氯化铜消耗氢氧化钠质量是m。
CuCl2+2NaOH=5NaCl+Cu(OH)2↓
135 80
30.375g m
=
m=18g
反应进行到图乙中A点时,加入的氢氧化钠溶液的质量是(8g+18g)÷16%=162.3g
答:反应进行到图乙中A点时,加入的氢氧化钠溶液的质量是162.5g。
一、选择题(本题共20小题,每小题3分,共60分。请选出每小题中一个符合题意的选项,不选、错选均不给分)
1.(3分)习近平总书记在党的二十大报告中提出:积极稳妥推进碳达峰、碳中和践行绿色发展理念,保护城市之肺为共建天蓝、地绿、水清的美丽家园,下列措施不可取的是( )
A.生活垃圾分类回收,垃圾资源化
B.加大空气质量检测,改善环境状况
C.大力开展五水共治,保护水资源
D.大量使用化肥农药,提高粮食产量
2.(3分)《易经》记载:“泽中有火”“上火下泽”。这是对甲烷气体在湖泊池沼水面上起火现象的描述。下列有关甲烷的叙述,正确的是( )
A.从分类上看:属于无机物
B.从变化上看:燃烧只生成一种物质
C.从性质上看:具有助燃性
D.从使用上看:点燃前要检验气体的纯度
3.(3分)科学实验要规范操作,下列初中科学实验操作你认为不正确的是( )
A.二氧化碳的验满 B.倾倒液体
C.检验气密性 D.用纸槽取用粉末
4.(3分)“灰汁团”是浙江传统小吃,制作过程中要用到大米和“灰汁”。“灰汁”制取方法如资料卡所示。下列说法错误的是( )
资料卡 传统方法:稻草烧灰一加水溶解→静置沉淀→过滤取汁
现代方法:将食用碱(纯碱和小苏打的混合物)与水按一定比例混合成汁
A.大米中含有的淀粉属于有机物
B.稻草燃烧属于化学变化
C.传统方法制得的“灰汁”是混合物
D.现代方法制得的“灰汁”不能使酚酞试液变红色
5.(3分)节约用电,从我做起。下列用电器正常工作时,在相同时间内消耗电能最多的是( )
A.台灯 B.液晶电视
C.笔记本电脑 D.空调
6.(3分)继麒鳞芯片后,华为发布业界最高性能处理器鲲鹏920,摆脱了对国外产品的依赖。芯片主要以高纯度的单质硅(Si),在半导体硅元件生产中,常用氢氟酸(HF),反应原理为SiO2+6HF=H2SiF6+2X。下列说法错误的是( )
A.生成物X的化学式是H2O
B.H2SiF6中硅元素显+4价
C.该反应是复分解反应
D.地壳中硅元素含量仅次于氧元素
7.(3分)下列事例中,改变物体内能的途径与其他三项不同的是( )
A.柴火烧水 B.压缩空气发热
C.冬天搓手取暖 D.钻木取火
8.(3分)杭州亚运会开幕式上,“数实结合”的点火方式点燃了开幕式的高光时刻。亚运会主火炬塔首次使用废碳再生的“绿色甲醇”作为燃料,实现了循环内的零排放。下面是“绿色甲醇”的转化方法:在催化剂作用下可实现二氧化碳高效转化为甲醇( )
A.图中只有甲是氧化物
B.生成丙和丁的质量比16:9
C.反应前后各元素的化合价无变化
D.反应前后,分子种类和数目均不变
9.(3分)废铜的回收利用意义重大,我国提出废铜回收率要达到70%的目标。小明设计如图的实验回收含铜垃圾,据图完成问题。
实验步骤②,也可以用一氧化碳代替氢气,由此推测一氧化碳具有( )
A.导热性 B.氧化性 C.导电性 D.还原性
10.(3分)哈尔滨、杭州等地将打造低真空超高速磁浮飞行巴士,时速可达1000公里以上。磁浮飞行巴士采用能量回收制动方式,巴士到站前停止动力供应,内部线圈切割磁感线产生电流,部分机械能转化为电能进行回收。下列四幅图中能反映能量回收原理的是( )
A.
B.
C.
D.
11.(3分)北仑中心充电站安装了新能源汽车充电桩,被称为雨城泊车“天花板”。下列说法正确的是( )
A.安装充电桩时,可以不连接地线
B.有经验的电工在安装充电桩时不必断开电路
C.充电桩为汽车充电时,将电能转化为化学能
D.充电桩起火,应迅速浇水扑灭
12.(3分)豌豆果实成熟后豆荚会突然炸裂开,同时种子被弹射出去,我们把这种传播种子的方式称为弹力传播。在种子被弹射出去至落到地面的过程中( )
A.豌豆弹射出去瞬间,所受的弹力等于重力
B.豌豆在空中飞行时,豆荚没有对豌豆做功
C.豌豆在空中飞行时,动能先增大后减小
D.豌豆弹射过程中,豌豆的机械能始终不变
13.(3分)用图象表示化学变化能提升思维方式,以下四个图象对应的变化过程正确的是( )
A.向稀盐酸中滴加过量的氢氧化钠溶液
B.浓硫酸长时间露置于空气中
C.向NaOH和BaCl2的混合溶液中加入足量的稀硫酸
D.向足量的硫酸铜溶液中加入铁和镁固体混合物
14.(3分)如图所示家庭电路中的某一部分,电工师傅按下面的顺序进行检测:①闭合S1,灯L1亮;②断开S1,闭合S2,灯L2不亮;③再用测电笔测a、b、c、d四个接线点,发现只有在c点氖管不发光。若电路中只有一处故障( )
A.灯L2短路 B.灯L2所在支路开路
C.c、d两点间开路 D.c点左侧的零线开路
15.(3分)体育中考测试时,小科选择了引体向上的项目,如图所示。他想要测量自己做“引体向上”时的功率,不需要测量的是( )
A.自身的质量
B.每次身体上升的高度
C.单杠的高度
D.完成“引体向上”的时间
16.(3分)如图所示,两只灯泡L1和L2上分别标有“6V4W”和“3V 1W”字样,将它们串联后接在电压可在3~6V之间调节的电源上,闭合开关S,则下列说法正确的是( )
A.通过灯L1的电流大于通过灯L2的电流
B.当电源电压调节到6V时,灯L1正常发光
C.在调节电源电压的过程中,灯L1始终比灯L2亮
D.在调节电源电压的过程中,两灯的功率变化量相等
17.(3分)小科按图示操作进行酸和碱反应的实验,下列有关分析正确的是( )
A.①中盛放NaOH溶液的试剂瓶瓶塞甲是玻璃塞
B.③反应过程中溶液由红色变为无色
C.⑤中稀释浓硫酸时,倒入的乙物质是水
D.⑥中酚酞试液用完后,滴管及时清洗
18.(3分)某科学兴趣小组在课余时间做了“开门大吉”的游戏,其规则是:每把钥匙代表一种试剂,每扇门代表需要鉴别的两种溶液,钥匙就能把门打开(每把钥匙只能使用一次),下列能够依次将四扇门打开的钥匙顺序是( )
A.①②③④ B.④②③① C.④③②① D.①③②④
19.(3分)如图是探究“电流通过导体时产生热量的多少跟什么因素有关”的实验装置。两个相同的透明容器中密封着等量且初温相同的空气,甲、乙两U形管中液面初始状态是等高相平,通电一段时间后液面的高度如图所示。以下说法错误的是( )
A.通电后电阻丝的内能增大是通过电流做功实现的
B.实验可以得出电流通过电阻产生的热量多少与电流大小有关
C.本实验利用U形管内液面的高度差反映产生热量的多少,这种方法是转换法
D.如果将乙图上方5Ω的电阻也放在右边的容器内,重复上述实验,一段时间后,乙管内液面的高度差比甲更大
20.(3分)模型能够直观反映化学变化的结果。将一定质量的镁条放入某一溶液(如图),其溶质硫酸锌和硫酸亚铁的质量相同,充分反应后烧杯内固体的组成和质量大小关系不可能的是( )
A. B.
C. D.
二、填空题(本题共5题,每空2分,共26分)
21.(6分)现有盐酸、浓硫酸、熟石灰、氯化钠、蛋白质和塑料六种物质,请回答下列问题:
(1)溶于水会放出大量热的是 。
(2)属于天然高分子化合物的是 。
(3)常用来改良酸性土壤的是 。
22.(4分)向稀盐酸中加入足量的金属镁至反应完全,反应的微观模型如图所示。
(1)写出该反应的化学方程式 。
(2)图中的“”“”“”表示溶液中由溶质电离产生的不同离子,则“”表示 。(填写离子符号)
23.(6分)如图甲所示为我国古代发明的取火器的模型图,把木制推杆迅速推入牛角套筒时,杆前端的艾绒立刻燃烧起来 的方式,使筒内空气内能 ,温度升高,达到艾绒的着火点。如图乙所示为单缸四冲程汽油机工作过程中的四个冲程,其中 (选填字母)与上述套筒内空气温度升高过程中能量的转化是一致的。
24.(4分)电脑的中央处理器(CPU),工作时发热显著,常采用铝合金散热片与风扇组合冷却。某笔记本电脑CPU正常工作功率为45W,CPU消耗电能 J。该散热片工作时利用了金属良好的 性。
25.(6分)每年校运动会中都会有跳远、实心球等传统项目。
(1)如图甲,小科在跳远比赛中助跑是为了增大 (选填“惯性”或“动能”),在最高点处 (选填“有”或“没有”)动能。
(2)如图乙是小科同学在投掷实心球的场景,若不计空气阻力,实心球刚脱离手时(A处) C处的动能(选填“大于”“小于”或“等于”)。
三、实验探究题(本题共6小题,每空2分,共42分)
26.(6分)小科利用铁架台、杠杆、钩码和弹簧测力计等器材探究杠杆的平衡条件,实验使用的钩码质量均相等,杠杆上每格长度均相等。
(1)当杠杆静止时如图甲所示,为了方便测量力臂,需要调节杠杆在水平位置平衡 (选填“左”或“右”)调节。
(2)在图乙所示的A、B位置各增加一个钩码,杠杆将会 (选填“仍然平衡”、“左端下沉”或“右端下沉”)。
(3)如图丙所示,用弹簧测力计先后在a、b位置拉杠杆上同一点C,杠杆都在水平位置平衡a,在b位置斜向上的拉力为Fb,则Fa Fb(选填“大于”、“等于”或“小于”)。
27.(8分)在学习了质量守恒定律后,某同学设计了以下几组实验:
(1)上述实验可以用来验证质量守恒定律的有 。(可多选)
(2)实验A中硫酸铜溶液与烧杯中铁粉混合后充分反应,过滤,往滤渣中加入足量的稀盐酸 。
(3)实验D中,若将稀盐酸逐滴滴入烧杯中时,混合物中4种离子(分别用a、b、c、d表示),当滴入稀盐酸的质量在哪个点(选填“甲、乙、丙”)时恰好完全反应 。
28.(6分)图甲是小科的哥哥测定小灯泡额定功率的电路,小灯泡上标有“2.5V”字样。
(1)测小灯泡电压的电压表有“0﹣3V”、“0﹣15V”两个量程,小科的哥哥正确选用了“ ”量程。
(2)闭合开关,移动滑动变阻器滑片,使电压表的示数为2.5V 。
(3)小科发现,与我们教材中测小灯泡电功率的电路相比,哥哥的实验电路多了一根导线 。(用图甲中导线旁的字母表示)
29.(8分)小科利用以下“认识物质性质“的思维模型,在老师的指导下学习未知气体X的性质。
(1)变化→性质:小科用图甲装置进行实验,向左侧塑料瓶里倒入足量的气体X,观察到试纸A不变红
(2)性质→变化:通过学习知道,气体能与氢氧化钠反应,且不产生其他气体。如图乙,反应结束后打开止水夹。预测将出现的现象 ,并写出对应的原因: 。
(3)性质→应用:根据以上性质,若要收集一瓶干燥的气体X,将气体X干燥后 (选填字母)进行收集。
30.(6分)某固体物质可能含有Na2SO4、Na2CO3、CaCl2、KCl和KOH中的一种或几种。为探究其组成,流程和现象记录如图:
(1)根据实验现象可知,固体物质中一定含有 ,一定不含有 。
(2)取无色溶液B,依次滴加AgNO3溶液和稀HNO3,有白色沉淀产生,通过该实验现象能否说明原固体中含有KCl,并说明理由 。
31.(8分)为了比较水和食用油的吸热能力,小科用两个相同的装置做了如图所示的实验。
物质 质量/g 初始温度/℃ 加热时间/min 最后温度/℃
水 60 20 6 42
食用油 60 20 6 62
实验数据记录如表。
(1)实验中,加热相同的时间,水吸收的热量 食用油吸收的热量(选填“大于”、“小于”或“等于”)。
(2)加热结束时,若不考虑蒸发,则水的内能比加热前 (选填“大”或“小”)。
(3)实验表明, (选填“水”或“食用油”)吸热的能力更强。
(4)若水的比热容为4.2×103J/(kg ℃),则食用油的比热容为 J/(kg ℃)。
四、解答题(本题共5小题,第32题4分,第33题6分,第34、35题各7分,第36题8分,共32分)
32.(4分)汽泡爽是一种冲调饮料。其主要原料为柠檬酸(C6H8O7)和小苏打(NaHCO3);使用时将一包汽泡爽粉末倒入玻璃杯中,加入200mL冷水,待粉末完全溶解,就得到一杯果味饮料。
(1)小苏打(NaHCO3)从组成上看,它属于一种 。
A.酸
B.碱
C.盐
D.氧化物
(2)一个柠檬酸分子(C6H8O7)由 个原子构成。
33.(6分)2022年北京冬奥会成功举办。使用的高科技场馆设施环保又节能,如:部分场馆采用地暖供热;氢能大巴首次上岗服务。开幕式上中国式浪漫惊艳世界;中国运动员的拼搏精神激励世人。
(1)地暖工作时水从热源吸热后,顺着管路流动,将热传至室内各个房间。地暖利用了水比热容大的性质 (填序号)选项也利用了该性质。
A.用水洗去衣服上的脏东西
B.将水用作汽车发动机的冷却液
C.用水扑灭大火
D.电解水产生氢气和氧气
(2)氢气的热值是1.4×108J/kg,氢能大巴在某次服务中消耗了2kg的氢气,则2kg氢气完全燃烧时释放的热量为 J(已知Q热量=mq热值)
(3)冰立方雪花台中的LED灯的电功率仅为同等亮度白炽灯的,请从能量转化效率的角度分析,使用LED灯照明比使用白炽灯更节能是因为 。
34.(7分)如图甲所示的装置,A是重12N的空吊篮,小科将A提升到高处,A上升的速度v随时间t变化关系如图丙所示。忽略绳重及摩擦,求:
(1)1~2s内拉力F的功率。
(2)动滑轮所受的重力。
(3)用此装置匀速提升34N重物时的机械效率(重物放在空吊篮内)。
35.(7分)某滚桶洗衣机自带加热功能,其洗衣过程分“加热水”、“保温洗涤”“脱水”三种状态,如图是其简化电路图1、R2的阻值分别为24.2Ω和242Ω。
(1)当开关置于2位置时,R2与电动机并联,此时洗衣机的工作状态是 (选填“加热水”、“保温洗涤”或“脱水”)。
(2)关闭其他用电器,只有洗衣机处于“脱水”状态,脱水一段时间后(kW h)的电能表转盘转过150转,则在这段时间内 焦耳。
(3)洗衣机处于“加热水”状态时(R1与R2并联),正常工作的功率为多少?
36.(8分)在探究酸、碱性质时,小科的操作过程如图甲所示,烧杯中固体质量与加入溶液的质量关系如图乙所示。请回答下列问题:
(1)根据图像分析,开始加入氢氧化钠溶液直到过量的过程,烧杯内的现象是 。
(2)求实验所用稀盐酸的溶质质量分数。
(3)当反应进行到图乙中A点时,求加入的氢氧化钠溶液的质量。
2023-2024学年浙江省宁波市北仑区九年级(上)期末科学试卷
参考答案与试题解析
一、选择题(本题共20小题,每小题3分,共60分。请选出每小题中一个符合题意的选项,不选、错选均不给分)
1.(3分)习近平总书记在党的二十大报告中提出:积极稳妥推进碳达峰、碳中和践行绿色发展理念,保护城市之肺为共建天蓝、地绿、水清的美丽家园,下列措施不可取的是( )
A.生活垃圾分类回收,垃圾资源化
B.加大空气质量检测,改善环境状况
C.大力开展五水共治,保护水资源
D.大量使用化肥农药,提高粮食产量
【答案】D
【解答】解:习近平总书记在党的二十大报告中提出:积极稳妥推进碳达峰、碳中和践行绿色发展理念、地绿,应该将生活垃圾分类回收;加大空气质量检测;大力开展五水共治;化肥和农药的使用,但是会造成水体和土壤污染,应合理使用。
故选:D。
2.(3分)《易经》记载:“泽中有火”“上火下泽”。这是对甲烷气体在湖泊池沼水面上起火现象的描述。下列有关甲烷的叙述,正确的是( )
A.从分类上看:属于无机物
B.从变化上看:燃烧只生成一种物质
C.从性质上看:具有助燃性
D.从使用上看:点燃前要检验气体的纯度
【答案】D
【解答】解:A、甲烷是一种含碳元素的化合物,说法错误;
B、甲烷燃烧生成二氧化碳和水,故不合题意;
C、甲烷具有可燃性,说法错误;
D、甲烷具有可燃性,因此点燃前要检验气体的纯度,故符合题意。
故选:D。
3.(3分)科学实验要规范操作,下列初中科学实验操作你认为不正确的是( )
A.二氧化碳的验满 B.倾倒液体
C.检验气密性 D.用纸槽取用粉末
【答案】A
【解答】解:A、二氧化碳验满时,故本选项操作错误;
B、取用液体时:①试剂瓶瓶口要紧挨试管口;②标签向着手心;③瓶塞倒放桌面上,从而污染药品;
C、检查装置的气密性时,然后用手握住试管外壁,故本选项操作正确;
D、固体粉末放入试管内时,然后放入平置的试管内,故本选项操作正确。
故选:A。
4.(3分)“灰汁团”是浙江传统小吃,制作过程中要用到大米和“灰汁”。“灰汁”制取方法如资料卡所示。下列说法错误的是( )
资料卡 传统方法:稻草烧灰一加水溶解→静置沉淀→过滤取汁
现代方法:将食用碱(纯碱和小苏打的混合物)与水按一定比例混合成汁
A.大米中含有的淀粉属于有机物
B.稻草燃烧属于化学变化
C.传统方法制得的“灰汁”是混合物
D.现代方法制得的“灰汁”不能使酚酞试液变红色
【答案】D
【解答】解:A、大米中含有的淀粉是一种含碳元素的化合物,说法正确;
B、稻草燃烧过程中有新物质生成,说法正确;
C、传统方法制得的“灰汁”中含有多种物质,说法正确;
D、现代方法制得的“灰汁”中含有碳酸钠和碳酸氢钠,能使酚酞试液变红色。
故选:D。
5.(3分)节约用电,从我做起。下列用电器正常工作时,在相同时间内消耗电能最多的是( )
A.台灯 B.液晶电视
C.笔记本电脑 D.空调
【答案】D
【解答】解:这四个用电器工作时,空调机的功率是最大的,由W=Pt可知。
故选:D。
6.(3分)继麒鳞芯片后,华为发布业界最高性能处理器鲲鹏920,摆脱了对国外产品的依赖。芯片主要以高纯度的单质硅(Si),在半导体硅元件生产中,常用氢氟酸(HF),反应原理为SiO2+6HF=H2SiF6+2X。下列说法错误的是( )
A.生成物X的化学式是H2O
B.H2SiF6中硅元素显+4价
C.该反应是复分解反应
D.地壳中硅元素含量仅次于氧元素
【答案】C
【解答】解:A、由SiO2+6HF═H3SiF6+2X可知,反应前后硅原子都是4个,反应后应该是2个,反应前氢原子是6个,其中8个包含在2X中,因此生成物X的化学式是H2O,该选项说法正确;
B、H3SiF6中氢元素化合价是+1,氟元素化合价是﹣3,硅元素显+4价;
C、该反应不是两种化合物相互交换成分生成新的两种化合物,该选项说法不正确;
D、地壳中硅元素含量仅次于氧元素;
故选:C。
7.(3分)下列事例中,改变物体内能的途径与其他三项不同的是( )
A.柴火烧水 B.压缩空气发热
C.冬天搓手取暖 D.钻木取火
【答案】A
【解答】解:
A、柴火烧水是通过热传递的方式改变内能的;
BCD、压缩空气发热、钻木取火都是做功使物体的内能增加的;
显然A选项与其它三个选项改变物体内能的方式不同。
故选:A。
8.(3分)杭州亚运会开幕式上,“数实结合”的点火方式点燃了开幕式的高光时刻。亚运会主火炬塔首次使用废碳再生的“绿色甲醇”作为燃料,实现了循环内的零排放。下面是“绿色甲醇”的转化方法:在催化剂作用下可实现二氧化碳高效转化为甲醇( )
A.图中只有甲是氧化物
B.生成丙和丁的质量比16:9
C.反应前后各元素的化合价无变化
D.反应前后,分子种类和数目均不变
【答案】B
【解答】解:由微观反应示意图可知,在催化剂的催化作用下,该反应的化学方程式是:CO2+3H8CH3OH+H2O;
A、氧化物是由两种元素组成,该反应中的二氧化碳和水均属于氧化物;
B、由化学方程式可知,故B说法正确;
C、反应物中的氢气是一种单质,反应后,氢元素的化合价不为零,氢元素的化合价一定发生改变;
D、由化学方程式可知,分子种类和数目均发生改变。
故选:B。
9.(3分)废铜的回收利用意义重大,我国提出废铜回收率要达到70%的目标。小明设计如图的实验回收含铜垃圾,据图完成问题。
实验步骤②,也可以用一氧化碳代替氢气,由此推测一氧化碳具有( )
A.导热性 B.氧化性 C.导电性 D.还原性
【答案】D
【解答】解:在实验步骤②中氢气与氧化铜反应生成铜和水,氢气夺取氧化铜中的氧,具有还原性,由此推测一氧化碳具有还原性,D正确。
故选:D。
10.(3分)哈尔滨、杭州等地将打造低真空超高速磁浮飞行巴士,时速可达1000公里以上。磁浮飞行巴士采用能量回收制动方式,巴士到站前停止动力供应,内部线圈切割磁感线产生电流,部分机械能转化为电能进行回收。下列四幅图中能反映能量回收原理的是( )
A.
B.
C.
D.
【答案】B
【解答】解:线圈随车轮转动并在磁场中切割磁感线产生感应电流,将机械能转化为电能;
A、该装置是电磁铁,故A不符合题意;
B、闭合电路的部分导体在磁场中做切割磁感线运动时,这种现象叫电磁感应现象,故B符合题意;
C、这是奥斯特实验,故C不符合题意;
D、通电导体在磁场中要受到力的作用,故D不符合题意。
故选:B。
11.(3分)北仑中心充电站安装了新能源汽车充电桩,被称为雨城泊车“天花板”。下列说法正确的是( )
A.安装充电桩时,可以不连接地线
B.有经验的电工在安装充电桩时不必断开电路
C.充电桩为汽车充电时,将电能转化为化学能
D.充电桩起火,应迅速浇水扑灭
【答案】C
【解答】解:A、安装充电桩时,要接地线;
B、安装充电桩时必须断开电源。
C、充电桩为汽车充电时,故C正确。
D、万一有充电桩起火,故B不符合安全用电要求;
故选:C。
12.(3分)豌豆果实成熟后豆荚会突然炸裂开,同时种子被弹射出去,我们把这种传播种子的方式称为弹力传播。在种子被弹射出去至落到地面的过程中( )
A.豌豆弹射出去瞬间,所受的弹力等于重力
B.豌豆在空中飞行时,豆荚没有对豌豆做功
C.豌豆在空中飞行时,动能先增大后减小
D.豌豆弹射过程中,豌豆的机械能始终不变
【答案】B
【解答】解:A.豌豆弹射出去瞬间,受力不平衡,故A错误;
B.豌豆在空中飞行时,没有对豌豆做功;
C.豌豆在空中飞行时,动能先变小后变大,动能一直增大;
D.豌豆弹射过程中,豌豆的机械能增大。
故选:B。
13.(3分)用图象表示化学变化能提升思维方式,以下四个图象对应的变化过程正确的是( )
A.向稀盐酸中滴加过量的氢氧化钠溶液
B.浓硫酸长时间露置于空气中
C.向NaOH和BaCl2的混合溶液中加入足量的稀硫酸
D.向足量的硫酸铜溶液中加入铁和镁固体混合物
【答案】D
【解答】解:A、向稀盐酸中滴加过量的氢氧化钠溶液,pH小于7,酸性越来越弱,溶液呈中性,酸反应完了,溶液呈碱性;故A图像错误;
B、浓硫酸具有吸水性,溶液质量越会增大;
C、向NaOH和BaCl2的混合溶液中加入足量的稀硫酸,硫酸根离子能与钡离子反应生成不溶于酸的硫酸钡沉淀,故C图错误;
D、镁、铁、铜的活动性顺序为:镁>铁>铜,镁先与硫酸铜溶液反应生成铜和硫酸镁2=Cu+MgSO4 可知,每24份质量的镁参加反应生成64份质量的铜;当镁完全反应后,由化学方程式Fe+CuSO4=Cu+FeSO8可知,每56份质量的铁参加反应生成64份质量的铜,但减少的幅度变小,溶液的质量不再减少;
故选:D。
14.(3分)如图所示家庭电路中的某一部分,电工师傅按下面的顺序进行检测:①闭合S1,灯L1亮;②断开S1,闭合S2,灯L2不亮;③再用测电笔测a、b、c、d四个接线点,发现只有在c点氖管不发光。若电路中只有一处故障( )
A.灯L2短路 B.灯L2所在支路开路
C.c、d两点间开路 D.c点左侧的零线开路
【答案】C
【解答】解:闭合S1,灯L1亮,电路中有电流,从保险丝→a→S8→L1→c以及c点左侧的零线都没有断路,故D错误;
断开S1,闭合S8,灯L2不亮,灯L2不亮的原因有两个:一个是断路、一个是短路,
若灯L7短路时,电路的电流会很大,灯泡L1也不会发光,a、b两个接线点上,故A错误;
若灯L2所在支路开路,d点氖管不发光;
若c、d两点间开路5与零线不能构成闭合电路,电路中没有电流,但d点会通过灯泡L2与火线间接相连,试电笔的氖管会发光。
故选:C。
15.(3分)体育中考测试时,小科选择了引体向上的项目,如图所示。他想要测量自己做“引体向上”时的功率,不需要测量的是( )
A.自身的质量
B.每次身体上升的高度
C.单杠的高度
D.完成“引体向上”的时间
【答案】C
【解答】解:做引体向上的功率P===需要测量的物理量是小科的质量、小科做引体向上的时间,故C符合题意。
故选:C。
16.(3分)如图所示,两只灯泡L1和L2上分别标有“6V4W”和“3V 1W”字样,将它们串联后接在电压可在3~6V之间调节的电源上,闭合开关S,则下列说法正确的是( )
A.通过灯L1的电流大于通过灯L2的电流
B.当电源电压调节到6V时,灯L1正常发光
C.在调节电源电压的过程中,灯L1始终比灯L2亮
D.在调节电源电压的过程中,两灯的功率变化量相等
【答案】D
【解答】解:由P=可得
R1===6Ω,R2===9Ω;
A、两灯泡串联2的电流等于通过灯L2的电流,故A错误;
BC、在调节电源电压的过程中2R可知,两灯泡的实际功率相等,故BC错误;
D、两灯泡串联,通过两灯泡的电流变化相同,由P=I4R可知,灯泡功率的变化相同。
故选:D。
17.(3分)小科按图示操作进行酸和碱反应的实验,下列有关分析正确的是( )
A.①中盛放NaOH溶液的试剂瓶瓶塞甲是玻璃塞
B.③反应过程中溶液由红色变为无色
C.⑤中稀释浓硫酸时,倒入的乙物质是水
D.⑥中酚酞试液用完后,滴管及时清洗
【答案】B
【解答】解:A、氢氧化钠溶液能与玻璃的主要成分反应,不能使用玻璃塞。
B、滴有酚酞溶液的氢氧化钠溶液显红色,至恰好完全反应,③反应过程中溶液由红色变为无色。
C、稀释浓硫酸时,同时用玻璃棒不断搅拌;一定不能把水注入浓硫酸中,倒入的乙物质是浓硫酸。
D、滴瓶上的滴管使用后直接插回原瓶,否则试剂瓶中的溶液将被稀释。
故选:B。
18.(3分)某科学兴趣小组在课余时间做了“开门大吉”的游戏,其规则是:每把钥匙代表一种试剂,每扇门代表需要鉴别的两种溶液,钥匙就能把门打开(每把钥匙只能使用一次),下列能够依次将四扇门打开的钥匙顺序是( )
A.①②③④ B.④②③① C.④③②① D.①③②④
【答案】B
【解答】解:由于碳酸钠溶液显碱性,鉴别碳酸钠和氢氧化钠时,检验碳酸根的存在,与氢氧化钠不反应)或④稀盐酸(与碳酸钠反应有气泡生成;鉴别氢氧化钠与氢氧化钙溶液,与氢氧化钠不反应)或③二氧化碳(与氢氧化钙反应有沉淀生成;鉴别氢氧化钙和氯化钙,与氯化钙不反应),与盐酸不反应),顺序为④②③①。
故选:B。
19.(3分)如图是探究“电流通过导体时产生热量的多少跟什么因素有关”的实验装置。两个相同的透明容器中密封着等量且初温相同的空气,甲、乙两U形管中液面初始状态是等高相平,通电一段时间后液面的高度如图所示。以下说法错误的是( )
A.通电后电阻丝的内能增大是通过电流做功实现的
B.实验可以得出电流通过电阻产生的热量多少与电流大小有关
C.本实验利用U形管内液面的高度差反映产生热量的多少,这种方法是转换法
D.如果将乙图上方5Ω的电阻也放在右边的容器内,重复上述实验,一段时间后,乙管内液面的高度差比甲更大
【答案】D
【解答】解:A、电流做功的过程就是电能转化为其它形式能的过程,电阻丝的内能增大是通过电流做功实现的;
B、上图中,容器内两电阻大小相等,通过左侧容器中电阻的电流大于通过右侧容器中电阻的电流,故可以研究电流产生的热量与电流的关系;
C、本实验利用U形管内液面的高度差反映产生热量的多少,故C正确;
D、如果将乙图上方5Ω的电阻也放在右边的容器内,容器内的总电阻小于5欧姆,根据Q=I3Rt可生可知,左侧电阻产生热量多,故D错误。
故选:D。
20.(3分)模型能够直观反映化学变化的结果。将一定质量的镁条放入某一溶液(如图),其溶质硫酸锌和硫酸亚铁的质量相同,充分反应后烧杯内固体的组成和质量大小关系不可能的是( )
A. B.
C. D.
【答案】C
【解答】解:在金属活动性顺序表中镁锌铁的活动性为:镁>锌>铁,将镁条加入硫酸锌和硫酸亚铁的溶液中,反应方程式为Mg+FeSO4=MgSO4+Fe,即每24份质量的镁能置换出56份质量的铁,若镁还有剩余,反应方程式为Mg+ZnSO4=MgSO4+Zn,即每24份质量的镁能置换出65份质量的锌,设等质量为m=0.5mg=0.37mg.
A、由图A知,可能硫酸亚铁完全反应完,则生成的铁和锌的质量可能相等;
B、由图B知,可能硫酸亚铁完全反应完,则生成的铁的质量可能大于生成的锌的质量;
C、由图C知,硫酸亚铁和硫酸锌均反应完全,生成铁的质量一定小于生成锌的质量,故C错误;
D、由图D知,硫酸亚铁和硫酸锌均反应完全,生成铁的质量一定小于生成锌的质量。
故选:C。
二、填空题(本题共5题,每空2分,共26分)
21.(6分)现有盐酸、浓硫酸、熟石灰、氯化钠、蛋白质和塑料六种物质,请回答下列问题:
(1)溶于水会放出大量热的是 浓硫酸 。
(2)属于天然高分子化合物的是 蛋白质 。
(3)常用来改良酸性土壤的是 熟石灰 。
【答案】(1)浓硫酸;
(2)蛋白质;
(3)熟石灰。
【解答】解:(1)浓硫酸溶于水会放出大量热;故答案为:浓硫酸;
(2)蛋白质属于天然高分子化合物;故答案为:蛋白质;
(3)熟石灰是氢氧化钙的俗称,是一种碱,因此常用来改良酸性土壤。
22.(4分)向稀盐酸中加入足量的金属镁至反应完全,反应的微观模型如图所示。
(1)写出该反应的化学方程式 Mg+2HCl=MgCl2+H2↑ 。
(2)图中的“”“”“”表示溶液中由溶质电离产生的不同离子,则“”表示 Mg2+ 。(填写离子符号)
【答案】(1)Mg+2HCl=MgCl2+H2↑;
(2)Mg2+。
【解答】解:(1)向稀盐酸中加入足量的金属镁至反应完全,镁和稀盐酸反应生成氯化镁和氢气2+H2↑。
(2)图中的“”“〇”“”表示溶液中由溶质电离产生的不同离子,由反应的化学方程式可知,反应后溶液中有镁离子和氯离子”表示镁离子,离子符号为:Mg2+。
故答案为:
(1)Mg+2HCl=MgCl2+H6↑;
(2)Mg2+。
23.(6分)如图甲所示为我国古代发明的取火器的模型图,把木制推杆迅速推入牛角套筒时,杆前端的艾绒立刻燃烧起来 做功 的方式,使筒内空气内能 增大 ,温度升高,达到艾绒的着火点。如图乙所示为单缸四冲程汽油机工作过程中的四个冲程,其中 D (选填字母)与上述套筒内空气温度升高过程中能量的转化是一致的。
【答案】做功;增大;D。
【解答】解:(1)把木制推杆迅速推入牛角套筒时,杆前端的艾绒立刻燃烧起来,使筒内空气内能增大,达到艾绒的着火点;
(2)此过程中压缩套筒内空气做功,使套筒内气体的内能增加。在该实验中,与汽油机的压缩冲程的能量转化相同,活塞向上运动,与上述实验过程的能量转化一致。
故答案为:做功;增大;D。
24.(4分)电脑的中央处理器(CPU),工作时发热显著,常采用铝合金散热片与风扇组合冷却。某笔记本电脑CPU正常工作功率为45W,CPU消耗电能 1.62×105 J。该散热片工作时利用了金属良好的 导热 性。
【答案】1.62×105;导热。
【解答】解:正常工作1小时,CPU消耗电能W=Pt=45W×1×3600s=7.62×105J;
该散热片工作时利用了金属良好的导热性。
故答案为:1.62×105;导热。
25.(6分)每年校运动会中都会有跳远、实心球等传统项目。
(1)如图甲,小科在跳远比赛中助跑是为了增大 动能 (选填“惯性”或“动能”),在最高点处 有 (选填“有”或“没有”)动能。
(2)如图乙是小科同学在投掷实心球的场景,若不计空气阻力,实心球刚脱离手时(A处) 小于 C处的动能(选填“大于”“小于”或“等于”)。
【答案】(1)动能;有;(2)小于。
【解答】解:(1)惯性是物体的性质,只与物体的质量有关,则人的惯性不变;经过最高点时人的速度不为零,若动能为零;
(2)若不计空气阻力,实心球的机械能守恒,重力势能较大,C的动能大。
故答案为:(1)动能;有;(2)小于。
三、实验探究题(本题共6小题,每空2分,共42分)
26.(6分)小科利用铁架台、杠杆、钩码和弹簧测力计等器材探究杠杆的平衡条件,实验使用的钩码质量均相等,杠杆上每格长度均相等。
(1)当杠杆静止时如图甲所示,为了方便测量力臂,需要调节杠杆在水平位置平衡 右 (选填“左”或“右”)调节。
(2)在图乙所示的A、B位置各增加一个钩码,杠杆将会 左端下沉 (选填“仍然平衡”、“左端下沉”或“右端下沉”)。
(3)如图丙所示,用弹簧测力计先后在a、b位置拉杠杆上同一点C,杠杆都在水平位置平衡a,在b位置斜向上的拉力为Fb,则Fa 小于 Fb(选填“大于”、“等于”或“小于”)。
【答案】(1)右;(2)左端下沉;(3)小于。
【解答】解:(1)当杠杆静止时,发现左端下沉,此时,直至杠杆在水平位置平衡;
(2)设钩码的重力为G,每一格的长度为L,A,
左侧=3G×3L=8GL,右侧=4G×2L=6GL,
所以左端下沉;
(3)根据杠杆的平衡条件分析,将测力计绕C点从a位置转动到b位置过程中,其阻力臂不变,而动力臂在从a到b的过程逐渐减小,即Fa<Fb。
故答案为:(1)右;(2)左端下沉。
27.(8分)在学习了质量守恒定律后,某同学设计了以下几组实验:
(1)上述实验可以用来验证质量守恒定律的有 ACD 。(可多选)
(2)实验A中硫酸铜溶液与烧杯中铁粉混合后充分反应,过滤,往滤渣中加入足量的稀盐酸 硫酸亚铁,硫酸亚铁、硫酸铜 。
(3)实验D中,若将稀盐酸逐滴滴入烧杯中时,混合物中4种离子(分别用a、b、c、d表示),当滴入稀盐酸的质量在哪个点(选填“甲、乙、丙”)时恰好完全反应 丙,这是因为c表示氢氧根离子数量,随着反应进行,氢离子和氢氧根离子结合生成水分子,当当滴入稀盐酸的质量在丙点时,氢氧根离子数量减小到0,说明氢氧化钠恰好和盐酸完全反应 。
【答案】见试题解答内容
【解答】解:(1)上述实验可以用来验证质量守恒定律的有ACD,B不能。
故填:ACD。
(2)实验A中硫酸铜溶液与烧杯中铁粉混合后充分反应,过滤,没有产生气泡,滤液中溶质的可能组成:硫酸亚铁(铁和硫酸铜恰好完全反应)。
故填:硫酸亚铁,硫酸亚铁。
(3)当滴入稀盐酸的质量在丙点时恰好完全反应,理由:c表示氢氧根离子数量,氢离子和氢氧根离子结合生成水分子,氢氧根离子数量减小到0。
故填:丙,这是因为c表示氢氧根离子数量,氢离子和氢氧根离子结合生成水分子,氢氧根离子数量减小到0。
28.(6分)图甲是小科的哥哥测定小灯泡额定功率的电路,小灯泡上标有“2.5V”字样。
(1)测小灯泡电压的电压表有“0﹣3V”、“0﹣15V”两个量程,小科的哥哥正确选用了“ 0﹣3V ”量程。
(2)闭合开关,移动滑动变阻器滑片,使电压表的示数为2.5V 0.75W 。
(3)小科发现,与我们教材中测小灯泡电功率的电路相比,哥哥的实验电路多了一根导线 b 。(用图甲中导线旁的字母表示)
【答案】(1)0﹣3V;(2)0.75W;(3)b。
【解答】解:(1)小灯泡上标有“2.5V”字样,故电压表选用“2﹣3V”量程;
(2)闭合开关,移动滑动变阻器滑片,此时电流表的示数如图乙所示,分度值0.02A,则小灯泡额定功率为:
P=UI=7.5V×0.2A=0.75W;
(3)原电路图中,滑动变阻器和灯泡并联是错误的,灯泡,电压表并联在灯泡两端,这根导线是b。
故答案为:(1)0﹣4V;(2)0.75W。
29.(8分)小科利用以下“认识物质性质“的思维模型,在老师的指导下学习未知气体X的性质。
(1)变化→性质:小科用图甲装置进行实验,向左侧塑料瓶里倒入足量的气体X,观察到试纸A不变红
(2)性质→变化:通过学习知道,气体能与氢氧化钠反应,且不产生其他气体。如图乙,反应结束后打开止水夹。预测将出现的现象 烧杯中的水倒吸进入烧瓶 ,并写出对应的原因: 气体X与氢氧化钠反应导致瓶内气压减小,大气压将水压入烧瓶 。
(3)性质→应用:根据以上性质,若要收集一瓶干燥的气体X,将气体X干燥后 B或E (选填字母)进行收集。
【答案】(1)气体X的密度比空气大,且能与水反应生成酸性物质;
(2)烧杯中的水倒吸进入烧瓶;气体X与氢氧化钠反应导致瓶内气压减小,大气压将水压入烧瓶;
(3)B或E。
【解答】解:(1)小科用图甲装置进行实验,向左侧塑料瓶里倒入足量的气体X,试纸B(湿润的紫色石蕊试纸)比C(湿润的紫色石蕊试纸)先变红(C在高处,据此推测气体X的性质有密度比空气大;
(2)气体X能与氢氧化钠反应,且不产生其他气体,小科向充满气体X的烧瓶中注入10mL氢氧化钠溶液,造成装置内的压强减小,在外界大气压的作用下;
(3)由上述实验可知,气体X的密度比空气大,可采用向上排空气法。
故答案为:
(1)气体X的密度比空气大,且能与水反应生成酸性物质;
(2)烧杯中的水倒吸进入烧瓶;气体X与氢氧化钠反应导致瓶内气压减小;
(3)B或E。
30.(6分)某固体物质可能含有Na2SO4、Na2CO3、CaCl2、KCl和KOH中的一种或几种。为探究其组成,流程和现象记录如图:
(1)根据实验现象可知,固体物质中一定含有 Na2SO4、Na2CO3 ,一定不含有 CaCl2、KOH 。
(2)取无色溶液B,依次滴加AgNO3溶液和稀HNO3,有白色沉淀产生,通过该实验现象能否说明原固体中含有KCl,并说明理由 步骤②中加入了氯化钡溶液引入了氯离子 。
【答案】见试题解答内容
【解答】解:固体物质溶于水得无色溶液,而碳酸钠和氯化钙反应能够生成沉淀,硫酸钠和氯化钡会生成不溶于酸的硫酸钡沉淀,氢氧化钾。
无色溶液A中加入氯化钡会生成白色沉淀和pH=7的溶液B,所以固体物质中一定不含氢氧化钾,白色沉淀溶于酸会生成气体,所以混合物中一定含有碳酸钠,一定不含氯化钙;
(1)由以上分析可知固体物质中一定含有Na2SO8、Na2CO3,一定没有CaCl7、KOH,可能含有KCl。
(2)取无色溶液B,依次滴加AgNO3和稀HNO3不能检验原固体中是否含有KCl,理由是:步骤②中加入了氯化钡溶液引入了氯离子。
故答案为:(1)Na4SO4、Na2CO2;CaCl2、KOH。
(2)步骤②中加入了氯化钡溶液引入了氯离子。
31.(8分)为了比较水和食用油的吸热能力,小科用两个相同的装置做了如图所示的实验。
物质 质量/g 初始温度/℃ 加热时间/min 最后温度/℃
水 60 20 6 42
食用油 60 20 6 62
实验数据记录如表。
(1)实验中,加热相同的时间,水吸收的热量 等于 食用油吸收的热量(选填“大于”、“小于”或“等于”)。
(2)加热结束时,若不考虑蒸发,则水的内能比加热前 大 (选填“大”或“小”)。
(3)实验表明, 水 (选填“水”或“食用油”)吸热的能力更强。
(4)若水的比热容为4.2×103J/(kg ℃),则食用油的比热容为 2.2×103 J/(kg ℃)。
【答案】(1)等于;(2)大;(3)水;(4)2.2×103。
【解答】解:(1)实验中,加热相同的时间,水吸收的热量等于食用油吸收的热量;
(2)加热结束时,水吸热温度升高,则水的内能比加热前大;
(3)根据表中数据可知,加热6分钟(吸热相同)
42℃﹣20℃=22℃
食用油升高的温度为
62℃﹣20℃=42℃
根据比较吸热能力的方法,水的吸热能力强。
根据Q=cmΔt可知,在质量和升高的温度相同的情况下,则食用油的比热容为
c=×4.3×103J/(kg ℃)=2.8×103J/(kg ℃)。
故答案为:(1)等于;(2)大;(4)2.7×103。
四、解答题(本题共5小题,第32题4分,第33题6分,第34、35题各7分,第36题8分,共32分)
32.(4分)汽泡爽是一种冲调饮料。其主要原料为柠檬酸(C6H8O7)和小苏打(NaHCO3);使用时将一包汽泡爽粉末倒入玻璃杯中,加入200mL冷水,待粉末完全溶解,就得到一杯果味饮料。
(1)小苏打(NaHCO3)从组成上看,它属于一种 C 。
A.酸
B.碱
C.盐
D.氧化物
(2)一个柠檬酸分子(C6H8O7)由 21 个原子构成。
【答案】(1)C;
(2)21。
【解答】解:(1)小苏打(NaHCO3)是由金属离子与酸根离子构成的化合物,属于盐;
(2)一个柠檬酸分子(C6H8O7)是由6个碳原子、8个氢原子和7个氧原子构成的;
故答案为:
(1)C;
(2)21。
33.(6分)2022年北京冬奥会成功举办。使用的高科技场馆设施环保又节能,如:部分场馆采用地暖供热;氢能大巴首次上岗服务。开幕式上中国式浪漫惊艳世界;中国运动员的拼搏精神激励世人。
(1)地暖工作时水从热源吸热后,顺着管路流动,将热传至室内各个房间。地暖利用了水比热容大的性质 B (填序号)选项也利用了该性质。
A.用水洗去衣服上的脏东西
B.将水用作汽车发动机的冷却液
C.用水扑灭大火
D.电解水产生氢气和氧气
(2)氢气的热值是1.4×108J/kg,氢能大巴在某次服务中消耗了2kg的氢气,则2kg氢气完全燃烧时释放的热量为 2.8×108 J(已知Q热量=mq热值)
(3)冰立方雪花台中的LED灯的电功率仅为同等亮度白炽灯的,请从能量转化效率的角度分析,使用LED灯照明比使用白炽灯更节能是因为 LED灯将电能转化为光能的效率更高 。
【答案】(1)B;(2)2.8×108;(3)LED灯将电能转化为光能的效率更高。
【解答】解:(1)地暖利用了水的比热容较大的性质,因此选项B也体现的是这个性质;
(2)2kg氢气完全燃烧时释放的热量Q放=mq=2kg×4.4×108J/kg=7.8×108J;
(3)白炽灯会将电能转化为热能用来发热,而LED灯主要将电能转化为光能。
故答案为:(1)B;(2)3.8×108;(3)LED灯将电能转化为光能的效率更高。
34.(7分)如图甲所示的装置,A是重12N的空吊篮,小科将A提升到高处,A上升的速度v随时间t变化关系如图丙所示。忽略绳重及摩擦,求:
(1)1~2s内拉力F的功率。
(2)动滑轮所受的重力。
(3)用此装置匀速提升34N重物时的机械效率(重物放在空吊篮内)。
【答案】(1)1~2s内拉力F的功率为40W;
(2)动滑轮所受的重力为4N;
(3)用此装置匀速提升34N重物时的机械效率为68%。
【解答】解:(1)由图丙可知1~2s内A的速度vA=8.5m/s,由图甲可知,拉力端移动速度v=nvA=2×4.5m/s=5m/s,由图乙可知3~2s内拉力F=8N,
因此5~2s内拉力F的功率:
P===Fv=8N×2m/s=40W;
(2)因为忽略绳重及摩擦,拉力F=A+G动),
所以动滑轮所受的重力:
G动=nF﹣GA=2×5N﹣12N=4N;
(3)因为忽略绳重及摩擦,C处绳子拉力FC=(G物+GA+G动)=×(34N+12N+4N)=25N,
用此装置匀速提升重物34N时的机械效率:
η=====×100%=68%。
答:(1)1~2s内拉力F的功率为40W;
(2)动滑轮所受的重力为6N;
(3)用此装置匀速提升34N重物时的机械效率为68%。
35.(7分)某滚桶洗衣机自带加热功能,其洗衣过程分“加热水”、“保温洗涤”“脱水”三种状态,如图是其简化电路图1、R2的阻值分别为24.2Ω和242Ω。
(1)当开关置于2位置时,R2与电动机并联,此时洗衣机的工作状态是 保温洗涤 (选填“加热水”、“保温洗涤”或“脱水”)。
(2)关闭其他用电器,只有洗衣机处于“脱水”状态,脱水一段时间后(kW h)的电能表转盘转过150转,则在这段时间内 1.8×105 焦耳。
(3)洗衣机处于“加热水”状态时(R1与R2并联),正常工作的功率为多少?
【答案】(1)保温洗涤;
(2)1.8×105;
(3)洗衣机处于“加热水”状态(R1与R2并联)正常工作的功率为2200W。
【解答】解:(1)由电路图可知,开关置于1位置时,R1与R7并联,电路的总电阻最小,洗衣机处于“加热水”状态,电动机与R2并联,洗衣机处于“保温洗涤”状态,电路中只有电动机工作;
(2)标有3000r/(kW h)的电能表转盘转过150转,消耗的电能:
W==0.05kW h=5.05×3.6×104J=1.8×103J;
(3)开关应置于1位置时,R1与R4并联,电路的总电阻最小,洗衣机处于“加热水”状态,
因并联电路中各支路两端的电压相等,所以
P加热=+=+=2200W。
答:(1)保温洗涤;
(2)1.6×105;
(3)洗衣机处于“加热水”状态(R1与R2并联)正常工作的功率为2200W。
36.(8分)在探究酸、碱性质时,小科的操作过程如图甲所示,烧杯中固体质量与加入溶液的质量关系如图乙所示。请回答下列问题:
(1)根据图像分析,开始加入氢氧化钠溶液直到过量的过程,烧杯内的现象是 产生蓝色沉淀 。
(2)求实验所用稀盐酸的溶质质量分数。
(3)当反应进行到图乙中A点时,求加入的氢氧化钠溶液的质量。
【答案】(1)产生蓝色沉淀。
(2)7.3%。
(3)162.5g。
【解答】解:(1)氢氧化钠和氯化铜反应生成蓝色沉淀氢氧化铜和氯化钠,烧杯内的现象是产生蓝色沉淀。
故答案为:产生蓝色沉淀。
(2)设与18g氧化铜反应的氯化氢质量是x,反应生成氯化铜质量是y。
CuO+2HCl═CuCl2+H7O
80 73
18g x y
= =
x=16.425g y=30.375g
所用稀盐酸的溶质质量分数是×100%=7.3%
答:所用稀盐酸的溶质质量分数是4.3%。
(3)设过量的100g稀盐酸消耗氢氧化钠质量为z。
NaOH+HCl═NaCl+H2O
40 36.5
z 100g×7.3%
=
z=3g
设30.375g氯化铜消耗氢氧化钠质量是m。
CuCl2+2NaOH=5NaCl+Cu(OH)2↓
135 80
30.375g m
=
m=18g
反应进行到图乙中A点时,加入的氢氧化钠溶液的质量是(8g+18g)÷16%=162.3g
答:反应进行到图乙中A点时,加入的氢氧化钠溶液的质量是162.5g。
同课章节目录
