2024年中考化学复习-流程图题 课件(共81张PPT)
文档属性
| 名称 | 2024年中考化学复习-流程图题 课件(共81张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-16 00:00:00 | ||
图片预览




文档简介
(共81张PPT)
中考化学流程图题
典题精析
考点 1 回收利用型流程图题
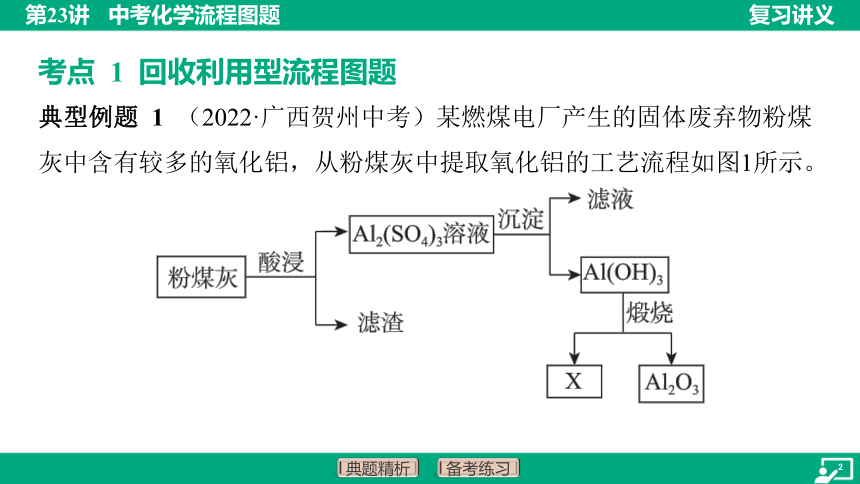
典型例题 1 (2022·广西贺州中考)某燃煤电厂产生的固体废弃物粉煤灰中含有较多的氧化铝,从粉煤灰中提取氧化铝的工艺流程如图1所示。
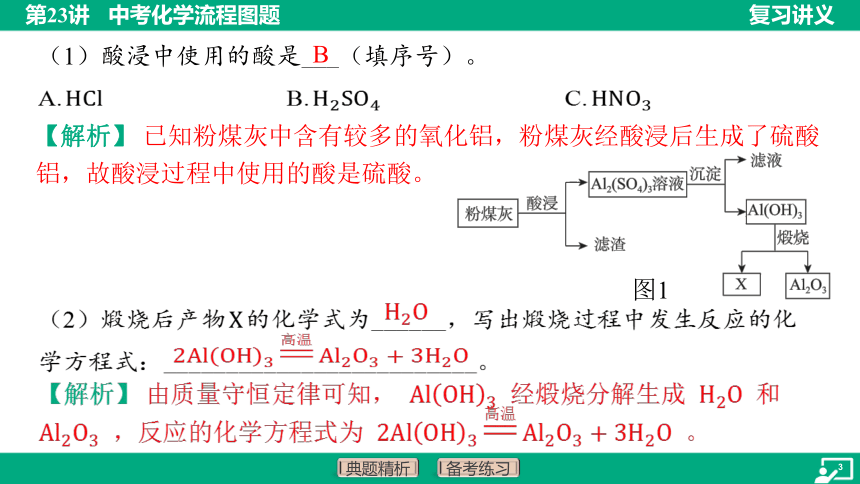
(1)酸浸中使用的酸是___(填序号)。
B
A. B. C.
(2)煅烧后产物 的化学式为______,写出煅烧过程中发生反应的化
学方程式:_________________________。
【解析】 已知粉煤灰中含有较多的氧化铝,粉煤灰经酸浸后生成了硫酸铝,故酸浸过程中使用的酸是硫酸。
图1
【解析】 由质量守恒定律可知, 经煅烧分解生成 和 ,反应的化学方程式为 。
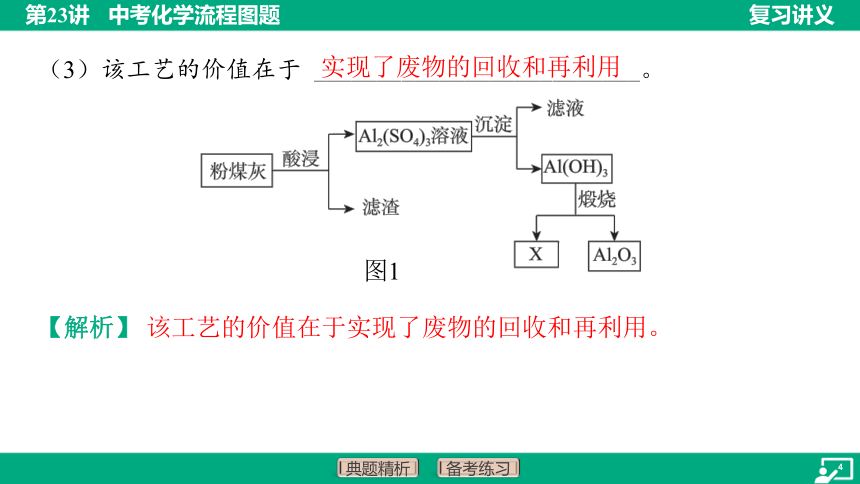
(3)该工艺的价值在于 __________________________。
实现了废物的回收和再利用
图1
【解析】 该工艺的价值在于实现了废物的回收和再利用。
思维点拨
(1)化工流程图中箭头指入的一般是投的料(即反应物),箭头指出的一般是生成物(包括主产物和副产物),返回的箭头一般是指被循环利用的物质。
(2)对原料进行预处理的常用方法及其作用。
①研磨、粉碎、喷淋:增大反应物的接触面积,提高反应速率。
②水浸:与水接触反应或溶解,分离水溶性和非水溶性物质。③酸浸:与酸接触反应或溶解,如溶解金属或金属氧化物。
④灼烧:除去可燃性杂质或使原料初步转化。
⑤煅烧:使一些杂质在高温下氧化、分解,如煅烧石灰石。
针对训练
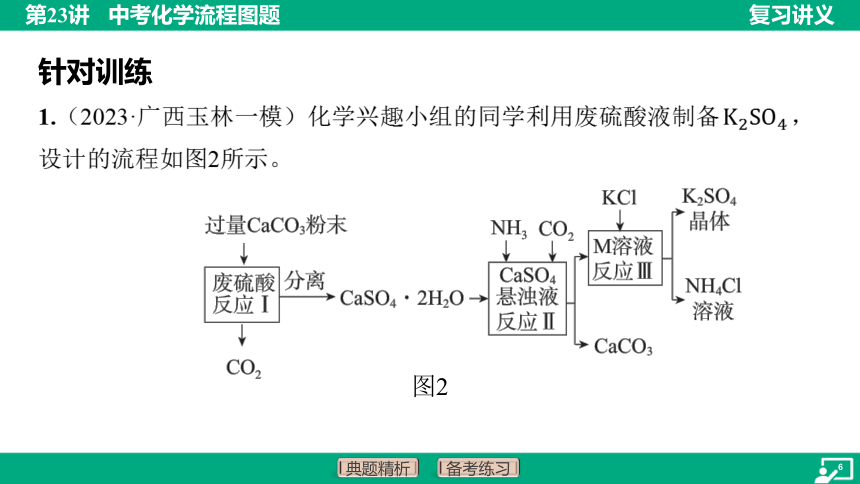
1.(2023·广西玉林一模)化学兴趣小组的同学利用废硫酸液制备 ,
设计的流程如图2所示。
图2
图2
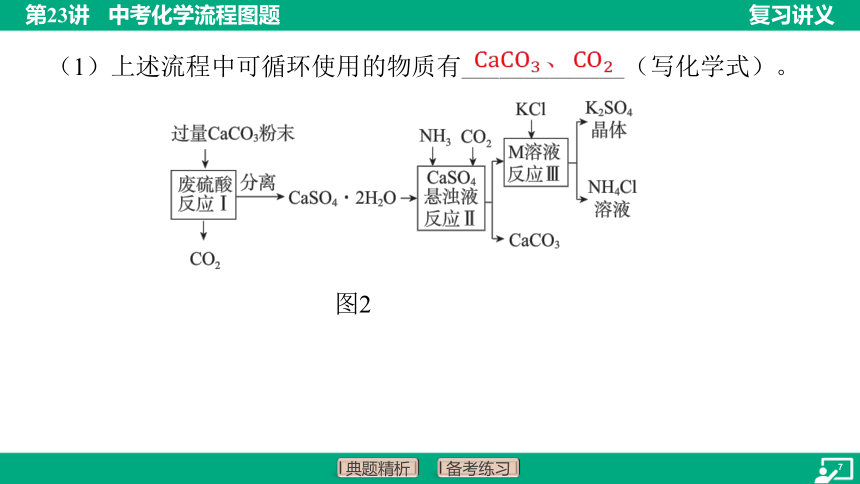
(1)上述流程中可循环使用的物质有_____________(写化学式)。
、
(2)反应Ⅱ中的温度控制在
,目的是_______
(填序号)。
A.提高温度至 ,增大反应速率
B.增大 的溶解度
C.温度不高于 ,防止氨水分解
A、
图2
图2
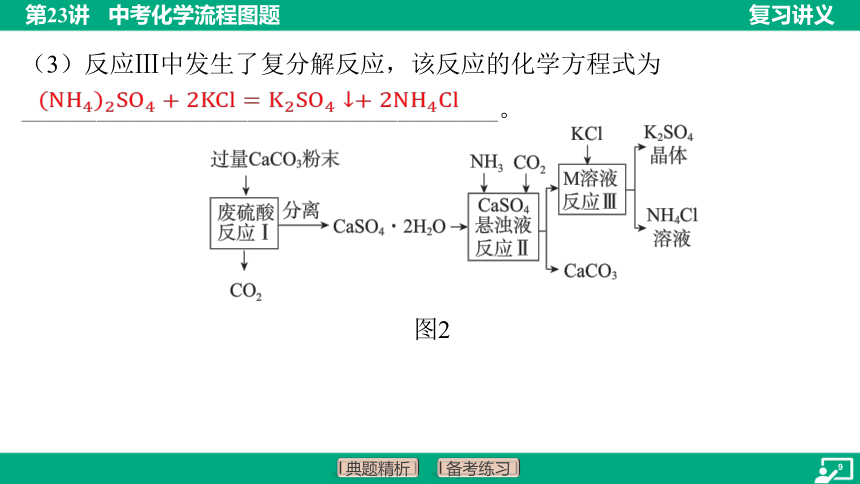
(3)反应Ⅲ中发生了复分解反应,该反应的化学方程式为
______________________________________。
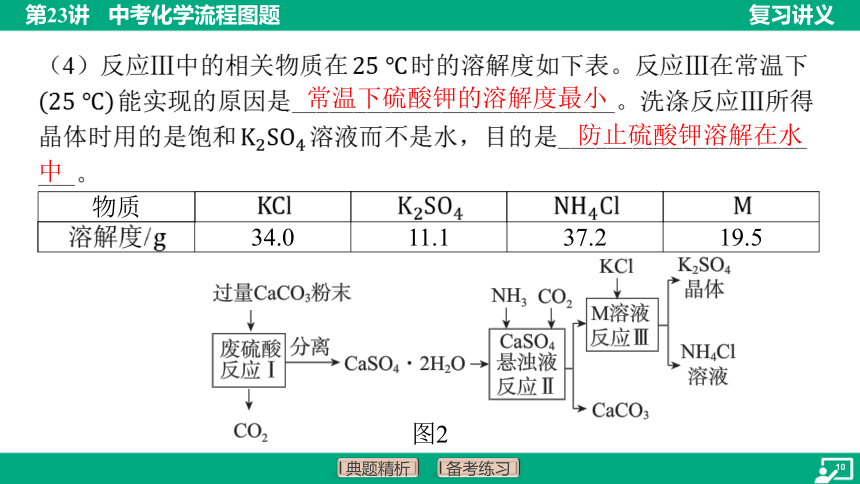
(4)反应Ⅲ中的相关物质在 时的溶解度如下表。反应Ⅲ在常温下
能实现的原因是__________________________。洗涤反应Ⅲ所得
晶体时用的是饱和 溶液而不是水,目的是____________________
___。
物质
溶解度/ 34.0 11.1 37.2 19.5
常温下硫酸钾的溶解度最小
防止硫酸钾溶解在水中
图2
图3
2.(2023·广西防城港二模)
波尔多液是一种保护性的杀
菌剂,有效成分为碱式硫酸
铜。它具有杀菌谱广、持效
期长、病菌不易产生抗药性、
对人和畜低毒等特点。波尔
多液是历史上使用时间最长的一种杀菌剂。图3是利用废弃铜料(只含
有铜和一定量的铁)和石灰石制备波尔多液的流程。请回答下列问题:
图3
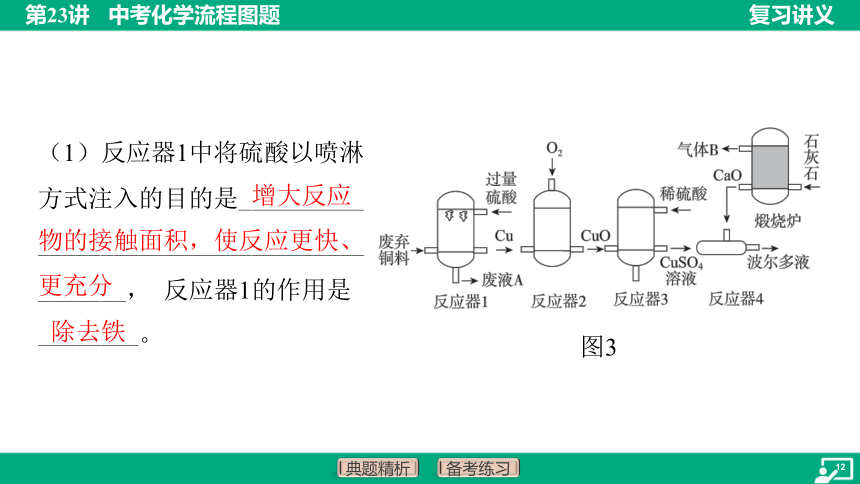
(1)反应器1中将硫酸以喷淋
方式注入的目的是__________
__________________________
_______, 反应器1的作用是
________。
增大反应物的接触面积,使反应更快、更充分
除去铁
(2)反应器4中发生反应的化学方程式为____________________________________________________________________(任写一个)。
(3)气体B的化学式为______。
[或
图3
图3
(4)反应器3和反应器4的内壁材质不能为铁或铝,原因是______________________。
硫酸铜能与铁、铝反应
考点 2 制备与生产型流程图题
典型例题 2 (2023·广西中考)柠檬酸亚铁 是一种易被吸收
的补血剂。利用硫酸厂的废渣(主要含 、 ,还有少量 )
制备柠檬酸亚铁的工艺流程如图4所示。请回答下列问题:
图4
资料 ;
。
资料 不溶于水,也不与稀硫酸反应。
(1)柠檬酸亚铁进入人体肠道后以________(填阳离子符号)的形式被吸收,从而达到补血的效果。
【解析】柠檬酸亚铁进入人体肠道后被电离为亚铁离子和柠檬酸根离子,其 中 被人体所吸收,达到补血的效果。
(2)固体C的成分是________。
图4
【解析】 步骤①中氧化铁与硫酸反应生成硫酸铁和水,四氧化三铁与硫酸反应生成硫酸铁、硫酸亚铁和水,步骤②中铁与硫酸铁反应生成硫酸亚铁,铁与硫酸反应生成硫酸亚铁和氢气,因此固体C的成分是 和剩余的 。
图4
【解析】 步骤①中氧化铁与硫酸反应生成硫酸铁和水,属于复分解反应;步骤②中铁与硫酸铁反应生成硫酸亚铁,属于化合反应,铁与硫酸反应生成硫酸亚铁和氢气,属于置换反应;步骤③中碳酸钠与硫酸亚铁反应生成硫酸钠和碳酸亚铁沉淀,属于复分解反应;步骤④中碳酸亚铁与柠檬酸反应生成柠檬酸亚铁、水和二氧化碳,属于复分解反应。
(3)步骤①②③④中涉及置换反应的是________(填序号)。
图4
(4)步骤③中发生反应的化学方程式为___________________________________________________。
(5)“一系列操作”中,将柠檬酸亚铁晶体与溶液分离的操作是________。
【解析】“一系列操作”中,将柠檬酸亚铁晶体与溶液分离的操作是过滤。
图4
思维点拨
制备与生产型流程图题的解题思路:①从题干获取有用信息,了解生产的产品。②分析流程中的每一个步骤,了解反应物是什么,发生了什么反应,该反应对制造产品有什么作用。要抓住一个关键点,即一切反应或操作都是为了获得产品。③从问题中获取信息,帮助解题。
针对训练
1.(2023·广西柳州三模)广西有着丰富的重晶石矿产资源。氯化钡是一
种可溶性重金属盐,广泛应用于化工领域。图5为工业上以重晶石(主
要成分为 ,杂质为 )为原料制备氯化钡晶体
的工艺流程。
图5
请回答下列问题:
已知: 。
能与水反应生成碱。
(1)流程图中过滤的作用是________________________。
将不溶性固体与液体分离
图5
图6
(2)“焙烧”工序中,焦炭与杂质 也会发生反应,写出反应的化学方程式:____________________________。硫酸钡转化率与温度的关系如图6所示,则反应的最佳温度约为_________。
(3)“酸溶”工序中,硫化钡 与盐酸发生的反应为
,写出 的化学式:_______。
图5
(4)气体 的成分除 和少量挥发出的 、水蒸气外,还含有
______(填名称)。
氢气
图5
2.(2023·广西崇左二模)金属锌在冶金、化学电源生产等方面具有重要
作用。以闪锌矿(主要含 ,还含有 和少量 、 、 等
杂质)为原料制备金属锌的流程如图7所示。请回答下列问题:
图7
已知: 不溶于水且不与硫酸反应。②常温下 难溶于水
和稀硫酸。
图7
(1)“焙烧”工序中金属硫化物转
化成金属氧化物。焙烧尾气必须进
行净化处理的原因是____________
_____________________________。
反应生成的 会污染空气(或形成酸雨)
(2)“溶浸”工序产生的滤渣的主要成分除 外,还有________。
硫酸铅
(3)“氧化除杂”工序的主要反应为 ,则 、 、 依次是_________。
6、4、
图7
(4)“还原除杂”工序利用了
锌粉与 的反应,该反应
的化学方程式为____________
_____________。
(5)“电解”工序中的反应为 ,
则电解得到的溶液可返回______(填“焙烧”“溶浸”“氧化除杂”或“还原除
杂”)工序继续使用。
溶浸
考点 3 分离、提纯和除杂型流程图题
图8
典型例题 3 (2022·广西河池中考)
五氧化二钒 广泛用于化工
行业。工业钒废催化剂中主要含硫
酸氧钒 和少量的 、
等杂质,现要除去钒废催化剂
中的杂质并得到 固体,其流
程如图8所示。请回答下列问题:
(1) 中硫元素的化合价为____。
(2)操作 的名称是______,废渣的主要成分为______。
过滤
图8
【解析】“ 已知 中钾
元素为 价,氧元素为
价,设硫元素的化合价为 ,则有 ,解得 。
【解析】操作 是将固体与液体分离的
操作,是过滤。已知工业上的钒废催化剂
中含有少量的 、 等杂质,因 不溶于水,故经操作 分离出的废渣的主要成分是 。
图8
(3)步骤 中发生反应的化学方程式为______________________________。
【解析】步骤 中, 经高温煅烧生成 、 和 ,反应的化学方程式为 。
图8
(4)该流程中可循环利用的物质是__________
氨气
【解析】由流程图可知, 经煅烧生成了氨气,氨气又可被配制成氨水用于调节溶液的 ,因此该流程中可循环利用的物质是氨气。
思维点拨
分离除杂型流程图题主要针对物质的分离和提纯问题。解答这类题要弄清整个流程中物质转化的基本原理和物质分离、提纯的过程,熟悉所涉及的物质的性质和化学反应,并结合题设的问题逐一分析解答。
常用的提纯方法:
①水溶法:除去可溶性杂质。
②酸溶法:除去碱性杂质。
③碱溶法:除去酸性杂质。
④氧化剂或还原剂法:除去还原性或氧化性杂质。
⑤灼烧法:除去受热易分解或易挥发的杂质。
⑥调节溶液的 法:使某些金属离子形成沉淀而除去。
⑦沉淀法:使某些离子,如 、 、 、 、 等,
形成沉淀而除去。
针对训练
1.(2023·广西柳州二模)氧化锌为白色粉末,可用于湿疹、癣等皮肤病
的治疗。提纯工业级粗氧化锌(含有 、 、 等杂质)的流
程如图9所示。
图9
已知:在反应①中,金属氧化物与硫酸反应生成盐和水,反应前后元素的化合价不变。
图9
请回答下列问题:
(1)反应①②③④后都进行了相同的操作,该操作的名称是______。
(2)反应③的基本反应类型为______反应。在金属活动性顺序中,
应该排在 的____面。
过滤
置换
前
图9
(3)滤液丙的主要溶质是_________(写化学式)。
(4)反应⑤的化学方程式为___________________________________。
图9
2.(2023·广西河池一模)某火力发电厂产生的固体废弃物粉煤灰中含有
较多的氧化铝 。从粉煤灰中提取氧化铝的工艺流程如图10所示。
请回答下列问题:
图10
图10
(1)操作 的名称是______。
过滤
(2)加入足量氨水能将 全部
转化成 ,写出氨水的化学
式:___________。
(3)“酸浸”工序中通常使用稀硫酸而不使用稀盐酸,主要原因是_____
_____________。
“酸浸”工序发生的主要反应的化学方程式为________________________
_________________。
稀盐酸具有挥发性
(4)“煅烧”工序涉及的主要反应的基本反应类型为______反应。
分解
考点 4 海水资源利用型流程图题
图11
典型例题 4 (2021·广西梧州中考)1926年,我国化工专家侯德榜发
资料:常温下,氨气的溶解度很大, 的溶解度很小。
明了“侯氏制碱法”,结束了由美、英、法等国垄断世界纯碱市场的时代。该法的基本工业流程如图11所示。
请回答下列问题:
(1)纯碱的化学式为________。
【解析】纯碱是碳酸钠的俗名,化学式为 。
图11
(2)侯氏制碱法的反应温度一般控制在 ,因为在此温度段,
的溶解度较________(填“大”或“小”)。
【解析】 侯氏制碱法的反应温度一般控制在 的原因是碳酸氢钠在该温度下的溶解度较小。
图11
(3)若向饱和食盐水中先通入 ,会导致 产量减少,原因是
_______________________________________________________。
【解析】 二氧化碳在水中的溶解度小,与水反应形成的碳酸也就少,不足以与氨气反应生成碳酸氢根,导致碳酸氢钠的产量减少。
图11
(4)写出步骤①②中发生的总反应的化学方程式:______________________________________________。
图11
【解析】 步骤①②的总反应是氯化钠、水、氨气和二氧化碳反应生成碳酸氢钠和氯化铵,化学方程式为 。
(5)侯氏制碱法中能循环利用的物质有 、 和________。
【解析】 碳酸氢钠在加热条件下反应生成碳酸钠、二氧化碳和水,二氧化碳可以重新通入步骤②中而得以循环利用。
图11
思维点拨
海水资源利用型流程图题主要涉及粗盐提纯、侯氏制碱法制纯碱和
海水制镁等内容。解答时,要注意通晓流程,了解生产过程的主线。
①粗盐 精盐:过滤除去粗盐水中的泥沙等不溶性杂质,用
除去 ,用 除去 ,用 除去 和加入的过量
,用稀盐酸除去加入的过量 和 ,蒸发结晶获得精盐。
②精盐水 纯碱:精盐水吸氨,通入二氧化碳酸化制
得 ,加热分解 得到 。
母液 母液中的 与
反应得到 , 与 反应得到 溶液,
溶液蒸发结晶得到 晶体,电解熔融的 得到 。
④贝壳 石灰乳: 、
。
针对训练
1.2023年6月8日是第15个世界海洋日。兴趣小组的同学设计的综合利用海水的部分流程如图12所示。请回答下列问题:
图12
图12
(1)海水制镁。步骤①②③是
利用母液制镁的流程,该流程
中发生中和反应的化学方程式是
______________________________。
步骤①制取氢氧化镁是向母液
母液中氯化镁的质量分数远大于海水中氯化镁的质量分数
中加入石灰乳,而不是向海水中直接加入石灰乳,原因是____________
__________________________________________。
图12
(2)海水晒盐。通常采用______
(填“降温”或“蒸发”)结晶的方法
使海水中的氯化钠析出。通过步骤
④可除去粗盐溶液中的泥沙等难溶
性杂质以及 、 、
蒸发
除去氯化钙和过量的氯化钡
等可溶性杂质。除去可溶性杂质时需要依次加入过量的 溶液、
过量的 溶液、过量的 溶液。其中加入过量 溶液的
目的是__________________________。
图12
(3)海水制碱。步骤⑧⑨是氨碱法制纯碱的流程,步骤⑧中需要向
饱和溶液中先后加入的两种物质是____________(写化学式)。
、
2.广西北部湾有漫长的海岸线,蕴藏着丰富的海洋资源。海水资源综合利用的部分途径如图13所示。请回答下列问题:
图13
(1)粗盐提纯。
①步骤Ⅲ得到的母液是 的______(填“饱和”或“不饱和”)溶液。
饱和
②步骤Ⅰ中,除去难溶性杂质后的食盐水中还含有 、 、
等杂质离子,为得到较纯净的氯化钠,可依次进行如下实验操作: .加入过量的 溶液; .加入过量的 溶液; .加入过量的 溶液; .过滤; .加入适量的盐酸,调节溶液的 等于7; 蒸发。经过步骤 后的溶液中主要含有的杂质离子为____________(写离子符号)。
、
图13
③验证除杂后的滤液中的 已完全转化为沉淀的方法是___________
______________________________________________________________
______________________________________。
取少量滤液于试管中,向其中加入适量的碳酸钠溶液,若没有白色沉淀生成,则说明除杂后滤液中的 已完全转化为沉淀
(2)从经济合理的角度考虑,在实际生产中,步骤Ⅳ常选用_________
作为沉淀剂。写出步骤Ⅴ中反应的化学方程式:_____________________
____________。
图13
中考化学流程图题
备考练习
达标练
图1
1.(2023·山东枣庄中考)
化学兴趣小组的同学根据
侯氏制碱法的原理,利用
、 、 、
制备氯化铵 ,设计
流程如图1所示。已知
极易溶于水,溶于水后得到氨水,向其中通入 时发生如下反应:
。
请回答下列问题:
(1)该流程中的最终产物
可作为肥料的是________。
(2)操作Ⅰ的名称是______,
要用到的玻璃仪器有漏斗、___________________(任写一种)等。
(3)第③步反应的化学方程式为__________________________________,
该反应属于____________(填基本反应类型)。
氯化铵
过滤
烧杯(或玻璃棒)
复分解反应
图1
图2
2.(2023·山东青岛中考)自然界
中的铝元素以化合物的形式存在
于各种矿石中。某铝土矿的主要
成分是 ,含少量 、
等杂质。从该铝土矿中提取
铝可采用图2所示工艺流程(不考
已知: 不溶于水且不与盐酸反应; 能与 溶液反应,
生成可溶性盐。
虑其他杂质参与反应)。请回答下列问题:
图2
(1)步骤①,加盐酸前先将铝土
矿粉碎的目的是________________
___________________________;
所得滤液A中的溶质有___种。
增大反应物的接触面积,使反应更快、更充分
3
(2)步骤②,所加 溶液须过
量的目的是____________________。
使氢氧化铝完全溶解
(3)步骤③, 加热分解生成两种氧化物,请写出该反应的化
学方程式:_________________________。
图2
(4)步骤④是通过电解熔融状态
的 来制备铝。 的熔点
是 ,很难达到熔融状态,
工业上通过加入冰晶石使其在
左右熔化,请写出这一做
法的意义:____________________
_________。
降低氧化铝的熔点,节约能源
3.(2023·湖南怀化中考)海水是一种重要的资源,利用海水可制取金属镁等物质。化学兴趣小组的同学设计了图3所示实验流程。
图3
请根据上述流程回答下列问题:
(1)操作Ⅰ的名称是______,该操
作用到的玻璃仪器有烧杯、漏斗和
________,填写的仪器在操作Ⅰ中的作用是______。操作Ⅰ中加入的
溶液应过量,其目的是 _______________________________。
过滤
玻璃棒
引流
将 完全转化为氢氧化镁沉淀
(2)试剂 是________(填名称),写出溶液A中加入试剂 后发生反
应的化学方程式:_________________________。
稀盐酸
图3
图4
4.(2023·湖北武汉中考)硫酸锌可
用于制备各种含锌材料,在防腐、
医学上有很多应用。菱锌矿的主要
成分是 ,还含有少量的二氧
化硅和氧化铁。以菱锌矿为原料制
备 的工艺流程如图4
所示。(二氧化硅难溶于水,也不
与稀硫酸反应)
请回答下列问题:
图4
(1)菱锌矿属于________(填“纯
净物”或“混合物”)。
混合物
(2)“酸浸”工序中观察到的现象
是____________________________
_____。
有气泡产生,溶液由无色变为黄色
(3)滤液1中含有的阳离子是
__________________(写离子符
号)。
、 、
(4)“转化”工序中加入足量锌粉,反应的化学方程式有
和__________________________。
图4
图4
(5)下列说法正确的是_______
(填序号)。
A.“粉碎”工序是为了使菱锌矿在“酸
浸”工序中与稀硫酸充分反应
B.在“转化”工序中加入锌粉,若无
气泡冒出,则说明锌粉已足量
C.滤渣甲、滤渣乙均能与稀硫酸反
A、D
应产生气体
D.滤液2的质量一定比滤液1的质量大
提分练
5.(2023·湖北黄冈中考)兴趣小组的同学利用某废镍材料(含有金属
及少量 、 )回收镍,设计流程如图5所示(部分产物已略去)。
图5
请根据上述流程回答下列问题:
(1)过滤时,玻璃棒的作用是______。
(2)写出“酸浸”时发生反应的化学方程式:_______________________
____________________________________(任写一个)。
(3)过氧化氢具有氧化性,“氧化”时发生反应的化学方程式为
,则 的化学式为_____。
(4) 、 、 的金属活动性由强到弱的顺序为_____________。
引流
(或 )
、 、
图5
(5)已知 和 开始沉淀和完全沉淀时的 如下表。“除铁”工
序中加入 溶液的目的是通过调节溶液的 使 完全沉淀而
不沉淀,则 的范围是___(填序号)。
离子 开始沉淀时的 完全沉淀时的
2.7 3.2
7.2 8.7
B
图5
A.
B.
C.
图6
6.(2023·四川雅安中考)金属
镁在生产生活中具有重要作用。
以白云石[主要成分为
为原料制备金属镁,
同时得到超细碳酸钙粉末的主
要流程如图6所示。
图6
(1)浸钙池中得到滤液和滤渣的
操作相当于化学实验中的______
(填操作名称)。
过滤
(2)煅烧窑中, 分解
时发生反应的化学方程式为___________________________________。
(3)制浆池中含有的阴离子是_____。
图6
(4)碳酸钙是常用的补钙剂,请
写出碳酸钙与胃酸发生反应的化学
方程式:______________________
____________。
(5)沉钙池中发生反应的化学方
程式为________________________
_________________________。
(6)该流程中可循环使用的物质除水外,还有_____、_______(填化
学式)。
冲刺练
7.(2023·江苏苏州中考)用蛋壳(主要含 ,还有少量 和有
机物)为原料通过图7所示步骤制取补钙剂醋酸钙 。
图7
已知:①醋酸钙易溶于水,高
于 时发生分解。
②醋酸 易挥发。
(1)焙烧。将蛋壳在高温下焙烧后冷却,得到含金属氧化物的固体。
①焙烧过程中, 发生反应的化学方程式为_____________________。
②焙烧过程中,产生烧焦羽毛的气味,说明蛋壳中含有________(填有
机物名称)。
蛋白质
图7
(2)酸溶。在焙烧后的固体中先加入适量水打浆,冷却后,再加入稍
过量的醋酸得到醋酸盐溶液。不能向焙烧后的固体中直接加入醋酸的原
因是__________________________________________________________
___________________________________。
焙烧后的固体为氧化钙,若直接向氧化钙固体中加入醋酸,则氧化钙与水反应放热,会加速醋酸的挥发
图7
(3)除镁。在酸溶后的溶液中加入 至碱性,将
转化为 沉淀除去。该反应属于____________(填基本反应类
型)。
复分解反应
图7
(4)中和。在除镁后的溶液中加入醋酸调节溶液 为7,其目的有:
①将溶液中的少量 转化为 ;②________________
__________。
防止溶液吸收空气中的
(5)将中和后的溶液蒸发浓缩至有大量晶体析出,过滤得到醋酸钙晶
体。蒸发时不能直接将溶液蒸干的原因是__________________________
_______________。
防止蒸干时局部温度过高,导致醋酸钙分解
(6)醋酸钙在高温下分解得到的氧化钙可作为气体吸收剂。使 溶质质量分数为 的 样品在高温下完全分解,计算分解得到的 的质量(写出计算过程)。
已知:
①醋酸钙的分解反应为 ,杂质不发生反应。
的相对分子质量为158。
解:醋酸钙样品中含 的质量为 。
解:设分解得到的 的质量为 。
答:分解得到的 的质量为
中考化学流程图题
典题精析
考点 1 回收利用型流程图题
典型例题 1 (2022·广西贺州中考)某燃煤电厂产生的固体废弃物粉煤灰中含有较多的氧化铝,从粉煤灰中提取氧化铝的工艺流程如图1所示。
(1)酸浸中使用的酸是___(填序号)。
B
A. B. C.
(2)煅烧后产物 的化学式为______,写出煅烧过程中发生反应的化
学方程式:_________________________。
【解析】 已知粉煤灰中含有较多的氧化铝,粉煤灰经酸浸后生成了硫酸铝,故酸浸过程中使用的酸是硫酸。
图1
【解析】 由质量守恒定律可知, 经煅烧分解生成 和 ,反应的化学方程式为 。
(3)该工艺的价值在于 __________________________。
实现了废物的回收和再利用
图1
【解析】 该工艺的价值在于实现了废物的回收和再利用。
思维点拨
(1)化工流程图中箭头指入的一般是投的料(即反应物),箭头指出的一般是生成物(包括主产物和副产物),返回的箭头一般是指被循环利用的物质。
(2)对原料进行预处理的常用方法及其作用。
①研磨、粉碎、喷淋:增大反应物的接触面积,提高反应速率。
②水浸:与水接触反应或溶解,分离水溶性和非水溶性物质。③酸浸:与酸接触反应或溶解,如溶解金属或金属氧化物。
④灼烧:除去可燃性杂质或使原料初步转化。
⑤煅烧:使一些杂质在高温下氧化、分解,如煅烧石灰石。
针对训练
1.(2023·广西玉林一模)化学兴趣小组的同学利用废硫酸液制备 ,
设计的流程如图2所示。
图2
图2
(1)上述流程中可循环使用的物质有_____________(写化学式)。
、
(2)反应Ⅱ中的温度控制在
,目的是_______
(填序号)。
A.提高温度至 ,增大反应速率
B.增大 的溶解度
C.温度不高于 ,防止氨水分解
A、
图2
图2
(3)反应Ⅲ中发生了复分解反应,该反应的化学方程式为
______________________________________。
(4)反应Ⅲ中的相关物质在 时的溶解度如下表。反应Ⅲ在常温下
能实现的原因是__________________________。洗涤反应Ⅲ所得
晶体时用的是饱和 溶液而不是水,目的是____________________
___。
物质
溶解度/ 34.0 11.1 37.2 19.5
常温下硫酸钾的溶解度最小
防止硫酸钾溶解在水中
图2
图3
2.(2023·广西防城港二模)
波尔多液是一种保护性的杀
菌剂,有效成分为碱式硫酸
铜。它具有杀菌谱广、持效
期长、病菌不易产生抗药性、
对人和畜低毒等特点。波尔
多液是历史上使用时间最长的一种杀菌剂。图3是利用废弃铜料(只含
有铜和一定量的铁)和石灰石制备波尔多液的流程。请回答下列问题:
图3
(1)反应器1中将硫酸以喷淋
方式注入的目的是__________
__________________________
_______, 反应器1的作用是
________。
增大反应物的接触面积,使反应更快、更充分
除去铁
(2)反应器4中发生反应的化学方程式为____________________________________________________________________(任写一个)。
(3)气体B的化学式为______。
[或
图3
图3
(4)反应器3和反应器4的内壁材质不能为铁或铝,原因是______________________。
硫酸铜能与铁、铝反应
考点 2 制备与生产型流程图题
典型例题 2 (2023·广西中考)柠檬酸亚铁 是一种易被吸收
的补血剂。利用硫酸厂的废渣(主要含 、 ,还有少量 )
制备柠檬酸亚铁的工艺流程如图4所示。请回答下列问题:
图4
资料 ;
。
资料 不溶于水,也不与稀硫酸反应。
(1)柠檬酸亚铁进入人体肠道后以________(填阳离子符号)的形式被吸收,从而达到补血的效果。
【解析】柠檬酸亚铁进入人体肠道后被电离为亚铁离子和柠檬酸根离子,其 中 被人体所吸收,达到补血的效果。
(2)固体C的成分是________。
图4
【解析】 步骤①中氧化铁与硫酸反应生成硫酸铁和水,四氧化三铁与硫酸反应生成硫酸铁、硫酸亚铁和水,步骤②中铁与硫酸铁反应生成硫酸亚铁,铁与硫酸反应生成硫酸亚铁和氢气,因此固体C的成分是 和剩余的 。
图4
【解析】 步骤①中氧化铁与硫酸反应生成硫酸铁和水,属于复分解反应;步骤②中铁与硫酸铁反应生成硫酸亚铁,属于化合反应,铁与硫酸反应生成硫酸亚铁和氢气,属于置换反应;步骤③中碳酸钠与硫酸亚铁反应生成硫酸钠和碳酸亚铁沉淀,属于复分解反应;步骤④中碳酸亚铁与柠檬酸反应生成柠檬酸亚铁、水和二氧化碳,属于复分解反应。
(3)步骤①②③④中涉及置换反应的是________(填序号)。
图4
(4)步骤③中发生反应的化学方程式为___________________________________________________。
(5)“一系列操作”中,将柠檬酸亚铁晶体与溶液分离的操作是________。
【解析】“一系列操作”中,将柠檬酸亚铁晶体与溶液分离的操作是过滤。
图4
思维点拨
制备与生产型流程图题的解题思路:①从题干获取有用信息,了解生产的产品。②分析流程中的每一个步骤,了解反应物是什么,发生了什么反应,该反应对制造产品有什么作用。要抓住一个关键点,即一切反应或操作都是为了获得产品。③从问题中获取信息,帮助解题。
针对训练
1.(2023·广西柳州三模)广西有着丰富的重晶石矿产资源。氯化钡是一
种可溶性重金属盐,广泛应用于化工领域。图5为工业上以重晶石(主
要成分为 ,杂质为 )为原料制备氯化钡晶体
的工艺流程。
图5
请回答下列问题:
已知: 。
能与水反应生成碱。
(1)流程图中过滤的作用是________________________。
将不溶性固体与液体分离
图5
图6
(2)“焙烧”工序中,焦炭与杂质 也会发生反应,写出反应的化学方程式:____________________________。硫酸钡转化率与温度的关系如图6所示,则反应的最佳温度约为_________。
(3)“酸溶”工序中,硫化钡 与盐酸发生的反应为
,写出 的化学式:_______。
图5
(4)气体 的成分除 和少量挥发出的 、水蒸气外,还含有
______(填名称)。
氢气
图5
2.(2023·广西崇左二模)金属锌在冶金、化学电源生产等方面具有重要
作用。以闪锌矿(主要含 ,还含有 和少量 、 、 等
杂质)为原料制备金属锌的流程如图7所示。请回答下列问题:
图7
已知: 不溶于水且不与硫酸反应。②常温下 难溶于水
和稀硫酸。
图7
(1)“焙烧”工序中金属硫化物转
化成金属氧化物。焙烧尾气必须进
行净化处理的原因是____________
_____________________________。
反应生成的 会污染空气(或形成酸雨)
(2)“溶浸”工序产生的滤渣的主要成分除 外,还有________。
硫酸铅
(3)“氧化除杂”工序的主要反应为 ,则 、 、 依次是_________。
6、4、
图7
(4)“还原除杂”工序利用了
锌粉与 的反应,该反应
的化学方程式为____________
_____________。
(5)“电解”工序中的反应为 ,
则电解得到的溶液可返回______(填“焙烧”“溶浸”“氧化除杂”或“还原除
杂”)工序继续使用。
溶浸
考点 3 分离、提纯和除杂型流程图题
图8
典型例题 3 (2022·广西河池中考)
五氧化二钒 广泛用于化工
行业。工业钒废催化剂中主要含硫
酸氧钒 和少量的 、
等杂质,现要除去钒废催化剂
中的杂质并得到 固体,其流
程如图8所示。请回答下列问题:
(1) 中硫元素的化合价为____。
(2)操作 的名称是______,废渣的主要成分为______。
过滤
图8
【解析】“ 已知 中钾
元素为 价,氧元素为
价,设硫元素的化合价为 ,则有 ,解得 。
【解析】操作 是将固体与液体分离的
操作,是过滤。已知工业上的钒废催化剂
中含有少量的 、 等杂质,因 不溶于水,故经操作 分离出的废渣的主要成分是 。
图8
(3)步骤 中发生反应的化学方程式为______________________________。
【解析】步骤 中, 经高温煅烧生成 、 和 ,反应的化学方程式为 。
图8
(4)该流程中可循环利用的物质是__________
氨气
【解析】由流程图可知, 经煅烧生成了氨气,氨气又可被配制成氨水用于调节溶液的 ,因此该流程中可循环利用的物质是氨气。
思维点拨
分离除杂型流程图题主要针对物质的分离和提纯问题。解答这类题要弄清整个流程中物质转化的基本原理和物质分离、提纯的过程,熟悉所涉及的物质的性质和化学反应,并结合题设的问题逐一分析解答。
常用的提纯方法:
①水溶法:除去可溶性杂质。
②酸溶法:除去碱性杂质。
③碱溶法:除去酸性杂质。
④氧化剂或还原剂法:除去还原性或氧化性杂质。
⑤灼烧法:除去受热易分解或易挥发的杂质。
⑥调节溶液的 法:使某些金属离子形成沉淀而除去。
⑦沉淀法:使某些离子,如 、 、 、 、 等,
形成沉淀而除去。
针对训练
1.(2023·广西柳州二模)氧化锌为白色粉末,可用于湿疹、癣等皮肤病
的治疗。提纯工业级粗氧化锌(含有 、 、 等杂质)的流
程如图9所示。
图9
已知:在反应①中,金属氧化物与硫酸反应生成盐和水,反应前后元素的化合价不变。
图9
请回答下列问题:
(1)反应①②③④后都进行了相同的操作,该操作的名称是______。
(2)反应③的基本反应类型为______反应。在金属活动性顺序中,
应该排在 的____面。
过滤
置换
前
图9
(3)滤液丙的主要溶质是_________(写化学式)。
(4)反应⑤的化学方程式为___________________________________。
图9
2.(2023·广西河池一模)某火力发电厂产生的固体废弃物粉煤灰中含有
较多的氧化铝 。从粉煤灰中提取氧化铝的工艺流程如图10所示。
请回答下列问题:
图10
图10
(1)操作 的名称是______。
过滤
(2)加入足量氨水能将 全部
转化成 ,写出氨水的化学
式:___________。
(3)“酸浸”工序中通常使用稀硫酸而不使用稀盐酸,主要原因是_____
_____________。
“酸浸”工序发生的主要反应的化学方程式为________________________
_________________。
稀盐酸具有挥发性
(4)“煅烧”工序涉及的主要反应的基本反应类型为______反应。
分解
考点 4 海水资源利用型流程图题
图11
典型例题 4 (2021·广西梧州中考)1926年,我国化工专家侯德榜发
资料:常温下,氨气的溶解度很大, 的溶解度很小。
明了“侯氏制碱法”,结束了由美、英、法等国垄断世界纯碱市场的时代。该法的基本工业流程如图11所示。
请回答下列问题:
(1)纯碱的化学式为________。
【解析】纯碱是碳酸钠的俗名,化学式为 。
图11
(2)侯氏制碱法的反应温度一般控制在 ,因为在此温度段,
的溶解度较________(填“大”或“小”)。
【解析】 侯氏制碱法的反应温度一般控制在 的原因是碳酸氢钠在该温度下的溶解度较小。
图11
(3)若向饱和食盐水中先通入 ,会导致 产量减少,原因是
_______________________________________________________。
【解析】 二氧化碳在水中的溶解度小,与水反应形成的碳酸也就少,不足以与氨气反应生成碳酸氢根,导致碳酸氢钠的产量减少。
图11
(4)写出步骤①②中发生的总反应的化学方程式:______________________________________________。
图11
【解析】 步骤①②的总反应是氯化钠、水、氨气和二氧化碳反应生成碳酸氢钠和氯化铵,化学方程式为 。
(5)侯氏制碱法中能循环利用的物质有 、 和________。
【解析】 碳酸氢钠在加热条件下反应生成碳酸钠、二氧化碳和水,二氧化碳可以重新通入步骤②中而得以循环利用。
图11
思维点拨
海水资源利用型流程图题主要涉及粗盐提纯、侯氏制碱法制纯碱和
海水制镁等内容。解答时,要注意通晓流程,了解生产过程的主线。
①粗盐 精盐:过滤除去粗盐水中的泥沙等不溶性杂质,用
除去 ,用 除去 ,用 除去 和加入的过量
,用稀盐酸除去加入的过量 和 ,蒸发结晶获得精盐。
②精盐水 纯碱:精盐水吸氨,通入二氧化碳酸化制
得 ,加热分解 得到 。
母液 母液中的 与
反应得到 , 与 反应得到 溶液,
溶液蒸发结晶得到 晶体,电解熔融的 得到 。
④贝壳 石灰乳: 、
。
针对训练
1.2023年6月8日是第15个世界海洋日。兴趣小组的同学设计的综合利用海水的部分流程如图12所示。请回答下列问题:
图12
图12
(1)海水制镁。步骤①②③是
利用母液制镁的流程,该流程
中发生中和反应的化学方程式是
______________________________。
步骤①制取氢氧化镁是向母液
母液中氯化镁的质量分数远大于海水中氯化镁的质量分数
中加入石灰乳,而不是向海水中直接加入石灰乳,原因是____________
__________________________________________。
图12
(2)海水晒盐。通常采用______
(填“降温”或“蒸发”)结晶的方法
使海水中的氯化钠析出。通过步骤
④可除去粗盐溶液中的泥沙等难溶
性杂质以及 、 、
蒸发
除去氯化钙和过量的氯化钡
等可溶性杂质。除去可溶性杂质时需要依次加入过量的 溶液、
过量的 溶液、过量的 溶液。其中加入过量 溶液的
目的是__________________________。
图12
(3)海水制碱。步骤⑧⑨是氨碱法制纯碱的流程,步骤⑧中需要向
饱和溶液中先后加入的两种物质是____________(写化学式)。
、
2.广西北部湾有漫长的海岸线,蕴藏着丰富的海洋资源。海水资源综合利用的部分途径如图13所示。请回答下列问题:
图13
(1)粗盐提纯。
①步骤Ⅲ得到的母液是 的______(填“饱和”或“不饱和”)溶液。
饱和
②步骤Ⅰ中,除去难溶性杂质后的食盐水中还含有 、 、
等杂质离子,为得到较纯净的氯化钠,可依次进行如下实验操作: .加入过量的 溶液; .加入过量的 溶液; .加入过量的 溶液; .过滤; .加入适量的盐酸,调节溶液的 等于7; 蒸发。经过步骤 后的溶液中主要含有的杂质离子为____________(写离子符号)。
、
图13
③验证除杂后的滤液中的 已完全转化为沉淀的方法是___________
______________________________________________________________
______________________________________。
取少量滤液于试管中,向其中加入适量的碳酸钠溶液,若没有白色沉淀生成,则说明除杂后滤液中的 已完全转化为沉淀
(2)从经济合理的角度考虑,在实际生产中,步骤Ⅳ常选用_________
作为沉淀剂。写出步骤Ⅴ中反应的化学方程式:_____________________
____________。
图13
中考化学流程图题
备考练习
达标练
图1
1.(2023·山东枣庄中考)
化学兴趣小组的同学根据
侯氏制碱法的原理,利用
、 、 、
制备氯化铵 ,设计
流程如图1所示。已知
极易溶于水,溶于水后得到氨水,向其中通入 时发生如下反应:
。
请回答下列问题:
(1)该流程中的最终产物
可作为肥料的是________。
(2)操作Ⅰ的名称是______,
要用到的玻璃仪器有漏斗、___________________(任写一种)等。
(3)第③步反应的化学方程式为__________________________________,
该反应属于____________(填基本反应类型)。
氯化铵
过滤
烧杯(或玻璃棒)
复分解反应
图1
图2
2.(2023·山东青岛中考)自然界
中的铝元素以化合物的形式存在
于各种矿石中。某铝土矿的主要
成分是 ,含少量 、
等杂质。从该铝土矿中提取
铝可采用图2所示工艺流程(不考
已知: 不溶于水且不与盐酸反应; 能与 溶液反应,
生成可溶性盐。
虑其他杂质参与反应)。请回答下列问题:
图2
(1)步骤①,加盐酸前先将铝土
矿粉碎的目的是________________
___________________________;
所得滤液A中的溶质有___种。
增大反应物的接触面积,使反应更快、更充分
3
(2)步骤②,所加 溶液须过
量的目的是____________________。
使氢氧化铝完全溶解
(3)步骤③, 加热分解生成两种氧化物,请写出该反应的化
学方程式:_________________________。
图2
(4)步骤④是通过电解熔融状态
的 来制备铝。 的熔点
是 ,很难达到熔融状态,
工业上通过加入冰晶石使其在
左右熔化,请写出这一做
法的意义:____________________
_________。
降低氧化铝的熔点,节约能源
3.(2023·湖南怀化中考)海水是一种重要的资源,利用海水可制取金属镁等物质。化学兴趣小组的同学设计了图3所示实验流程。
图3
请根据上述流程回答下列问题:
(1)操作Ⅰ的名称是______,该操
作用到的玻璃仪器有烧杯、漏斗和
________,填写的仪器在操作Ⅰ中的作用是______。操作Ⅰ中加入的
溶液应过量,其目的是 _______________________________。
过滤
玻璃棒
引流
将 完全转化为氢氧化镁沉淀
(2)试剂 是________(填名称),写出溶液A中加入试剂 后发生反
应的化学方程式:_________________________。
稀盐酸
图3
图4
4.(2023·湖北武汉中考)硫酸锌可
用于制备各种含锌材料,在防腐、
医学上有很多应用。菱锌矿的主要
成分是 ,还含有少量的二氧
化硅和氧化铁。以菱锌矿为原料制
备 的工艺流程如图4
所示。(二氧化硅难溶于水,也不
与稀硫酸反应)
请回答下列问题:
图4
(1)菱锌矿属于________(填“纯
净物”或“混合物”)。
混合物
(2)“酸浸”工序中观察到的现象
是____________________________
_____。
有气泡产生,溶液由无色变为黄色
(3)滤液1中含有的阳离子是
__________________(写离子符
号)。
、 、
(4)“转化”工序中加入足量锌粉,反应的化学方程式有
和__________________________。
图4
图4
(5)下列说法正确的是_______
(填序号)。
A.“粉碎”工序是为了使菱锌矿在“酸
浸”工序中与稀硫酸充分反应
B.在“转化”工序中加入锌粉,若无
气泡冒出,则说明锌粉已足量
C.滤渣甲、滤渣乙均能与稀硫酸反
A、D
应产生气体
D.滤液2的质量一定比滤液1的质量大
提分练
5.(2023·湖北黄冈中考)兴趣小组的同学利用某废镍材料(含有金属
及少量 、 )回收镍,设计流程如图5所示(部分产物已略去)。
图5
请根据上述流程回答下列问题:
(1)过滤时,玻璃棒的作用是______。
(2)写出“酸浸”时发生反应的化学方程式:_______________________
____________________________________(任写一个)。
(3)过氧化氢具有氧化性,“氧化”时发生反应的化学方程式为
,则 的化学式为_____。
(4) 、 、 的金属活动性由强到弱的顺序为_____________。
引流
(或 )
、 、
图5
(5)已知 和 开始沉淀和完全沉淀时的 如下表。“除铁”工
序中加入 溶液的目的是通过调节溶液的 使 完全沉淀而
不沉淀,则 的范围是___(填序号)。
离子 开始沉淀时的 完全沉淀时的
2.7 3.2
7.2 8.7
B
图5
A.
B.
C.
图6
6.(2023·四川雅安中考)金属
镁在生产生活中具有重要作用。
以白云石[主要成分为
为原料制备金属镁,
同时得到超细碳酸钙粉末的主
要流程如图6所示。
图6
(1)浸钙池中得到滤液和滤渣的
操作相当于化学实验中的______
(填操作名称)。
过滤
(2)煅烧窑中, 分解
时发生反应的化学方程式为___________________________________。
(3)制浆池中含有的阴离子是_____。
图6
(4)碳酸钙是常用的补钙剂,请
写出碳酸钙与胃酸发生反应的化学
方程式:______________________
____________。
(5)沉钙池中发生反应的化学方
程式为________________________
_________________________。
(6)该流程中可循环使用的物质除水外,还有_____、_______(填化
学式)。
冲刺练
7.(2023·江苏苏州中考)用蛋壳(主要含 ,还有少量 和有
机物)为原料通过图7所示步骤制取补钙剂醋酸钙 。
图7
已知:①醋酸钙易溶于水,高
于 时发生分解。
②醋酸 易挥发。
(1)焙烧。将蛋壳在高温下焙烧后冷却,得到含金属氧化物的固体。
①焙烧过程中, 发生反应的化学方程式为_____________________。
②焙烧过程中,产生烧焦羽毛的气味,说明蛋壳中含有________(填有
机物名称)。
蛋白质
图7
(2)酸溶。在焙烧后的固体中先加入适量水打浆,冷却后,再加入稍
过量的醋酸得到醋酸盐溶液。不能向焙烧后的固体中直接加入醋酸的原
因是__________________________________________________________
___________________________________。
焙烧后的固体为氧化钙,若直接向氧化钙固体中加入醋酸,则氧化钙与水反应放热,会加速醋酸的挥发
图7
(3)除镁。在酸溶后的溶液中加入 至碱性,将
转化为 沉淀除去。该反应属于____________(填基本反应类
型)。
复分解反应
图7
(4)中和。在除镁后的溶液中加入醋酸调节溶液 为7,其目的有:
①将溶液中的少量 转化为 ;②________________
__________。
防止溶液吸收空气中的
(5)将中和后的溶液蒸发浓缩至有大量晶体析出,过滤得到醋酸钙晶
体。蒸发时不能直接将溶液蒸干的原因是__________________________
_______________。
防止蒸干时局部温度过高,导致醋酸钙分解
(6)醋酸钙在高温下分解得到的氧化钙可作为气体吸收剂。使 溶质质量分数为 的 样品在高温下完全分解,计算分解得到的 的质量(写出计算过程)。
已知:
①醋酸钙的分解反应为 ,杂质不发生反应。
的相对分子质量为158。
解:醋酸钙样品中含 的质量为 。
解:设分解得到的 的质量为 。
答:分解得到的 的质量为
同课章节目录
