2023—2024学年人教化学九年级下册第十一单元 盐 化肥 达标练习(含答案)
文档属性
| 名称 | 2023—2024学年人教化学九年级下册第十一单元 盐 化肥 达标练习(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 704.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-17 00:00:00 | ||
图片预览




文档简介
2023—2024学年人教化学九年级下册第十一单元 盐 化肥 达标练习附答案
一、选择题。
1、下列各组物质混合后不能发生反应的是( )
A. 银和稀盐酸 B. 氢氧化钡溶液和硝酸
C. 铝和稀硫酸 D. 氯化钡溶液和硫酸钠溶液
2、化学与日常生活、工农业生产密切相关。下列说法中不正确的是( )
A. 用含有碳酸氢钠的发酵粉焙制糕点
B. 工业上用熟石灰处理硫酸厂的污水
C. 医疗上用纯酒精作消毒剂
D. 生活中用含有NaOH的清洁剂去油污
3、已知粉末X样品是下列四种物质中的一种,取三等份该粉末,分别加入足量的氢氧化钙溶液、氯化钡溶液、稀盐酸中并振荡,产生的现象如下表。则该固体粉末X是( )
加入物质 氢氧化钙溶液 氯化钡溶液 稀盐酸
现象 产生白色沉淀 产生白色沉淀 固体溶解,产生无色气体
A.CuSO4 B.Na2SO4 C.K2CO3 D.Mg
4、属于复分解反应的是( )
A.4NH3+3O26H2O+2N2
B.Na2SiO3+H2SO4===H2SiO3↓+Na2SO4
C.2FeCl2+Cl2===2FeCl3
D.2HgO2Hg+O2↑
5、尿素【CO(NH2)2】是一种常用的化肥,工业上生产尿素的反应的微观示意图,如下图所示:则下列说法正确的是( )
A.A、B、D三种物质都是氧化物
B.反应中A、B两种物质的质量比为17∶22
C.该反应属于复分解反应
D.该反应前后分子种类没有改变
6、德国化学家弗里茨·哈伯由于发明了合成氨的方法而获得1918年诺贝尔化学奖,他的发明大大提高了农作物的产量同时也提高了硝酸、炸药的产量。下列说法中正确的是( )
A.氮气和氢气在点燃或光照条件下可合成氨
B.氨水显酸性
C.氨气遇到浓盐酸会发生反应产生白烟
D.干燥氨气可用浓硫酸
7、下列关于化肥的说法正确的是( )
A.过磷酸钙[Ca(H2PO4)2和CaSO4的混合物] 属于氮肥
B.凡施用过化肥的蔬菜都会危害健康
C.氯化钾与熟石灰混合、研磨,能闻到刺激性气味
D.硫酸铵与磷矿粉从外观即可区分
8、物质的提纯是生活和科学研究的重要内容。某兴趣小组同学按如图操作完成粗盐(含有难溶性杂质)提纯实验。下列说法正确的是( )
A.去除难溶性杂质的步骤是③
B.④操作中待溶剂全部蒸干后再停止加热
C.正确的操作顺序为①⑤②③⑥④
D.所得精盐潮湿会使产率偏低
9、分别向下列化肥中加入稀盐酸,有气体生成的是( )。
A.NH4HCO3 B.Ca3(PO4)2 C.K2SO4 D.KC1
10、下列实验操作中不能达到实验目的的是( )
选项 物质 目的 主要实验操作
A H2和CO 鉴别 点燃,火焰上罩干冷烧杯,观察现象
B N2和CO2 检验 用燃着的木条伸入集气瓶中,观察现象
C MnO2和KCl的混合物 分离 溶解,过滤,洗涤固体并烘干,蒸发滤液
D Cu中含有少量Fe 除杂 加入过量的稀硫酸,过滤,洗涤干燥
A. A B. B C. C D. D
11、现有4种试剂:①紫色石蕊试液;②稀硫酸;③碳酸钾溶液;④氯化钡溶液。能用来一次性鉴别稀盐酸、氢氧化钡溶液、碳酸钠溶液的试剂有( )
A.② B.②③ C.①②③ D.②③④
12、保护环境的做法很多。下列做法不正确的是( )
A.深埋电池,消除污染 B.合理使用农药,保护水体资源
C.植树造林,净化环境 D.垃圾分类回收,资源合理利用
13、现有以下物质,对它们的分类正确的是( )
①澄清石灰水 ②氧化铜 ③五氧化二磷
④硝酸钾⑤醋酸 ⑥洁净的空气 ⑦纯碱⑧硫酸钾
A.①⑥属于纯净物 B.④⑧属于复合肥
C.①⑦属于碱 D.②③属于氧化物
14、某同学家中种植的植物比正常的植株矮小瘦弱,叶片发黄,有的叶脉呈淡棕色,你认为应该施加下列哪一种化肥( )。
A.氯化钾 B.过磷酸钙 C.硫酸钾 D.尿素
15、下列说法正确的是( )
A. 糖类都具有甜味
B. 油脂和淀粉的组成元素相同,分子组成和结构也相同
C. 碘酒可用来检验食物中是否含有淀粉
D. 摄入人体内的糖类最终都转化为二氧化碳和水
16、下列各组物质分别加入足量的水中,能得到无色透明溶液的是( )
A.FeCl3、NaOH、NaCl B.Na2SO4、HCl、BaCl2
C.CuSO4、KCl、HCl D.Na2CO3、NaCl、Na2SO4
二、填空题。
17、写出下列反应的化学方程式,并按要求填空。
(1)用石灰浆粉刷墙壁,干燥后又白又硬:______________________________。
(2)工业炼铁的主要原理是一氧化碳和氧化铁在高温下反应:_______________________ 。工业炼铁的主要设备是__________________。
(3)车用乙醇汽油不但可以节省石油资源和有效地减少汽车尾气的污染,还可以促进农业生产。乙醇(C2H5OH)完全燃烧的化学方程式为_______________,该反应属于____________(选填:“吸热”或“放热”)反应。
(4)工业上,常用电解氯化钠溶液的方法来制取氢氧化钠,同时还能获得氢气、氯气两种化工产品,其反应的化学方程式为_____________________。
(5)医疗上“钡餐”的主要成分是硫酸钡,不能用碳酸钡替代硫酸钡的原因是用方程式表示_____________,该反应的基本反应类型是__________。
18、我国古代劳动人民常将草木灰(主要成分K2CO3)和生石灰在水中混合,用上层清液漂白丝帛。清液的主要成分及溶解度如图所示。
(1)t1 ℃时3种物质的饱和溶液中溶质质量分数由小到大的顺序是 。
(2)20 ℃时,向4个盛有50 g水的烧杯中,分别加入一定质量的氢氧化钾并充分溶解。4组实验数据如下:
实验序号 A B C D
加入氢氧化钾的质量/g 7 14 56 70
溶液质量/g 57 64 106 106
由上述实验数据可知:
①所得溶液是不饱和溶液的是 (填序号);
②20℃时,将C继续恒温蒸发25 g水,过滤,得到质量为 g的固体。
19、小明在进行粗盐提纯和配制一定溶质质量分数的氯化钠溶液时,遇到了如下的问题,请你帮助小明来解答下列问题。
(1)粗盐提纯的步骤为:溶解、________ 、蒸发、计算产率。
(2)经过滤后,食盐水仍浑浊的可能原因是____________________(答一点即可)。
(3)在蒸发实验操作中,当蒸发皿中出现_________________时停止加热。
(4)将配制好的氯化钠溶液,装入试剂瓶时不小心溅出,则剩余溶液中溶质的质量分数_______(填“偏大”、“偏小”或“不变”)。
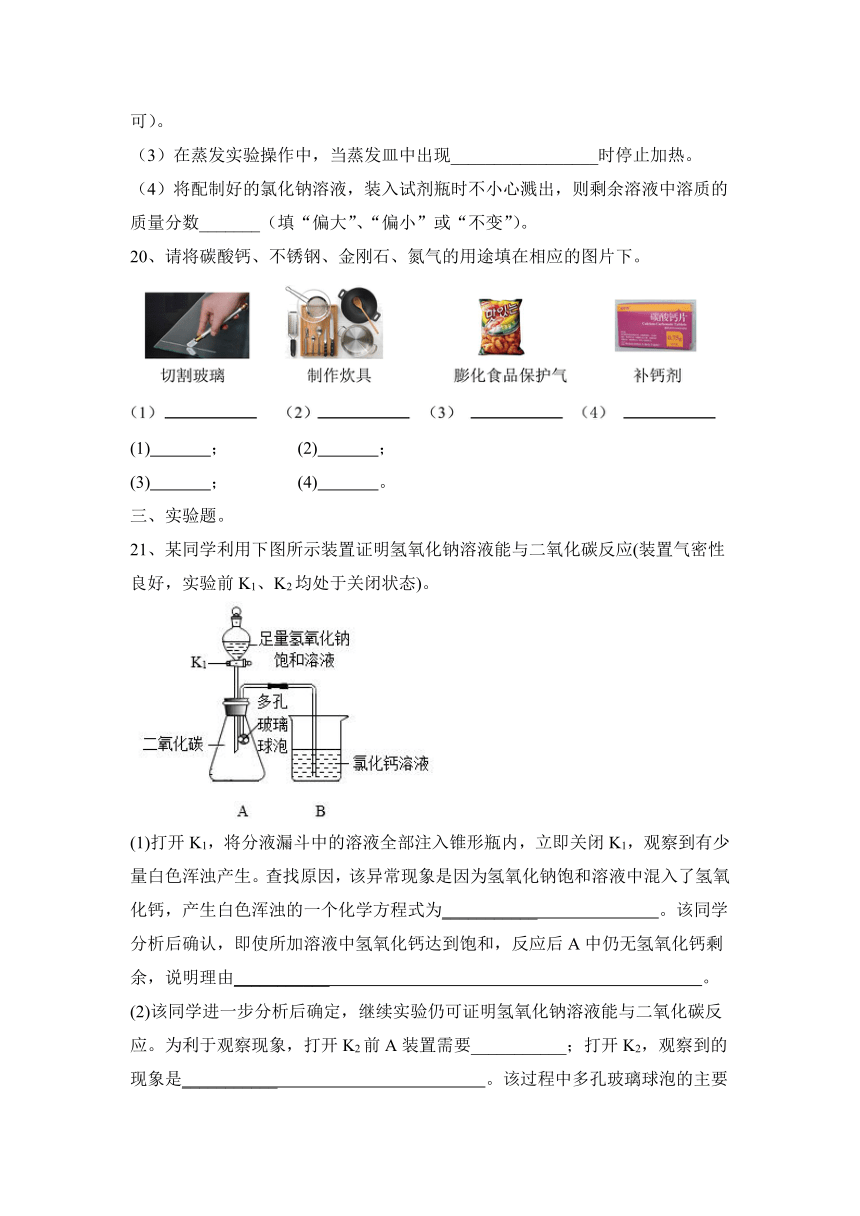
20、请将碳酸钙、不锈钢、金刚石、氮气的用途填在相应的图片下。
(1) ; (2) ;
(3) ; (4) 。
三、实验题。
21、某同学利用下图所示装置证明氢氧化钠溶液能与二氧化碳反应(装置气密性良好,实验前K1、K2均处于关闭状态)。
(1)打开K1,将分液漏斗中的溶液全部注入锥形瓶内,立即关闭K1,观察到有少量白色浑浊产生。查找原因,该异常现象是因为氢氧化钠饱和溶液中混入了氢氧化钙,产生白色浑浊的一个化学方程式为___________ 。该同学分析后确认,即使所加溶液中氢氧化钙达到饱和,反应后A中仍无氢氧化钙剩余,说明理由___________ 。
(2)该同学进一步分析后确定,继续实验仍可证明氢氧化钠溶液能与二氧化碳反应。为利于观察现象,打开K2前A装置需要___________;打开K2,观察到的现象是___________ 。该过程中多孔玻璃球泡的主要作用是___________ 。
(3)实验后,将A中物质过滤,向滤液中滴加酚酞溶液,变红。对滤液进行无害化处理,需加入的一种试剂是___________。
22、某实验小组的甲、乙两同学围绕Na2CO3进行了如图一所示的实验。实验结束后,丙同学把A、B两支试管中的物质倒入同一洁净的烧杯中(如图二),充分混合后发现白色沉淀明显增加。
(1)甲同学的实验完成后,A试管中一定有剩余的物质是 。
(2)乙同学的实验发生的化学方程式是 。
小组同学将C中液体过滤后,对所得滤液的主要成分进行了如下探究:
【猜想与假设】 实验小组的同学对滤液的成分作出了如下猜想:
猜想一:滤液中的溶质是NaCl、Na2CO3
猜想二:滤液中的溶质是NaCl、CaCl2
猜想三:滤液中的溶质是NaCl、CaCl2、HCl
猜想四:滤液中的溶质是NaCl
【讨论与交流】 通过认真讨论,小组同学排除了其中一种不合理的猜想。
(3)不合理的是猜想三,理由是 。
【进行实验】 丁同学取少量滤液置于试管中,向试管中滴加一种物质,发现有无色气泡生成。
(4)你认为丁同学向滤液中滴加的物质是 。
【实验结论】 通过探究,小组同学得出了猜想一是正确的结论。
四、计算题。
23、某课外活动小组对失去标签的稀硫酸浓度进行测定:取稀硫酸50 g于烧杯中,逐滴滴加3.42%的氢氧化钡溶液,烧杯内溶质质量与滴加氢氧化钡溶液质量关系如图所示。(结果保留两位小数)
(1)参加反应的Ba(OH)2质量共有 g。当滴加Ba(OH)2溶液50g时,烧杯内溶液的pH 7(填“>”“<”或“=”)。
(2)求该硫酸溶液的溶质质量分数。
(3)通过计算,在图中画出产生沉淀质量与滴加Ba(OH)2溶液的质量关系。
(4)滴加Ba(OH)2溶液至150g时,所得溶液的溶质质量分数 。
2023—2024学年人教化学九年级下册第十一单元 盐 化肥 达标练习附答案
一、选择题。
1、下列各组物质混合后不能发生反应的是( )
A. 银和稀盐酸 B. 氢氧化钡溶液和硝酸
C. 铝和稀硫酸 D. 氯化钡溶液和硫酸钠溶液
【答案】A
2、化学与日常生活、工农业生产密切相关。下列说法中不正确的是( )
A. 用含有碳酸氢钠的发酵粉焙制糕点
B. 工业上用熟石灰处理硫酸厂的污水
C. 医疗上用纯酒精作消毒剂
D. 生活中用含有NaOH的清洁剂去油污
【答案】C
3、已知粉末X样品是下列四种物质中的一种,取三等份该粉末,分别加入足量的氢氧化钙溶液、氯化钡溶液、稀盐酸中并振荡,产生的现象如下表。则该固体粉末X是( )
加入物质 氢氧化钙溶液 氯化钡溶液 稀盐酸
现象 产生白色沉淀 产生白色沉淀 固体溶解,产生无色气体
A.CuSO4 B.Na2SO4 C.K2CO3 D.Mg
【答案】C
4、属于复分解反应的是( )
A.4NH3+3O26H2O+2N2
B.Na2SiO3+H2SO4===H2SiO3↓+Na2SO4
C.2FeCl2+Cl2===2FeCl3
D.2HgO2Hg+O2↑
【答案】B
5、尿素【CO(NH2)2】是一种常用的化肥,工业上生产尿素的反应的微观示意图,如下图所示:则下列说法正确的是( )
A.A、B、D三种物质都是氧化物
B.反应中A、B两种物质的质量比为17∶22
C.该反应属于复分解反应
D.该反应前后分子种类没有改变
【答案】B
6、德国化学家弗里茨·哈伯由于发明了合成氨的方法而获得1918年诺贝尔化学奖,他的发明大大提高了农作物的产量同时也提高了硝酸、炸药的产量。下列说法中正确的是( )
A.氮气和氢气在点燃或光照条件下可合成氨
B.氨水显酸性
C.氨气遇到浓盐酸会发生反应产生白烟
D.干燥氨气可用浓硫酸
【答案】C
7、下列关于化肥的说法正确的是( )
A.过磷酸钙[Ca(H2PO4)2和CaSO4的混合物] 属于氮肥
B.凡施用过化肥的蔬菜都会危害健康
C.氯化钾与熟石灰混合、研磨,能闻到刺激性气味
D.硫酸铵与磷矿粉从外观即可区分
【答案】D
8、物质的提纯是生活和科学研究的重要内容。某兴趣小组同学按如图操作完成粗盐(含有难溶性杂质)提纯实验。下列说法正确的是( )
A.去除难溶性杂质的步骤是③
B.④操作中待溶剂全部蒸干后再停止加热
C.正确的操作顺序为①⑤②③⑥④
D.所得精盐潮湿会使产率偏低
【答案】C
9、分别向下列化肥中加入稀盐酸,有气体生成的是( )。
A.NH4HCO3 B.Ca3(PO4)2 C.K2SO4 D.KC1
【答案】A
10、下列实验操作中不能达到实验目的的是( )
选项 物质 目的 主要实验操作
A H2和CO 鉴别 点燃,火焰上罩干冷烧杯,观察现象
B N2和CO2 检验 用燃着的木条伸入集气瓶中,观察现象
C MnO2和KCl的混合物 分离 溶解,过滤,洗涤固体并烘干,蒸发滤液
D Cu中含有少量Fe 除杂 加入过量的稀硫酸,过滤,洗涤干燥
A. A B. B C. C D. D
【答案】B
11、现有4种试剂:①紫色石蕊试液;②稀硫酸;③碳酸钾溶液;④氯化钡溶液。能用来一次性鉴别稀盐酸、氢氧化钡溶液、碳酸钠溶液的试剂有( )
A.② B.②③ C.①②③ D.②③④
【答案】C
12、保护环境的做法很多。下列做法不正确的是( )
A.深埋电池,消除污染 B.合理使用农药,保护水体资源
C.植树造林,净化环境 D.垃圾分类回收,资源合理利用
【答案】A
13、现有以下物质,对它们的分类正确的是( )
①澄清石灰水 ②氧化铜 ③五氧化二磷
④硝酸钾⑤醋酸 ⑥洁净的空气 ⑦纯碱⑧硫酸钾
A.①⑥属于纯净物 B.④⑧属于复合肥
C.①⑦属于碱 D.②③属于氧化物
【答案】D
14、某同学家中种植的植物比正常的植株矮小瘦弱,叶片发黄,有的叶脉呈淡棕色,你认为应该施加下列哪一种化肥( )。
A.氯化钾 B.过磷酸钙 C.硫酸钾 D.尿素
【答案】D
15、下列说法正确的是( )
A. 糖类都具有甜味
B. 油脂和淀粉的组成元素相同,分子组成和结构也相同
C. 碘酒可用来检验食物中是否含有淀粉
D. 摄入人体内的糖类最终都转化为二氧化碳和水
【答案】C
16、下列各组物质分别加入足量的水中,能得到无色透明溶液的是( )
A.FeCl3、NaOH、NaCl B.Na2SO4、HCl、BaCl2
C.CuSO4、KCl、HCl D.Na2CO3、NaCl、Na2SO4
【答案】D
二、填空题。
17、写出下列反应的化学方程式,并按要求填空。
(1)用石灰浆粉刷墙壁,干燥后又白又硬:______________________________。
(2)工业炼铁的主要原理是一氧化碳和氧化铁在高温下反应:_______________________ 。工业炼铁的主要设备是__________________。
(3)车用乙醇汽油不但可以节省石油资源和有效地减少汽车尾气的污染,还可以促进农业生产。乙醇(C2H5OH)完全燃烧的化学方程式为_______________,该反应属于____________(选填:“吸热”或“放热”)反应。
(4)工业上,常用电解氯化钠溶液的方法来制取氢氧化钠,同时还能获得氢气、氯气两种化工产品,其反应的化学方程式为_____________________。
(5)医疗上“钡餐”的主要成分是硫酸钡,不能用碳酸钡替代硫酸钡的原因是用方程式表示_____________,该反应的基本反应类型是__________。
【答案】CO2 + Ca(OH)2 == CaCO3↓+ H2O Fe2O3+3CO 2Fe+3CO2 高炉 C2H5OH+3O23H2O+2CO2 放热 2NaCl+ H2O2NaOH + H2↑+Cl2↑ BaCO3+2HCl == BaCl2 + H2O + CO2↑ 复分解反应
18、我国古代劳动人民常将草木灰(主要成分K2CO3)和生石灰在水中混合,用上层清液漂白丝帛。清液的主要成分及溶解度如图所示。
(1)t1 ℃时3种物质的饱和溶液中溶质质量分数由小到大的顺序是 。
(2)20 ℃时,向4个盛有50 g水的烧杯中,分别加入一定质量的氢氧化钾并充分溶解。4组实验数据如下:
实验序号 A B C D
加入氢氧化钾的质量/g 7 14 56 70
溶液质量/g 57 64 106 106
由上述实验数据可知:
①所得溶液是不饱和溶液的是 (填序号);
②20℃时,将C继续恒温蒸发25 g水,过滤,得到质量为 g的固体。
【答案】(1)Ca(OH)2 <KOH<K2CO3; (2)①AB;②28。
19、小明在进行粗盐提纯和配制一定溶质质量分数的氯化钠溶液时,遇到了如下的问题,请你帮助小明来解答下列问题。
(1)粗盐提纯的步骤为:溶解、________ 、蒸发、计算产率。
(2)经过滤后,食盐水仍浑浊的可能原因是____________________(答一点即可)。
(3)在蒸发实验操作中,当蒸发皿中出现_________________时停止加热。
(4)将配制好的氯化钠溶液,装入试剂瓶时不小心溅出,则剩余溶液中溶质的质量分数_______(填“偏大”、“偏小”或“不变”)。
【答案】(1)过滤 (2)滤纸破损 (3)较多固体 (4)不变
20、请将碳酸钙、不锈钢、金刚石、氮气的用途填在相应的图片下。
(1) ; (2) ;
(3) ; (4) 。
【答案】 (1)金刚石 (2)不锈钢 (3)氮气 (4)碳酸钙
三、实验题。
21、某同学利用下图所示装置证明氢氧化钠溶液能与二氧化碳反应(装置气密性良好,实验前K1、K2均处于关闭状态)。
(1)打开K1,将分液漏斗中的溶液全部注入锥形瓶内,立即关闭K1,观察到有少量白色浑浊产生。查找原因,该异常现象是因为氢氧化钠饱和溶液中混入了氢氧化钙,产生白色浑浊的一个化学方程式为___________ 。该同学分析后确认,即使所加溶液中氢氧化钙达到饱和,反应后A中仍无氢氧化钙剩余,说明理由___________ 。
(2)该同学进一步分析后确定,继续实验仍可证明氢氧化钠溶液能与二氧化碳反应。为利于观察现象,打开K2前A装置需要___________;打开K2,观察到的现象是___________ 。该过程中多孔玻璃球泡的主要作用是___________ 。
(3)实验后,将A中物质过滤,向滤液中滴加酚酞溶液,变红。对滤液进行无害化处理,需加入的一种试剂是___________。
【答案】(1)
(或)
氢氧化钙的溶解度远小于氢氧化钠,所加溶液中即使氢氧化钙饱和,其含量也远小于其中氢氧化钠的量,溶液中的氢氧化钙既能与二氧化碳反应,又能与生成的碳酸钠反应,故反应后氢氧化钙不会剩余。
(2) 充分静置 B中液体倒流入A,A的上层清液中有大量白色沉淀生成
减缓倒流液体对A中溶液的冲击,防止A中已沉淀的碳酸钙的干扰
(3)稀盐酸(其他合理答案也可)
22、某实验小组的甲、乙两同学围绕Na2CO3进行了如图一所示的实验。实验结束后,丙同学把A、B两支试管中的物质倒入同一洁净的烧杯中(如图二),充分混合后发现白色沉淀明显增加。
(1)甲同学的实验完成后,A试管中一定有剩余的物质是 。
(2)乙同学的实验发生的化学方程式是 。
小组同学将C中液体过滤后,对所得滤液的主要成分进行了如下探究:
【猜想与假设】 实验小组的同学对滤液的成分作出了如下猜想:
猜想一:滤液中的溶质是NaCl、Na2CO3
猜想二:滤液中的溶质是NaCl、CaCl2
猜想三:滤液中的溶质是NaCl、CaCl2、HCl
猜想四:滤液中的溶质是NaCl
【讨论与交流】 通过认真讨论,小组同学排除了其中一种不合理的猜想。
(3)不合理的是猜想三,理由是 。
【进行实验】 丁同学取少量滤液置于试管中,向试管中滴加一种物质,发现有无色气泡生成。
(4)你认为丁同学向滤液中滴加的物质是 。
【实验结论】 通过探究,小组同学得出了猜想一是正确的结论。
【答案】Na2CO3
氯化钙和碳酸钠不共存 稀盐酸
四、计算题。
23、某课外活动小组对失去标签的稀硫酸浓度进行测定:取稀硫酸50 g于烧杯中,逐滴滴加3.42%的氢氧化钡溶液,烧杯内溶质质量与滴加氢氧化钡溶液质量关系如图所示。(结果保留两位小数)
(1)参加反应的Ba(OH)2质量共有 g。当滴加Ba(OH)2溶液50g时,烧杯内溶液的pH 7(填“>”“<”或“=”)。
(2)求该硫酸溶液的溶质质量分数。
(3)通过计算,在图中画出产生沉淀质量与滴加Ba(OH)2溶液的质量关系。
(4)滴加Ba(OH)2溶液至150g时,所得溶液的溶质质量分数 。
【答案】(1)3.42; <; (2)3.92%
(3)如图所示:
;
(4)0.88%
一、选择题。
1、下列各组物质混合后不能发生反应的是( )
A. 银和稀盐酸 B. 氢氧化钡溶液和硝酸
C. 铝和稀硫酸 D. 氯化钡溶液和硫酸钠溶液
2、化学与日常生活、工农业生产密切相关。下列说法中不正确的是( )
A. 用含有碳酸氢钠的发酵粉焙制糕点
B. 工业上用熟石灰处理硫酸厂的污水
C. 医疗上用纯酒精作消毒剂
D. 生活中用含有NaOH的清洁剂去油污
3、已知粉末X样品是下列四种物质中的一种,取三等份该粉末,分别加入足量的氢氧化钙溶液、氯化钡溶液、稀盐酸中并振荡,产生的现象如下表。则该固体粉末X是( )
加入物质 氢氧化钙溶液 氯化钡溶液 稀盐酸
现象 产生白色沉淀 产生白色沉淀 固体溶解,产生无色气体
A.CuSO4 B.Na2SO4 C.K2CO3 D.Mg
4、属于复分解反应的是( )
A.4NH3+3O26H2O+2N2
B.Na2SiO3+H2SO4===H2SiO3↓+Na2SO4
C.2FeCl2+Cl2===2FeCl3
D.2HgO2Hg+O2↑
5、尿素【CO(NH2)2】是一种常用的化肥,工业上生产尿素的反应的微观示意图,如下图所示:则下列说法正确的是( )
A.A、B、D三种物质都是氧化物
B.反应中A、B两种物质的质量比为17∶22
C.该反应属于复分解反应
D.该反应前后分子种类没有改变
6、德国化学家弗里茨·哈伯由于发明了合成氨的方法而获得1918年诺贝尔化学奖,他的发明大大提高了农作物的产量同时也提高了硝酸、炸药的产量。下列说法中正确的是( )
A.氮气和氢气在点燃或光照条件下可合成氨
B.氨水显酸性
C.氨气遇到浓盐酸会发生反应产生白烟
D.干燥氨气可用浓硫酸
7、下列关于化肥的说法正确的是( )
A.过磷酸钙[Ca(H2PO4)2和CaSO4的混合物] 属于氮肥
B.凡施用过化肥的蔬菜都会危害健康
C.氯化钾与熟石灰混合、研磨,能闻到刺激性气味
D.硫酸铵与磷矿粉从外观即可区分
8、物质的提纯是生活和科学研究的重要内容。某兴趣小组同学按如图操作完成粗盐(含有难溶性杂质)提纯实验。下列说法正确的是( )
A.去除难溶性杂质的步骤是③
B.④操作中待溶剂全部蒸干后再停止加热
C.正确的操作顺序为①⑤②③⑥④
D.所得精盐潮湿会使产率偏低
9、分别向下列化肥中加入稀盐酸,有气体生成的是( )。
A.NH4HCO3 B.Ca3(PO4)2 C.K2SO4 D.KC1
10、下列实验操作中不能达到实验目的的是( )
选项 物质 目的 主要实验操作
A H2和CO 鉴别 点燃,火焰上罩干冷烧杯,观察现象
B N2和CO2 检验 用燃着的木条伸入集气瓶中,观察现象
C MnO2和KCl的混合物 分离 溶解,过滤,洗涤固体并烘干,蒸发滤液
D Cu中含有少量Fe 除杂 加入过量的稀硫酸,过滤,洗涤干燥
A. A B. B C. C D. D
11、现有4种试剂:①紫色石蕊试液;②稀硫酸;③碳酸钾溶液;④氯化钡溶液。能用来一次性鉴别稀盐酸、氢氧化钡溶液、碳酸钠溶液的试剂有( )
A.② B.②③ C.①②③ D.②③④
12、保护环境的做法很多。下列做法不正确的是( )
A.深埋电池,消除污染 B.合理使用农药,保护水体资源
C.植树造林,净化环境 D.垃圾分类回收,资源合理利用
13、现有以下物质,对它们的分类正确的是( )
①澄清石灰水 ②氧化铜 ③五氧化二磷
④硝酸钾⑤醋酸 ⑥洁净的空气 ⑦纯碱⑧硫酸钾
A.①⑥属于纯净物 B.④⑧属于复合肥
C.①⑦属于碱 D.②③属于氧化物
14、某同学家中种植的植物比正常的植株矮小瘦弱,叶片发黄,有的叶脉呈淡棕色,你认为应该施加下列哪一种化肥( )。
A.氯化钾 B.过磷酸钙 C.硫酸钾 D.尿素
15、下列说法正确的是( )
A. 糖类都具有甜味
B. 油脂和淀粉的组成元素相同,分子组成和结构也相同
C. 碘酒可用来检验食物中是否含有淀粉
D. 摄入人体内的糖类最终都转化为二氧化碳和水
16、下列各组物质分别加入足量的水中,能得到无色透明溶液的是( )
A.FeCl3、NaOH、NaCl B.Na2SO4、HCl、BaCl2
C.CuSO4、KCl、HCl D.Na2CO3、NaCl、Na2SO4
二、填空题。
17、写出下列反应的化学方程式,并按要求填空。
(1)用石灰浆粉刷墙壁,干燥后又白又硬:______________________________。
(2)工业炼铁的主要原理是一氧化碳和氧化铁在高温下反应:_______________________ 。工业炼铁的主要设备是__________________。
(3)车用乙醇汽油不但可以节省石油资源和有效地减少汽车尾气的污染,还可以促进农业生产。乙醇(C2H5OH)完全燃烧的化学方程式为_______________,该反应属于____________(选填:“吸热”或“放热”)反应。
(4)工业上,常用电解氯化钠溶液的方法来制取氢氧化钠,同时还能获得氢气、氯气两种化工产品,其反应的化学方程式为_____________________。
(5)医疗上“钡餐”的主要成分是硫酸钡,不能用碳酸钡替代硫酸钡的原因是用方程式表示_____________,该反应的基本反应类型是__________。
18、我国古代劳动人民常将草木灰(主要成分K2CO3)和生石灰在水中混合,用上层清液漂白丝帛。清液的主要成分及溶解度如图所示。
(1)t1 ℃时3种物质的饱和溶液中溶质质量分数由小到大的顺序是 。
(2)20 ℃时,向4个盛有50 g水的烧杯中,分别加入一定质量的氢氧化钾并充分溶解。4组实验数据如下:
实验序号 A B C D
加入氢氧化钾的质量/g 7 14 56 70
溶液质量/g 57 64 106 106
由上述实验数据可知:
①所得溶液是不饱和溶液的是 (填序号);
②20℃时,将C继续恒温蒸发25 g水,过滤,得到质量为 g的固体。
19、小明在进行粗盐提纯和配制一定溶质质量分数的氯化钠溶液时,遇到了如下的问题,请你帮助小明来解答下列问题。
(1)粗盐提纯的步骤为:溶解、________ 、蒸发、计算产率。
(2)经过滤后,食盐水仍浑浊的可能原因是____________________(答一点即可)。
(3)在蒸发实验操作中,当蒸发皿中出现_________________时停止加热。
(4)将配制好的氯化钠溶液,装入试剂瓶时不小心溅出,则剩余溶液中溶质的质量分数_______(填“偏大”、“偏小”或“不变”)。
20、请将碳酸钙、不锈钢、金刚石、氮气的用途填在相应的图片下。
(1) ; (2) ;
(3) ; (4) 。
三、实验题。
21、某同学利用下图所示装置证明氢氧化钠溶液能与二氧化碳反应(装置气密性良好,实验前K1、K2均处于关闭状态)。
(1)打开K1,将分液漏斗中的溶液全部注入锥形瓶内,立即关闭K1,观察到有少量白色浑浊产生。查找原因,该异常现象是因为氢氧化钠饱和溶液中混入了氢氧化钙,产生白色浑浊的一个化学方程式为___________ 。该同学分析后确认,即使所加溶液中氢氧化钙达到饱和,反应后A中仍无氢氧化钙剩余,说明理由___________ 。
(2)该同学进一步分析后确定,继续实验仍可证明氢氧化钠溶液能与二氧化碳反应。为利于观察现象,打开K2前A装置需要___________;打开K2,观察到的现象是___________ 。该过程中多孔玻璃球泡的主要作用是___________ 。
(3)实验后,将A中物质过滤,向滤液中滴加酚酞溶液,变红。对滤液进行无害化处理,需加入的一种试剂是___________。
22、某实验小组的甲、乙两同学围绕Na2CO3进行了如图一所示的实验。实验结束后,丙同学把A、B两支试管中的物质倒入同一洁净的烧杯中(如图二),充分混合后发现白色沉淀明显增加。
(1)甲同学的实验完成后,A试管中一定有剩余的物质是 。
(2)乙同学的实验发生的化学方程式是 。
小组同学将C中液体过滤后,对所得滤液的主要成分进行了如下探究:
【猜想与假设】 实验小组的同学对滤液的成分作出了如下猜想:
猜想一:滤液中的溶质是NaCl、Na2CO3
猜想二:滤液中的溶质是NaCl、CaCl2
猜想三:滤液中的溶质是NaCl、CaCl2、HCl
猜想四:滤液中的溶质是NaCl
【讨论与交流】 通过认真讨论,小组同学排除了其中一种不合理的猜想。
(3)不合理的是猜想三,理由是 。
【进行实验】 丁同学取少量滤液置于试管中,向试管中滴加一种物质,发现有无色气泡生成。
(4)你认为丁同学向滤液中滴加的物质是 。
【实验结论】 通过探究,小组同学得出了猜想一是正确的结论。
四、计算题。
23、某课外活动小组对失去标签的稀硫酸浓度进行测定:取稀硫酸50 g于烧杯中,逐滴滴加3.42%的氢氧化钡溶液,烧杯内溶质质量与滴加氢氧化钡溶液质量关系如图所示。(结果保留两位小数)
(1)参加反应的Ba(OH)2质量共有 g。当滴加Ba(OH)2溶液50g时,烧杯内溶液的pH 7(填“>”“<”或“=”)。
(2)求该硫酸溶液的溶质质量分数。
(3)通过计算,在图中画出产生沉淀质量与滴加Ba(OH)2溶液的质量关系。
(4)滴加Ba(OH)2溶液至150g时,所得溶液的溶质质量分数 。
2023—2024学年人教化学九年级下册第十一单元 盐 化肥 达标练习附答案
一、选择题。
1、下列各组物质混合后不能发生反应的是( )
A. 银和稀盐酸 B. 氢氧化钡溶液和硝酸
C. 铝和稀硫酸 D. 氯化钡溶液和硫酸钠溶液
【答案】A
2、化学与日常生活、工农业生产密切相关。下列说法中不正确的是( )
A. 用含有碳酸氢钠的发酵粉焙制糕点
B. 工业上用熟石灰处理硫酸厂的污水
C. 医疗上用纯酒精作消毒剂
D. 生活中用含有NaOH的清洁剂去油污
【答案】C
3、已知粉末X样品是下列四种物质中的一种,取三等份该粉末,分别加入足量的氢氧化钙溶液、氯化钡溶液、稀盐酸中并振荡,产生的现象如下表。则该固体粉末X是( )
加入物质 氢氧化钙溶液 氯化钡溶液 稀盐酸
现象 产生白色沉淀 产生白色沉淀 固体溶解,产生无色气体
A.CuSO4 B.Na2SO4 C.K2CO3 D.Mg
【答案】C
4、属于复分解反应的是( )
A.4NH3+3O26H2O+2N2
B.Na2SiO3+H2SO4===H2SiO3↓+Na2SO4
C.2FeCl2+Cl2===2FeCl3
D.2HgO2Hg+O2↑
【答案】B
5、尿素【CO(NH2)2】是一种常用的化肥,工业上生产尿素的反应的微观示意图,如下图所示:则下列说法正确的是( )
A.A、B、D三种物质都是氧化物
B.反应中A、B两种物质的质量比为17∶22
C.该反应属于复分解反应
D.该反应前后分子种类没有改变
【答案】B
6、德国化学家弗里茨·哈伯由于发明了合成氨的方法而获得1918年诺贝尔化学奖,他的发明大大提高了农作物的产量同时也提高了硝酸、炸药的产量。下列说法中正确的是( )
A.氮气和氢气在点燃或光照条件下可合成氨
B.氨水显酸性
C.氨气遇到浓盐酸会发生反应产生白烟
D.干燥氨气可用浓硫酸
【答案】C
7、下列关于化肥的说法正确的是( )
A.过磷酸钙[Ca(H2PO4)2和CaSO4的混合物] 属于氮肥
B.凡施用过化肥的蔬菜都会危害健康
C.氯化钾与熟石灰混合、研磨,能闻到刺激性气味
D.硫酸铵与磷矿粉从外观即可区分
【答案】D
8、物质的提纯是生活和科学研究的重要内容。某兴趣小组同学按如图操作完成粗盐(含有难溶性杂质)提纯实验。下列说法正确的是( )
A.去除难溶性杂质的步骤是③
B.④操作中待溶剂全部蒸干后再停止加热
C.正确的操作顺序为①⑤②③⑥④
D.所得精盐潮湿会使产率偏低
【答案】C
9、分别向下列化肥中加入稀盐酸,有气体生成的是( )。
A.NH4HCO3 B.Ca3(PO4)2 C.K2SO4 D.KC1
【答案】A
10、下列实验操作中不能达到实验目的的是( )
选项 物质 目的 主要实验操作
A H2和CO 鉴别 点燃,火焰上罩干冷烧杯,观察现象
B N2和CO2 检验 用燃着的木条伸入集气瓶中,观察现象
C MnO2和KCl的混合物 分离 溶解,过滤,洗涤固体并烘干,蒸发滤液
D Cu中含有少量Fe 除杂 加入过量的稀硫酸,过滤,洗涤干燥
A. A B. B C. C D. D
【答案】B
11、现有4种试剂:①紫色石蕊试液;②稀硫酸;③碳酸钾溶液;④氯化钡溶液。能用来一次性鉴别稀盐酸、氢氧化钡溶液、碳酸钠溶液的试剂有( )
A.② B.②③ C.①②③ D.②③④
【答案】C
12、保护环境的做法很多。下列做法不正确的是( )
A.深埋电池,消除污染 B.合理使用农药,保护水体资源
C.植树造林,净化环境 D.垃圾分类回收,资源合理利用
【答案】A
13、现有以下物质,对它们的分类正确的是( )
①澄清石灰水 ②氧化铜 ③五氧化二磷
④硝酸钾⑤醋酸 ⑥洁净的空气 ⑦纯碱⑧硫酸钾
A.①⑥属于纯净物 B.④⑧属于复合肥
C.①⑦属于碱 D.②③属于氧化物
【答案】D
14、某同学家中种植的植物比正常的植株矮小瘦弱,叶片发黄,有的叶脉呈淡棕色,你认为应该施加下列哪一种化肥( )。
A.氯化钾 B.过磷酸钙 C.硫酸钾 D.尿素
【答案】D
15、下列说法正确的是( )
A. 糖类都具有甜味
B. 油脂和淀粉的组成元素相同,分子组成和结构也相同
C. 碘酒可用来检验食物中是否含有淀粉
D. 摄入人体内的糖类最终都转化为二氧化碳和水
【答案】C
16、下列各组物质分别加入足量的水中,能得到无色透明溶液的是( )
A.FeCl3、NaOH、NaCl B.Na2SO4、HCl、BaCl2
C.CuSO4、KCl、HCl D.Na2CO3、NaCl、Na2SO4
【答案】D
二、填空题。
17、写出下列反应的化学方程式,并按要求填空。
(1)用石灰浆粉刷墙壁,干燥后又白又硬:______________________________。
(2)工业炼铁的主要原理是一氧化碳和氧化铁在高温下反应:_______________________ 。工业炼铁的主要设备是__________________。
(3)车用乙醇汽油不但可以节省石油资源和有效地减少汽车尾气的污染,还可以促进农业生产。乙醇(C2H5OH)完全燃烧的化学方程式为_______________,该反应属于____________(选填:“吸热”或“放热”)反应。
(4)工业上,常用电解氯化钠溶液的方法来制取氢氧化钠,同时还能获得氢气、氯气两种化工产品,其反应的化学方程式为_____________________。
(5)医疗上“钡餐”的主要成分是硫酸钡,不能用碳酸钡替代硫酸钡的原因是用方程式表示_____________,该反应的基本反应类型是__________。
【答案】CO2 + Ca(OH)2 == CaCO3↓+ H2O Fe2O3+3CO 2Fe+3CO2 高炉 C2H5OH+3O23H2O+2CO2 放热 2NaCl+ H2O2NaOH + H2↑+Cl2↑ BaCO3+2HCl == BaCl2 + H2O + CO2↑ 复分解反应
18、我国古代劳动人民常将草木灰(主要成分K2CO3)和生石灰在水中混合,用上层清液漂白丝帛。清液的主要成分及溶解度如图所示。
(1)t1 ℃时3种物质的饱和溶液中溶质质量分数由小到大的顺序是 。
(2)20 ℃时,向4个盛有50 g水的烧杯中,分别加入一定质量的氢氧化钾并充分溶解。4组实验数据如下:
实验序号 A B C D
加入氢氧化钾的质量/g 7 14 56 70
溶液质量/g 57 64 106 106
由上述实验数据可知:
①所得溶液是不饱和溶液的是 (填序号);
②20℃时,将C继续恒温蒸发25 g水,过滤,得到质量为 g的固体。
【答案】(1)Ca(OH)2 <KOH<K2CO3; (2)①AB;②28。
19、小明在进行粗盐提纯和配制一定溶质质量分数的氯化钠溶液时,遇到了如下的问题,请你帮助小明来解答下列问题。
(1)粗盐提纯的步骤为:溶解、________ 、蒸发、计算产率。
(2)经过滤后,食盐水仍浑浊的可能原因是____________________(答一点即可)。
(3)在蒸发实验操作中,当蒸发皿中出现_________________时停止加热。
(4)将配制好的氯化钠溶液,装入试剂瓶时不小心溅出,则剩余溶液中溶质的质量分数_______(填“偏大”、“偏小”或“不变”)。
【答案】(1)过滤 (2)滤纸破损 (3)较多固体 (4)不变
20、请将碳酸钙、不锈钢、金刚石、氮气的用途填在相应的图片下。
(1) ; (2) ;
(3) ; (4) 。
【答案】 (1)金刚石 (2)不锈钢 (3)氮气 (4)碳酸钙
三、实验题。
21、某同学利用下图所示装置证明氢氧化钠溶液能与二氧化碳反应(装置气密性良好,实验前K1、K2均处于关闭状态)。
(1)打开K1,将分液漏斗中的溶液全部注入锥形瓶内,立即关闭K1,观察到有少量白色浑浊产生。查找原因,该异常现象是因为氢氧化钠饱和溶液中混入了氢氧化钙,产生白色浑浊的一个化学方程式为___________ 。该同学分析后确认,即使所加溶液中氢氧化钙达到饱和,反应后A中仍无氢氧化钙剩余,说明理由___________ 。
(2)该同学进一步分析后确定,继续实验仍可证明氢氧化钠溶液能与二氧化碳反应。为利于观察现象,打开K2前A装置需要___________;打开K2,观察到的现象是___________ 。该过程中多孔玻璃球泡的主要作用是___________ 。
(3)实验后,将A中物质过滤,向滤液中滴加酚酞溶液,变红。对滤液进行无害化处理,需加入的一种试剂是___________。
【答案】(1)
(或)
氢氧化钙的溶解度远小于氢氧化钠,所加溶液中即使氢氧化钙饱和,其含量也远小于其中氢氧化钠的量,溶液中的氢氧化钙既能与二氧化碳反应,又能与生成的碳酸钠反应,故反应后氢氧化钙不会剩余。
(2) 充分静置 B中液体倒流入A,A的上层清液中有大量白色沉淀生成
减缓倒流液体对A中溶液的冲击,防止A中已沉淀的碳酸钙的干扰
(3)稀盐酸(其他合理答案也可)
22、某实验小组的甲、乙两同学围绕Na2CO3进行了如图一所示的实验。实验结束后,丙同学把A、B两支试管中的物质倒入同一洁净的烧杯中(如图二),充分混合后发现白色沉淀明显增加。
(1)甲同学的实验完成后,A试管中一定有剩余的物质是 。
(2)乙同学的实验发生的化学方程式是 。
小组同学将C中液体过滤后,对所得滤液的主要成分进行了如下探究:
【猜想与假设】 实验小组的同学对滤液的成分作出了如下猜想:
猜想一:滤液中的溶质是NaCl、Na2CO3
猜想二:滤液中的溶质是NaCl、CaCl2
猜想三:滤液中的溶质是NaCl、CaCl2、HCl
猜想四:滤液中的溶质是NaCl
【讨论与交流】 通过认真讨论,小组同学排除了其中一种不合理的猜想。
(3)不合理的是猜想三,理由是 。
【进行实验】 丁同学取少量滤液置于试管中,向试管中滴加一种物质,发现有无色气泡生成。
(4)你认为丁同学向滤液中滴加的物质是 。
【实验结论】 通过探究,小组同学得出了猜想一是正确的结论。
【答案】Na2CO3
氯化钙和碳酸钠不共存 稀盐酸
四、计算题。
23、某课外活动小组对失去标签的稀硫酸浓度进行测定:取稀硫酸50 g于烧杯中,逐滴滴加3.42%的氢氧化钡溶液,烧杯内溶质质量与滴加氢氧化钡溶液质量关系如图所示。(结果保留两位小数)
(1)参加反应的Ba(OH)2质量共有 g。当滴加Ba(OH)2溶液50g时,烧杯内溶液的pH 7(填“>”“<”或“=”)。
(2)求该硫酸溶液的溶质质量分数。
(3)通过计算,在图中画出产生沉淀质量与滴加Ba(OH)2溶液的质量关系。
(4)滴加Ba(OH)2溶液至150g时,所得溶液的溶质质量分数 。
【答案】(1)3.42; <; (2)3.92%
(3)如图所示:
;
(4)0.88%
同课章节目录
