第八章 常见的酸、碱、盐 课后训练题(含答案) -2023-2024学年科粤版(2012)化学九年级下册
文档属性
| 名称 | 第八章 常见的酸、碱、盐 课后训练题(含答案) -2023-2024学年科粤版(2012)化学九年级下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 284.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-18 00:00:00 | ||
图片预览




文档简介
第八章 常见的酸、碱、盐 课后训练题(含答案)2023—2024学年科粤版(2012)化学九年级下册
一、选择题。
1、下列溶液能使紫色石蕊溶液变成蓝色的是( )
A.澄清石灰水 B.NaCl溶液 C.稀硫酸 D.KNO3溶液
2、关于酸和碱的描述正确的是( )
A.紫色石蕊溶液遇碱溶液变蓝色 B.生石灰和熟石灰都属于碱
C.酸就是有酸味的物质 D.碱就是有腐蚀性的物质
3、将下列不同pH的各组溶液混合,得到溶液的pH可能为7的是( )
A.pH=3 pH=4 B.pH=11 pH=7
C.pH=6 pH=8 D.pH=0 pH=5
4、下列变化中不能一步实现的是( )
A.Ba(OH)2→BaCl2 B.Fe2O3→Fe
C.BaCl2→BaSO4 D.CuO→Cu(OH)2
5、下列说法中,正确的是( )
A.若某雨水的pH 7,则该雨水一定呈酸性
B.某物质与酸反应放出气体,则该物质一定是碳酸盐
C.草木灰的主要成分碳酸钾属于盐类,所以能与铵盐混合使用
D.一种无色气体能使燃着的木条熄灭,那么该气体一定是二氧化碳
6、以下物质名称、俗名及分类对应正确的是( )
A.C60一金刚石一单质 B.氢氧化钠一纯碱一碱
C.氧化钙一熟石灰一氧化物 D.碳酸钠一苏打一盐
7、头发油腻是因为油脂的分泌,清洗时碱性溶液效果更好。从pH角度考虑效果最好的洗发水的pH为( )
A.8 B.7 C.6 D.4
8、小李在学习酸碱指示剂与常见酸、碱溶液作用时,归纳成如右图所示的关系。图中A、B、C、D是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示出的颜色,则其中表示不正确的是( )
A.紫色 B.蓝色 C.红色 D.无色
9、我们知道物质的性质决定其用途。下列对应关系不成立的( )
A.稀有气体化学性质稳定——作保护气
B.熟石灰显碱性—一用来改良酸性土壤
C.二氧化碳能与水反应—一可作制冷剂用于人工降雨
D.小苏打能与盐酸反应——可用于治疗胃酸过多
10、下列物质中,属于氧化物的是( )
A.水 B.高锰酸钾 C.氧气 D.氯酸钾
11、下列实验方案设计合理的是( )
选项 实验目的 实验方案
A 除去氢氧化钠溶液中少量碳酸钠 加过量的氢氧化钙溶液后过滤
B 除去氧化钙中少量碳酸钙 加适量的稀盐酸
C 鉴别硝酸钾和氯化铵固体 取样,分别与熟石灰混合研磨
D 鉴别硬水和软水 取样,加热
A.A B.B C.C D.D
12、下列含氮的化肥中,含氮量最高的是( )
A.硫铵 B.尿素 C.碳铵 D.硝铵
13、下列溶液显碱性的是( )
A.酸雨 B.食醋 C.NaOH溶液 D.盐酸
14、在托盘天平两边各放一只烧杯,调节至平衡.在两只烧杯里注入相同质量、相同质量分数的足量稀盐酸,然后分别向左右两端烧杯中加入质量相等的和金属.有气体产生时,托盘天平指针慢慢向左偏转(如图所示);指针偏转到一定角度后,又慢慢向右偏转;反应结束,托盘天平指针指向右端.则托盘天平右端加入的金属可能是( )
A. B. C. D.
15、性质决定用途,性质和用途均正确的是( )
A.氢氧化钠能与酸反应,可治疗胃酸过多
B.活性炭具有吸附性,作自来水消毒剂
C.一氧化碳有还原性,冶炼金属
D.稀有气体化学性质稳定,制霓虹灯
16、中盐河南盐业配送中心设置盐文化展区。盐汽水是一种能补充人体盐分的饮品,你认为盐汽水的成分和普通汽水最大的不同是增加了( )
A.水 B.氯化钠 C.二氧化碳 D.碳酸钙
二、填空题。
17、“十三五”以来,我省污染防治攻坚战取得阶段性成果,生态环境质量明显好转。
(1)在蓝天保卫战中,全省城市空气质量持续改善,重污染天数逐年减少。煤改气有利于减少酸雨的形成,造成酸雨的有害气体主要是 (写一种即可)。
(2)在净土保卫战中,实行重金属污染物排放限值标准。重金属污染物“铅、镉、汞”等指的是 (填“分子”“原子”或“元素”)。
18、(1)在稀释浓硫酸时,一定要把___________________________ ,并不断 ___________ 。
(2)下图是课本上的一个重要探究性实验,
请说出由该实验得出的两个重要结论是:
① _______________________________________________________ ;
② _______________________________________________________ 。
19、向盐酸中滴加氢氧化钠溶液时,当溶液的pH=5时,溶液显____性,溶液中的溶质是__________,(填化学式)当溶液的pH=7时,溶液显____性,溶液中的溶质是__________(填化学式),当溶液的pH=13时,溶液显____性,溶液中的溶质是_________(填化学式)。
20、回答下列与含碳物质有关的问题。
(1)普通干电池采用石墨作为电极材料,是利用其优良的__________性;
(2)高炉炼铁的主要反应为3CO+ Fe2O32Fe + 3CO2 ,该反应利用CO化学性质中的____性;
(3)碳酸钠、碳酸钙都含有CO32-,都能与盐酸反应生成盐、水和__________。
21、写出相应物质的化学式
〔1)某淡黄色粉末在氧气中燃烧产生一种刺激性气味的气体A,该气体能使稀高锰酸钾溶液褪色,A为_________。
(2)银白色固体B,能与酸反应,在空气中燃烧产生耀眼强光,B是_______。
(3)白色固体C,加热完全反应后无固体残留,并生成水同时产生一种刺激性气味的气体,C可能是__________。
22、近年科学家提出绿色自由”构想:把含有大量CO2的空气吹入盛有饱和碳酸钾( K2CO3)溶液的反应池中,反应生成碳酸氢钾(KHCO3),然后再把 CO2从分解池溶液中提取出来,在合成塔中经化学反应后使之变为可再生燃料甲醇(CH3OH)。“绿色自由”构想工艺流程如图所示:
已知:(1) 吸收池中的反应为
(2)分解池中的反应为
回答下列问题:
(1)进入分解池中的主要物质是 。
(2)该工艺在哪些方面体现了“绿色自由”构想中的“绿色”:
。(答一条即可)
(3)该流程中可以循环利用的物质是 。
(4)写出合成塔中生成甲醇的化学方程式: 。
三、实验题。
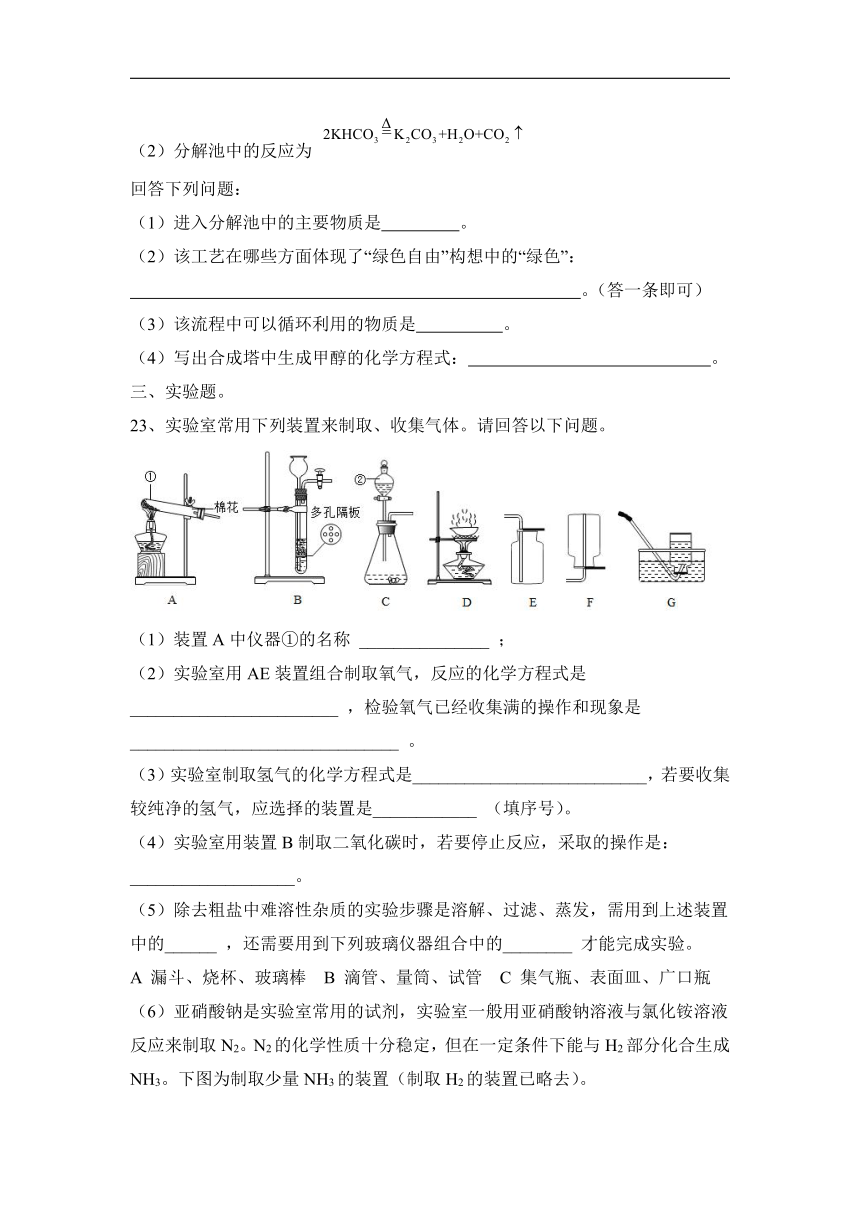
23、实验室常用下列装置来制取、收集气体。请回答以下问题。
(1)装置A中仪器①的名称 _______________ ;
(2)实验室用AE装置组合制取氧气,反应的化学方程式是 ________________________ ,检验氧气已经收集满的操作和现象是 _______________________________ 。
(3)实验室制取氢气的化学方程式是___________________________,若要收集较纯净的氢气,应选择的装置是____________ (填序号)。
(4)实验室用装置B制取二氧化碳时,若要停止反应,采取的操作是:
___________________。
(5)除去粗盐中难溶性杂质的实验步骤是溶解、过滤、蒸发,需用到上述装置中的______ ,还需要用到下列玻璃仪器组合中的________ 才能完成实验。
A 漏斗、烧杯、玻璃棒 B 滴管、量筒、试管 C 集气瓶、表面皿、广口瓶
(6)亚硝酸钠是实验室常用的试剂,实验室一般用亚硝酸钠溶液与氯化铵溶液反应来制取N2。N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3。下图为制取少量NH3的装置(制取H2的装置已略去)。
①C装置的硬质试管中发生反应的化学方程式为 ________________________ 。
②反应时N2和H2的最佳质量比是 _________ 。如果按此比例进行反应,反应时,若D中导管口有气泡逸出,(已知NH3极易溶于水),说明逸出气泡的原因:
_____________ 。
③用实验方法证明确实有NH3生成:________________________________ 。
四、科普阅读题。
24、化学用语是化学学科的专用语言,也是学习化学的重要工具。
(1)请从氧气、二氧化碳、氯化钠、盐酸、硫酸、氢氧化钙中选择合适的物质,将其化学式填写在下列横线上。
①可供给呼吸的气体单质_____ ②参与光合作用的氧化物_____
③一种不易挥发的无机酸 _____ ④常用于食品调味的盐 _____
(2)铁缺乏被认为是全球三大“隐性饥饿”之首(微量营养元素缺乏),全球约有1/5的人患缺铁性贫血。食物铁强化是目前国际公认的最经济、有效和可持续的给人群补铁的方法。中国疾控中心研制的新型铁强化剂(EDTA钠铁)在人体内的铁吸收、利用率高于其他铁剂,是传统补铁剂硫酸亚铁的2倍至3倍。它在酱油中的溶解性较好,不影响食品口感,不改变酱油的原有口味。此外,EDTA钠铁在食品加工和储存过程中性质稳定,它在酱油中可稳定保持两年以上。研究表明,应用铁强化酱油补铁效果显著。EDTA钠铁的化学式为C10H12FeN2NaO8,它是一种淡土黄色结晶性粉末,易溶于水,性质稳定,不易被氧化,其水溶液pH在3.5~5.5之间。
根据上述信息,请回答下列问题:
①EDTA钠铁属于_____ 。(选填“混合物”、“有机物”、“无机物”或“氧化物”之一)
②EDTA钠铁中,碳、氧原子个数比为_____ (填最简整数比)。
③EDTA钠铁中,元素质量分数最小的是_____ 元素。
④EDTA钠铁的化学性质_____ (至少答一条)。
⑤若经常使用铁锅炒菜做饭,也能有效预防缺铁性贫血,其反应原理的化学方程式为:(已知胃液中含有盐酸)_____ 。
五、计算题。
25、某课外兴趣小组对实验室中的一瓶稀硫酸样品进行分析。他们分别用100 g稀硫酸与不同质量的锌粒(含杂质,杂质不与稀硫酸反应)反应,三次实验的数据如下表。
实验次数 1 2 3
加入锌粒的质量(g) 4 8 12
充分反应后剩余物质的总质量(g) 103.9 107.8 111.8
请回答下列问题:
(1)第 次实验,锌粒与稀硫酸恰好完全反应。
(2)计算稀硫酸的溶质质量分数为 。【写出计算过程】
第八章 常见的酸、碱、盐 课后训练题(含答案)2023—2024学年科粤版(2012)化学九年级下册
一、选择题。
1、下列溶液能使紫色石蕊溶液变成蓝色的是( )
A.澄清石灰水 B.NaCl溶液 C.稀硫酸 D.KNO3溶液
【答案】A
2、关于酸和碱的描述正确的是( )
A.紫色石蕊溶液遇碱溶液变蓝色 B.生石灰和熟石灰都属于碱
C.酸就是有酸味的物质 D.碱就是有腐蚀性的物质
【答案】A
3、将下列不同pH的各组溶液混合,得到溶液的pH可能为7的是( )
A.pH=3 pH=4 B.pH=11 pH=7
C.pH=6 pH=8 D.pH=0 pH=5
【答案】C
4、下列变化中不能一步实现的是( )
A.Ba(OH)2→BaCl2 B.Fe2O3→Fe
C.BaCl2→BaSO4 D.CuO→Cu(OH)2
【答案】D
5、下列说法中,正确的是( )
A.若某雨水的pH 7,则该雨水一定呈酸性
B.某物质与酸反应放出气体,则该物质一定是碳酸盐
C.草木灰的主要成分碳酸钾属于盐类,所以能与铵盐混合使用
D.一种无色气体能使燃着的木条熄灭,那么该气体一定是二氧化碳
【答案】A
6、以下物质名称、俗名及分类对应正确的是( )
A.C60一金刚石一单质 B.氢氧化钠一纯碱一碱
C.氧化钙一熟石灰一氧化物 D.碳酸钠一苏打一盐
【答案】D
7、头发油腻是因为油脂的分泌,清洗时碱性溶液效果更好。从pH角度考虑效果最好的洗发水的pH为( )
A.8 B.7 C.6 D.4
【答案】A
8、小李在学习酸碱指示剂与常见酸、碱溶液作用时,归纳成如右图所示的关系。图中A、B、C、D是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示出的颜色,则其中表示不正确的是( )
A.紫色 B.蓝色 C.红色 D.无色
【答案】A
9、我们知道物质的性质决定其用途。下列对应关系不成立的( )
A.稀有气体化学性质稳定——作保护气
B.熟石灰显碱性—一用来改良酸性土壤
C.二氧化碳能与水反应—一可作制冷剂用于人工降雨
D.小苏打能与盐酸反应——可用于治疗胃酸过多
【答案】C
10、下列物质中,属于氧化物的是( )
A.水 B.高锰酸钾 C.氧气 D.氯酸钾
【答案】A
11、下列实验方案设计合理的是( )
选项 实验目的 实验方案
A 除去氢氧化钠溶液中少量碳酸钠 加过量的氢氧化钙溶液后过滤
B 除去氧化钙中少量碳酸钙 加适量的稀盐酸
C 鉴别硝酸钾和氯化铵固体 取样,分别与熟石灰混合研磨
D 鉴别硬水和软水 取样,加热
A.A B.B C.C D.D
【答案】C
12、下列含氮的化肥中,含氮量最高的是( )
A.硫铵 B.尿素 C.碳铵 D.硝铵
【答案】B
13、下列溶液显碱性的是( )
A.酸雨 B.食醋 C.NaOH溶液 D.盐酸
【答案】C
14、在托盘天平两边各放一只烧杯,调节至平衡.在两只烧杯里注入相同质量、相同质量分数的足量稀盐酸,然后分别向左右两端烧杯中加入质量相等的和金属.有气体产生时,托盘天平指针慢慢向左偏转(如图所示);指针偏转到一定角度后,又慢慢向右偏转;反应结束,托盘天平指针指向右端.则托盘天平右端加入的金属可能是( )
A. B. C. D.
【答案】A
15、性质决定用途,性质和用途均正确的是( )
A.氢氧化钠能与酸反应,可治疗胃酸过多
B.活性炭具有吸附性,作自来水消毒剂
C.一氧化碳有还原性,冶炼金属
D.稀有气体化学性质稳定,制霓虹灯
【答案】C
16、中盐河南盐业配送中心设置盐文化展区。盐汽水是一种能补充人体盐分的饮品,你认为盐汽水的成分和普通汽水最大的不同是增加了( )
A.水 B.氯化钠 C.二氧化碳 D.碳酸钙
【答案】B
二、填空题。
17、“十三五”以来,我省污染防治攻坚战取得阶段性成果,生态环境质量明显好转。
(1)在蓝天保卫战中,全省城市空气质量持续改善,重污染天数逐年减少。煤改气有利于减少酸雨的形成,造成酸雨的有害气体主要是 (写一种即可)。
(2)在净土保卫战中,实行重金属污染物排放限值标准。重金属污染物“铅、镉、汞”等指的是 (填“分子”“原子”或“元素”)。
【答案】(1)SO2(或NO2); (2)元素。
18、(1)在稀释浓硫酸时,一定要把___________________________ ,并不断 ___________ 。
(2)下图是课本上的一个重要探究性实验,
请说出由该实验得出的两个重要结论是:
① _______________________________________________________ ;
② _______________________________________________________ 。
【答案】(1)浓硫酸沿器壁慢慢注入水里 用玻璃棒搅拌
(2)可燃物的燃烧需要氧气 可燃物的燃烧需要温度达到着火点
19、向盐酸中滴加氢氧化钠溶液时,当溶液的pH=5时,溶液显____性,溶液中的溶质是__________,(填化学式)当溶液的pH=7时,溶液显____性,溶液中的溶质是__________(填化学式),当溶液的pH=13时,溶液显____性,溶液中的溶质是_________(填化学式)。
【答案】酸 HCl和NaCl 中 NaCl 碱 NaCl和NaOH
20、回答下列与含碳物质有关的问题。
(1)普通干电池采用石墨作为电极材料,是利用其优良的__________性;
(2)高炉炼铁的主要反应为3CO+ Fe2O32Fe + 3CO2 ,该反应利用CO化学性质中的____性;
(3)碳酸钠、碳酸钙都含有CO32-,都能与盐酸反应生成盐、水和__________。
【答案】导电性 还原性 二氧化碳
21、写出相应物质的化学式
〔1)某淡黄色粉末在氧气中燃烧产生一种刺激性气味的气体A,该气体能使稀高锰酸钾溶液褪色,A为_________。
(2)银白色固体B,能与酸反应,在空气中燃烧产生耀眼强光,B是_______。
(3)白色固体C,加热完全反应后无固体残留,并生成水同时产生一种刺激性气味的气体,C可能是__________。
【答案】
22、近年科学家提出绿色自由”构想:把含有大量CO2的空气吹入盛有饱和碳酸钾( K2CO3)溶液的反应池中,反应生成碳酸氢钾(KHCO3),然后再把 CO2从分解池溶液中提取出来,在合成塔中经化学反应后使之变为可再生燃料甲醇(CH3OH)。“绿色自由”构想工艺流程如图所示:
已知:(1) 吸收池中的反应为
(2)分解池中的反应为
回答下列问题:
(1)进入分解池中的主要物质是 。
(2)该工艺在哪些方面体现了“绿色自由”构想中的“绿色”:
。(答一条即可)
(3)该流程中可以循环利用的物质是 。
(4)写出合成塔中生成甲醇的化学方程式: 。
【答案】(1)KHCO3
减少大气中的CO2,产生清洁能源,实现低碳经济(合理即可)
(3)K2CO3 (4)
三、实验题。
23、实验室常用下列装置来制取、收集气体。请回答以下问题。
(1)装置A中仪器①的名称 _______________ ;
(2)实验室用AE装置组合制取氧气,反应的化学方程式是 ________________________ ,检验氧气已经收集满的操作和现象是 _______________________________ 。
(3)实验室制取氢气的化学方程式是___________________________,若要收集较纯净的氢气,应选择的装置是____________ (填序号)。
(4)实验室用装置B制取二氧化碳时,若要停止反应,采取的操作是:
___________________。
(5)除去粗盐中难溶性杂质的实验步骤是溶解、过滤、蒸发,需用到上述装置中的______ ,还需要用到下列玻璃仪器组合中的________ 才能完成实验。
A 漏斗、烧杯、玻璃棒 B 滴管、量筒、试管 C 集气瓶、表面皿、广口瓶
(6)亚硝酸钠是实验室常用的试剂,实验室一般用亚硝酸钠溶液与氯化铵溶液反应来制取N2。N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3。下图为制取少量NH3的装置(制取H2的装置已略去)。
①C装置的硬质试管中发生反应的化学方程式为 ________________________ 。
②反应时N2和H2的最佳质量比是 _________ 。如果按此比例进行反应,反应时,若D中导管口有气泡逸出,(已知NH3极易溶于水),说明逸出气泡的原因:
_____________ 。
③用实验方法证明确实有NH3生成:________________________________ 。
【答案】(1)试管
(2)把带火星的木条放到集气瓶口,如果木条复燃,说明氧气已收集满
(3)Zn+H2SO4(稀)=ZnSO4+H2↑ G
(4)关闭导气管上的开关 (5)D A
(6)N2+3H22NH3 28∶6
氮气和氢气是部分化合,还有未反应的氮气和氢气逸出
向D中滴入无色酚酞试液,酚酞变红,说明有氨气生成
四、科普阅读题。
24、化学用语是化学学科的专用语言,也是学习化学的重要工具。
(1)请从氧气、二氧化碳、氯化钠、盐酸、硫酸、氢氧化钙中选择合适的物质,将其化学式填写在下列横线上。
①可供给呼吸的气体单质_____ ②参与光合作用的氧化物_____
③一种不易挥发的无机酸 _____ ④常用于食品调味的盐 _____
(2)铁缺乏被认为是全球三大“隐性饥饿”之首(微量营养元素缺乏),全球约有1/5的人患缺铁性贫血。食物铁强化是目前国际公认的最经济、有效和可持续的给人群补铁的方法。中国疾控中心研制的新型铁强化剂(EDTA钠铁)在人体内的铁吸收、利用率高于其他铁剂,是传统补铁剂硫酸亚铁的2倍至3倍。它在酱油中的溶解性较好,不影响食品口感,不改变酱油的原有口味。此外,EDTA钠铁在食品加工和储存过程中性质稳定,它在酱油中可稳定保持两年以上。研究表明,应用铁强化酱油补铁效果显著。EDTA钠铁的化学式为C10H12FeN2NaO8,它是一种淡土黄色结晶性粉末,易溶于水,性质稳定,不易被氧化,其水溶液pH在3.5~5.5之间。
根据上述信息,请回答下列问题:
①EDTA钠铁属于_____ 。(选填“混合物”、“有机物”、“无机物”或“氧化物”之一)
②EDTA钠铁中,碳、氧原子个数比为_____ (填最简整数比)。
③EDTA钠铁中,元素质量分数最小的是_____ 元素。
④EDTA钠铁的化学性质_____ (至少答一条)。
⑤若经常使用铁锅炒菜做饭,也能有效预防缺铁性贫血,其反应原理的化学方程式为:(已知胃液中含有盐酸)_____ 。
【答案】(1)O2 CO2 H2SO4 NaCl
(2)有机物 5∶4 H 不易被氧化,其水溶液显酸性
五、计算题。
25、某课外兴趣小组对实验室中的一瓶稀硫酸样品进行分析。他们分别用100 g稀硫酸与不同质量的锌粒(含杂质,杂质不与稀硫酸反应)反应,三次实验的数据如下表。
实验次数 1 2 3
加入锌粒的质量(g) 4 8 12
充分反应后剩余物质的总质量(g) 103.9 107.8 111.8
请回答下列问题:
(1)第 次实验,锌粒与稀硫酸恰好完全反应。
(2)计算稀硫酸的溶质质量分数为 。【写出计算过程】
【答案】2 9.8%
【详解】(1)由三次实验数据可知,可发现每加入4g锌粒样品就可放出氢气的质量;而第2次加入8g和第3次加入12g同样的锌粒后放出氢气的质量均为0.2g,第2次所加的8g锌恰好与100g稀硫酸完全反应,故第2次实验,锌粒与稀硫酸恰好完全反应。
(2)8克锌粒完全反应生成氢气的质量是
设生成0.2g氢气需H2SO4的质量为x
该稀硫酸的质量分数为
一、选择题。
1、下列溶液能使紫色石蕊溶液变成蓝色的是( )
A.澄清石灰水 B.NaCl溶液 C.稀硫酸 D.KNO3溶液
2、关于酸和碱的描述正确的是( )
A.紫色石蕊溶液遇碱溶液变蓝色 B.生石灰和熟石灰都属于碱
C.酸就是有酸味的物质 D.碱就是有腐蚀性的物质
3、将下列不同pH的各组溶液混合,得到溶液的pH可能为7的是( )
A.pH=3 pH=4 B.pH=11 pH=7
C.pH=6 pH=8 D.pH=0 pH=5
4、下列变化中不能一步实现的是( )
A.Ba(OH)2→BaCl2 B.Fe2O3→Fe
C.BaCl2→BaSO4 D.CuO→Cu(OH)2
5、下列说法中,正确的是( )
A.若某雨水的pH 7,则该雨水一定呈酸性
B.某物质与酸反应放出气体,则该物质一定是碳酸盐
C.草木灰的主要成分碳酸钾属于盐类,所以能与铵盐混合使用
D.一种无色气体能使燃着的木条熄灭,那么该气体一定是二氧化碳
6、以下物质名称、俗名及分类对应正确的是( )
A.C60一金刚石一单质 B.氢氧化钠一纯碱一碱
C.氧化钙一熟石灰一氧化物 D.碳酸钠一苏打一盐
7、头发油腻是因为油脂的分泌,清洗时碱性溶液效果更好。从pH角度考虑效果最好的洗发水的pH为( )
A.8 B.7 C.6 D.4
8、小李在学习酸碱指示剂与常见酸、碱溶液作用时,归纳成如右图所示的关系。图中A、B、C、D是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示出的颜色,则其中表示不正确的是( )
A.紫色 B.蓝色 C.红色 D.无色
9、我们知道物质的性质决定其用途。下列对应关系不成立的( )
A.稀有气体化学性质稳定——作保护气
B.熟石灰显碱性—一用来改良酸性土壤
C.二氧化碳能与水反应—一可作制冷剂用于人工降雨
D.小苏打能与盐酸反应——可用于治疗胃酸过多
10、下列物质中,属于氧化物的是( )
A.水 B.高锰酸钾 C.氧气 D.氯酸钾
11、下列实验方案设计合理的是( )
选项 实验目的 实验方案
A 除去氢氧化钠溶液中少量碳酸钠 加过量的氢氧化钙溶液后过滤
B 除去氧化钙中少量碳酸钙 加适量的稀盐酸
C 鉴别硝酸钾和氯化铵固体 取样,分别与熟石灰混合研磨
D 鉴别硬水和软水 取样,加热
A.A B.B C.C D.D
12、下列含氮的化肥中,含氮量最高的是( )
A.硫铵 B.尿素 C.碳铵 D.硝铵
13、下列溶液显碱性的是( )
A.酸雨 B.食醋 C.NaOH溶液 D.盐酸
14、在托盘天平两边各放一只烧杯,调节至平衡.在两只烧杯里注入相同质量、相同质量分数的足量稀盐酸,然后分别向左右两端烧杯中加入质量相等的和金属.有气体产生时,托盘天平指针慢慢向左偏转(如图所示);指针偏转到一定角度后,又慢慢向右偏转;反应结束,托盘天平指针指向右端.则托盘天平右端加入的金属可能是( )
A. B. C. D.
15、性质决定用途,性质和用途均正确的是( )
A.氢氧化钠能与酸反应,可治疗胃酸过多
B.活性炭具有吸附性,作自来水消毒剂
C.一氧化碳有还原性,冶炼金属
D.稀有气体化学性质稳定,制霓虹灯
16、中盐河南盐业配送中心设置盐文化展区。盐汽水是一种能补充人体盐分的饮品,你认为盐汽水的成分和普通汽水最大的不同是增加了( )
A.水 B.氯化钠 C.二氧化碳 D.碳酸钙
二、填空题。
17、“十三五”以来,我省污染防治攻坚战取得阶段性成果,生态环境质量明显好转。
(1)在蓝天保卫战中,全省城市空气质量持续改善,重污染天数逐年减少。煤改气有利于减少酸雨的形成,造成酸雨的有害气体主要是 (写一种即可)。
(2)在净土保卫战中,实行重金属污染物排放限值标准。重金属污染物“铅、镉、汞”等指的是 (填“分子”“原子”或“元素”)。
18、(1)在稀释浓硫酸时,一定要把___________________________ ,并不断 ___________ 。
(2)下图是课本上的一个重要探究性实验,
请说出由该实验得出的两个重要结论是:
① _______________________________________________________ ;
② _______________________________________________________ 。
19、向盐酸中滴加氢氧化钠溶液时,当溶液的pH=5时,溶液显____性,溶液中的溶质是__________,(填化学式)当溶液的pH=7时,溶液显____性,溶液中的溶质是__________(填化学式),当溶液的pH=13时,溶液显____性,溶液中的溶质是_________(填化学式)。
20、回答下列与含碳物质有关的问题。
(1)普通干电池采用石墨作为电极材料,是利用其优良的__________性;
(2)高炉炼铁的主要反应为3CO+ Fe2O32Fe + 3CO2 ,该反应利用CO化学性质中的____性;
(3)碳酸钠、碳酸钙都含有CO32-,都能与盐酸反应生成盐、水和__________。
21、写出相应物质的化学式
〔1)某淡黄色粉末在氧气中燃烧产生一种刺激性气味的气体A,该气体能使稀高锰酸钾溶液褪色,A为_________。
(2)银白色固体B,能与酸反应,在空气中燃烧产生耀眼强光,B是_______。
(3)白色固体C,加热完全反应后无固体残留,并生成水同时产生一种刺激性气味的气体,C可能是__________。
22、近年科学家提出绿色自由”构想:把含有大量CO2的空气吹入盛有饱和碳酸钾( K2CO3)溶液的反应池中,反应生成碳酸氢钾(KHCO3),然后再把 CO2从分解池溶液中提取出来,在合成塔中经化学反应后使之变为可再生燃料甲醇(CH3OH)。“绿色自由”构想工艺流程如图所示:
已知:(1) 吸收池中的反应为
(2)分解池中的反应为
回答下列问题:
(1)进入分解池中的主要物质是 。
(2)该工艺在哪些方面体现了“绿色自由”构想中的“绿色”:
。(答一条即可)
(3)该流程中可以循环利用的物质是 。
(4)写出合成塔中生成甲醇的化学方程式: 。
三、实验题。
23、实验室常用下列装置来制取、收集气体。请回答以下问题。
(1)装置A中仪器①的名称 _______________ ;
(2)实验室用AE装置组合制取氧气,反应的化学方程式是 ________________________ ,检验氧气已经收集满的操作和现象是 _______________________________ 。
(3)实验室制取氢气的化学方程式是___________________________,若要收集较纯净的氢气,应选择的装置是____________ (填序号)。
(4)实验室用装置B制取二氧化碳时,若要停止反应,采取的操作是:
___________________。
(5)除去粗盐中难溶性杂质的实验步骤是溶解、过滤、蒸发,需用到上述装置中的______ ,还需要用到下列玻璃仪器组合中的________ 才能完成实验。
A 漏斗、烧杯、玻璃棒 B 滴管、量筒、试管 C 集气瓶、表面皿、广口瓶
(6)亚硝酸钠是实验室常用的试剂,实验室一般用亚硝酸钠溶液与氯化铵溶液反应来制取N2。N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3。下图为制取少量NH3的装置(制取H2的装置已略去)。
①C装置的硬质试管中发生反应的化学方程式为 ________________________ 。
②反应时N2和H2的最佳质量比是 _________ 。如果按此比例进行反应,反应时,若D中导管口有气泡逸出,(已知NH3极易溶于水),说明逸出气泡的原因:
_____________ 。
③用实验方法证明确实有NH3生成:________________________________ 。
四、科普阅读题。
24、化学用语是化学学科的专用语言,也是学习化学的重要工具。
(1)请从氧气、二氧化碳、氯化钠、盐酸、硫酸、氢氧化钙中选择合适的物质,将其化学式填写在下列横线上。
①可供给呼吸的气体单质_____ ②参与光合作用的氧化物_____
③一种不易挥发的无机酸 _____ ④常用于食品调味的盐 _____
(2)铁缺乏被认为是全球三大“隐性饥饿”之首(微量营养元素缺乏),全球约有1/5的人患缺铁性贫血。食物铁强化是目前国际公认的最经济、有效和可持续的给人群补铁的方法。中国疾控中心研制的新型铁强化剂(EDTA钠铁)在人体内的铁吸收、利用率高于其他铁剂,是传统补铁剂硫酸亚铁的2倍至3倍。它在酱油中的溶解性较好,不影响食品口感,不改变酱油的原有口味。此外,EDTA钠铁在食品加工和储存过程中性质稳定,它在酱油中可稳定保持两年以上。研究表明,应用铁强化酱油补铁效果显著。EDTA钠铁的化学式为C10H12FeN2NaO8,它是一种淡土黄色结晶性粉末,易溶于水,性质稳定,不易被氧化,其水溶液pH在3.5~5.5之间。
根据上述信息,请回答下列问题:
①EDTA钠铁属于_____ 。(选填“混合物”、“有机物”、“无机物”或“氧化物”之一)
②EDTA钠铁中,碳、氧原子个数比为_____ (填最简整数比)。
③EDTA钠铁中,元素质量分数最小的是_____ 元素。
④EDTA钠铁的化学性质_____ (至少答一条)。
⑤若经常使用铁锅炒菜做饭,也能有效预防缺铁性贫血,其反应原理的化学方程式为:(已知胃液中含有盐酸)_____ 。
五、计算题。
25、某课外兴趣小组对实验室中的一瓶稀硫酸样品进行分析。他们分别用100 g稀硫酸与不同质量的锌粒(含杂质,杂质不与稀硫酸反应)反应,三次实验的数据如下表。
实验次数 1 2 3
加入锌粒的质量(g) 4 8 12
充分反应后剩余物质的总质量(g) 103.9 107.8 111.8
请回答下列问题:
(1)第 次实验,锌粒与稀硫酸恰好完全反应。
(2)计算稀硫酸的溶质质量分数为 。【写出计算过程】
第八章 常见的酸、碱、盐 课后训练题(含答案)2023—2024学年科粤版(2012)化学九年级下册
一、选择题。
1、下列溶液能使紫色石蕊溶液变成蓝色的是( )
A.澄清石灰水 B.NaCl溶液 C.稀硫酸 D.KNO3溶液
【答案】A
2、关于酸和碱的描述正确的是( )
A.紫色石蕊溶液遇碱溶液变蓝色 B.生石灰和熟石灰都属于碱
C.酸就是有酸味的物质 D.碱就是有腐蚀性的物质
【答案】A
3、将下列不同pH的各组溶液混合,得到溶液的pH可能为7的是( )
A.pH=3 pH=4 B.pH=11 pH=7
C.pH=6 pH=8 D.pH=0 pH=5
【答案】C
4、下列变化中不能一步实现的是( )
A.Ba(OH)2→BaCl2 B.Fe2O3→Fe
C.BaCl2→BaSO4 D.CuO→Cu(OH)2
【答案】D
5、下列说法中,正确的是( )
A.若某雨水的pH 7,则该雨水一定呈酸性
B.某物质与酸反应放出气体,则该物质一定是碳酸盐
C.草木灰的主要成分碳酸钾属于盐类,所以能与铵盐混合使用
D.一种无色气体能使燃着的木条熄灭,那么该气体一定是二氧化碳
【答案】A
6、以下物质名称、俗名及分类对应正确的是( )
A.C60一金刚石一单质 B.氢氧化钠一纯碱一碱
C.氧化钙一熟石灰一氧化物 D.碳酸钠一苏打一盐
【答案】D
7、头发油腻是因为油脂的分泌,清洗时碱性溶液效果更好。从pH角度考虑效果最好的洗发水的pH为( )
A.8 B.7 C.6 D.4
【答案】A
8、小李在学习酸碱指示剂与常见酸、碱溶液作用时,归纳成如右图所示的关系。图中A、B、C、D是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示出的颜色,则其中表示不正确的是( )
A.紫色 B.蓝色 C.红色 D.无色
【答案】A
9、我们知道物质的性质决定其用途。下列对应关系不成立的( )
A.稀有气体化学性质稳定——作保护气
B.熟石灰显碱性—一用来改良酸性土壤
C.二氧化碳能与水反应—一可作制冷剂用于人工降雨
D.小苏打能与盐酸反应——可用于治疗胃酸过多
【答案】C
10、下列物质中,属于氧化物的是( )
A.水 B.高锰酸钾 C.氧气 D.氯酸钾
【答案】A
11、下列实验方案设计合理的是( )
选项 实验目的 实验方案
A 除去氢氧化钠溶液中少量碳酸钠 加过量的氢氧化钙溶液后过滤
B 除去氧化钙中少量碳酸钙 加适量的稀盐酸
C 鉴别硝酸钾和氯化铵固体 取样,分别与熟石灰混合研磨
D 鉴别硬水和软水 取样,加热
A.A B.B C.C D.D
【答案】C
12、下列含氮的化肥中,含氮量最高的是( )
A.硫铵 B.尿素 C.碳铵 D.硝铵
【答案】B
13、下列溶液显碱性的是( )
A.酸雨 B.食醋 C.NaOH溶液 D.盐酸
【答案】C
14、在托盘天平两边各放一只烧杯,调节至平衡.在两只烧杯里注入相同质量、相同质量分数的足量稀盐酸,然后分别向左右两端烧杯中加入质量相等的和金属.有气体产生时,托盘天平指针慢慢向左偏转(如图所示);指针偏转到一定角度后,又慢慢向右偏转;反应结束,托盘天平指针指向右端.则托盘天平右端加入的金属可能是( )
A. B. C. D.
【答案】A
15、性质决定用途,性质和用途均正确的是( )
A.氢氧化钠能与酸反应,可治疗胃酸过多
B.活性炭具有吸附性,作自来水消毒剂
C.一氧化碳有还原性,冶炼金属
D.稀有气体化学性质稳定,制霓虹灯
【答案】C
16、中盐河南盐业配送中心设置盐文化展区。盐汽水是一种能补充人体盐分的饮品,你认为盐汽水的成分和普通汽水最大的不同是增加了( )
A.水 B.氯化钠 C.二氧化碳 D.碳酸钙
【答案】B
二、填空题。
17、“十三五”以来,我省污染防治攻坚战取得阶段性成果,生态环境质量明显好转。
(1)在蓝天保卫战中,全省城市空气质量持续改善,重污染天数逐年减少。煤改气有利于减少酸雨的形成,造成酸雨的有害气体主要是 (写一种即可)。
(2)在净土保卫战中,实行重金属污染物排放限值标准。重金属污染物“铅、镉、汞”等指的是 (填“分子”“原子”或“元素”)。
【答案】(1)SO2(或NO2); (2)元素。
18、(1)在稀释浓硫酸时,一定要把___________________________ ,并不断 ___________ 。
(2)下图是课本上的一个重要探究性实验,
请说出由该实验得出的两个重要结论是:
① _______________________________________________________ ;
② _______________________________________________________ 。
【答案】(1)浓硫酸沿器壁慢慢注入水里 用玻璃棒搅拌
(2)可燃物的燃烧需要氧气 可燃物的燃烧需要温度达到着火点
19、向盐酸中滴加氢氧化钠溶液时,当溶液的pH=5时,溶液显____性,溶液中的溶质是__________,(填化学式)当溶液的pH=7时,溶液显____性,溶液中的溶质是__________(填化学式),当溶液的pH=13时,溶液显____性,溶液中的溶质是_________(填化学式)。
【答案】酸 HCl和NaCl 中 NaCl 碱 NaCl和NaOH
20、回答下列与含碳物质有关的问题。
(1)普通干电池采用石墨作为电极材料,是利用其优良的__________性;
(2)高炉炼铁的主要反应为3CO+ Fe2O32Fe + 3CO2 ,该反应利用CO化学性质中的____性;
(3)碳酸钠、碳酸钙都含有CO32-,都能与盐酸反应生成盐、水和__________。
【答案】导电性 还原性 二氧化碳
21、写出相应物质的化学式
〔1)某淡黄色粉末在氧气中燃烧产生一种刺激性气味的气体A,该气体能使稀高锰酸钾溶液褪色,A为_________。
(2)银白色固体B,能与酸反应,在空气中燃烧产生耀眼强光,B是_______。
(3)白色固体C,加热完全反应后无固体残留,并生成水同时产生一种刺激性气味的气体,C可能是__________。
【答案】
22、近年科学家提出绿色自由”构想:把含有大量CO2的空气吹入盛有饱和碳酸钾( K2CO3)溶液的反应池中,反应生成碳酸氢钾(KHCO3),然后再把 CO2从分解池溶液中提取出来,在合成塔中经化学反应后使之变为可再生燃料甲醇(CH3OH)。“绿色自由”构想工艺流程如图所示:
已知:(1) 吸收池中的反应为
(2)分解池中的反应为
回答下列问题:
(1)进入分解池中的主要物质是 。
(2)该工艺在哪些方面体现了“绿色自由”构想中的“绿色”:
。(答一条即可)
(3)该流程中可以循环利用的物质是 。
(4)写出合成塔中生成甲醇的化学方程式: 。
【答案】(1)KHCO3
减少大气中的CO2,产生清洁能源,实现低碳经济(合理即可)
(3)K2CO3 (4)
三、实验题。
23、实验室常用下列装置来制取、收集气体。请回答以下问题。
(1)装置A中仪器①的名称 _______________ ;
(2)实验室用AE装置组合制取氧气,反应的化学方程式是 ________________________ ,检验氧气已经收集满的操作和现象是 _______________________________ 。
(3)实验室制取氢气的化学方程式是___________________________,若要收集较纯净的氢气,应选择的装置是____________ (填序号)。
(4)实验室用装置B制取二氧化碳时,若要停止反应,采取的操作是:
___________________。
(5)除去粗盐中难溶性杂质的实验步骤是溶解、过滤、蒸发,需用到上述装置中的______ ,还需要用到下列玻璃仪器组合中的________ 才能完成实验。
A 漏斗、烧杯、玻璃棒 B 滴管、量筒、试管 C 集气瓶、表面皿、广口瓶
(6)亚硝酸钠是实验室常用的试剂,实验室一般用亚硝酸钠溶液与氯化铵溶液反应来制取N2。N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3。下图为制取少量NH3的装置(制取H2的装置已略去)。
①C装置的硬质试管中发生反应的化学方程式为 ________________________ 。
②反应时N2和H2的最佳质量比是 _________ 。如果按此比例进行反应,反应时,若D中导管口有气泡逸出,(已知NH3极易溶于水),说明逸出气泡的原因:
_____________ 。
③用实验方法证明确实有NH3生成:________________________________ 。
【答案】(1)试管
(2)把带火星的木条放到集气瓶口,如果木条复燃,说明氧气已收集满
(3)Zn+H2SO4(稀)=ZnSO4+H2↑ G
(4)关闭导气管上的开关 (5)D A
(6)N2+3H22NH3 28∶6
氮气和氢气是部分化合,还有未反应的氮气和氢气逸出
向D中滴入无色酚酞试液,酚酞变红,说明有氨气生成
四、科普阅读题。
24、化学用语是化学学科的专用语言,也是学习化学的重要工具。
(1)请从氧气、二氧化碳、氯化钠、盐酸、硫酸、氢氧化钙中选择合适的物质,将其化学式填写在下列横线上。
①可供给呼吸的气体单质_____ ②参与光合作用的氧化物_____
③一种不易挥发的无机酸 _____ ④常用于食品调味的盐 _____
(2)铁缺乏被认为是全球三大“隐性饥饿”之首(微量营养元素缺乏),全球约有1/5的人患缺铁性贫血。食物铁强化是目前国际公认的最经济、有效和可持续的给人群补铁的方法。中国疾控中心研制的新型铁强化剂(EDTA钠铁)在人体内的铁吸收、利用率高于其他铁剂,是传统补铁剂硫酸亚铁的2倍至3倍。它在酱油中的溶解性较好,不影响食品口感,不改变酱油的原有口味。此外,EDTA钠铁在食品加工和储存过程中性质稳定,它在酱油中可稳定保持两年以上。研究表明,应用铁强化酱油补铁效果显著。EDTA钠铁的化学式为C10H12FeN2NaO8,它是一种淡土黄色结晶性粉末,易溶于水,性质稳定,不易被氧化,其水溶液pH在3.5~5.5之间。
根据上述信息,请回答下列问题:
①EDTA钠铁属于_____ 。(选填“混合物”、“有机物”、“无机物”或“氧化物”之一)
②EDTA钠铁中,碳、氧原子个数比为_____ (填最简整数比)。
③EDTA钠铁中,元素质量分数最小的是_____ 元素。
④EDTA钠铁的化学性质_____ (至少答一条)。
⑤若经常使用铁锅炒菜做饭,也能有效预防缺铁性贫血,其反应原理的化学方程式为:(已知胃液中含有盐酸)_____ 。
【答案】(1)O2 CO2 H2SO4 NaCl
(2)有机物 5∶4 H 不易被氧化,其水溶液显酸性
五、计算题。
25、某课外兴趣小组对实验室中的一瓶稀硫酸样品进行分析。他们分别用100 g稀硫酸与不同质量的锌粒(含杂质,杂质不与稀硫酸反应)反应,三次实验的数据如下表。
实验次数 1 2 3
加入锌粒的质量(g) 4 8 12
充分反应后剩余物质的总质量(g) 103.9 107.8 111.8
请回答下列问题:
(1)第 次实验,锌粒与稀硫酸恰好完全反应。
(2)计算稀硫酸的溶质质量分数为 。【写出计算过程】
【答案】2 9.8%
【详解】(1)由三次实验数据可知,可发现每加入4g锌粒样品就可放出氢气的质量;而第2次加入8g和第3次加入12g同样的锌粒后放出氢气的质量均为0.2g,第2次所加的8g锌恰好与100g稀硫酸完全反应,故第2次实验,锌粒与稀硫酸恰好完全反应。
(2)8克锌粒完全反应生成氢气的质量是
设生成0.2g氢气需H2SO4的质量为x
该稀硫酸的质量分数为
