广东省肇庆市地质中学2023-2024学年九年级下学期摸底考试化学试题(含答案)
文档属性
| 名称 | 广东省肇庆市地质中学2023-2024学年九年级下学期摸底考试化学试题(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 571.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-19 00:00:00 | ||
图片预览



文档简介
广东省肇庆市地质中学2023-2024学年九年级下学期摸底考试化学试题
可能用到的相对原子质量:H-1;C-12;N-14;S-32;
一、选择题(本大题共10小题,每小题3分,满分30分)。
1.英德红茶的制作工艺中,一定没有发生化学变化的工序是( )
A.采摘:将茶叶从茶树枝上摘下 B.揉捻:轻轻揉搓使茶叶发生酶促氧化
c.发酵:使茶叶由绿色变为红色 D.烘干:高温烘焙,终止酶活性,防止发酵过度
2.下列实验操作错误的是( )
A.氢气验纯 B.移走蒸发皿 C.二氧化碳验满 D.称量
3.2023 年“世界环境日”中国的主题为“建设人与自然和谐共生的现代化”。下列做法与该主题相符的是( )
A.使用一次性塑料袋 B.节约用水用电 C.直接排放工厂废气 D.填埋废旧电池
4.化学促进了人类的进步,推动了社会的发展,科学家为此作出了巨大的贡献。下列科学家与其贡献对应的是( )
A.门捷列夫——创立分子学说 B.拉瓦锡——发现元素周期表
C.道尔顿——提出近代原子学说 D.张青莲——提取青蒿素
5.下列有关微观粒子的说法正确的是( )
A.氯化钠是由氯化钠分子构成的 B.分子可以分成原子而原子不能再分
C.分子是保持物质性质的最小粒子 D.原子是由原子核和核外电子构成的
6.机制炭(如右图)常用作烧烤燃料,引燃它可以使用固体酒精,盖灭炭火可以使用燃烧后产生的炭灰。下列说法错误的是( )
A.机制炭做成空心增大了与空气的接触面积
B.炭灰可以盖灭炭火是因为隔绝了空气
C.烧烤应该在空气流通的地方进行
D.酒精的燃烧是为了升高机制炭的着火点
7.下列说法的不正确的是( )
A.干冰升华一一分子间隔变大
B.红磷在空气中燃烧的现象一一黄白色火燃,放热,有大量白烟
C.水在通电的条件下发生分解反应一一2H2OO2+2H2
D 金刚石和石墨物理性质不同一一碳原子排列方式不同
8.下列跨学科实践活动涉及的化学知识错误的是( )
选项 实践活动 化学知识
A 用自制简易净水器净化雨水 净化后得到纯水
B 给大棚蔬菜施加气体肥料CO2 CO2是光合作用的原料
C 用微型空气质量检测仪测SO2含量 O2 属于空气污染物
D 用橡皮泥制作氨分子的结构模型 氨分子由氮原子和氢原子构成
9.2023年6月7日,力箭一号遥二运载火箭成功发射升空。发射火箭所用的燃料液态偏二肼(C2H8N2)与N2O4发射的反应为:C2H8N2+2N2O43N2↑+2X↑+4H2O,则X为( )
A.C B.CO C.CO2 D.H2CO3
10.学好化学,就要学会归纳和总结。下列总结的化学知识有错误的一组是( )A 安全常识 C 生活知识
电器着火——切断电源煤气中毒——先开窗通风 洗洁精去除油污——乳化作用活性炭净水——吸附作用
B 物质的性质与用途 D 物质分类
用墨书写字画——稳定性氢气作高能燃料—可燃性 生铁、糖水——混合物水、高锰酸钾——氧化物
11.2022年1月26日,我国采用长征四号丙运载火箭成功发射陆地探测一号01组A星,该火箭采用C2H8N2(偏二甲)推荐剂,如图为N2O4和C2H8N2反应微观示意图人列有关该反应的说法错误的是( )
A.生成3种分子 B.戊的化学式为CO2
C.反应前后原子种类不变 D.反应前后分子数目不变
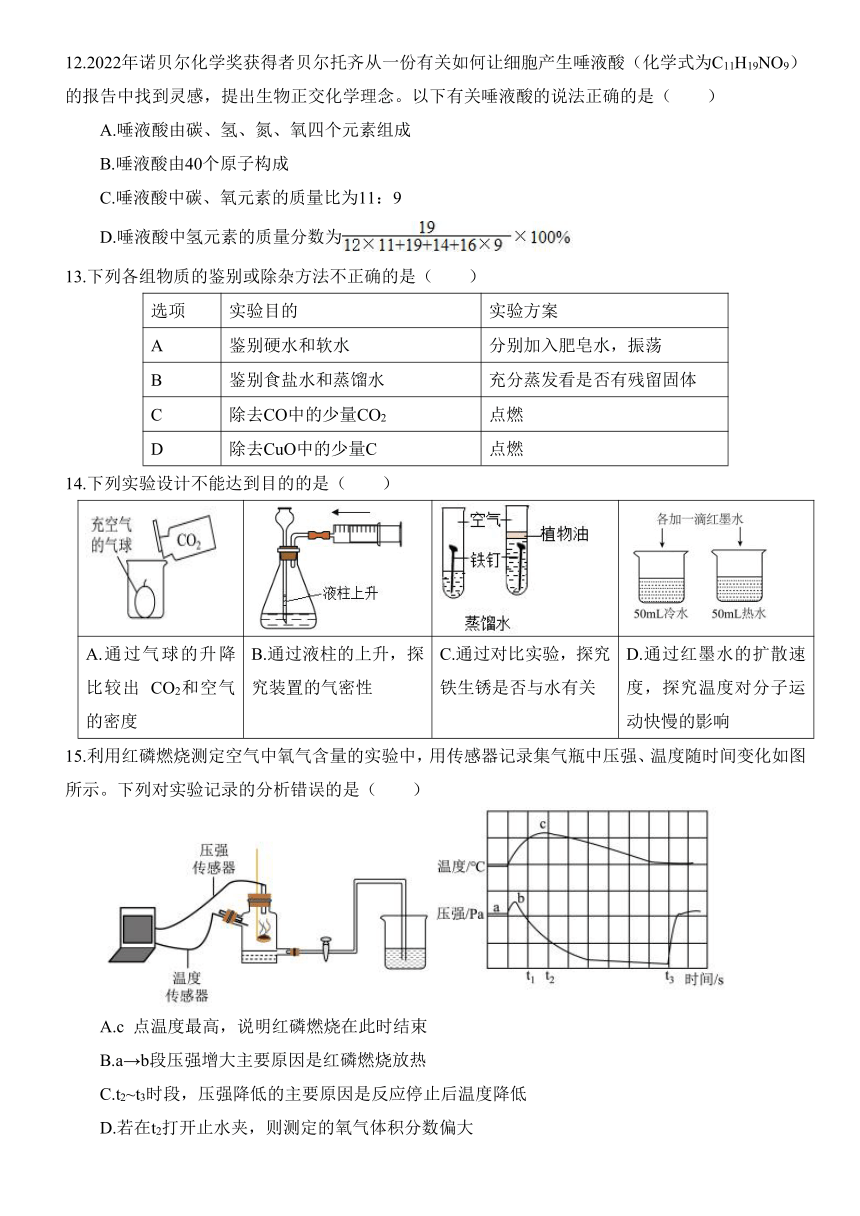
12.2022年诺贝尔化学奖获得者贝尔托齐从一份有关如何让细胞产生唾液酸(化学式为C11H19NO9)的报告中找到灵感,提出生物正交化学理念。以下有关唾液酸的说法正确的是( )
A.唾液酸由碳、氢、氮、氧四个元素组成
B.唾液酸由40个原子构成
C.唾液酸中碳、氧元素的质量比为11:9
D.唾液酸中氢元素的质量分数为
13.下列各组物质的鉴别或除杂方法不正确的是( )
选项 实验目的 实验方案
A 鉴别硬水和软水 分别加入肥皂水,振荡
B 鉴别食盐水和蒸馏水 充分蒸发看是否有残留固体
C 除去CO中的少量CO2 点燃
D 除去CuO中的少量C 点燃
14.下列实验设计不能达到目的的是( )
A.通过气球的升降比较出 CO2和空气的密度 B.通过液柱的上升,探究装置的气密性 C.通过对比实验,探究铁生锈是否与水有关 D.通过红墨水的扩散速度,探究温度对分子运动快慢的影响
15.利用红磷燃烧测定空气中氧气含量的实验中,用传感器记录集气瓶中压强、温度随时间变化如图所示。下列对实验记录的分析错误的是( )
A.c 点温度最高,说明红磷燃烧在此时结束
B.a→b段压强增大主要原因是红磷燃烧放热
C.t2~t3时段,压强降低的主要原因是反应停止后温度降低
D.若在t2打开止水夹,则测定的氧气体积分数偏大
二、填空题(本大题共2小题,共15分)。
16.(7分)“宏观-微观-符号”三重表征是体现化学学科特征的思维方法。如图是几种元素的粒子结构示意图或元素的信息,请回答:
(1)图E为硫原子结构示意图,X=_____,硫的相对原子质量为_____.
(2)氢-1、氢-2、氢-3它们都是同一种元素的原因是_______________.我国“嫦娥五号”探测器取回土壤含有丰富的氦-3,它是由一个中子和两个质子构成的,其原子结构示意图为图中_____.(选 A、B、C、D 中一项)
(3)根据表中信息,填写与化学符号或符号意义相对应的①-③空格:
化学符号 ①__________ 3O2 ③_______________
符号的意义 2个硫酸根离子 ②_______________ 氧化铝中铝元素为+3 价
17,(8分)溶液与人类生产、生活密切相关。
(1)把少量下列物质分别放入水中,充分搅拌,能得到溶液的是________(填序号)
A.硝酸钾 B.植物油 C.面粉
(2)衣服上沾有的油污,可用汽油洗去,是因为汽油能________(填“溶解”或“乳化”)油污。
(3)生理盐水是医疗上常用的一种溶液,其溶质是________,溶液里存在的微粒是________(用符号表示)。
(4)在盛有水的烧杯中加入以下某种物质,形成溶液过程中,温度升高,这种物质是________(填字母)。
A.氯化钠 B.硝酸铵 C.氢氧化钠
(5)如图为甲、乙、丙三种固体物质的溶解度曲线。
①t1℃时,甲、乙两种物质的溶解度______(填“相等”或“不相等”)。
②t1℃时,将 100g水加入盛有50g甲物质的烧杯中,充分溶解后,得到甲的______(填“饱和”或“不饱和”)溶液。保持温度不变,该烧杯中再加入10g水,充分搅拌后,甲溶液的溶质为______g.
三、(本大题包括2小题,满分20分)。
18.(10分)请根据下列装置图,回答有关问题:
(1)仪器 a 的名称是_____
(2)实验室用可以用A和_____(填字母序号,下同)来制取并收集氧气,组装好仪器后,应先_______________,该装置发生的反应化学方程式是_________________________。按下列顺序①→⑤→④→_______(填数字序号)连接,可测收集氧气的体积。
(3)实验室制取二氧化碳的发生装置是_________,该反应的化学方程式是______________
若小明同学以“棒棒冰”塑料管为材料,制成气体发生装置(图2),若想让反应发生,操作是
____________________________
19.(10分)某化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,设计实验探究:
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】①含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;
②白色无水 CuSO4粉末遇水变蓝色;
③CO 与人体内的血红蛋白结合,会造成人中毒缺氧。
【猜想与假设】猜想一:CO2、H2O;
猜想二:CO、H2O;
猜想三:___________.
【实验探究】将甲烷在一定量的纯净氧气中燃烧的产物依次通过 C-G装置(部分夹持、固定装置省略)进行验证:
(1)若实验过程中观察到A中白色粉末变为蓝色,则证明甲烷燃烧后生成了H2O;若B、E中澄清石灰水变浑浊,D中红棕色粉末变成黑色,由此推断猜想_______成立。
(2)实验过程中B装置的作用是_____________________.
(3)D装置中发生反应的化学方程式是___________________________________.
(4)实验过程中用纯净O2而不用空气的原因是____________________________.
【反思与交流】气球的作用是__________________________________.实验结束,对相关装置进行称量(忽略空气成分对实验的干扰):A装置增重3.6g,BC装置增重2.2g。那么燃烧甲烷的质量为____________g,并写出甲烷完全燃烧的化学方程式__________________________________.
四、(本大题包括1小题,共10分)
20.(10分)实验室有100g废液,其中含有硫酸铜、硫酸亚铁、硫酸锌。现对废液进行处理得到铜和硫酸锌溶液,实验流程如图所示.
(1)步骤I、II、III中均包含的操作名称是__________
(2)步骤Ⅰ反应的化学方程式______________________________。其基本反应类型是______.
滤液B的主要成分是____________。(填其中一个)。
(3)步骤II当观察到___________________________时,说明滤渣A中铁已经完全反应,该反应的化学方程式___________________________
(4)步骤Ⅲ中加入的X是_________(填化学式),理论上所得硫酸锌溶液的质量________(填“<”“>”或“=”)原废液中硫酸锌溶液的质量。
五、(本大题包括1小题,共10分)
21.(10分)为了测定某黄铜(铜锌合金)样品的组成,某化学兴趣小组的同学进行了以下实验:取四份相同质量的样品分别放入等质量的烧杯中,然后分别加入硫酸,充分反应后用天平称量,记录实验数据如下:
试验次序 第1次 第2次 第3次 第4次
所取样品的质量/g 50.0 50.0 50.0 50.0
加入稀硫酸的质量/g 20.0 40.0 60.0 80.0
生成气体的质量/g 0.2 0.4 0.6 0.6
请回答下列问题并计算:
(1)50.0g 样品与足量稀硫酸反应最多能生成气体_____g .
(2)计算稀硫酸中溶质的质量分数(写出具体计算过程)。
(3)请在图中画出加入稀硫酸的质量与生成气体的质量的变化关系。
(4)第4次反应后生成物溶液的溶质是__________.
参考答案
一、选择题(本大题共10小题,每小题3分,满分30分)
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
A B B C D D C A C D D D D C D
二、填空题(本大题共2小题,共15分)。
16. (1)6;32.06
(2)质子数相同;A
(3)①2SO42- ;
②3个氧分子;
③
17 (1)A
(2)溶解
(3)NaCl; Na+、Cl-、H2O
(4)C
(5)①相等
②饱和;33
三、(本大题包括2小题,满分20分)。
18. (1)量筒
(2)D;检查装置的气密性;2KClO3 2KCl+3O2;⑦
(3)C;CaCO3+2HCl=CaCl2+H2O+CO2;捏住塑料管的下端
19. 【猜想与假设】:CO2、H2O、 CO
【实验探究】:(1)三
(2)除去混合气体中的CO2,消除对是否有CO的判断;
(3)3CO+Fe2O32Fe+3CO2
(4)空气中含有水蒸气和二氧化碳,影响实验结果
【反思与交流】:尾气处理装置,避免CO气体泄露到空气中; 1.6
CH4+ 2O2= 2H2O +CO2
四、(本大题包括1小题,共10分)
20.(1)过滤
(2)Fe+CuSO4=FeSO4+Cu;置换反应;硫酸亚铁(或硫酸锌)
(3)不再产生气泡;Fe+H2SO4= FeSO4+ H2
(4)Zn;>
五、(本大题包括1小题,共10分)
21. (1)0.6;
(2)稀硫酸中溶质的质量分数x
Zn+H2SO4= ZnSO4 + H2
98 2
20g×x 0.2g
=
x =49%
答:稀硫酸中溶质的质量分数为49%
(3)如下图
(4)ZnSO4和H2SO4
可能用到的相对原子质量:H-1;C-12;N-14;S-32;
一、选择题(本大题共10小题,每小题3分,满分30分)。
1.英德红茶的制作工艺中,一定没有发生化学变化的工序是( )
A.采摘:将茶叶从茶树枝上摘下 B.揉捻:轻轻揉搓使茶叶发生酶促氧化
c.发酵:使茶叶由绿色变为红色 D.烘干:高温烘焙,终止酶活性,防止发酵过度
2.下列实验操作错误的是( )
A.氢气验纯 B.移走蒸发皿 C.二氧化碳验满 D.称量
3.2023 年“世界环境日”中国的主题为“建设人与自然和谐共生的现代化”。下列做法与该主题相符的是( )
A.使用一次性塑料袋 B.节约用水用电 C.直接排放工厂废气 D.填埋废旧电池
4.化学促进了人类的进步,推动了社会的发展,科学家为此作出了巨大的贡献。下列科学家与其贡献对应的是( )
A.门捷列夫——创立分子学说 B.拉瓦锡——发现元素周期表
C.道尔顿——提出近代原子学说 D.张青莲——提取青蒿素
5.下列有关微观粒子的说法正确的是( )
A.氯化钠是由氯化钠分子构成的 B.分子可以分成原子而原子不能再分
C.分子是保持物质性质的最小粒子 D.原子是由原子核和核外电子构成的
6.机制炭(如右图)常用作烧烤燃料,引燃它可以使用固体酒精,盖灭炭火可以使用燃烧后产生的炭灰。下列说法错误的是( )
A.机制炭做成空心增大了与空气的接触面积
B.炭灰可以盖灭炭火是因为隔绝了空气
C.烧烤应该在空气流通的地方进行
D.酒精的燃烧是为了升高机制炭的着火点
7.下列说法的不正确的是( )
A.干冰升华一一分子间隔变大
B.红磷在空气中燃烧的现象一一黄白色火燃,放热,有大量白烟
C.水在通电的条件下发生分解反应一一2H2OO2+2H2
D 金刚石和石墨物理性质不同一一碳原子排列方式不同
8.下列跨学科实践活动涉及的化学知识错误的是( )
选项 实践活动 化学知识
A 用自制简易净水器净化雨水 净化后得到纯水
B 给大棚蔬菜施加气体肥料CO2 CO2是光合作用的原料
C 用微型空气质量检测仪测SO2含量 O2 属于空气污染物
D 用橡皮泥制作氨分子的结构模型 氨分子由氮原子和氢原子构成
9.2023年6月7日,力箭一号遥二运载火箭成功发射升空。发射火箭所用的燃料液态偏二肼(C2H8N2)与N2O4发射的反应为:C2H8N2+2N2O43N2↑+2X↑+4H2O,则X为( )
A.C B.CO C.CO2 D.H2CO3
10.学好化学,就要学会归纳和总结。下列总结的化学知识有错误的一组是( )A 安全常识 C 生活知识
电器着火——切断电源煤气中毒——先开窗通风 洗洁精去除油污——乳化作用活性炭净水——吸附作用
B 物质的性质与用途 D 物质分类
用墨书写字画——稳定性氢气作高能燃料—可燃性 生铁、糖水——混合物水、高锰酸钾——氧化物
11.2022年1月26日,我国采用长征四号丙运载火箭成功发射陆地探测一号01组A星,该火箭采用C2H8N2(偏二甲)推荐剂,如图为N2O4和C2H8N2反应微观示意图人列有关该反应的说法错误的是( )
A.生成3种分子 B.戊的化学式为CO2
C.反应前后原子种类不变 D.反应前后分子数目不变
12.2022年诺贝尔化学奖获得者贝尔托齐从一份有关如何让细胞产生唾液酸(化学式为C11H19NO9)的报告中找到灵感,提出生物正交化学理念。以下有关唾液酸的说法正确的是( )
A.唾液酸由碳、氢、氮、氧四个元素组成
B.唾液酸由40个原子构成
C.唾液酸中碳、氧元素的质量比为11:9
D.唾液酸中氢元素的质量分数为
13.下列各组物质的鉴别或除杂方法不正确的是( )
选项 实验目的 实验方案
A 鉴别硬水和软水 分别加入肥皂水,振荡
B 鉴别食盐水和蒸馏水 充分蒸发看是否有残留固体
C 除去CO中的少量CO2 点燃
D 除去CuO中的少量C 点燃
14.下列实验设计不能达到目的的是( )
A.通过气球的升降比较出 CO2和空气的密度 B.通过液柱的上升,探究装置的气密性 C.通过对比实验,探究铁生锈是否与水有关 D.通过红墨水的扩散速度,探究温度对分子运动快慢的影响
15.利用红磷燃烧测定空气中氧气含量的实验中,用传感器记录集气瓶中压强、温度随时间变化如图所示。下列对实验记录的分析错误的是( )
A.c 点温度最高,说明红磷燃烧在此时结束
B.a→b段压强增大主要原因是红磷燃烧放热
C.t2~t3时段,压强降低的主要原因是反应停止后温度降低
D.若在t2打开止水夹,则测定的氧气体积分数偏大
二、填空题(本大题共2小题,共15分)。
16.(7分)“宏观-微观-符号”三重表征是体现化学学科特征的思维方法。如图是几种元素的粒子结构示意图或元素的信息,请回答:
(1)图E为硫原子结构示意图,X=_____,硫的相对原子质量为_____.
(2)氢-1、氢-2、氢-3它们都是同一种元素的原因是_______________.我国“嫦娥五号”探测器取回土壤含有丰富的氦-3,它是由一个中子和两个质子构成的,其原子结构示意图为图中_____.(选 A、B、C、D 中一项)
(3)根据表中信息,填写与化学符号或符号意义相对应的①-③空格:
化学符号 ①__________ 3O2 ③_______________
符号的意义 2个硫酸根离子 ②_______________ 氧化铝中铝元素为+3 价
17,(8分)溶液与人类生产、生活密切相关。
(1)把少量下列物质分别放入水中,充分搅拌,能得到溶液的是________(填序号)
A.硝酸钾 B.植物油 C.面粉
(2)衣服上沾有的油污,可用汽油洗去,是因为汽油能________(填“溶解”或“乳化”)油污。
(3)生理盐水是医疗上常用的一种溶液,其溶质是________,溶液里存在的微粒是________(用符号表示)。
(4)在盛有水的烧杯中加入以下某种物质,形成溶液过程中,温度升高,这种物质是________(填字母)。
A.氯化钠 B.硝酸铵 C.氢氧化钠
(5)如图为甲、乙、丙三种固体物质的溶解度曲线。
①t1℃时,甲、乙两种物质的溶解度______(填“相等”或“不相等”)。
②t1℃时,将 100g水加入盛有50g甲物质的烧杯中,充分溶解后,得到甲的______(填“饱和”或“不饱和”)溶液。保持温度不变,该烧杯中再加入10g水,充分搅拌后,甲溶液的溶质为______g.
三、(本大题包括2小题,满分20分)。
18.(10分)请根据下列装置图,回答有关问题:
(1)仪器 a 的名称是_____
(2)实验室用可以用A和_____(填字母序号,下同)来制取并收集氧气,组装好仪器后,应先_______________,该装置发生的反应化学方程式是_________________________。按下列顺序①→⑤→④→_______(填数字序号)连接,可测收集氧气的体积。
(3)实验室制取二氧化碳的发生装置是_________,该反应的化学方程式是______________
若小明同学以“棒棒冰”塑料管为材料,制成气体发生装置(图2),若想让反应发生,操作是
____________________________
19.(10分)某化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,设计实验探究:
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】①含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;
②白色无水 CuSO4粉末遇水变蓝色;
③CO 与人体内的血红蛋白结合,会造成人中毒缺氧。
【猜想与假设】猜想一:CO2、H2O;
猜想二:CO、H2O;
猜想三:___________.
【实验探究】将甲烷在一定量的纯净氧气中燃烧的产物依次通过 C-G装置(部分夹持、固定装置省略)进行验证:
(1)若实验过程中观察到A中白色粉末变为蓝色,则证明甲烷燃烧后生成了H2O;若B、E中澄清石灰水变浑浊,D中红棕色粉末变成黑色,由此推断猜想_______成立。
(2)实验过程中B装置的作用是_____________________.
(3)D装置中发生反应的化学方程式是___________________________________.
(4)实验过程中用纯净O2而不用空气的原因是____________________________.
【反思与交流】气球的作用是__________________________________.实验结束,对相关装置进行称量(忽略空气成分对实验的干扰):A装置增重3.6g,BC装置增重2.2g。那么燃烧甲烷的质量为____________g,并写出甲烷完全燃烧的化学方程式__________________________________.
四、(本大题包括1小题,共10分)
20.(10分)实验室有100g废液,其中含有硫酸铜、硫酸亚铁、硫酸锌。现对废液进行处理得到铜和硫酸锌溶液,实验流程如图所示.
(1)步骤I、II、III中均包含的操作名称是__________
(2)步骤Ⅰ反应的化学方程式______________________________。其基本反应类型是______.
滤液B的主要成分是____________。(填其中一个)。
(3)步骤II当观察到___________________________时,说明滤渣A中铁已经完全反应,该反应的化学方程式___________________________
(4)步骤Ⅲ中加入的X是_________(填化学式),理论上所得硫酸锌溶液的质量________(填“<”“>”或“=”)原废液中硫酸锌溶液的质量。
五、(本大题包括1小题,共10分)
21.(10分)为了测定某黄铜(铜锌合金)样品的组成,某化学兴趣小组的同学进行了以下实验:取四份相同质量的样品分别放入等质量的烧杯中,然后分别加入硫酸,充分反应后用天平称量,记录实验数据如下:
试验次序 第1次 第2次 第3次 第4次
所取样品的质量/g 50.0 50.0 50.0 50.0
加入稀硫酸的质量/g 20.0 40.0 60.0 80.0
生成气体的质量/g 0.2 0.4 0.6 0.6
请回答下列问题并计算:
(1)50.0g 样品与足量稀硫酸反应最多能生成气体_____g .
(2)计算稀硫酸中溶质的质量分数(写出具体计算过程)。
(3)请在图中画出加入稀硫酸的质量与生成气体的质量的变化关系。
(4)第4次反应后生成物溶液的溶质是__________.
参考答案
一、选择题(本大题共10小题,每小题3分,满分30分)
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
A B B C D D C A C D D D D C D
二、填空题(本大题共2小题,共15分)。
16. (1)6;32.06
(2)质子数相同;A
(3)①2SO42- ;
②3个氧分子;
③
17 (1)A
(2)溶解
(3)NaCl; Na+、Cl-、H2O
(4)C
(5)①相等
②饱和;33
三、(本大题包括2小题,满分20分)。
18. (1)量筒
(2)D;检查装置的气密性;2KClO3 2KCl+3O2;⑦
(3)C;CaCO3+2HCl=CaCl2+H2O+CO2;捏住塑料管的下端
19. 【猜想与假设】:CO2、H2O、 CO
【实验探究】:(1)三
(2)除去混合气体中的CO2,消除对是否有CO的判断;
(3)3CO+Fe2O32Fe+3CO2
(4)空气中含有水蒸气和二氧化碳,影响实验结果
【反思与交流】:尾气处理装置,避免CO气体泄露到空气中; 1.6
CH4+ 2O2= 2H2O +CO2
四、(本大题包括1小题,共10分)
20.(1)过滤
(2)Fe+CuSO4=FeSO4+Cu;置换反应;硫酸亚铁(或硫酸锌)
(3)不再产生气泡;Fe+H2SO4= FeSO4+ H2
(4)Zn;>
五、(本大题包括1小题,共10分)
21. (1)0.6;
(2)稀硫酸中溶质的质量分数x
Zn+H2SO4= ZnSO4 + H2
98 2
20g×x 0.2g
=
x =49%
答:稀硫酸中溶质的质量分数为49%
(3)如下图
(4)ZnSO4和H2SO4
同课章节目录
