利用化学方程式的简单计算第二课时
图片预览






文档简介
课件18张PPT。 你 清 楚 吗?1、表示什么物质参加反应,结果生成什么物质
及反应的条件。2、表示各反应物、生成物之间的粒子个数之比。3、表示反应物、生成物各物质之间的质量比。化学方程式的意义有哪些?(以电解水的反应为例)2H2O 2H2↑+O2↑1、表示水通电生成氢气和氧气。2、表示每36份质量的水完全反应,生成4份质
量的氢气和32份质量的氧气。3643218Kg?3、表示2个水分子通电生成2个氢分子和1个
氧分子 在生产、科研中,人们研究物质变化,常常涉及量的计算。 如:一定量的原料,最多可以生产多少产品; 如 : 每天生产50吨钢,最少需要多少吨炼铁的铁矿石。根据化学方程式计算的步骤设未知量
写出化学方程式并配平
写出有关物质的相对分子 质量和已知量、未知量
列出比例式、求解
简明地写出答案例1 加热分解6g高锰酸钾,可以得到多少克氧气?设:加热分解 6g高锰酸钾,可以得到氧气的质量为x2×158
6g32
x答:加热分解 6g高锰酸钾,可以得到0.6g氧气。 给你提个醒根据化学方程式计算的正确解题步骤[解](1)设未知数(未知数不带单位)(2)正确写出化学方程式(3)写出相关物质的相对分子质量
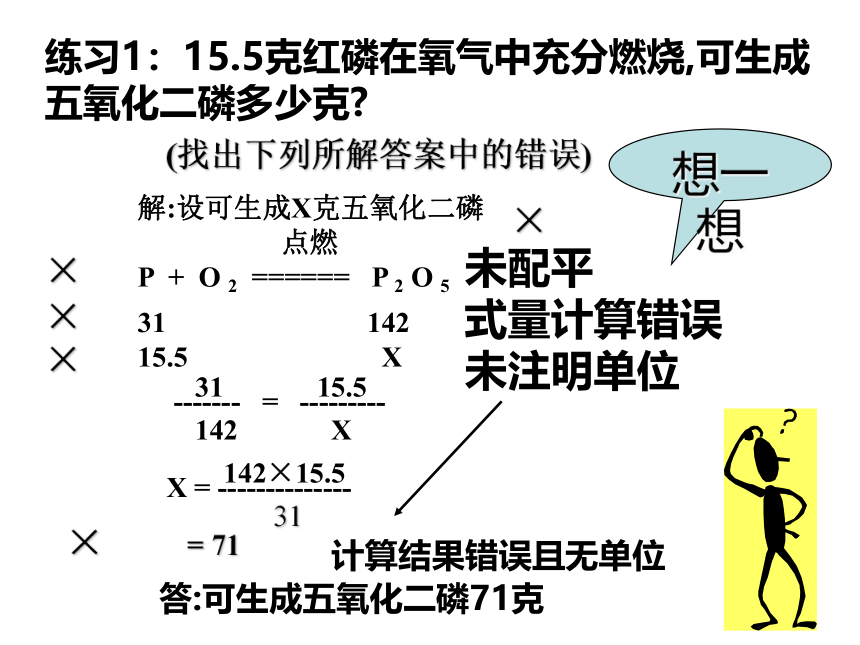
和已知量、未知量(4)列出比例,求解(5)简明地写出答案练习1:15.5克红磷在氧气中充分燃烧,可生成五氧化二磷多少克?(找出下列所解答案中的错误)解:设可生成X克五氧化二磷
点燃
P + O 2 ====== P 2 O 5
31 142
15.5 X 31 15.5------- = ---------142 XX = --------------142×15.531= 71答:可生成五氧化二磷71克××××未配平
式量计算错误
未注明单位计算结果错误且无单位×想一想 例2工业上,高温煅烧石灰石(CaCO3)可制得生石灰(CaO)和二氧化碳。如果要制取10t氧化钙,需要碳酸钙多少吨?
解:设制取10吨氧化钙需要碳酸钙的质量为X答:需要碳酸钙的质量为17.9t。例3.用含碳酸钙90%的石灰石100g,与足量稀盐酸充分反应(杂质不与盐酸反应),可制得二氧化碳多少克?标准状况下制得二氧化碳多少升?(标准状况下二氧化碳的密度约为2.0g/L.)
(CaCO3 + 2HCl = CaCl2 + H2O +CO2 )解:设可制得二氧化碳的质量为X100g×90% X
39.6g答:制得二氧化碳39.6g,标准状况下制得二氧化碳19.8L
例4. 实验室有5g锌粒跟10ml稀硫酸待反应完成后,剩余锌粒3.7克,问可生成H2多少克?体积是多少升?(密度是0.09g/L)
(Zn + H2SO4 == H2 + ZnSO4)
解:设可制得H2的质量为XZn + H2SO4 == H2 + ZnSO465 25g-3.7g X答:可生成H20.04g,体积是0.44L解题注意事项:1、在化学方程式中,反应物与生成物之间的质量比,是各化学式的相对分子质量与化学式前边的化学计量数(系数)的乘积之比,因此要准确计算。2、化学方程式中,各物质的质量比都是纯量间的比,因此代入的量必须是纯净的质量。如提供的量不是纯量,必须换算成纯量后才能代入。3、注意解题格式要规范化,注意单位和数据精确度。 1、4克氧气可跟( )克氢气完全反应.。 A 、 1 B、 0.5 C、 2 D 、 4
2、3克镁在足量的氧气中完全燃烧,可得到氧化镁( )克。 A、10 B、 6 C 、5 D、 12 B 、C练习 3.有氢气和氧气的混合气体10克,经点燃充分反应后,恢复到常温,还有1克气体剩余,则混合物可能的成分是( )。
A、H2 5克、O25克
B 、H2 1克、O29克 C 、H2 2克、O28克
D 、H2 4克、O26克 答案:B、C练习:1、3g的碳完全燃烧可以消耗氧气多少g?解:设3g的碳完全燃烧可以消耗氧气X12C + O2=== CO232点燃3gX答: 3g的碳完全燃烧可以消耗氧气8g。X = 8 g2、用氢气还原氧化铜得到金属铜,那么如果想得到32g的铜,应需要氧化铜多少g?H2 + CuO === Cu + H2O解:设如果想得到32g的铜,应需要氧化铜x答:设如果想得到32g的铜,应需要氧化铜40g。32gX = 40 g80?X643、某医院急需给病人输氧气,但是没有现成的氧气,需要用分解过氧化氢的方法制取氧气,那么如果需要氧气的体积是23L,则需要分解多少g的过氧化氢?(氧气的密度是1.4g/L)X2H2O2 ==== 2H2O + O2↑设制取氧气32.2g需要分解过氧化氢X68解:氧气的质量为:m=ρV=23×1.4=32.2g32.2g32MnO2X = 68.4 g答:制取23L氧气需要分解68.4g过氧化氢。分析:S + O2 === SO24、38g硫在32g氧气中燃烧生成二氧化硫的质量是多少?点燃3238g3238g解:设38g硫反应需要氧气XS + O2 === SO2点燃323238gXX = 38 g设38g硫在32g氧气中燃烧生成二氧化硫的质量是Y∴38g硫和38克氧气恰好完全反应,所以氧气完全反应点燃326432gYY = 64 g答:38g硫在32g氧气中燃烧生成二氧化硫的质量是64g。
解:氧气的质量是:m=20-15.2=4.8g 分析:找完全反应物质的质量,起始20g不是反应后的15.2g也不是。看反应找质量差。反应前是固体,反应后是固体和气体,气体益出剩下的是固体所以质量要减小,减小的质量就是气体的质量。即O2的质量是4.8g。5、氯酸钾和二氧化锰的混合固体20g,加热完全反应后剩余固体的质量是15.2g,求原混合物种氯酸钾的质量。设混合物中的氯酸钾的质量是X2KClO3===2KCl+3O2↑△MnO26、含杂质(杂质与空气不反应)的镁条3.0g,在空气中充分燃烧所得固体的质量是4.6g,那么原镁条中镁的质量分数是多少?设混合物中镁的质量是 X2Mg+O2====2MgO分析:3.0不是纯净的镁,不能用;4.6也不是纯净的氧化镁也不能用。看反应找质量差,差值是氧气的质量。点燃解:反应的氧气的质量是:4.6-3.0=1.6g
及反应的条件。2、表示各反应物、生成物之间的粒子个数之比。3、表示反应物、生成物各物质之间的质量比。化学方程式的意义有哪些?(以电解水的反应为例)2H2O 2H2↑+O2↑1、表示水通电生成氢气和氧气。2、表示每36份质量的水完全反应,生成4份质
量的氢气和32份质量的氧气。3643218Kg?3、表示2个水分子通电生成2个氢分子和1个
氧分子 在生产、科研中,人们研究物质变化,常常涉及量的计算。 如:一定量的原料,最多可以生产多少产品; 如 : 每天生产50吨钢,最少需要多少吨炼铁的铁矿石。根据化学方程式计算的步骤设未知量
写出化学方程式并配平
写出有关物质的相对分子 质量和已知量、未知量
列出比例式、求解
简明地写出答案例1 加热分解6g高锰酸钾,可以得到多少克氧气?设:加热分解 6g高锰酸钾,可以得到氧气的质量为x2×158
6g32
x答:加热分解 6g高锰酸钾,可以得到0.6g氧气。 给你提个醒根据化学方程式计算的正确解题步骤[解](1)设未知数(未知数不带单位)(2)正确写出化学方程式(3)写出相关物质的相对分子质量
和已知量、未知量(4)列出比例,求解(5)简明地写出答案练习1:15.5克红磷在氧气中充分燃烧,可生成五氧化二磷多少克?(找出下列所解答案中的错误)解:设可生成X克五氧化二磷
点燃
P + O 2 ====== P 2 O 5
31 142
15.5 X 31 15.5------- = ---------142 XX = --------------142×15.531= 71答:可生成五氧化二磷71克××××未配平
式量计算错误
未注明单位计算结果错误且无单位×想一想 例2工业上,高温煅烧石灰石(CaCO3)可制得生石灰(CaO)和二氧化碳。如果要制取10t氧化钙,需要碳酸钙多少吨?
解:设制取10吨氧化钙需要碳酸钙的质量为X答:需要碳酸钙的质量为17.9t。例3.用含碳酸钙90%的石灰石100g,与足量稀盐酸充分反应(杂质不与盐酸反应),可制得二氧化碳多少克?标准状况下制得二氧化碳多少升?(标准状况下二氧化碳的密度约为2.0g/L.)
(CaCO3 + 2HCl = CaCl2 + H2O +CO2 )解:设可制得二氧化碳的质量为X100g×90% X
39.6g答:制得二氧化碳39.6g,标准状况下制得二氧化碳19.8L
例4. 实验室有5g锌粒跟10ml稀硫酸待反应完成后,剩余锌粒3.7克,问可生成H2多少克?体积是多少升?(密度是0.09g/L)
(Zn + H2SO4 == H2 + ZnSO4)
解:设可制得H2的质量为XZn + H2SO4 == H2 + ZnSO465 25g-3.7g X答:可生成H20.04g,体积是0.44L解题注意事项:1、在化学方程式中,反应物与生成物之间的质量比,是各化学式的相对分子质量与化学式前边的化学计量数(系数)的乘积之比,因此要准确计算。2、化学方程式中,各物质的质量比都是纯量间的比,因此代入的量必须是纯净的质量。如提供的量不是纯量,必须换算成纯量后才能代入。3、注意解题格式要规范化,注意单位和数据精确度。 1、4克氧气可跟( )克氢气完全反应.。 A 、 1 B、 0.5 C、 2 D 、 4
2、3克镁在足量的氧气中完全燃烧,可得到氧化镁( )克。 A、10 B、 6 C 、5 D、 12 B 、C练习 3.有氢气和氧气的混合气体10克,经点燃充分反应后,恢复到常温,还有1克气体剩余,则混合物可能的成分是( )。
A、H2 5克、O25克
B 、H2 1克、O29克 C 、H2 2克、O28克
D 、H2 4克、O26克 答案:B、C练习:1、3g的碳完全燃烧可以消耗氧气多少g?解:设3g的碳完全燃烧可以消耗氧气X12C + O2=== CO232点燃3gX答: 3g的碳完全燃烧可以消耗氧气8g。X = 8 g2、用氢气还原氧化铜得到金属铜,那么如果想得到32g的铜,应需要氧化铜多少g?H2 + CuO === Cu + H2O解:设如果想得到32g的铜,应需要氧化铜x答:设如果想得到32g的铜,应需要氧化铜40g。32gX = 40 g80?X643、某医院急需给病人输氧气,但是没有现成的氧气,需要用分解过氧化氢的方法制取氧气,那么如果需要氧气的体积是23L,则需要分解多少g的过氧化氢?(氧气的密度是1.4g/L)X2H2O2 ==== 2H2O + O2↑设制取氧气32.2g需要分解过氧化氢X68解:氧气的质量为:m=ρV=23×1.4=32.2g32.2g32MnO2X = 68.4 g答:制取23L氧气需要分解68.4g过氧化氢。分析:S + O2 === SO24、38g硫在32g氧气中燃烧生成二氧化硫的质量是多少?点燃3238g3238g解:设38g硫反应需要氧气XS + O2 === SO2点燃323238gXX = 38 g设38g硫在32g氧气中燃烧生成二氧化硫的质量是Y∴38g硫和38克氧气恰好完全反应,所以氧气完全反应点燃326432gYY = 64 g答:38g硫在32g氧气中燃烧生成二氧化硫的质量是64g。
解:氧气的质量是:m=20-15.2=4.8g 分析:找完全反应物质的质量,起始20g不是反应后的15.2g也不是。看反应找质量差。反应前是固体,反应后是固体和气体,气体益出剩下的是固体所以质量要减小,减小的质量就是气体的质量。即O2的质量是4.8g。5、氯酸钾和二氧化锰的混合固体20g,加热完全反应后剩余固体的质量是15.2g,求原混合物种氯酸钾的质量。设混合物中的氯酸钾的质量是X2KClO3===2KCl+3O2↑△MnO26、含杂质(杂质与空气不反应)的镁条3.0g,在空气中充分燃烧所得固体的质量是4.6g,那么原镁条中镁的质量分数是多少?设混合物中镁的质量是 X2Mg+O2====2MgO分析:3.0不是纯净的镁,不能用;4.6也不是纯净的氧化镁也不能用。看反应找质量差,差值是氧气的质量。点燃解:反应的氧气的质量是:4.6-3.0=1.6g
