化学人教版(2019)选择性必修2 3.1物质的聚集状态与晶体的常识(共37张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修2 3.1物质的聚集状态与晶体的常识(共37张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 20.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-20 00:00:00 | ||
图片预览











文档简介
(共37张PPT)
1. 知道在一定条件下,物质的聚集状态随构成物质的粒子种类、粒子间相互作用、粒子聚集程度的不同而有所不同。
2. 了解等离子体、液晶的概念及其应用。
3. 知道晶体与非晶体的区别,能结合实例描述晶体中粒子排列的周期性规律。
第三章 第一节
《物质的聚集状态 晶体与非晶体》
你知道吗
日常生活中所接触到的物质会有哪些状态呢?
钻石
松香
塑料
玻璃
固态:
流水
液态:
氧气
气态:
极光
雷电
那么雷电和极光里的物质又是什么状态的呢?
物质的聚集状态只有固态、液态、气态三种吗?
观察思考
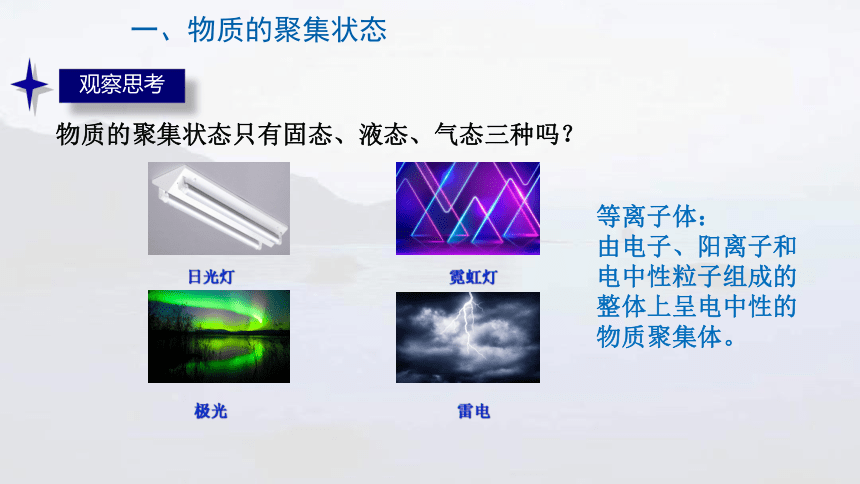
一、物质的聚集状态
观察思考
日光灯
物质的聚集状态只有固态、液态、气态三种吗?
霓虹灯
等离子体:
由电子、阳离子和
电中性粒子组成的
整体上呈电中性的
物质聚集体。
极光
雷电
一、物质的聚集状态
观察思考
等离子体的用途:
一、物质的聚集状态
利用等离子体进行化学合成
核聚变在等离子体状态下发生
制造等离子体显示器
观察思考
物质的聚集状态只有固态、液态、气态三种吗?
液晶显示器
液晶:介于液态和晶态之间的物质状态
物质的聚集状态除了固态、液态、气态,等离子体、晶态、非晶态等等
一、物质的聚集状态
实验室常见固体
观察思考
白磷
磷
硫磺
胆矾
碳酸钙
二、晶体与非晶体
自然界中矿物固体
观察思考
萤石
方解石
翡翠石
透辉石
二、晶体与非晶体
生活中的固体
观察思考
二、晶体与非晶体
一些不法商人用玻璃制造假宝石来牟取暴利,如何鉴别真假宝石?
情境导入
二、晶体与非晶体
固体有晶体和非晶体之分,天然晶体外观特征?
观察思考
二、晶体与非晶体
资料卡片
晶体能够自发地呈现封闭的、规则的多面体外形。
晶体的自范性
二、晶体与非晶体
晶体与非晶体有什么本质的差异?
思考讨论
为什么晶体呈现规则的几何外形?
微观结构
宏观性质
决定
晶体的自范性是晶体内部微粒在微观空间里呈现周期性有序排列的宏观表象。
二、晶体与非晶体
资料卡片
晶体自范性的条件之一是生长的速率适当
水晶球 玛瑙 水晶
二、晶体与非晶体
熔融态物质凝固
气态物质冷却不经液态直接凝固(凝华)
溶质从溶液中析出
除了冷却,还有没有其它途径得到晶体?
思考讨论
二、晶体与非晶体
资料卡片
晶体在不同的方向上具有不同的物理性质。
晶体的各向异性
如光学性质(折射率等) 力学性质(硬度等)、热学性质(导热性等)、电学性质(导电性)。
二、晶体与非晶体
云母片的蜡熔化成椭圆形,玻璃片的蜡熔化成圆形
思考讨论
云母片上的长轴方向与短轴方向传热速度不同,
热导率有各向异性。
蜡滴
玻璃片
云母片
蜡滴
二、晶体与非晶体
不同方向观察红宝石,发现宝石的颜色不同
思考讨论
在不同方向,晶体对光线的吸收与反射是不同的,
折射率有各向异性。
二、晶体与非晶体
石墨在平行于层的方向上电导率高; 而在垂直于层的方向上电导率低。
思考讨论
在不同方向,石墨的导电能力不同,导电率有各向异性。
二、晶体与非晶体
思考讨论
为什么晶体各向异性?
微观结构
宏观性质
决定
晶体的各向异性是晶体内部的微粒在空间各个方向上排列规律不同的宏观表象。
A
B
C
D
二、晶体与非晶体
资料卡片
晶体有确定的熔点
晶体加热至熔点开始熔化,
熔化过程中温度保持不变,
熔化成液态后温度才继续上升。
非晶体在加热时,由开始软化到完全熔化,整个过程中温度不断的变化,没有温度停顿的时候,很难指出哪一点是熔点
二、晶体与非晶体
思考讨论
为什么晶体有确定的熔点?
微观结构
宏观性质
决定
晶体有确定的熔点晶体内部微粒在微观空间里呈现周期性有序排列的宏观表象。
二、晶体与非晶体
学以致用
外观 自范性 各向异性 熔、沸点
晶体 具有规则几何外形 有 各向异性 固定
非晶体 不具有规则几何外形 无 各向同性 不固定
本质区别 微观粒子在三维空间是否呈现周期性有序排列
二、晶体与非晶体
一些不法商人用玻璃制造假宝石来牟取暴利,如何鉴别真假宝石?
常见非晶体:
玻璃、石蜡、松香、沥青、橡胶、炭黑。
许多固体粉末用肉眼看不到晶体外形,但在光学显微镜或电子显微镜
下可观察到规则的晶体外形。
观察思考
晶体结构的周期大小和X-射线的波长相当(1-10000pm),使它成为天然的三维光栅,能够对X-射线产生衍射:
X-射线衍射实验区分晶体和非晶体最可靠的科学方法
二、晶体与非晶体
资料卡片
晶体材料的应用
二、晶体与非晶体
资料卡片
非晶体的优异性能
非晶态合金强度、硬度比相应晶态合金的高5-10倍
非晶态合金在中性或酸性溶液中耐腐蚀性能比不锈钢好的多
二、晶体与非晶体
晶体 非晶体
微观结构特征 粒子周期性有序排列 粒子排列相对无序
性质 特征 自范性 有 无
各向异性 有 无
熔点 固定 不固定
鉴别方法 间接方法 看是否具有固定的熔点或根据某些物理性质的各向异性 科学方法 对固体进行X-射线衍射实验 举例 NaCl、I2、SiO2、Na晶体等 玻璃、橡胶等
小结
一、晶体结构的测定
—— X 射线衍射实验
当单一波长的 X 射线通过晶体时,X 射线和晶体中的电子相互作用,会在记录仪上产生分立的斑点或者明锐的衍射峰
X 射线衍射仪
单晶衍射图
非晶态和晶态 SiO2 衍射图谱
一、晶体结构的测定
—— X 射线衍射实验
晶体的X射线衍射实验图经过计算,可以获得包括晶胞形状和大小、分子或原子在微观空间有序排列呈现的对称类型、原子在晶胞里的数目和位置等,以及结合晶体化学组成的信息推出原子之间的相互关系。
乙酸晶体
乙酸晶胞
什么是晶胞?
二、晶胞
1. 概念:
描述晶体结构的基本单元叫做晶胞
铜晶体
二、晶胞
1. 概念:
描述晶体结构的基本单元叫做晶胞
8 个顶角相同
三套各两个平行面分别相同
三套各4根平行棱分别相同
最小平行六面体
二、晶胞
2. 晶胞与晶体的关系
常规晶胞为平行六面体,晶体可看作是数量巨大的晶胞“无隙并置”而成
①无隙:相邻晶胞之间无任何间隙
②并置:所有晶胞都是平行排列的,取向相同
③所有晶胞的形状及其内部的原子种类、个数及几何排列(包括取向)是完全相同的。
二、晶胞
下图铜晶胞中,含有几个铜原子?
14
4
二、晶胞
3. 晶胞中粒子数目的计算
顶角:
1/8
棱上:
1/4
面上:
1/2
内部:
1
—— 均摊法
某个粒子若被 n 个晶胞所共用,
则该粒子有 1/n 属于这个晶胞。
试着计算一个铜晶胞中含有几个铜原子
顶角位置:8× =1
8
1
面上位置:6× =3
2
1
金属铜的一个晶胞的原子数=8× +6× =4
2
1
8
1
下图为 NaCl 的晶胞,它含有几个钠离子和氯离子?晶胞中钠离子和氯离子的个数比是多少?
钠离子数=12× +1×1=4
4
1
晶胞中钠离子和氯离子的个数比是 1∶1
氯离子数= 8× +6× =4
8
1
2
1
计算下图晶胞中分别平均含有几个原子
I2
金刚石
Na
Zn
8× + 1×1=2
8
1
8× + 1×1=2
8
1
2×(8× + 6× )=8
8
1
2
1
8× + 6× + 4×1=8
8
1
2
1
1. 知道在一定条件下,物质的聚集状态随构成物质的粒子种类、粒子间相互作用、粒子聚集程度的不同而有所不同。
2. 了解等离子体、液晶的概念及其应用。
3. 知道晶体与非晶体的区别,能结合实例描述晶体中粒子排列的周期性规律。
第三章 第一节
《物质的聚集状态 晶体与非晶体》
你知道吗
日常生活中所接触到的物质会有哪些状态呢?
钻石
松香
塑料
玻璃
固态:
流水
液态:
氧气
气态:
极光
雷电
那么雷电和极光里的物质又是什么状态的呢?
物质的聚集状态只有固态、液态、气态三种吗?
观察思考
一、物质的聚集状态
观察思考
日光灯
物质的聚集状态只有固态、液态、气态三种吗?
霓虹灯
等离子体:
由电子、阳离子和
电中性粒子组成的
整体上呈电中性的
物质聚集体。
极光
雷电
一、物质的聚集状态
观察思考
等离子体的用途:
一、物质的聚集状态
利用等离子体进行化学合成
核聚变在等离子体状态下发生
制造等离子体显示器
观察思考
物质的聚集状态只有固态、液态、气态三种吗?
液晶显示器
液晶:介于液态和晶态之间的物质状态
物质的聚集状态除了固态、液态、气态,等离子体、晶态、非晶态等等
一、物质的聚集状态
实验室常见固体
观察思考
白磷
磷
硫磺
胆矾
碳酸钙
二、晶体与非晶体
自然界中矿物固体
观察思考
萤石
方解石
翡翠石
透辉石
二、晶体与非晶体
生活中的固体
观察思考
二、晶体与非晶体
一些不法商人用玻璃制造假宝石来牟取暴利,如何鉴别真假宝石?
情境导入
二、晶体与非晶体
固体有晶体和非晶体之分,天然晶体外观特征?
观察思考
二、晶体与非晶体
资料卡片
晶体能够自发地呈现封闭的、规则的多面体外形。
晶体的自范性
二、晶体与非晶体
晶体与非晶体有什么本质的差异?
思考讨论
为什么晶体呈现规则的几何外形?
微观结构
宏观性质
决定
晶体的自范性是晶体内部微粒在微观空间里呈现周期性有序排列的宏观表象。
二、晶体与非晶体
资料卡片
晶体自范性的条件之一是生长的速率适当
水晶球 玛瑙 水晶
二、晶体与非晶体
熔融态物质凝固
气态物质冷却不经液态直接凝固(凝华)
溶质从溶液中析出
除了冷却,还有没有其它途径得到晶体?
思考讨论
二、晶体与非晶体
资料卡片
晶体在不同的方向上具有不同的物理性质。
晶体的各向异性
如光学性质(折射率等) 力学性质(硬度等)、热学性质(导热性等)、电学性质(导电性)。
二、晶体与非晶体
云母片的蜡熔化成椭圆形,玻璃片的蜡熔化成圆形
思考讨论
云母片上的长轴方向与短轴方向传热速度不同,
热导率有各向异性。
蜡滴
玻璃片
云母片
蜡滴
二、晶体与非晶体
不同方向观察红宝石,发现宝石的颜色不同
思考讨论
在不同方向,晶体对光线的吸收与反射是不同的,
折射率有各向异性。
二、晶体与非晶体
石墨在平行于层的方向上电导率高; 而在垂直于层的方向上电导率低。
思考讨论
在不同方向,石墨的导电能力不同,导电率有各向异性。
二、晶体与非晶体
思考讨论
为什么晶体各向异性?
微观结构
宏观性质
决定
晶体的各向异性是晶体内部的微粒在空间各个方向上排列规律不同的宏观表象。
A
B
C
D
二、晶体与非晶体
资料卡片
晶体有确定的熔点
晶体加热至熔点开始熔化,
熔化过程中温度保持不变,
熔化成液态后温度才继续上升。
非晶体在加热时,由开始软化到完全熔化,整个过程中温度不断的变化,没有温度停顿的时候,很难指出哪一点是熔点
二、晶体与非晶体
思考讨论
为什么晶体有确定的熔点?
微观结构
宏观性质
决定
晶体有确定的熔点晶体内部微粒在微观空间里呈现周期性有序排列的宏观表象。
二、晶体与非晶体
学以致用
外观 自范性 各向异性 熔、沸点
晶体 具有规则几何外形 有 各向异性 固定
非晶体 不具有规则几何外形 无 各向同性 不固定
本质区别 微观粒子在三维空间是否呈现周期性有序排列
二、晶体与非晶体
一些不法商人用玻璃制造假宝石来牟取暴利,如何鉴别真假宝石?
常见非晶体:
玻璃、石蜡、松香、沥青、橡胶、炭黑。
许多固体粉末用肉眼看不到晶体外形,但在光学显微镜或电子显微镜
下可观察到规则的晶体外形。
观察思考
晶体结构的周期大小和X-射线的波长相当(1-10000pm),使它成为天然的三维光栅,能够对X-射线产生衍射:
X-射线衍射实验区分晶体和非晶体最可靠的科学方法
二、晶体与非晶体
资料卡片
晶体材料的应用
二、晶体与非晶体
资料卡片
非晶体的优异性能
非晶态合金强度、硬度比相应晶态合金的高5-10倍
非晶态合金在中性或酸性溶液中耐腐蚀性能比不锈钢好的多
二、晶体与非晶体
晶体 非晶体
微观结构特征 粒子周期性有序排列 粒子排列相对无序
性质 特征 自范性 有 无
各向异性 有 无
熔点 固定 不固定
鉴别方法 间接方法 看是否具有固定的熔点或根据某些物理性质的各向异性 科学方法 对固体进行X-射线衍射实验 举例 NaCl、I2、SiO2、Na晶体等 玻璃、橡胶等
小结
一、晶体结构的测定
—— X 射线衍射实验
当单一波长的 X 射线通过晶体时,X 射线和晶体中的电子相互作用,会在记录仪上产生分立的斑点或者明锐的衍射峰
X 射线衍射仪
单晶衍射图
非晶态和晶态 SiO2 衍射图谱
一、晶体结构的测定
—— X 射线衍射实验
晶体的X射线衍射实验图经过计算,可以获得包括晶胞形状和大小、分子或原子在微观空间有序排列呈现的对称类型、原子在晶胞里的数目和位置等,以及结合晶体化学组成的信息推出原子之间的相互关系。
乙酸晶体
乙酸晶胞
什么是晶胞?
二、晶胞
1. 概念:
描述晶体结构的基本单元叫做晶胞
铜晶体
二、晶胞
1. 概念:
描述晶体结构的基本单元叫做晶胞
8 个顶角相同
三套各两个平行面分别相同
三套各4根平行棱分别相同
最小平行六面体
二、晶胞
2. 晶胞与晶体的关系
常规晶胞为平行六面体,晶体可看作是数量巨大的晶胞“无隙并置”而成
①无隙:相邻晶胞之间无任何间隙
②并置:所有晶胞都是平行排列的,取向相同
③所有晶胞的形状及其内部的原子种类、个数及几何排列(包括取向)是完全相同的。
二、晶胞
下图铜晶胞中,含有几个铜原子?
14
4
二、晶胞
3. 晶胞中粒子数目的计算
顶角:
1/8
棱上:
1/4
面上:
1/2
内部:
1
—— 均摊法
某个粒子若被 n 个晶胞所共用,
则该粒子有 1/n 属于这个晶胞。
试着计算一个铜晶胞中含有几个铜原子
顶角位置:8× =1
8
1
面上位置:6× =3
2
1
金属铜的一个晶胞的原子数=8× +6× =4
2
1
8
1
下图为 NaCl 的晶胞,它含有几个钠离子和氯离子?晶胞中钠离子和氯离子的个数比是多少?
钠离子数=12× +1×1=4
4
1
晶胞中钠离子和氯离子的个数比是 1∶1
氯离子数= 8× +6× =4
8
1
2
1
计算下图晶胞中分别平均含有几个原子
I2
金刚石
Na
Zn
8× + 1×1=2
8
1
8× + 1×1=2
8
1
2×(8× + 6× )=8
8
1
2
1
8× + 6× + 4×1=8
8
1
2
1
