化学能转化为电能——金属的腐蚀与防护1.2课件(共21张PPT)发展中的化学电源鲁科版 选择性必修1
文档属性
| 名称 | 化学能转化为电能——金属的腐蚀与防护1.2课件(共21张PPT)发展中的化学电源鲁科版 选择性必修1 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-20 00:00:00 | ||
图片预览







文档简介
(共21张PPT)
金属腐蚀与防护
鲁科版 选择性必修1 第一章 化学反应与能量转化
目标与素养:
1.科学探究与创新意识:通过实验科学探究金属腐蚀的
本质及其原因,认识金属腐蚀的主要类型,能正确书写析氢
腐蚀和吸氧腐蚀的电极反应式。
2.科学态度与社会责任:认识金属腐蚀产生的危害和影
响,树立防止金属腐蚀的意识,熟知金属腐蚀常用的防护方
法。
探究金属腐蚀的原理
环节一
实验药品:铁钉、食盐水
实验仪器:具支试管、试管、玻璃管
实验方案:如右图
实验现象: 一段时间后,导管口水柱明显上升
实验结论: 具支试管里的气体减少
活动一 探究海水环境中O2是否参与钢铁的腐蚀
资料卡片
铁氰化钾溶液(K3 [Fe(CN)6]) 遇 Fe2+生成蓝色沉淀,常用于Fe2+ 的检验
铁钉在腐蚀过程中发生的反应是什么?
你想通过什么试剂验证你的推测?
活动二 钢铁化学腐蚀过程中的物质转化
活动三 钢铁电化学腐蚀过程中的物质转化
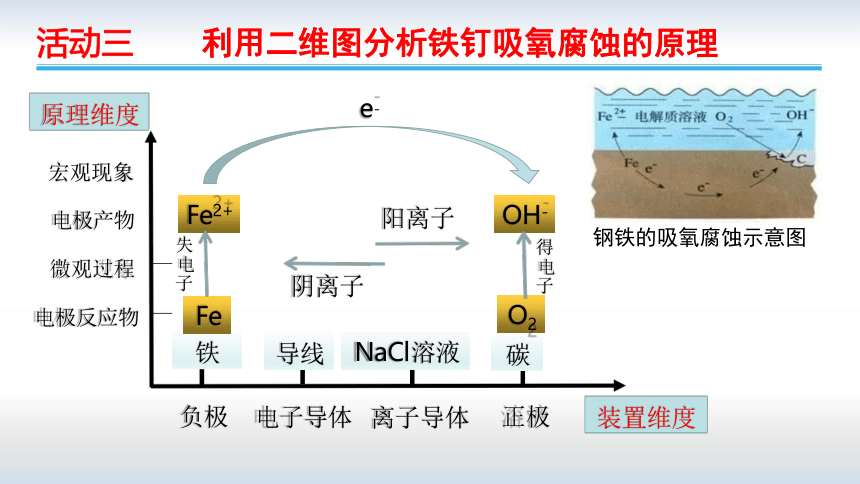
活动三 利用二维图分析铁钉吸氧腐蚀的原理
NaCl
钢铁的吸氧腐蚀示意图
装置维度
原理维度
阴离子
离子导体
电子导体
电极反应物
宏观现象
微观过程
电极产物
导线
铁
阳离子
Fe
OH-
碳
溶液
正极
负极
Fe
2
O
-
失
子
子
电
电
e
得
2+
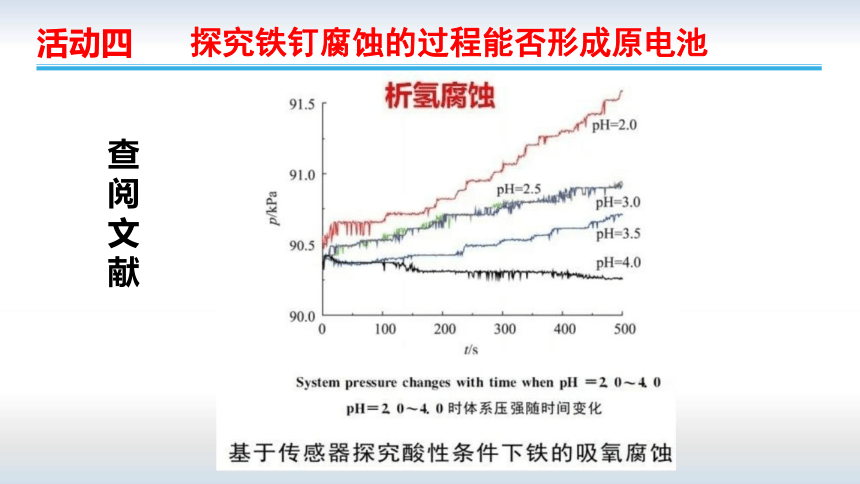
活动四 探究铁钉腐蚀的过程能否形成原电池
请你设计实验验证铁钉腐蚀过程中形成了原电池?
活动四 探究铁钉腐蚀的过程能否形成原电池
查 阅 文 献
【归纳总结】
NaCl
阴离子
装置维度
原理维度
电极反应物
微观过程
宏观现象
离子导体
电子导体
电极产物
钢铁的析氢腐蚀示意图
钢铁的吸氧腐蚀示意图
导线
2
碳
阳离子
OH-
Fe
铁
溶液
Fe
O
H
正 极
负 极
2
子
子
子
失
电
电
电
e
H
得
得
2+
+
-
析氢腐蚀
吸氧腐蚀
条件 水膜呈酸性(PH<4.3)
水膜呈中性或酸性很弱
电极反应 负极Fe(-) Fe-2e-=Fe2+
2Fe-4e-=2Fe2+
正极C(+) 2H++2e-= H2 ↑
O2+2H2O+4e-=4OH-
总反应 Fe+2H+=Fe2+ + H2 ↑
2Fe+2H2O+O2=2Fe(OH)2
4Fe(OH)2+2H2O+O2= 4Fe(OH)3 Fe2O3 · nH2O
联系 金属的腐蚀以电化学腐蚀为主, 电化学腐蚀又以吸氧腐蚀为主。
电化学腐蚀:不纯的金属或者合金与电解质溶液接触, 较活泼的金属发生氧化还原反应,形成电流的腐蚀
(铁锈)
化学腐蚀:金属与其表面接触的物质直接反应
【归纳总结】 钢铁的析氢腐蚀和吸氧腐蚀比较
1、定义:金属或合金与周围接触到的气体或液体
进行化学反应而腐蚀损耗的过程。
2、本质: M - ne- = Mn+ (发生氧化反应)
化学腐蚀
吸氧腐蚀
电化学腐蚀 析氢腐蚀
3、金属腐蚀的类型
金属的腐蚀
【归纳总结】
烤蓝
镀铬
烤漆
涂凡士林 镀锌
1 覆盖保护层
金属防护的方法
涂机油
知识卡片:
改变金属材料的组成 ,在金属中添加其他 金属或非金属可以制成性能优异的合金。
在钢铁中加入一定比例的铬和镍(14%~8%Cr, 7%~9%Ni) ,改变钢铁内部的组成和结构, 可极大程度的提高钢铁的抗腐蚀性能,这就 是常见的“不锈钢”(合金)。
金属防护的方法
千年不锈之谜:越王勾践剑的含铜量约为80%-83%、 含锡量约为16%- 17%。
2 改变组成结构
环节二
金属防护的方法
锌 片
一天后
利用模型 设计方案
环节二
NaCl溶液
锌 片
铜 片
铜 片
环节二 金属防护的方法
牺牲阳极的阴极保护法
原理: 原电池原理
3 电化学防护法
金属腐蚀中产生的能量及物质可否科学地进行应用?
环节三
金属腐蚀的应用
知识卡片
蛭石:是一种与蒙脱石相似的粘土矿物, 为层状结构的硅酸盐,具有很强的保温 隔热性能。
吸水性树脂:高吸水性树脂是一种新型 的高分子材料,它能够吸收自身重量几 百倍至千倍的水分,无毒、无害、无污 染;吸水能力特强,保水能力特高
交流与讨论:
1. 你们针对暖宝宝发热原理的猜想?
2. 能否设计实验来模仿“暖宝宝发热原理”
活动 探究暖宝宝的发热原理
实验仪器及仪器:氧气传感器、烧杯、 具支试管、试管、蒸馏水、暖宝宝
并证明是氧气参加了反应呢?
负极: Fe-2e-=Fe2+
正极: O2+4e-+2H2O=4OH-
总反应: 2Fe+O2+2H2O=2Fe(OH)2
活动 探究暖宝宝的发热原理
O2参与反应生成了OH-
宏观现象
微观原理
符号表征
吸氧腐蚀
双吸剂(吸氧、吸水)
主要成分:铁粉、碳粉、钠盐、卤化物。
特点:反应迅速,可在2小时内使包装袋内氧的浓度降到0.01%
环节三
金属腐蚀的应用
金属腐蚀与防护
鲁科版 选择性必修1 第一章 化学反应与能量转化
目标与素养:
1.科学探究与创新意识:通过实验科学探究金属腐蚀的
本质及其原因,认识金属腐蚀的主要类型,能正确书写析氢
腐蚀和吸氧腐蚀的电极反应式。
2.科学态度与社会责任:认识金属腐蚀产生的危害和影
响,树立防止金属腐蚀的意识,熟知金属腐蚀常用的防护方
法。
探究金属腐蚀的原理
环节一
实验药品:铁钉、食盐水
实验仪器:具支试管、试管、玻璃管
实验方案:如右图
实验现象: 一段时间后,导管口水柱明显上升
实验结论: 具支试管里的气体减少
活动一 探究海水环境中O2是否参与钢铁的腐蚀
资料卡片
铁氰化钾溶液(K3 [Fe(CN)6]) 遇 Fe2+生成蓝色沉淀,常用于Fe2+ 的检验
铁钉在腐蚀过程中发生的反应是什么?
你想通过什么试剂验证你的推测?
活动二 钢铁化学腐蚀过程中的物质转化
活动三 钢铁电化学腐蚀过程中的物质转化
活动三 利用二维图分析铁钉吸氧腐蚀的原理
NaCl
钢铁的吸氧腐蚀示意图
装置维度
原理维度
阴离子
离子导体
电子导体
电极反应物
宏观现象
微观过程
电极产物
导线
铁
阳离子
Fe
OH-
碳
溶液
正极
负极
Fe
2
O
-
失
子
子
电
电
e
得
2+
活动四 探究铁钉腐蚀的过程能否形成原电池
请你设计实验验证铁钉腐蚀过程中形成了原电池?
活动四 探究铁钉腐蚀的过程能否形成原电池
查 阅 文 献
【归纳总结】
NaCl
阴离子
装置维度
原理维度
电极反应物
微观过程
宏观现象
离子导体
电子导体
电极产物
钢铁的析氢腐蚀示意图
钢铁的吸氧腐蚀示意图
导线
2
碳
阳离子
OH-
Fe
铁
溶液
Fe
O
H
正 极
负 极
2
子
子
子
失
电
电
电
e
H
得
得
2+
+
-
析氢腐蚀
吸氧腐蚀
条件 水膜呈酸性(PH<4.3)
水膜呈中性或酸性很弱
电极反应 负极Fe(-) Fe-2e-=Fe2+
2Fe-4e-=2Fe2+
正极C(+) 2H++2e-= H2 ↑
O2+2H2O+4e-=4OH-
总反应 Fe+2H+=Fe2+ + H2 ↑
2Fe+2H2O+O2=2Fe(OH)2
4Fe(OH)2+2H2O+O2= 4Fe(OH)3 Fe2O3 · nH2O
联系 金属的腐蚀以电化学腐蚀为主, 电化学腐蚀又以吸氧腐蚀为主。
电化学腐蚀:不纯的金属或者合金与电解质溶液接触, 较活泼的金属发生氧化还原反应,形成电流的腐蚀
(铁锈)
化学腐蚀:金属与其表面接触的物质直接反应
【归纳总结】 钢铁的析氢腐蚀和吸氧腐蚀比较
1、定义:金属或合金与周围接触到的气体或液体
进行化学反应而腐蚀损耗的过程。
2、本质: M - ne- = Mn+ (发生氧化反应)
化学腐蚀
吸氧腐蚀
电化学腐蚀 析氢腐蚀
3、金属腐蚀的类型
金属的腐蚀
【归纳总结】
烤蓝
镀铬
烤漆
涂凡士林 镀锌
1 覆盖保护层
金属防护的方法
涂机油
知识卡片:
改变金属材料的组成 ,在金属中添加其他 金属或非金属可以制成性能优异的合金。
在钢铁中加入一定比例的铬和镍(14%~8%Cr, 7%~9%Ni) ,改变钢铁内部的组成和结构, 可极大程度的提高钢铁的抗腐蚀性能,这就 是常见的“不锈钢”(合金)。
金属防护的方法
千年不锈之谜:越王勾践剑的含铜量约为80%-83%、 含锡量约为16%- 17%。
2 改变组成结构
环节二
金属防护的方法
锌 片
一天后
利用模型 设计方案
环节二
NaCl溶液
锌 片
铜 片
铜 片
环节二 金属防护的方法
牺牲阳极的阴极保护法
原理: 原电池原理
3 电化学防护法
金属腐蚀中产生的能量及物质可否科学地进行应用?
环节三
金属腐蚀的应用
知识卡片
蛭石:是一种与蒙脱石相似的粘土矿物, 为层状结构的硅酸盐,具有很强的保温 隔热性能。
吸水性树脂:高吸水性树脂是一种新型 的高分子材料,它能够吸收自身重量几 百倍至千倍的水分,无毒、无害、无污 染;吸水能力特强,保水能力特高
交流与讨论:
1. 你们针对暖宝宝发热原理的猜想?
2. 能否设计实验来模仿“暖宝宝发热原理”
活动 探究暖宝宝的发热原理
实验仪器及仪器:氧气传感器、烧杯、 具支试管、试管、蒸馏水、暖宝宝
并证明是氧气参加了反应呢?
负极: Fe-2e-=Fe2+
正极: O2+4e-+2H2O=4OH-
总反应: 2Fe+O2+2H2O=2Fe(OH)2
活动 探究暖宝宝的发热原理
O2参与反应生成了OH-
宏观现象
微观原理
符号表征
吸氧腐蚀
双吸剂(吸氧、吸水)
主要成分:铁粉、碳粉、钠盐、卤化物。
特点:反应迅速,可在2小时内使包装袋内氧的浓度降到0.01%
环节三
金属腐蚀的应用
同课章节目录
- 第1章 化学反应与能量转化
- 第1节 化学反应的热效应
- 第2节 化学能转化为电能——电池
- 第3节 电能转化为化学能——电解
- 第4节 金属的腐蚀与防护
- 微项目 设计载人航天器用化学电池与氧气再生方案——化学反应中能量及物质的转化利用
- 第2章 化学反应的方向、 限度与速率
- 第1节 化学反应的方向
- 第2节 化学反应的限度
- 第3节 化学反应的速率
- 第4节 化学反应条件的优化——工业合成氨
- 微项目 探讨如何利用工业废气中的二氧化碳合成甲醇——化学反应选择与反应条件优化
- 第3章 物质在水溶液中的行为
- 第1节 水与水溶液
- 第2节 弱电解质的电离 盐类的水解
- 第3节 沉淀溶解平衡
- 第4节 离子反应
- 微项目 揭秘索尔维制碱法和侯氏制碱法——化学平衡思想的创造性应用
