化学人教版(2019)选择性必修3 2.1.1烷烃的结构和性质(共20张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 2.1.1烷烃的结构和性质(共20张ppt) |  | |
| 格式 | pptx | ||
| 文件大小 | 4.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-21 00:45:40 | ||
图片预览






文档简介
(共20张PPT)
第二章
烃
第一节 烷烃
课时1 烷烃的结构和性质
烷 烃
只含______两种元素,分子中的碳原子之间都以____结合,碳原子的剩余价键均与______结合,使碳原子的化合价都达到“_____”,这样的一类有机化合物称为______,也称为烷烃。
碳和氢
单键
氢原子
饱和
饱和烃
烷烃
链状烷烃
环烷烃
甲烷、乙烷、丙烷等
环己烷
新课导入
新课导入
烷烃是一种饱和链烃,属于脂肪烃。生活中的一些常见物质,例如天然气、液化石油气、汽油、柴油、凡士林、石蜡等,它们的主要成分都是烷烃。
甲烷
丙烷和丁烷
丁烷
C17~C21的烷烃
C18~C30的烷烃
C5~C11的烷烃
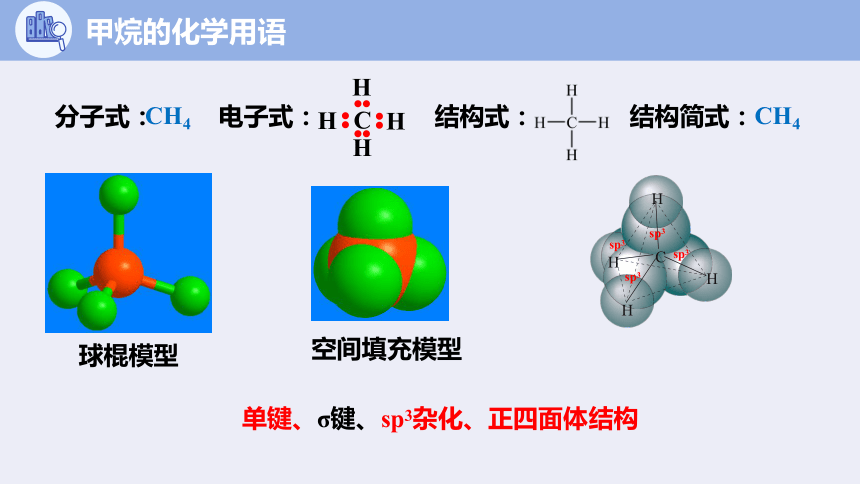
CH4
分子式:
电子式:
C
H
H
H
H
CH4
结构式:
结构简式:
球棍模型
空间填充模型
H
H
H
C
H
sp3
sp3
sp3
sp3
单键、σ键、sp3杂化、正四面体结构
甲烷的化学用语
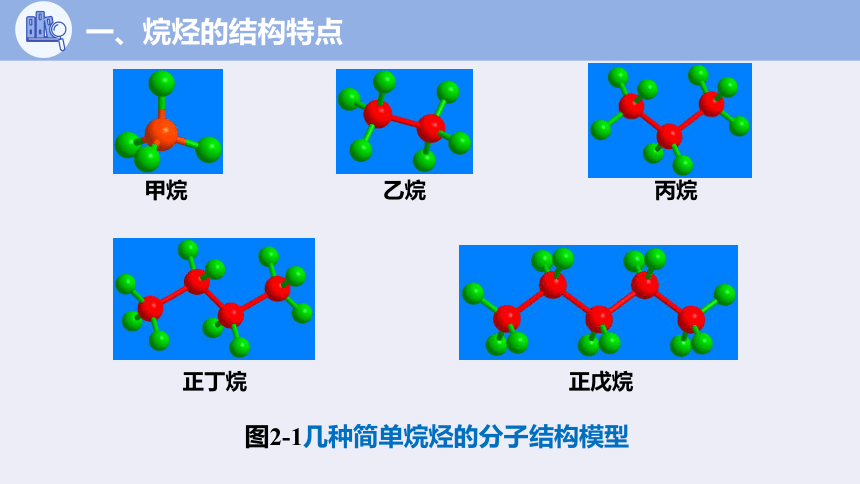
图2-1几种简单烷烃的分子结构模型
甲烷
乙烷
丙烷
正丁烷
正戊烷
一、烷烃的结构特点
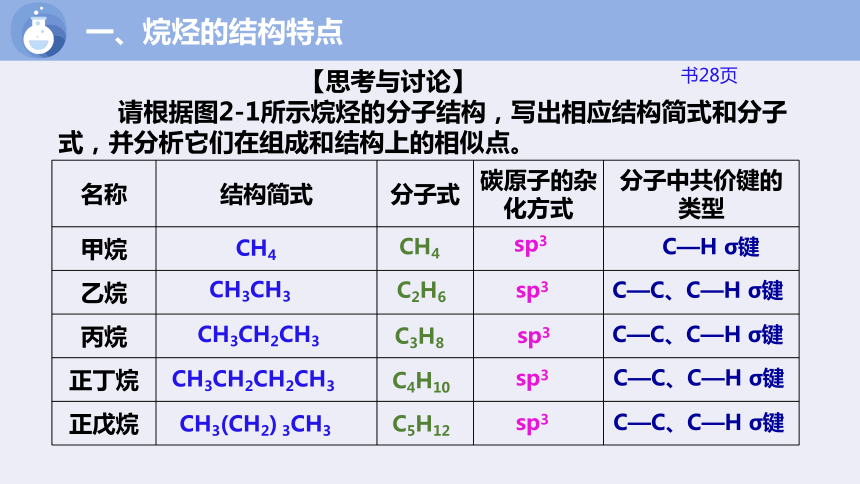
【思考与讨论】
书28页
请根据图2-1所示烷烃的分子结构,写出相应结构简式和分子式,并分析它们在组成和结构上的相似点。
名称 结构简式 分子式 碳原子的杂化方式 分子中共价键的类型
甲烷
乙烷
丙烷
正丁烷
正戊烷
CH4
CH3CH3
CH3CH2CH3
CH3CH2CH2CH3
CH3(CH2) 3CH3
CH4
C2H6
C3H8
C4H10
C5H12
sp3
sp3
sp3
sp3
sp3
C—H σ键
C—C、C—H σ键
C—C、C—H σ键
C—C、C—H σ键
C—C、C—H σ键
一、烷烃的结构特点
1、烷烃的结构与甲烷的相似;
2、其分子中的碳原子都采取sp3杂化;
3、以伸向四面体四个顶点方向的sp3杂化轨道与其他碳原子或氢原子结合,形成σ键;
4、烷烃分子中的共价键全部是单键。
①烷烃的性质与甲烷的相似;
烷烃的所有原子不可能共平面。
②分子中的碳原子并非直线状排列,而是锯齿状。
一、烷烃的结构特点
σ键可旋转
CH3-CH2-CH2-CH3
CH2-CH2
CH3
│
CH3
│
CH3
│
CH3-CH2-CH2
以上三种结构简式都表示正丁烷
链状烷烃的分子式通式:CnH2n+2(n≥1)
①符合该通式的一定是链状烷烃。
②链状烷烃随着n的增加,含氢的质量分数越来越小。
一、烷烃的结构特点
同系物的判断规律:
同系物:结构相似、分子组成上相差一个或若干个_________原子团的化合物称为___________。同系物可用通式表示。
CH2
同系物
1、同通式,同类别(官能团种类、数目相同)
2、分子组成相差一个或若干个CH2原子团
注意:
(1)同系物间物理性质递变,但化学性质相似。
(2)同系物间通式一定相同,但通式相同,不一定是同系物。
例如:C3H6(环丙烷)和C4H8(丁烯)
一、烷烃的结构特点
烷烃名称 分子式 结构简式 常温下状态 熔点/℃ 沸点/℃ 密度/(g/cm3)
甲烷 CH4 CH4 气 -182 -164 0.423
乙烷 C2H6 CH3CH3 气 -172 -89 0.545
丙烷 C3H8 CH3CH2CH3 气 -187 -42 0.501
正丁烷 C4H10 CH3CH2CH2CH3 气 -138 -0.5 0.579
正戊烷 C5H12 CH3(CH2)3CH3 液 -129 36 0.626
正壬烷 C9H20 CH3(CH2)7CH3 液 -54 151 0.718
十一烷 C11H24 CH3(CH2)9CH3 液 -26 196 0.740
十六烷 C16H34 CH3(CH2)14CH3 液 18 280 0.775
十八烷 C18H38 CH3(CH2)16CH3 固 28 308 0.777
观察上表,分析烷烃的密度、熔点和沸点等物理性质变化的基本规律。
二、烷烃的物理性质
2、随着分子中碳原子数的递增,烷烃的相对分子质量增大,分子间作用力增强,烷烃的熔、沸点逐渐升高。
1、常温的状态:气→液→固
C1~C4:气态 C5~C16:液态 C17以上:固态
注意:新戊烷为气态
C数相同,支链越多,沸点越低。
3、所有烷烃均难溶于水,易溶于有机溶剂。
二、烷烃的物理性质
4、所有烷烃密度均小于1。碳原子数的增加,密度逐渐增大。
三、烷烃的化学性质
烷烃的结构决定了其性质与甲烷相似
知识回顾
甲烷的化学性质:
1、稳定性:常温下,不与____、_____、___________反应。
2、____反应(可燃性):______________________
3、____反应:_________________、_________________、
_________________、_________________、
4、高温分解:____________________
强酸 强碱 强氧化剂
CH4+Cl2 CH3Cl+HCl
光
CH3Cl+Cl2 CH2Cl2+HCl
光
CH2Cl2+Cl2 CHCl3+HCl
光
CHCl3+Cl2 CCl4+HCl
光
CH4 C + 2H2
高温
氧化
取代
若1mol甲烷中的H全部被Cl取代,需要多少molCl2?
4mol
若1mol 甲烷全部参加反应最多可以生成多少mol HCl?
4mol
01稳定性
常温下,烷烃很不活泼,与强酸、强碱、强氧化剂(如酸性KMnO4)、溴的四氯化碳溶液等都不发生反应
02氧化反应
烷烃燃烧的通式为
氧化反应||可燃性
(因为烷烃分子中化学键全是σ键,不易断裂)
三、烷烃的化学性质
现象:当碳含量少时,产生淡蓝色火焰,但随着碳原子数的增多,碳的质量分数逐渐增大,有黑烟产生
在常温、常压下,取下列四种气态烃各1 mol,分别在足量的氧气中燃烧,消耗氧气最多的是( ),取同质量的下列四种气态烃分别在足量的氧气中燃烧,消耗氧气最多的是 ( )
A.CH4 B.C3H8 C.C4H10 D.C2H6
C
A
分析:由C~O2~CO2, 4H~O2~2H2O进行比较,
消耗1mol O2,需要12g C,
而消耗1mol O2,需要4g H,
可知有机物含氢量越大,等质量时消耗的O2越多,以此进行比较。
规律:完全燃烧相同质量的烃时,消耗氧气的量随着碳原子数的
递增而减小。
03特征反应 — 取代反应
三、烷烃的化学性质
一氯乙烷
二氯乙烷
三氯乙烷
四氯乙烷
五氯乙烷
六氯乙烷
乙烷与氯气在光照下反应,可能生成哪些产物?请写出它们的结构简式。
可能的产物有:HCl + 9种有机产物
CH3CH2Cl
CH3CHCl2
CH2ClCH2Cl
CH3CCl3
CH2ClCHCl2
CH2ClCCl3
CHCl2CHCl2
CHCl2CCl3
CCl3CCl3
1种
2种
2种
2种
1种
1种
03特征反应 — 取代反应
三、烷烃的化学性质
(4)反应产物:混合物(多种卤代烃),不适宜制备卤代烃。
(3)反应的特点:氢原子被卤素原子逐步取代,多步反应同时进行。
(2)反应物状态:气态卤素单质(F2、Cl2、Br2、I2), 而不是其水溶液。
(1)反应的条件:光照。
04受热分解
长链烷烃高温隔绝氧气条件下可分解成短链烷烃和烯烃,这在石油化工上称为石油的裂化。
C16H34 C8H18+C8H16
催化剂
加热、加压
烷烃
烷烃
烯烃
C4H10 CH4+C3H6
催化剂
加热、加压
C4H10 C2H4+C2H6
催化剂
加热、加压
环烷烃
如:
环丙烷
C3H6
环丁烷C4H8
环戊烷
C5H10
环己烷C6H12
CnH2n(n≥3)
1、环烷烃分子式通式:
2、性质与烷烃相似:
常温下有稳定性,不能被酸性高锰酸钾溶液氧化而使其褪色,能燃烧氧化;能发生光照取代反应。
+
Cl2
光
+ HCl
Cl
1、下列有关烷烃的叙述中,正确的是( )
①在烷烃分子中,所有的化学键都是单键
②烷烃中除甲烷外,很多都能使酸性KMnO4溶液的紫色褪去
③分子通式为CnH2n+2的烃不一定是烷烃
④所有烷烃在光照条件都能与氯气发生取代反应
⑤光照条件下,乙烷通入溴水中,可使溴水褪色
⑥所有的烷烃都可以在空气中燃烧
A.①②③⑥ B.①④⑥ C.②③④ D.①②③④
B
(1)烷烃分子中的所有共价键全部是σ键。 ( )
(2)汽油、煤油、石蜡中的主要成分为烷烃。 ( )
(3)烷烃的化学性质稳定,不能发生氧化反应。 ( )
(4)乙烷的熔、沸点比丙烷的高。 ( )
(5)烷烃能使酸性KMnO4溶液褪色。 ( )
(6)制取1-氯乙烷时可用乙烷和氯气反应。( )
(7)丙烷分子中所有碳原子在一条直线上。( )
(8)光照条件下,1 mol Cl2与2 mol CH4充分反应后可得到
1 mol CH3Cl。( )
(9)标况下,11.2 L己烷所含共价键的数目为9.5NA。( )
2、正误判断
×
√
√
×
×
×
×
×
×
3、丁烷有两种不同结构,分别为正丁烷和异丁烷,均可用作制冷剂,下列关于丁烷的说法正确的是( )
A.异丁烷的沸点高于正丁烷的沸点
B.正丁烷和异丁烷中碳原子均不可能共平面
C.可以通过酸性KMnO4溶液鉴别正丁烷和异丁烷
D.丁烷的一氯取代物共有4种结构(不包含立体异构)
D
第二章
烃
第一节 烷烃
课时1 烷烃的结构和性质
烷 烃
只含______两种元素,分子中的碳原子之间都以____结合,碳原子的剩余价键均与______结合,使碳原子的化合价都达到“_____”,这样的一类有机化合物称为______,也称为烷烃。
碳和氢
单键
氢原子
饱和
饱和烃
烷烃
链状烷烃
环烷烃
甲烷、乙烷、丙烷等
环己烷
新课导入
新课导入
烷烃是一种饱和链烃,属于脂肪烃。生活中的一些常见物质,例如天然气、液化石油气、汽油、柴油、凡士林、石蜡等,它们的主要成分都是烷烃。
甲烷
丙烷和丁烷
丁烷
C17~C21的烷烃
C18~C30的烷烃
C5~C11的烷烃
CH4
分子式:
电子式:
C
H
H
H
H
CH4
结构式:
结构简式:
球棍模型
空间填充模型
H
H
H
C
H
sp3
sp3
sp3
sp3
单键、σ键、sp3杂化、正四面体结构
甲烷的化学用语
图2-1几种简单烷烃的分子结构模型
甲烷
乙烷
丙烷
正丁烷
正戊烷
一、烷烃的结构特点
【思考与讨论】
书28页
请根据图2-1所示烷烃的分子结构,写出相应结构简式和分子式,并分析它们在组成和结构上的相似点。
名称 结构简式 分子式 碳原子的杂化方式 分子中共价键的类型
甲烷
乙烷
丙烷
正丁烷
正戊烷
CH4
CH3CH3
CH3CH2CH3
CH3CH2CH2CH3
CH3(CH2) 3CH3
CH4
C2H6
C3H8
C4H10
C5H12
sp3
sp3
sp3
sp3
sp3
C—H σ键
C—C、C—H σ键
C—C、C—H σ键
C—C、C—H σ键
C—C、C—H σ键
一、烷烃的结构特点
1、烷烃的结构与甲烷的相似;
2、其分子中的碳原子都采取sp3杂化;
3、以伸向四面体四个顶点方向的sp3杂化轨道与其他碳原子或氢原子结合,形成σ键;
4、烷烃分子中的共价键全部是单键。
①烷烃的性质与甲烷的相似;
烷烃的所有原子不可能共平面。
②分子中的碳原子并非直线状排列,而是锯齿状。
一、烷烃的结构特点
σ键可旋转
CH3-CH2-CH2-CH3
CH2-CH2
CH3
│
CH3
│
CH3
│
CH3-CH2-CH2
以上三种结构简式都表示正丁烷
链状烷烃的分子式通式:CnH2n+2(n≥1)
①符合该通式的一定是链状烷烃。
②链状烷烃随着n的增加,含氢的质量分数越来越小。
一、烷烃的结构特点
同系物的判断规律:
同系物:结构相似、分子组成上相差一个或若干个_________原子团的化合物称为___________。同系物可用通式表示。
CH2
同系物
1、同通式,同类别(官能团种类、数目相同)
2、分子组成相差一个或若干个CH2原子团
注意:
(1)同系物间物理性质递变,但化学性质相似。
(2)同系物间通式一定相同,但通式相同,不一定是同系物。
例如:C3H6(环丙烷)和C4H8(丁烯)
一、烷烃的结构特点
烷烃名称 分子式 结构简式 常温下状态 熔点/℃ 沸点/℃ 密度/(g/cm3)
甲烷 CH4 CH4 气 -182 -164 0.423
乙烷 C2H6 CH3CH3 气 -172 -89 0.545
丙烷 C3H8 CH3CH2CH3 气 -187 -42 0.501
正丁烷 C4H10 CH3CH2CH2CH3 气 -138 -0.5 0.579
正戊烷 C5H12 CH3(CH2)3CH3 液 -129 36 0.626
正壬烷 C9H20 CH3(CH2)7CH3 液 -54 151 0.718
十一烷 C11H24 CH3(CH2)9CH3 液 -26 196 0.740
十六烷 C16H34 CH3(CH2)14CH3 液 18 280 0.775
十八烷 C18H38 CH3(CH2)16CH3 固 28 308 0.777
观察上表,分析烷烃的密度、熔点和沸点等物理性质变化的基本规律。
二、烷烃的物理性质
2、随着分子中碳原子数的递增,烷烃的相对分子质量增大,分子间作用力增强,烷烃的熔、沸点逐渐升高。
1、常温的状态:气→液→固
C1~C4:气态 C5~C16:液态 C17以上:固态
注意:新戊烷为气态
C数相同,支链越多,沸点越低。
3、所有烷烃均难溶于水,易溶于有机溶剂。
二、烷烃的物理性质
4、所有烷烃密度均小于1。碳原子数的增加,密度逐渐增大。
三、烷烃的化学性质
烷烃的结构决定了其性质与甲烷相似
知识回顾
甲烷的化学性质:
1、稳定性:常温下,不与____、_____、___________反应。
2、____反应(可燃性):______________________
3、____反应:_________________、_________________、
_________________、_________________、
4、高温分解:____________________
强酸 强碱 强氧化剂
CH4+Cl2 CH3Cl+HCl
光
CH3Cl+Cl2 CH2Cl2+HCl
光
CH2Cl2+Cl2 CHCl3+HCl
光
CHCl3+Cl2 CCl4+HCl
光
CH4 C + 2H2
高温
氧化
取代
若1mol甲烷中的H全部被Cl取代,需要多少molCl2?
4mol
若1mol 甲烷全部参加反应最多可以生成多少mol HCl?
4mol
01稳定性
常温下,烷烃很不活泼,与强酸、强碱、强氧化剂(如酸性KMnO4)、溴的四氯化碳溶液等都不发生反应
02氧化反应
烷烃燃烧的通式为
氧化反应||可燃性
(因为烷烃分子中化学键全是σ键,不易断裂)
三、烷烃的化学性质
现象:当碳含量少时,产生淡蓝色火焰,但随着碳原子数的增多,碳的质量分数逐渐增大,有黑烟产生
在常温、常压下,取下列四种气态烃各1 mol,分别在足量的氧气中燃烧,消耗氧气最多的是( ),取同质量的下列四种气态烃分别在足量的氧气中燃烧,消耗氧气最多的是 ( )
A.CH4 B.C3H8 C.C4H10 D.C2H6
C
A
分析:由C~O2~CO2, 4H~O2~2H2O进行比较,
消耗1mol O2,需要12g C,
而消耗1mol O2,需要4g H,
可知有机物含氢量越大,等质量时消耗的O2越多,以此进行比较。
规律:完全燃烧相同质量的烃时,消耗氧气的量随着碳原子数的
递增而减小。
03特征反应 — 取代反应
三、烷烃的化学性质
一氯乙烷
二氯乙烷
三氯乙烷
四氯乙烷
五氯乙烷
六氯乙烷
乙烷与氯气在光照下反应,可能生成哪些产物?请写出它们的结构简式。
可能的产物有:HCl + 9种有机产物
CH3CH2Cl
CH3CHCl2
CH2ClCH2Cl
CH3CCl3
CH2ClCHCl2
CH2ClCCl3
CHCl2CHCl2
CHCl2CCl3
CCl3CCl3
1种
2种
2种
2种
1种
1种
03特征反应 — 取代反应
三、烷烃的化学性质
(4)反应产物:混合物(多种卤代烃),不适宜制备卤代烃。
(3)反应的特点:氢原子被卤素原子逐步取代,多步反应同时进行。
(2)反应物状态:气态卤素单质(F2、Cl2、Br2、I2), 而不是其水溶液。
(1)反应的条件:光照。
04受热分解
长链烷烃高温隔绝氧气条件下可分解成短链烷烃和烯烃,这在石油化工上称为石油的裂化。
C16H34 C8H18+C8H16
催化剂
加热、加压
烷烃
烷烃
烯烃
C4H10 CH4+C3H6
催化剂
加热、加压
C4H10 C2H4+C2H6
催化剂
加热、加压
环烷烃
如:
环丙烷
C3H6
环丁烷C4H8
环戊烷
C5H10
环己烷C6H12
CnH2n(n≥3)
1、环烷烃分子式通式:
2、性质与烷烃相似:
常温下有稳定性,不能被酸性高锰酸钾溶液氧化而使其褪色,能燃烧氧化;能发生光照取代反应。
+
Cl2
光
+ HCl
Cl
1、下列有关烷烃的叙述中,正确的是( )
①在烷烃分子中,所有的化学键都是单键
②烷烃中除甲烷外,很多都能使酸性KMnO4溶液的紫色褪去
③分子通式为CnH2n+2的烃不一定是烷烃
④所有烷烃在光照条件都能与氯气发生取代反应
⑤光照条件下,乙烷通入溴水中,可使溴水褪色
⑥所有的烷烃都可以在空气中燃烧
A.①②③⑥ B.①④⑥ C.②③④ D.①②③④
B
(1)烷烃分子中的所有共价键全部是σ键。 ( )
(2)汽油、煤油、石蜡中的主要成分为烷烃。 ( )
(3)烷烃的化学性质稳定,不能发生氧化反应。 ( )
(4)乙烷的熔、沸点比丙烷的高。 ( )
(5)烷烃能使酸性KMnO4溶液褪色。 ( )
(6)制取1-氯乙烷时可用乙烷和氯气反应。( )
(7)丙烷分子中所有碳原子在一条直线上。( )
(8)光照条件下,1 mol Cl2与2 mol CH4充分反应后可得到
1 mol CH3Cl。( )
(9)标况下,11.2 L己烷所含共价键的数目为9.5NA。( )
2、正误判断
×
√
√
×
×
×
×
×
×
3、丁烷有两种不同结构,分别为正丁烷和异丁烷,均可用作制冷剂,下列关于丁烷的说法正确的是( )
A.异丁烷的沸点高于正丁烷的沸点
B.正丁烷和异丁烷中碳原子均不可能共平面
C.可以通过酸性KMnO4溶液鉴别正丁烷和异丁烷
D.丁烷的一氯取代物共有4种结构(不包含立体异构)
D
