化学人教版(2019)选择性必修3 3.4乙酸(共23张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 3.4乙酸(共23张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-21 00:00:00 | ||
图片预览






文档简介
(共23张PPT)
自然界中许多动植物中含有各种各样的羧酸物质,如蚂蚁体内含有的蚁酸、
柠檬中含有的柠檬酸、苹果中含有的苹果酸等成分。
蚁酸(甲酸)
HCOOH
柠檬酸
苹果酸
乙酸
人教版选择性必修3 第三章第三节醇醛羧酸及其衍生物
01
醛
羧酸
醇
01
复习导入
RCH2OH
RCOOH
RCHO
颜色、状态
无色液体
气 味
有强烈刺激性气味(可消毒)
沸 点
117.9℃ (易挥发)
熔 点
16.6℃ (无水乙酸又称为冰醋酸)
溶解性
易溶于水、乙醇等溶剂
乙酸的物理性质
你知道厨房中的醋是什么味吗?通过观察乙酸,阅读课本总
结乙酸的物理性质。
02
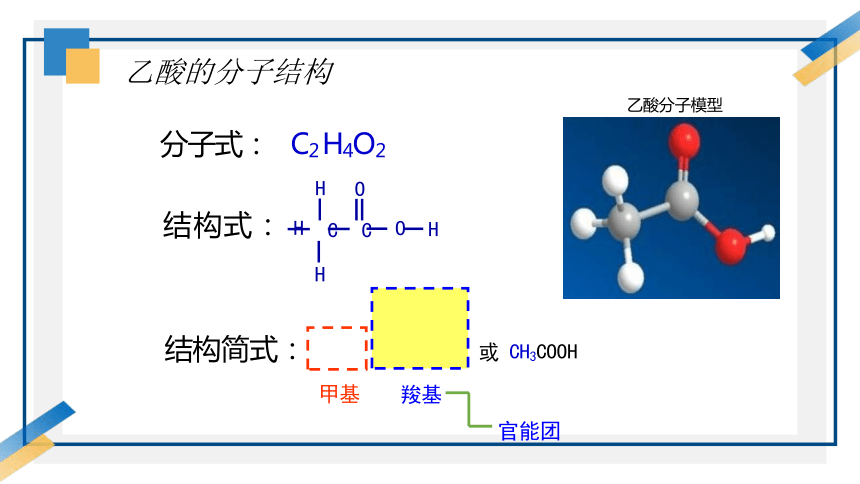
乙酸的分子结构
乙酸分子模型
分子式: C2 H4O2
H O
结构式: H C C O H
H
结构简式: 或 CH3COOH
甲基 羧基
官能团
通过这个生活常识你能得到什么启示?
水垢主要成份: Mg(OH)2和CaCO3
温故知新
初中学过酸的通性有哪些?
1、能够使酸碱指示剂变色
2、能够和活泼金属反应
3、能和某些盐反应
4、能和碱反应
5、能和碱性氧化物反应
03
探究· 证明乙酸的酸性的可行方案:
酸性: CH3COOH > H2CO3
04
“加点酒”
“ ”
为什么?
酒是陈的香
注意:不能伸到液面下(防倒吸)
②药品的添加顺序如何?
先加乙醇再加浓H2SO4最后加乙酸
③浓硫酸的作用是什么?
催化剂 吸水剂
①图中发生装置有何特点?为什么使用长 导管?导管口为什么要在溶液的液面上方
酯化反应原理分析
导管的作用:导气、冷疑
讨论:
?
⑤为什么要用饱和的碳酸钠溶液来吸收产品?
中和乙酸、溶解乙醇,降低乙酸乙酯 在水中的溶解度
几种物质的物理性质
④得到的产物是否纯净?主要杂质有哪些
含有乙醇、乙酸
?
概念:酸和醇反应生成酯和水的反应。
现象: 在饱和碳酸钠溶液上方有透明的不溶于水 的油状液体产生,并可以闻到香味。
CH3COOCH2CH3 + H2O
乙酸乙酯
酯化反应本质
CH3COOH + HOCH2CH3
可逆反应
浓H2SO4
△
乙酸
乙醇
思考·讨论
书本实验酯化反应有什么局限性?
通过实际操作实验我们发现书本学生实验采用浓硫酸 做催化剂进行实验,存在以下几个问题:
1、学生在使用浓硫酸的时候存在较多安全隐患
2、副反应较多且产生污染性气体。
思考·探究
如何改进酯化反应装置?
通过所学知识和查阅相关文献资料,发现酯化反应 所需温度在80℃左右,理论上在水浴条件下可以生成大 量的乙酸乙酯。沪科版教材在药品及用量均不变的情况 下,选择水浴加热。认为可以有效缓解溶液的炭化以及 副反应过多的问题。
验"# $%
&论
人教版(直接加热)
加热3min后振荡静置试 管内出现明显的分层现 象
沪科版(水浴加热) 结论: 针对沪科版实验装 10min 置改进问题,老师通过实际实验过程中
水浴加热10min后振荡 静置试管内的分层现象 不明显
发现,该实验耗时过多,一般
要 左右才会出现少许乙酸乙酯,并且试管内的分层现象也不明显,所以大部分课堂演示
实验教师还是会采用直接加热的方式来进行该实验。
思考·探究
如何改进酯化反应装置?
通过所学知识和查阅相关文献资料,发现酯化反 应起催化作用的主要是氢离子,由于酯化反应生成的 乙酸乙酯沸点低,加热条件下很容易从体系中分离, 所以大胆推测很多酸性试剂都可以做催化剂,但是这 种酸性试剂不能容易挥发,老师今天和同学们共同探 究一种新的催化剂 (FeCl3 ·6H2O)。
探究实验一
3ml乙醇, 2ml乙酸 (99.7%) ,
催化剂:
FeCl3 ·6H2O晶体
05 探究· 不同条件下三氯化铁催化酯化反应的效果
探究实验二
3ml乙醇, 2ml乙酸 (36%) ,
催化剂:
FeCl3 ·6H2O晶体
05 探究· 不同条件下三氯化铁催化酯化反应的效果
实验序号 实验现象
加热3min后振荡静置 收集到酯层高度/cm
(试管规格
15mm*100mm)
书本实验 生成乙酸乙酯,但同时伴随着副反应 的发生
1.1
探究实验一 生成乙酸乙酯,现象明显,但是略显 黄色
1.2
探究实验二 生成乙酸乙酯,现象明显
1.5
结论: 综合上述实验现象和数据,学生实验条件可以改进为探究实验二的
反应条件: 3ml乙醇, 2ml乙酸(36%),催化剂: FeCl3 ·6H2O晶体
实际探究对比得出酯化反应选择的最优条件:
选择这种催化剂:FeCl3 ·6H2O晶体
相比于书本使用的硫酸作为催化剂具有什么好处呢?
思考·讨论
三、乙酸的化学性质
1.乙酸的酸性: 乙酸是一种一元弱酸,其酸性大于碳酸
2.乙酸的酯化反应(取代)
一、羧酸的物理性质
二、羧酸的分子结构 结构简式:RCOOH
特征基团: —COOH(羧基)
06
板书设计
四、羧酸的用途
谢谢大家
自然界中许多动植物中含有各种各样的羧酸物质,如蚂蚁体内含有的蚁酸、
柠檬中含有的柠檬酸、苹果中含有的苹果酸等成分。
蚁酸(甲酸)
HCOOH
柠檬酸
苹果酸
乙酸
人教版选择性必修3 第三章第三节醇醛羧酸及其衍生物
01
醛
羧酸
醇
01
复习导入
RCH2OH
RCOOH
RCHO
颜色、状态
无色液体
气 味
有强烈刺激性气味(可消毒)
沸 点
117.9℃ (易挥发)
熔 点
16.6℃ (无水乙酸又称为冰醋酸)
溶解性
易溶于水、乙醇等溶剂
乙酸的物理性质
你知道厨房中的醋是什么味吗?通过观察乙酸,阅读课本总
结乙酸的物理性质。
02
乙酸的分子结构
乙酸分子模型
分子式: C2 H4O2
H O
结构式: H C C O H
H
结构简式: 或 CH3COOH
甲基 羧基
官能团
通过这个生活常识你能得到什么启示?
水垢主要成份: Mg(OH)2和CaCO3
温故知新
初中学过酸的通性有哪些?
1、能够使酸碱指示剂变色
2、能够和活泼金属反应
3、能和某些盐反应
4、能和碱反应
5、能和碱性氧化物反应
03
探究· 证明乙酸的酸性的可行方案:
酸性: CH3COOH > H2CO3
04
“加点酒”
“ ”
为什么?
酒是陈的香
注意:不能伸到液面下(防倒吸)
②药品的添加顺序如何?
先加乙醇再加浓H2SO4最后加乙酸
③浓硫酸的作用是什么?
催化剂 吸水剂
①图中发生装置有何特点?为什么使用长 导管?导管口为什么要在溶液的液面上方
酯化反应原理分析
导管的作用:导气、冷疑
讨论:
?
⑤为什么要用饱和的碳酸钠溶液来吸收产品?
中和乙酸、溶解乙醇,降低乙酸乙酯 在水中的溶解度
几种物质的物理性质
④得到的产物是否纯净?主要杂质有哪些
含有乙醇、乙酸
?
概念:酸和醇反应生成酯和水的反应。
现象: 在饱和碳酸钠溶液上方有透明的不溶于水 的油状液体产生,并可以闻到香味。
CH3COOCH2CH3 + H2O
乙酸乙酯
酯化反应本质
CH3COOH + HOCH2CH3
可逆反应
浓H2SO4
△
乙酸
乙醇
思考·讨论
书本实验酯化反应有什么局限性?
通过实际操作实验我们发现书本学生实验采用浓硫酸 做催化剂进行实验,存在以下几个问题:
1、学生在使用浓硫酸的时候存在较多安全隐患
2、副反应较多且产生污染性气体。
思考·探究
如何改进酯化反应装置?
通过所学知识和查阅相关文献资料,发现酯化反应 所需温度在80℃左右,理论上在水浴条件下可以生成大 量的乙酸乙酯。沪科版教材在药品及用量均不变的情况 下,选择水浴加热。认为可以有效缓解溶液的炭化以及 副反应过多的问题。
验"# $%
&论
人教版(直接加热)
加热3min后振荡静置试 管内出现明显的分层现 象
沪科版(水浴加热) 结论: 针对沪科版实验装 10min 置改进问题,老师通过实际实验过程中
水浴加热10min后振荡 静置试管内的分层现象 不明显
发现,该实验耗时过多,一般
要 左右才会出现少许乙酸乙酯,并且试管内的分层现象也不明显,所以大部分课堂演示
实验教师还是会采用直接加热的方式来进行该实验。
思考·探究
如何改进酯化反应装置?
通过所学知识和查阅相关文献资料,发现酯化反 应起催化作用的主要是氢离子,由于酯化反应生成的 乙酸乙酯沸点低,加热条件下很容易从体系中分离, 所以大胆推测很多酸性试剂都可以做催化剂,但是这 种酸性试剂不能容易挥发,老师今天和同学们共同探 究一种新的催化剂 (FeCl3 ·6H2O)。
探究实验一
3ml乙醇, 2ml乙酸 (99.7%) ,
催化剂:
FeCl3 ·6H2O晶体
05 探究· 不同条件下三氯化铁催化酯化反应的效果
探究实验二
3ml乙醇, 2ml乙酸 (36%) ,
催化剂:
FeCl3 ·6H2O晶体
05 探究· 不同条件下三氯化铁催化酯化反应的效果
实验序号 实验现象
加热3min后振荡静置 收集到酯层高度/cm
(试管规格
15mm*100mm)
书本实验 生成乙酸乙酯,但同时伴随着副反应 的发生
1.1
探究实验一 生成乙酸乙酯,现象明显,但是略显 黄色
1.2
探究实验二 生成乙酸乙酯,现象明显
1.5
结论: 综合上述实验现象和数据,学生实验条件可以改进为探究实验二的
反应条件: 3ml乙醇, 2ml乙酸(36%),催化剂: FeCl3 ·6H2O晶体
实际探究对比得出酯化反应选择的最优条件:
选择这种催化剂:FeCl3 ·6H2O晶体
相比于书本使用的硫酸作为催化剂具有什么好处呢?
思考·讨论
三、乙酸的化学性质
1.乙酸的酸性: 乙酸是一种一元弱酸,其酸性大于碳酸
2.乙酸的酯化反应(取代)
一、羧酸的物理性质
二、羧酸的分子结构 结构简式:RCOOH
特征基团: —COOH(羧基)
06
板书设计
四、羧酸的用途
谢谢大家
