3.2.2共价晶体课件(共20张PPT) 人教版(2019)选择性必修2
文档属性
| 名称 | 3.2.2共价晶体课件(共20张PPT) 人教版(2019)选择性必修2 |

|
|
| 格式 | pptx | ||
| 文件大小 | 13.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-21 00:00:00 | ||
图片预览







文档简介
(共20张PPT)
第二节 分子晶体与共价晶体
第2课时 共价晶体
新课导入
熔点/℃ 沸点/℃
-56.2 -78.5
熔点/℃ 沸点/℃
1723 2230
干冰(CO2)
二氧化硅(SiO2)
同为第四主族元素的氧化物,两种晶体的熔沸点却相差很大,这是为什么呢?
分子晶体
共价晶体
学习目标
1.知道共价晶体的结构特点,能借助共价晶体模型说明共价晶体中粒子间的相互作用。
2.能结合具体实例,说出共价晶体的粒子间与其性质(熔点、硬度等)的关系。
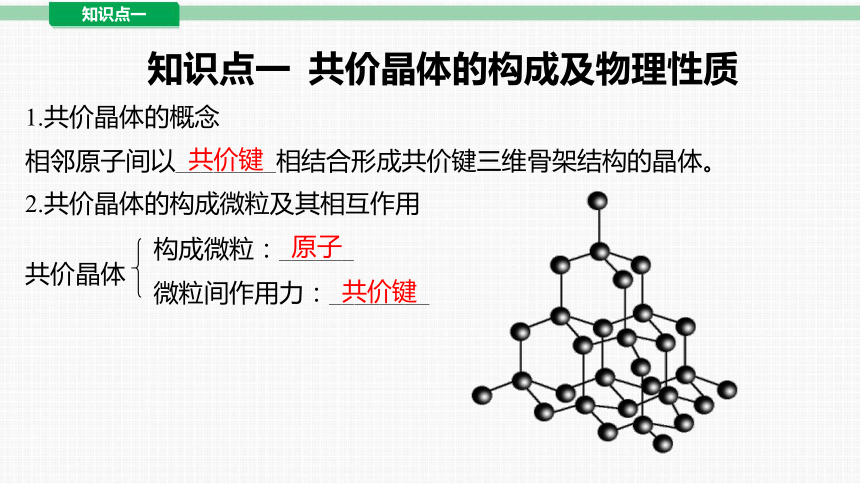
1.共价晶体的概念
相邻原子间以________相结合形成共价键三维骨架结构的晶体。
2.共价晶体的构成微粒及其相互作用
构成微粒:______
微粒间作用力:________
共价键
原子
共价键
共价晶体
知识点一 共价晶体的构成及物理性质
3.共价晶体的物理性质
(1)共价晶体中,各原子均以共价键相结合,因此一般地,共价晶体的
熔点____,硬度____。
(2)结构相似的共价晶体,原子半径越小,键长越____,键能越____,
晶体的熔点越____。
(3)难溶于一般溶剂。
高
大
短
大
高
4.常见的共价晶体
物质类别 实例
某些单质 金刚石 、硅 、硼 、锗 、灰锡
某些非金属氧化物 二氧化硅
某些化合物 碳化硅( ,俗称金刚砂)、氮化硅 、氮化硼 等
极少数金属氧化物 Al2O3(刚玉)
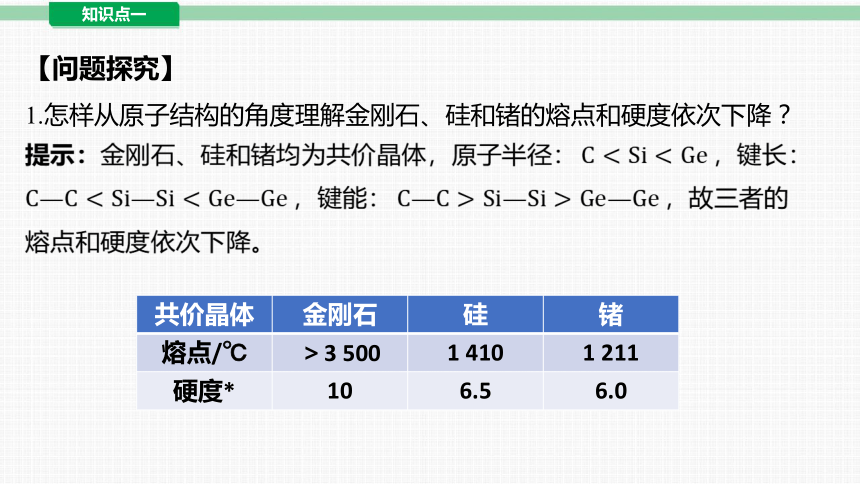
【问题探究】
1.怎样从原子结构的角度理解金刚石、硅和锗的熔点和硬度依次下降?
提示:金刚石、硅和锗均为共价晶体,原子半径: ,键长:
,键能: ,故三者的
熔点和硬度依次下降。
共价晶体 金刚石 硅 锗
熔点/℃ >3 500 1 410 1 211
硬度* 10 6.5 6.0
2.根据下列物质的物理性质,你能判断出下列晶体的类型吗?
(1) 与金属 形成的 的熔点为 ,沸点为 。
(2)碳化铝,黄色晶体,熔点为 ,熔融态不导电。
(3)溴化铝,无色晶体,熔点为 ,熔融态不导电。
(4)硼,熔点为 ,沸点为 ,硬度大。
(5)氮化碳 的硬度比金刚石还大,不溶于水,也不导电。
提示:(1)分子晶体。(2)共价晶体。(3)分子晶体。
(4)共价晶体。(5)共价晶体。
共价晶体和分子晶体的判断方法
(1)依据构成晶体的粒子和粒子间的作用力判断
构成共价晶体的粒子是原子,粒子间的作用力是共价键;构成分子晶体的
粒子是分子,粒子间的作用力是分子间作用力。
(2)依据晶体的熔点判断
共价晶体的熔点高,常在 以上;而分子晶体的熔点低,常在数百
摄氏度以下,甚至更低。
(3)依据晶体的导电性判断
共价晶体多数为绝缘体,但晶体 、晶体 为半导体;分子晶体为绝缘
体,但部分分子晶体溶于水后能导电,如 晶体。
(4)依据晶体的硬度和机械性能判断
共价晶体的硬度大,机械强度高;分子晶体的硬度小且较脆。
1.金刚石
(1)在金刚石晶体中,每个碳原子以4个共价单键对称地与相邻的4个碳
原子结合, 夹角为________,即金刚石中的碳采取____杂化轨
道形成共价键三维骨架结构。
知识点二 典型共价晶体的结构特征
12
(2)晶体中最小的碳环由___个碳原子构成,且不在同一平面内,最多有
___个碳原子在同一平面。
(3)每个 占有___个C,每个C
形成4个 ,即C原子与 个数
之比为_____。
(4)每个C原子被____个六元环共用,
1个碳环平均占有的碳原子有_____个。
6
4
0.5
2
2.二氧化硅
(1)二氧化硅晶体
①1个 原子和__个 原子形成__个键,每个 原子和__个 原子结合。
4
4
2
② 中含___ 。
③最小环由___个 原子和___个 原子构成。
4
6
6
④每个 原子被____个十二元环共用,每个 原子被___个十二元环共用。
12
6
(2)低温石英
在低温石英的结构中,顶角相连的____________形成螺旋上升的长链,这
一结构决定了它具有______(左、右型),被广泛用作压电材料,如制作
石英手表。
硅氧四面体
手性
课后小结
3.金刚石的晶胞结构如图所示,回答下列问题。
(1)一个金刚石晶胞中含有___个碳原子。
8
(2)已知晶胞参数为 ,则金刚石的密度为
__________
(3)晶体中两个最邻近的碳原子之间的距离为_ ____ 。
(4)若碳原子的半径为 ,则 、 的关系表达式为_ _______ 。
谢谢观看
第二节 分子晶体与共价晶体
第2课时 共价晶体
新课导入
熔点/℃ 沸点/℃
-56.2 -78.5
熔点/℃ 沸点/℃
1723 2230
干冰(CO2)
二氧化硅(SiO2)
同为第四主族元素的氧化物,两种晶体的熔沸点却相差很大,这是为什么呢?
分子晶体
共价晶体
学习目标
1.知道共价晶体的结构特点,能借助共价晶体模型说明共价晶体中粒子间的相互作用。
2.能结合具体实例,说出共价晶体的粒子间与其性质(熔点、硬度等)的关系。
1.共价晶体的概念
相邻原子间以________相结合形成共价键三维骨架结构的晶体。
2.共价晶体的构成微粒及其相互作用
构成微粒:______
微粒间作用力:________
共价键
原子
共价键
共价晶体
知识点一 共价晶体的构成及物理性质
3.共价晶体的物理性质
(1)共价晶体中,各原子均以共价键相结合,因此一般地,共价晶体的
熔点____,硬度____。
(2)结构相似的共价晶体,原子半径越小,键长越____,键能越____,
晶体的熔点越____。
(3)难溶于一般溶剂。
高
大
短
大
高
4.常见的共价晶体
物质类别 实例
某些单质 金刚石 、硅 、硼 、锗 、灰锡
某些非金属氧化物 二氧化硅
某些化合物 碳化硅( ,俗称金刚砂)、氮化硅 、氮化硼 等
极少数金属氧化物 Al2O3(刚玉)
【问题探究】
1.怎样从原子结构的角度理解金刚石、硅和锗的熔点和硬度依次下降?
提示:金刚石、硅和锗均为共价晶体,原子半径: ,键长:
,键能: ,故三者的
熔点和硬度依次下降。
共价晶体 金刚石 硅 锗
熔点/℃ >3 500 1 410 1 211
硬度* 10 6.5 6.0
2.根据下列物质的物理性质,你能判断出下列晶体的类型吗?
(1) 与金属 形成的 的熔点为 ,沸点为 。
(2)碳化铝,黄色晶体,熔点为 ,熔融态不导电。
(3)溴化铝,无色晶体,熔点为 ,熔融态不导电。
(4)硼,熔点为 ,沸点为 ,硬度大。
(5)氮化碳 的硬度比金刚石还大,不溶于水,也不导电。
提示:(1)分子晶体。(2)共价晶体。(3)分子晶体。
(4)共价晶体。(5)共价晶体。
共价晶体和分子晶体的判断方法
(1)依据构成晶体的粒子和粒子间的作用力判断
构成共价晶体的粒子是原子,粒子间的作用力是共价键;构成分子晶体的
粒子是分子,粒子间的作用力是分子间作用力。
(2)依据晶体的熔点判断
共价晶体的熔点高,常在 以上;而分子晶体的熔点低,常在数百
摄氏度以下,甚至更低。
(3)依据晶体的导电性判断
共价晶体多数为绝缘体,但晶体 、晶体 为半导体;分子晶体为绝缘
体,但部分分子晶体溶于水后能导电,如 晶体。
(4)依据晶体的硬度和机械性能判断
共价晶体的硬度大,机械强度高;分子晶体的硬度小且较脆。
1.金刚石
(1)在金刚石晶体中,每个碳原子以4个共价单键对称地与相邻的4个碳
原子结合, 夹角为________,即金刚石中的碳采取____杂化轨
道形成共价键三维骨架结构。
知识点二 典型共价晶体的结构特征
12
(2)晶体中最小的碳环由___个碳原子构成,且不在同一平面内,最多有
___个碳原子在同一平面。
(3)每个 占有___个C,每个C
形成4个 ,即C原子与 个数
之比为_____。
(4)每个C原子被____个六元环共用,
1个碳环平均占有的碳原子有_____个。
6
4
0.5
2
2.二氧化硅
(1)二氧化硅晶体
①1个 原子和__个 原子形成__个键,每个 原子和__个 原子结合。
4
4
2
② 中含___ 。
③最小环由___个 原子和___个 原子构成。
4
6
6
④每个 原子被____个十二元环共用,每个 原子被___个十二元环共用。
12
6
(2)低温石英
在低温石英的结构中,顶角相连的____________形成螺旋上升的长链,这
一结构决定了它具有______(左、右型),被广泛用作压电材料,如制作
石英手表。
硅氧四面体
手性
课后小结
3.金刚石的晶胞结构如图所示,回答下列问题。
(1)一个金刚石晶胞中含有___个碳原子。
8
(2)已知晶胞参数为 ,则金刚石的密度为
__________
(3)晶体中两个最邻近的碳原子之间的距离为_ ____ 。
(4)若碳原子的半径为 ,则 、 的关系表达式为_ _______ 。
谢谢观看
