2023-2024学年科粤版九年级化学上册第二章《空气、物质的构成》单元测试卷3(含解析)
文档属性
| 名称 | 2023-2024学年科粤版九年级化学上册第二章《空气、物质的构成》单元测试卷3(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 242.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-21 00:00:00 | ||
图片预览




文档简介
第二章《空气、物质的构成》测试卷
一、选择题(共16题)
1.下列物质中,属于纯净物的是( )
A.井水 B.硬铝 C.沼气 D.纯碱
2.下列关于稀有气体的叙述中,错误的是( )
A.空气中稀有气体含量虽少,但却包含了氦;氖;氩、氪、氙等多种气体
B.因为稀有气体化学性质很不活泼,所以很难与其它物质发生化学反应
C.稀有气体不仅可作保护气,还可以填充气球代替氢气球
D.稀有气体充入灯泡内,不仅能使灯泡经久耐用,而且还能发出不同颜色的光
3.下列物质中,属于纯净物的是( )
A.食用醋 B.酒精 C.精制碘盐 D.“雪碧”可乐
4.下列各组物质,均属于纯净物的是( )
A.大理石、氨气、高锰酸钾 B.干冰、液氧、冰水混合物
C.石灰水、牛奶、石墨 D.过氧化氢溶液、空气、娃哈哈纯净水
5.镓的化合物用于半导体、太阳能电池等多种领域,有“电子工业脊梁”的美誉。镓在元素周期表中的信息见图。下列说法错误的是( )
A.镓属于金属元素 B.镓的原子序数是31
C.镓原子中的质子数为31 D.镓的相对原子质量是69.72g
6.把分别充满红棕色NO2气体和无色N2的集气瓶,按照图A、B两种方式放置,然后把中间的玻璃片抽走,使两瓶口密合在一起(不振荡)可观察到A中两瓶气体颜色很快稳于一致(两种气体不反应),而B中需很长时间才能达到同样效果。不能由此现象直接得出的结论是( )
A.分子之间有间隙 B.分子在不断地运动
C.分子由原子构成 D.NO2气体的密度比N2大
7.根据下列三种微粒结构示意图,所获取信息不正确的是( )
A.它们表示两种元素 B.②③化学性质相同
C.①表示的是原子,②表示的是阳离子 D.②表示的元素是金属元素
8.根据分子的相关性质解释下列现象,其中正确的是( )
A.食物腐败—分子停止运动 B.闻到花香—分子间有间隔
C.水结冰—分子变成了原子 D.湿衣服在阳光下干得快—温度高,分子运动快
9.下列化学符号既表示一种元素,又表示一个原子,同时还表示一种物质的是 。
A.H2 B.O C.NO D.C
10.根据下列各组元素的原子结构示意图分析:具有相似化学性质的一组是( )
A. B.
C. D.
11.根据下列原子结构示意图判断,化学性质最稳定的是( )
A. B. C. D.
12.居里夫人在1898年从几吨的含铀废料中提炼出0.3g镭。已知镭元素的核电荷数为88,相对原子质量为226,则镭原子的核内中子数为( )
A.226 B.88 C.138 D.31
13.对以下四种微粒的结构示意图,分析错误的是( )
A.①②属于同一种微粒 B.①④的化学性质相似
C.①得到电子可形成② D.②③表示不同种离子
14.逻辑推理是一种重要的化学思维方法,以下说法中正确的是( )
A.分子和原子都不带电,所以不带电的微粒都是分子和原子
B.H2O和的H2O2的分子构成不同,所以它们的化学性质不同
C.原子是化学变化中的最小粒子,所以原子任何情况下不能再分
D.O2-、Na+、Mg2+、Cl-的最外层电子数均为8,所以离子最外层电子数均为8
15.下列物质都属于纯净物的是( )
A.液氧、石灰水 B.臭氧、糖水 C.双氧水、水 D.二氧化碳、冰水混合物
16.下列关于空气的说法不正确的是( )
A.炼钢、气焊、航空航天都要用到氧气
B.超导材料在液氮的低温环境下能显示超导性能
C.广告灯的灯管中充入氖气,发出红光
D.空气中二氧化碳含量过高会引起温室效应,二氧化碳属于空气污染物
二、综合题(共8题)
17.“酒香不怕巷子深”蕴含着什么化学道理?用所学过的知识解释_______.
18.从分子的角度分析并解释下列问题。
(1)墙内开花墙外可闻到花香_____。
(2)混合物与纯净物有什么不同______
19.在元素周期表中有关氧元素、铝元素的信息如图中甲乙所示,丙丁为两种粒子的结构示意图。
请回答下列问题:
(1)铝元素的原子序数为___________。
(2)铝离子的结构示意图是___________(丙或丁);
(3)氧元素与铝元素最本质的区别是___________(填序号);
A.中子数不同 B.质子数不同 C.相对原子质量不同 D.电子数不同
20.核电荷数为1-18的元素的原子结构示意图等信息如图,回答下列问题
(1)锂原子的核电荷数为______.
(2)请画出16号元素原子结构示意图____________,在化学反应中该原子比较容易______填“得”或“失”电子,该元素属于_____填“金属”或“非金属”元素.
(3)在第三周期中,各原子核外电子排布的变化规律是 .
(4)写出核外电子排布与氖原子相同的阳离子符号:____________答案不唯一,合理即可.
21.在化学学习中运用适当的方法可以起到事半功倍的效果。请回答下列问题:
(1)下列是一些粒子结构示意图,请按照一定的标准将其平均分为两类。
其中的—个分类标准是①__________,包含微粒为②___________(填字母);
(2)将数据进行图表化总结,是化学学习中经常用到的方法。如图所示,三种方法各有优势:
图1 一些国家的人均水量 图2 地壳运动的元素含量 图3 生物细胞中的元素组成
请你模仿图1和图2,将图3表格所表示的内容在答题卡分别以柱状图和饼状图的形式大略地呈现出来__________ 。
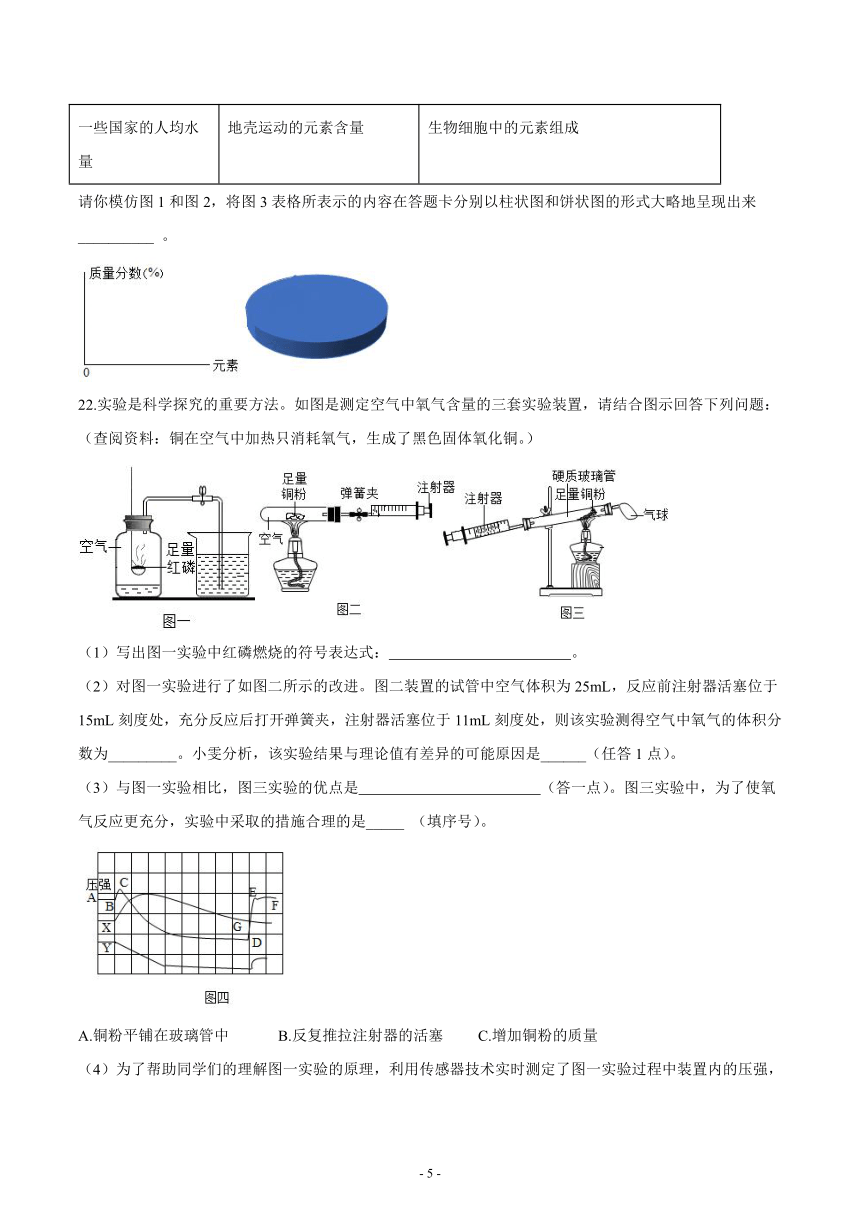
22.实验是科学探究的重要方法。如图是测定空气中氧气含量的三套实验装置,请结合图示回答下列问题:(查阅资料:铜在空气中加热只消耗氧气,生成了黑色固体氧化铜。)
(1)写出图一实验中红磷燃烧的符号表达式: 。
(2)对图一实验进行了如图二所示的改进。图二装置的试管中空气体积为25mL,反应前注射器活塞位于15mL刻度处,充分反应后打开弹簧夹,注射器活塞位于11mL刻度处,则该实验测得空气中氧气的体积分数为_________。小雯分析,该实验结果与理论值有差异的可能原因是______(任答1点)。
(3)与图一实验相比,图三实验的优点是 (答一点)。图三实验中,为了使氧气反应更充分,实验中采取的措施合理的是_____ (填序号)。
A.铜粉平铺在玻璃管中 B.反复推拉注射器的活塞 C.增加铜粉的质量
(4)为了帮助同学们的理解图一实验的原理,利用传感器技术实时测定了图一实验过程中装置内的压强,温度和氧气浓度,三条曲线变化趋势如图四所示。试回答:
①其中Y曲线表示的是_________(填“温度”或“氧气浓度”)。
②结合X,Y两条曲线,解释图四中BC段压强变化的原因是 。
23.在宏观、微观和符号之间建立联系是化学学科的重要思维方式。
(1)如图1所示,X是___________________________________________;Y是___________________________________________。
(2)从宏观角度看,汞由________________________________________组成;从微观角度看,汞由__________________________________________构成。
(3)图2是钙元素的原子结构示意图,下列结构示意图中,共有__________________________(填数字)种元素,其中与钙原子具有相似化学性质的是__________________________(填字母)。
24.在宏观、微观和符号之间建立联系是化学学科的特点。
(一)化学是在分子、原子层次上研究物质的科学。根据下图提供的信息,回答下列问题:
(1)A图表示原子其中X的值是______。
(2)化学性质相似的原子是____________(填字母序号,下同)。
(3)具有稳定结构的原子_______________。
(4)C、D中___________________相同,属于同种元素。
(二)下图是某物质发生反应的微观示意图。
(5)丙图中所示物质都是由________________构成的(选填“分子”“ 原子”或“离子”);
(6)结合上图分析,化学变化中的最小的粒子是_____________________;
(7)甲图中一个分子是由________个原子构成
(8)该反应的符号表达式是________________,属于_________反应(基本反应类型)。
参考答案
1.D
【解析】A、井水中含有水和溶于水的物质,属于混合物,故错误;B、硬铝是铝合金,主要成分是铝,还含有一些其它物质,属于混合物,故错误;C、沼气主要成分是甲烷,还含有一些杂质,属于混合物,故错误;D、纯碱是碳酸钠的俗称,是由一种物质组成的,属于纯净物,故正确。故选D。
2.C
【详解】
A、空气中稀有气体含量虽少,但却包含了氦;氖;氩、氪、氙等多种气体,故A说法正确;
B、稀有气体化学性质很不活泼,所以不易与其它物质发生化学反应,在一定条件下可以与其他物质反应,故B说法正确;
C、稀有气体中的氦气的密度比空气小,所以可以用于填充探空气球,故C说法错误;
D、稀有气体充入灯泡内,不仅能使灯泡经久耐用,而且还能发出不同颜色的光,做多种电光源,故D说法正确。
故选C。
3.B
【详解】
A、食用醋中含有水、醋酸等物质,是混合物,不符合题意;
B、酒精中只含一种物质,是纯净物,符合题意;
C、精制碘盐中含有食盐和碘酸钾,是混合物,不符合题意;
D、雪碧可乐中含有水、碳酸等物质,是混合物,不符合题意。
故选B。
4.B
【详解】
A、大理石的主要成分是碳酸钙,还含有其它物质,属于混合物;氨气和高锰酸钾中都只含有一种物质,属于纯净物,选项不符合题意;
B、干冰是二氧化碳的固态、液氧是液态的氧气、冰水混合物中都只含有一种物质,属于纯净物,选项符合题意;
C、石灰水中含有氢氧化钙和水,属于混合物;牛奶中含有水和蛋白质等,属于混合物;石墨中只含有一种物质,属于纯净物,选项不符合题意;
D、过氧化氢溶液中含有过氧化氢和水,属于混合物;空气中含有氮气、氧气等物质,属于混合物;娃哈哈纯净水中含有水和可溶性物质,属于混合物,选项不符合题意。
故选B。
5.D
【详解】
A、镓属于金属元素,该选项说法正确;
B、元素周期表一格中右上角数字表示原子序数,图中31表示镓的原子序数是31,该选项说法正确;
C、镓原子中的质子数为31,该选项说法正确;
D、镓的相对原子质量是69.72,单位不是g,该选项说法不正确。
故选:D。
6.C
【详解】
实验A中两瓶气体颜色很快趋于一致,而B中需很长时间才能达到同样效果;说明分子之间有间隙、分子在不断地运动、并且 NO2 气体的密度比N2 大;该实验是一个物理变化,不能说明分子由原子构成。
故选C。
7.B
【详解】
A、由三种微粒结构示意图,其核内质子数分别是7、13、13,表示两种元素,故选项说法正确。
B、元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,②③的最外层电子数不同,化学性质不相同,故选项说法错误。
C、①质子数=核外电子数=7,为原子;②质子数=13,核外电子数=10,质子数>核外电子数,为阳离子;故选项说法正确。
D、②的核内质子数为13,为铝元素,属于金属元素,故选项说法正确。
故选:B。
8.D
【详解】
A、食物腐烂,有新物质生成,属于化学变化,分子本身发生了改变,选项A错误。
B、闻到花香,因为花香中的分子是在不断运动的,向四周扩散,使人们闻到花香,选项B错误。
C、水结冰,属于物理变化,分子本身没有发生改变,选项C错误。
D、湿衣服在阳光下干得快,是因为温度升高,分子运动的速率加快,选项D正确。
故选:D。
9.D
【详解】
A、H2该符号是氢气的化学式,表示氢气这种物质和一个氢气分子,不能表示一种元素,故选项不符合题意。
B、O可表示氧元素,表示一个氧原子,但不能表示一种物质,故选项不符合题意。
C、NO该符号是一氧化氮的化学式,表示一氧化氮这种物质和一个一氧化氮分子,不能表示一种元素,故选项不符合题意。
D、C属于固体非金属元素,可表示碳元素,表示一个碳原子,还能表示碳这一物质,故选项符合题意。
故选:D。
10.A
【详解】
决定元素化学性质的是原子结构中的最外层电子数,原子的最外层电子数相同,具有相似的化学性质。
A、前者中原子的最外层电子数为2,但其核外只有一个电子层,属于稀有气体元素的原子,化学性质稳定;后者的最外层电子数为8,属于稀有气体元素的原子,化学性质稳定;它们的化学性质相似,故选项正确。
B、两者的最外层电子数分别为7、1,原子的最外层电子数不同,化学性质不相似,故选项错误。
C、前者中原子的最外层电子数为2,但其核外只有一个电子层,属于稀有气体元素的原子,化学性质稳定;后者原子的最外层电子数为2,在发生化学反应时易失去2个电子形成阳离子;两者的最外层电子数相同,但化学性质不相似,故选项错误。
D、前者的最外层电子数为8,质子数为12,是镁离子,化学性质稳定;后者最外层电子数为6;原子的最外层电子数不同,化学性质不相似,故选项错误。
故选:A。
11.C
【详解】
选C。元素的性质与原子最外层上的电子数目密切相关,最外层电子数是8的属于稳定结构。
12.C
13.A
【详解】
A、①②的质子数都是8,核外电子数不同,属于同一种元素,故A错误;B、由于元素的化学性质与其最外层电子数关系密切,而①④最外层电子数相同,故两者化学性质相似,故B正确;C、①最外层电子数是6,得2个电子可形成②,故C正确;D、②③的质子数不同,核内质子数都不等于核外电子数,表示不同种离子,故D正确。故选A。
14.B
【详解】
A、分子和原子都不带电,但不带电的微粒除了分子、原子还可以是中子等,错误;
B、水是由水分子构成的,过氧化氢是由过氧化氢分子构成的,分子的构成不同,化学性质不同,正确;
C、原子在化学变化中不可分,不在化学变化中,原子可分为原子核和电子,错误;
D、离子如锂离子,最外层电子数为2,不是8,错误;
故选B。
15.D
【详解】
A、液氧是纯净物,石灰水含有氢氧化钙和水是混合物,不符合题意;
B、臭氧是纯净物,糖水含有蔗糖和水是混合物,不符合题意;
C、双氧水是水和过氧化氢的混合物,水是纯净物,不符合题意;
D、二氧化碳、冰水混合物都是纯净物,符合题意;
故选:D
16.D
【详解】
A、炼钢、气焊、航空航天都要用到氧气,A正确。
B、超导材料在液氮的低温环境下能显示超导性能,B正确。
C、稀有气体通电发出特俗颜色的光,广告灯的灯管中充入氖气,发出红光,C正确。
D、空气中二氧化碳含量过高会引起温室效应,但是二氧化碳不属于空气污染物,D错误。
故选:D。
17.分子在不断运动
【详解】
由于分子在不断运动,构成酒精的分子在断运动,所以在远处能闻到酒香。
18.分子在不停地运动 混合物中有多种分子,纯净物中只有一种分子
【详解】
(1)墙内开花墙外可闻到花香是因为分子在不停地运动。
(2)混合物是由两种或两种以上的分子构成,纯净物是由一种分子构成。
19.(1)13(2)丁(3)B
【分析】
元素周期表中,方格中左上角是原子序数,右上角是元素符号,中间是元素名称,下面是相对原子质量;
原子中,核电荷数=核内质子数=核外电子数=原子序数
除汞外,金属元素的名称都带金字旁,非金属元素的名称不带金字旁:
相对原子质量质子数+中子数,单位不是g。
(1)
由图可知,铝元素的原子序数为13。
(2)
铝离子的结构示意图是丁,因为核内质子数为13,核外电子数为10,质子数不等于电子数的是离子,相等的是原子。
(3)
元素是质子数相同的一类原子的总称,故氧元素与铝元素最本质的区别是质子数不同。
故选:B
3 得 非金属 原子核外电子层数相同,最外层电子数依次增加(合理即可) Na+ 或Mg2+或Al3+(答案不唯一,合理即可)
【详解】
(1)锂是3号元素,锂原子的核电荷数为3;
(2)根据原子结构示意图的画法画出硫原子的结构示意图为,它属于非金属,最外层有6个电子,易得到两个成为8电子稳定结构;
(3)在第三周期中,各原子结构的共同之处是原子核外电子层数相同;该周期中,从左到右,各原子核外电子排布的变化规律是最外层电子数依次增加;
(4)核外电子排布与氖原子相同的阳离子可能是钠离子或镁离子以及铝离子;
答案:
(1)14
(2);得; 非金属;
(3)原子核外电子层数相同,最外层电子数依次增加;
(4)Na+。
21.化学性质相似(或元素周期表中同一纵行元素)的原子 b、c
【详解】
(1) 其中的—个分类标准是化学性质相似(或元素周期表中同一纵行元素)的原子,最外层电子数相同,元素的化学性质相似,故包含微粒为b、c;(2) 图3表格所表示的内容以柱状图和饼状图的形式大略地表示为: 。
22.(1)(2) 16% 红磷不足,装置漏气,没有冷却至室温就打开弹簧夹等
(3)更环保或结果更准确等 AB (4)氧气浓度 氧气减少压强减小,温度升高压强增大,温度升高导致压强增大大于氧气减少导致的压强减小
【分析】
(1)红磷燃烧生成五氧化二磷,反应的符合表达式为:;
(2)该实验测得空气中氧气的体积分数为:;小明分析,该实验结果偏小原因可能是:红磷不足(未能完全消耗氧气),装置漏气(有空气进入装置导致进入水的体积偏少),没有冷却至室温就打开弹簧夹(气体膨胀进入水的体积偏少)等;
(3)与图一实验相比,图三实验的优点是:防止了燃烧匙伸入集气瓶中时导致的部分气体受热膨胀逸出,实验结果更准确,同时防止了反应生成的五氧化二磷扩散到空气中污染环境;
图三实验中,为了使氧气反应更充分,实验中采取的措施合理的是:A.铜粉平铺在玻璃管中,以增大反应物接触面积,使反应更充分,正确;
B. 反复推拉注射器的活塞,使反应物充分接触,反应更充分,正确;
C. 增加铜粉的质量不能使反应更充分,错误,故选:AB;
(4)①其中Y曲线表示的是氧气浓度,这是因为随着反应进行,氧气浓度减小,符合Y曲线;
②图三中BC段压强变化的原因是:氧气减少压强减小,温度升高压强增大,温度升高导致压强增大大于氧气减少导致的压强减小。
23.原子 原子核 汞元素 汞原子 3 B
【详解】(1)构成物质的微粒有分子、原子、离子,所以X是原子;原子由原子核和核外电子构成,所以Y为原子核。
(2)物质由元素组成,汞是由汞元素组成的单质;汞由汞原子直接构成。
(3)元素的种类由该元素原子中质子数决定,图中A、B、C3种粒子的质子数各不相同,所以共有3种元素。
元素的化学性质由原子核外最外层电子数决定。钙原子的最外层电子数为2,化学反应中容易失去2个电子。A为氦原子的结构示意图,最外层虽然也有2个电子,但它是第一层,是一种相对稳定结构,B中最外层(第三层)上有2个电子,与钙原子化学性质相似。故选B。
9 AC B 质子数 。 分子 氢原子、氧原子 ; 4 , 分解 。
【详解】(1)A是原子,所以X=2+7=9;
(2)A和C最外层电子数相同,都是7,所以二者的化学性质相似;
(3)B原子的最外层电子数是8,所以其结构比较稳定;
(4)质子数相同的原子是同种元素,C和D的质子数都是17,所以是同种元素;
(5)由微观示意图可知,丙图中有氧分子和水分子;
(6)化学变化中的最小微粒是原子;
(7)由图可知,甲图中一个分子由2个氢原子和2个氧原子构成,共4个原子;
(8)该反应的表达式是,反应由一种物质反应生成两种新物质,所以是分解反应。
一、选择题(共16题)
1.下列物质中,属于纯净物的是( )
A.井水 B.硬铝 C.沼气 D.纯碱
2.下列关于稀有气体的叙述中,错误的是( )
A.空气中稀有气体含量虽少,但却包含了氦;氖;氩、氪、氙等多种气体
B.因为稀有气体化学性质很不活泼,所以很难与其它物质发生化学反应
C.稀有气体不仅可作保护气,还可以填充气球代替氢气球
D.稀有气体充入灯泡内,不仅能使灯泡经久耐用,而且还能发出不同颜色的光
3.下列物质中,属于纯净物的是( )
A.食用醋 B.酒精 C.精制碘盐 D.“雪碧”可乐
4.下列各组物质,均属于纯净物的是( )
A.大理石、氨气、高锰酸钾 B.干冰、液氧、冰水混合物
C.石灰水、牛奶、石墨 D.过氧化氢溶液、空气、娃哈哈纯净水
5.镓的化合物用于半导体、太阳能电池等多种领域,有“电子工业脊梁”的美誉。镓在元素周期表中的信息见图。下列说法错误的是( )
A.镓属于金属元素 B.镓的原子序数是31
C.镓原子中的质子数为31 D.镓的相对原子质量是69.72g
6.把分别充满红棕色NO2气体和无色N2的集气瓶,按照图A、B两种方式放置,然后把中间的玻璃片抽走,使两瓶口密合在一起(不振荡)可观察到A中两瓶气体颜色很快稳于一致(两种气体不反应),而B中需很长时间才能达到同样效果。不能由此现象直接得出的结论是( )
A.分子之间有间隙 B.分子在不断地运动
C.分子由原子构成 D.NO2气体的密度比N2大
7.根据下列三种微粒结构示意图,所获取信息不正确的是( )
A.它们表示两种元素 B.②③化学性质相同
C.①表示的是原子,②表示的是阳离子 D.②表示的元素是金属元素
8.根据分子的相关性质解释下列现象,其中正确的是( )
A.食物腐败—分子停止运动 B.闻到花香—分子间有间隔
C.水结冰—分子变成了原子 D.湿衣服在阳光下干得快—温度高,分子运动快
9.下列化学符号既表示一种元素,又表示一个原子,同时还表示一种物质的是 。
A.H2 B.O C.NO D.C
10.根据下列各组元素的原子结构示意图分析:具有相似化学性质的一组是( )
A. B.
C. D.
11.根据下列原子结构示意图判断,化学性质最稳定的是( )
A. B. C. D.
12.居里夫人在1898年从几吨的含铀废料中提炼出0.3g镭。已知镭元素的核电荷数为88,相对原子质量为226,则镭原子的核内中子数为( )
A.226 B.88 C.138 D.31
13.对以下四种微粒的结构示意图,分析错误的是( )
A.①②属于同一种微粒 B.①④的化学性质相似
C.①得到电子可形成② D.②③表示不同种离子
14.逻辑推理是一种重要的化学思维方法,以下说法中正确的是( )
A.分子和原子都不带电,所以不带电的微粒都是分子和原子
B.H2O和的H2O2的分子构成不同,所以它们的化学性质不同
C.原子是化学变化中的最小粒子,所以原子任何情况下不能再分
D.O2-、Na+、Mg2+、Cl-的最外层电子数均为8,所以离子最外层电子数均为8
15.下列物质都属于纯净物的是( )
A.液氧、石灰水 B.臭氧、糖水 C.双氧水、水 D.二氧化碳、冰水混合物
16.下列关于空气的说法不正确的是( )
A.炼钢、气焊、航空航天都要用到氧气
B.超导材料在液氮的低温环境下能显示超导性能
C.广告灯的灯管中充入氖气,发出红光
D.空气中二氧化碳含量过高会引起温室效应,二氧化碳属于空气污染物
二、综合题(共8题)
17.“酒香不怕巷子深”蕴含着什么化学道理?用所学过的知识解释_______.
18.从分子的角度分析并解释下列问题。
(1)墙内开花墙外可闻到花香_____。
(2)混合物与纯净物有什么不同______
19.在元素周期表中有关氧元素、铝元素的信息如图中甲乙所示,丙丁为两种粒子的结构示意图。
请回答下列问题:
(1)铝元素的原子序数为___________。
(2)铝离子的结构示意图是___________(丙或丁);
(3)氧元素与铝元素最本质的区别是___________(填序号);
A.中子数不同 B.质子数不同 C.相对原子质量不同 D.电子数不同
20.核电荷数为1-18的元素的原子结构示意图等信息如图,回答下列问题
(1)锂原子的核电荷数为______.
(2)请画出16号元素原子结构示意图____________,在化学反应中该原子比较容易______填“得”或“失”电子,该元素属于_____填“金属”或“非金属”元素.
(3)在第三周期中,各原子核外电子排布的变化规律是 .
(4)写出核外电子排布与氖原子相同的阳离子符号:____________答案不唯一,合理即可.
21.在化学学习中运用适当的方法可以起到事半功倍的效果。请回答下列问题:
(1)下列是一些粒子结构示意图,请按照一定的标准将其平均分为两类。
其中的—个分类标准是①__________,包含微粒为②___________(填字母);
(2)将数据进行图表化总结,是化学学习中经常用到的方法。如图所示,三种方法各有优势:
图1 一些国家的人均水量 图2 地壳运动的元素含量 图3 生物细胞中的元素组成
请你模仿图1和图2,将图3表格所表示的内容在答题卡分别以柱状图和饼状图的形式大略地呈现出来__________ 。
22.实验是科学探究的重要方法。如图是测定空气中氧气含量的三套实验装置,请结合图示回答下列问题:(查阅资料:铜在空气中加热只消耗氧气,生成了黑色固体氧化铜。)
(1)写出图一实验中红磷燃烧的符号表达式: 。
(2)对图一实验进行了如图二所示的改进。图二装置的试管中空气体积为25mL,反应前注射器活塞位于15mL刻度处,充分反应后打开弹簧夹,注射器活塞位于11mL刻度处,则该实验测得空气中氧气的体积分数为_________。小雯分析,该实验结果与理论值有差异的可能原因是______(任答1点)。
(3)与图一实验相比,图三实验的优点是 (答一点)。图三实验中,为了使氧气反应更充分,实验中采取的措施合理的是_____ (填序号)。
A.铜粉平铺在玻璃管中 B.反复推拉注射器的活塞 C.增加铜粉的质量
(4)为了帮助同学们的理解图一实验的原理,利用传感器技术实时测定了图一实验过程中装置内的压强,温度和氧气浓度,三条曲线变化趋势如图四所示。试回答:
①其中Y曲线表示的是_________(填“温度”或“氧气浓度”)。
②结合X,Y两条曲线,解释图四中BC段压强变化的原因是 。
23.在宏观、微观和符号之间建立联系是化学学科的重要思维方式。
(1)如图1所示,X是___________________________________________;Y是___________________________________________。
(2)从宏观角度看,汞由________________________________________组成;从微观角度看,汞由__________________________________________构成。
(3)图2是钙元素的原子结构示意图,下列结构示意图中,共有__________________________(填数字)种元素,其中与钙原子具有相似化学性质的是__________________________(填字母)。
24.在宏观、微观和符号之间建立联系是化学学科的特点。
(一)化学是在分子、原子层次上研究物质的科学。根据下图提供的信息,回答下列问题:
(1)A图表示原子其中X的值是______。
(2)化学性质相似的原子是____________(填字母序号,下同)。
(3)具有稳定结构的原子_______________。
(4)C、D中___________________相同,属于同种元素。
(二)下图是某物质发生反应的微观示意图。
(5)丙图中所示物质都是由________________构成的(选填“分子”“ 原子”或“离子”);
(6)结合上图分析,化学变化中的最小的粒子是_____________________;
(7)甲图中一个分子是由________个原子构成
(8)该反应的符号表达式是________________,属于_________反应(基本反应类型)。
参考答案
1.D
【解析】A、井水中含有水和溶于水的物质,属于混合物,故错误;B、硬铝是铝合金,主要成分是铝,还含有一些其它物质,属于混合物,故错误;C、沼气主要成分是甲烷,还含有一些杂质,属于混合物,故错误;D、纯碱是碳酸钠的俗称,是由一种物质组成的,属于纯净物,故正确。故选D。
2.C
【详解】
A、空气中稀有气体含量虽少,但却包含了氦;氖;氩、氪、氙等多种气体,故A说法正确;
B、稀有气体化学性质很不活泼,所以不易与其它物质发生化学反应,在一定条件下可以与其他物质反应,故B说法正确;
C、稀有气体中的氦气的密度比空气小,所以可以用于填充探空气球,故C说法错误;
D、稀有气体充入灯泡内,不仅能使灯泡经久耐用,而且还能发出不同颜色的光,做多种电光源,故D说法正确。
故选C。
3.B
【详解】
A、食用醋中含有水、醋酸等物质,是混合物,不符合题意;
B、酒精中只含一种物质,是纯净物,符合题意;
C、精制碘盐中含有食盐和碘酸钾,是混合物,不符合题意;
D、雪碧可乐中含有水、碳酸等物质,是混合物,不符合题意。
故选B。
4.B
【详解】
A、大理石的主要成分是碳酸钙,还含有其它物质,属于混合物;氨气和高锰酸钾中都只含有一种物质,属于纯净物,选项不符合题意;
B、干冰是二氧化碳的固态、液氧是液态的氧气、冰水混合物中都只含有一种物质,属于纯净物,选项符合题意;
C、石灰水中含有氢氧化钙和水,属于混合物;牛奶中含有水和蛋白质等,属于混合物;石墨中只含有一种物质,属于纯净物,选项不符合题意;
D、过氧化氢溶液中含有过氧化氢和水,属于混合物;空气中含有氮气、氧气等物质,属于混合物;娃哈哈纯净水中含有水和可溶性物质,属于混合物,选项不符合题意。
故选B。
5.D
【详解】
A、镓属于金属元素,该选项说法正确;
B、元素周期表一格中右上角数字表示原子序数,图中31表示镓的原子序数是31,该选项说法正确;
C、镓原子中的质子数为31,该选项说法正确;
D、镓的相对原子质量是69.72,单位不是g,该选项说法不正确。
故选:D。
6.C
【详解】
实验A中两瓶气体颜色很快趋于一致,而B中需很长时间才能达到同样效果;说明分子之间有间隙、分子在不断地运动、并且 NO2 气体的密度比N2 大;该实验是一个物理变化,不能说明分子由原子构成。
故选C。
7.B
【详解】
A、由三种微粒结构示意图,其核内质子数分别是7、13、13,表示两种元素,故选项说法正确。
B、元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,②③的最外层电子数不同,化学性质不相同,故选项说法错误。
C、①质子数=核外电子数=7,为原子;②质子数=13,核外电子数=10,质子数>核外电子数,为阳离子;故选项说法正确。
D、②的核内质子数为13,为铝元素,属于金属元素,故选项说法正确。
故选:B。
8.D
【详解】
A、食物腐烂,有新物质生成,属于化学变化,分子本身发生了改变,选项A错误。
B、闻到花香,因为花香中的分子是在不断运动的,向四周扩散,使人们闻到花香,选项B错误。
C、水结冰,属于物理变化,分子本身没有发生改变,选项C错误。
D、湿衣服在阳光下干得快,是因为温度升高,分子运动的速率加快,选项D正确。
故选:D。
9.D
【详解】
A、H2该符号是氢气的化学式,表示氢气这种物质和一个氢气分子,不能表示一种元素,故选项不符合题意。
B、O可表示氧元素,表示一个氧原子,但不能表示一种物质,故选项不符合题意。
C、NO该符号是一氧化氮的化学式,表示一氧化氮这种物质和一个一氧化氮分子,不能表示一种元素,故选项不符合题意。
D、C属于固体非金属元素,可表示碳元素,表示一个碳原子,还能表示碳这一物质,故选项符合题意。
故选:D。
10.A
【详解】
决定元素化学性质的是原子结构中的最外层电子数,原子的最外层电子数相同,具有相似的化学性质。
A、前者中原子的最外层电子数为2,但其核外只有一个电子层,属于稀有气体元素的原子,化学性质稳定;后者的最外层电子数为8,属于稀有气体元素的原子,化学性质稳定;它们的化学性质相似,故选项正确。
B、两者的最外层电子数分别为7、1,原子的最外层电子数不同,化学性质不相似,故选项错误。
C、前者中原子的最外层电子数为2,但其核外只有一个电子层,属于稀有气体元素的原子,化学性质稳定;后者原子的最外层电子数为2,在发生化学反应时易失去2个电子形成阳离子;两者的最外层电子数相同,但化学性质不相似,故选项错误。
D、前者的最外层电子数为8,质子数为12,是镁离子,化学性质稳定;后者最外层电子数为6;原子的最外层电子数不同,化学性质不相似,故选项错误。
故选:A。
11.C
【详解】
选C。元素的性质与原子最外层上的电子数目密切相关,最外层电子数是8的属于稳定结构。
12.C
13.A
【详解】
A、①②的质子数都是8,核外电子数不同,属于同一种元素,故A错误;B、由于元素的化学性质与其最外层电子数关系密切,而①④最外层电子数相同,故两者化学性质相似,故B正确;C、①最外层电子数是6,得2个电子可形成②,故C正确;D、②③的质子数不同,核内质子数都不等于核外电子数,表示不同种离子,故D正确。故选A。
14.B
【详解】
A、分子和原子都不带电,但不带电的微粒除了分子、原子还可以是中子等,错误;
B、水是由水分子构成的,过氧化氢是由过氧化氢分子构成的,分子的构成不同,化学性质不同,正确;
C、原子在化学变化中不可分,不在化学变化中,原子可分为原子核和电子,错误;
D、离子如锂离子,最外层电子数为2,不是8,错误;
故选B。
15.D
【详解】
A、液氧是纯净物,石灰水含有氢氧化钙和水是混合物,不符合题意;
B、臭氧是纯净物,糖水含有蔗糖和水是混合物,不符合题意;
C、双氧水是水和过氧化氢的混合物,水是纯净物,不符合题意;
D、二氧化碳、冰水混合物都是纯净物,符合题意;
故选:D
16.D
【详解】
A、炼钢、气焊、航空航天都要用到氧气,A正确。
B、超导材料在液氮的低温环境下能显示超导性能,B正确。
C、稀有气体通电发出特俗颜色的光,广告灯的灯管中充入氖气,发出红光,C正确。
D、空气中二氧化碳含量过高会引起温室效应,但是二氧化碳不属于空气污染物,D错误。
故选:D。
17.分子在不断运动
【详解】
由于分子在不断运动,构成酒精的分子在断运动,所以在远处能闻到酒香。
18.分子在不停地运动 混合物中有多种分子,纯净物中只有一种分子
【详解】
(1)墙内开花墙外可闻到花香是因为分子在不停地运动。
(2)混合物是由两种或两种以上的分子构成,纯净物是由一种分子构成。
19.(1)13(2)丁(3)B
【分析】
元素周期表中,方格中左上角是原子序数,右上角是元素符号,中间是元素名称,下面是相对原子质量;
原子中,核电荷数=核内质子数=核外电子数=原子序数
除汞外,金属元素的名称都带金字旁,非金属元素的名称不带金字旁:
相对原子质量质子数+中子数,单位不是g。
(1)
由图可知,铝元素的原子序数为13。
(2)
铝离子的结构示意图是丁,因为核内质子数为13,核外电子数为10,质子数不等于电子数的是离子,相等的是原子。
(3)
元素是质子数相同的一类原子的总称,故氧元素与铝元素最本质的区别是质子数不同。
故选:B
3 得 非金属 原子核外电子层数相同,最外层电子数依次增加(合理即可) Na+ 或Mg2+或Al3+(答案不唯一,合理即可)
【详解】
(1)锂是3号元素,锂原子的核电荷数为3;
(2)根据原子结构示意图的画法画出硫原子的结构示意图为,它属于非金属,最外层有6个电子,易得到两个成为8电子稳定结构;
(3)在第三周期中,各原子结构的共同之处是原子核外电子层数相同;该周期中,从左到右,各原子核外电子排布的变化规律是最外层电子数依次增加;
(4)核外电子排布与氖原子相同的阳离子可能是钠离子或镁离子以及铝离子;
答案:
(1)14
(2);得; 非金属;
(3)原子核外电子层数相同,最外层电子数依次增加;
(4)Na+。
21.化学性质相似(或元素周期表中同一纵行元素)的原子 b、c
【详解】
(1) 其中的—个分类标准是化学性质相似(或元素周期表中同一纵行元素)的原子,最外层电子数相同,元素的化学性质相似,故包含微粒为b、c;(2) 图3表格所表示的内容以柱状图和饼状图的形式大略地表示为: 。
22.(1)(2) 16% 红磷不足,装置漏气,没有冷却至室温就打开弹簧夹等
(3)更环保或结果更准确等 AB (4)氧气浓度 氧气减少压强减小,温度升高压强增大,温度升高导致压强增大大于氧气减少导致的压强减小
【分析】
(1)红磷燃烧生成五氧化二磷,反应的符合表达式为:;
(2)该实验测得空气中氧气的体积分数为:;小明分析,该实验结果偏小原因可能是:红磷不足(未能完全消耗氧气),装置漏气(有空气进入装置导致进入水的体积偏少),没有冷却至室温就打开弹簧夹(气体膨胀进入水的体积偏少)等;
(3)与图一实验相比,图三实验的优点是:防止了燃烧匙伸入集气瓶中时导致的部分气体受热膨胀逸出,实验结果更准确,同时防止了反应生成的五氧化二磷扩散到空气中污染环境;
图三实验中,为了使氧气反应更充分,实验中采取的措施合理的是:A.铜粉平铺在玻璃管中,以增大反应物接触面积,使反应更充分,正确;
B. 反复推拉注射器的活塞,使反应物充分接触,反应更充分,正确;
C. 增加铜粉的质量不能使反应更充分,错误,故选:AB;
(4)①其中Y曲线表示的是氧气浓度,这是因为随着反应进行,氧气浓度减小,符合Y曲线;
②图三中BC段压强变化的原因是:氧气减少压强减小,温度升高压强增大,温度升高导致压强增大大于氧气减少导致的压强减小。
23.原子 原子核 汞元素 汞原子 3 B
【详解】(1)构成物质的微粒有分子、原子、离子,所以X是原子;原子由原子核和核外电子构成,所以Y为原子核。
(2)物质由元素组成,汞是由汞元素组成的单质;汞由汞原子直接构成。
(3)元素的种类由该元素原子中质子数决定,图中A、B、C3种粒子的质子数各不相同,所以共有3种元素。
元素的化学性质由原子核外最外层电子数决定。钙原子的最外层电子数为2,化学反应中容易失去2个电子。A为氦原子的结构示意图,最外层虽然也有2个电子,但它是第一层,是一种相对稳定结构,B中最外层(第三层)上有2个电子,与钙原子化学性质相似。故选B。
9 AC B 质子数 。 分子 氢原子、氧原子 ; 4 , 分解 。
【详解】(1)A是原子,所以X=2+7=9;
(2)A和C最外层电子数相同,都是7,所以二者的化学性质相似;
(3)B原子的最外层电子数是8,所以其结构比较稳定;
(4)质子数相同的原子是同种元素,C和D的质子数都是17,所以是同种元素;
(5)由微观示意图可知,丙图中有氧分子和水分子;
(6)化学变化中的最小微粒是原子;
(7)由图可知,甲图中一个分子由2个氢原子和2个氧原子构成,共4个原子;
(8)该反应的表达式是,反应由一种物质反应生成两种新物质,所以是分解反应。
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
