5.1化学反应中的质量守恒课件(共17张PPT内嵌视频)---2023--2024学年九年级化学鲁教版上册
文档属性
| 名称 | 5.1化学反应中的质量守恒课件(共17张PPT内嵌视频)---2023--2024学年九年级化学鲁教版上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 49.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-23 00:00:00 | ||
图片预览






文档简介
(共17张PPT)
化学反应中的质量守恒
化学鲁教版 九年级上
课堂练习
新知讲解
新知导入
木炭燃烧
铁钉生锈
树木生长
葡萄酿酒
化学反应过程中,反应物和生成物的质量是否改变?
课堂练习
新知讲解
新知导入
过氧化氢分解了,分子变了,质量当然也就变了?
质量怎么会变呢?在化学反应中,分子虽然变了,但是原子没有改变,质量应该不变吧?
课堂练习
新知讲解
活动天地
如何用微观图解的形式表示该反应过程?
思考
这个反应前后都有哪些分子和原子?
01
02
课堂练习
新知讲解
活动天地
用图示表示过氧化氢分解生成水和氧气的反应。你认为哪个图示是正确的?为什么?
1.你选择了___,为什么做出这样的选择?
2.根据你的选择,请推测在化学反应前后,物质的总质量会发生怎样的变化?
(丙)
不变
课堂练习
实验探究
现在要做实验来验证自己的推测是否正确,有哪些问题必须思考呢?
1.容易发生的反应
2.如何测定反应前后质量
3.需要哪些仪器,药品
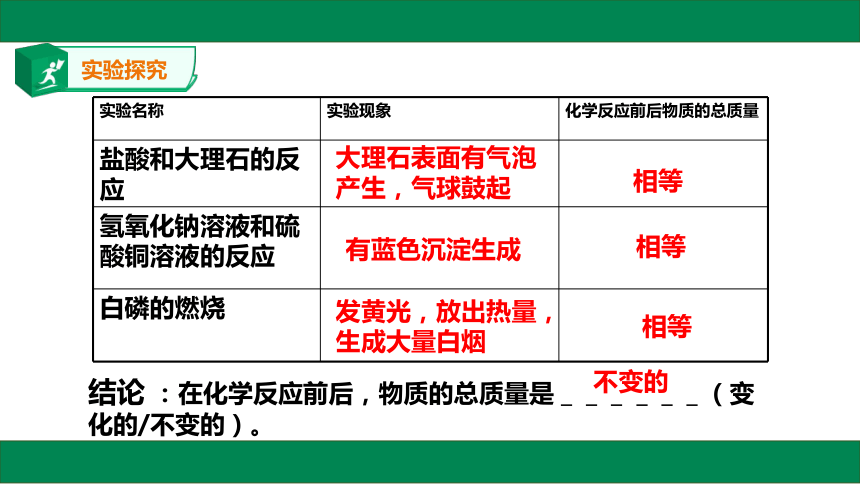
结论 :在化学反应前后,物质的总质量是______(变化的/不变的)。
实验名称 实验现象 化学反应前后物质的总质量
盐酸和大理石的反应
氢氧化钠溶液和硫酸铜溶液的反应
白磷的燃烧
大理石表面有气泡产生,气球鼓起
有蓝色沉淀生成
发黄光,放出热量,生成大量白烟
相等
相等
相等
不变的
课堂练习
实验探究
课堂练习
活动探究
1.在稀盐酸和大理石的反应中,如果锥形瓶上方位套有气球,天平会保持平衡吗?为什么?
不会,稀盐酸和大理石反应产生的气体逸出,天平指针向砝码一侧倾斜。
2.若果装置气密性良好,操作无误差,但发现反应后,天平指针仍旧向砝码一侧倾斜,可能的原因是什么?
气球变大,受到空气的浮力增大。
质量守恒定律
定义:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。
注意事项
1.指的是实际参与反应的各物质的质量。
2.所有化学反应都符合质量守恒定律。
3.强调质量的关系而不是其他的物理量。
课堂练习
新知讲解
复习回顾
课堂练习
课堂练习
讨论
说法一
10 g过氧化氢溶液完全分解后所得液体的质量小于10 g,所以在该实验中生成物质量减少。
说法二
镁条完全燃烧后生成物的质量大于反应前镁条的质量,所以在该实验中生成物质量增加。
以上两种说法正确吗?
不正确。因为参加反应的过氧化氢的质量,应该等于生成的水的质量和氧气的质量之和,题中漏掉了生成的氧气。
不正确。因为参加反应的镁条的质量和氧气的质量之和,应该等于生成的氧化镁的质量,题中漏掉了参加反应的氧气。
课堂练习
新知讲解
复习回顾
课堂练习
课堂练习
讨论
已知3 g碳可以与8 g氧气恰好完全反应,生成11 g二氧化碳。请你考虑:将3 g碳放在10 g氧气中充分燃烧后,能生成多少克二氧化碳?
生成11g二氧化碳。因为3 g碳可以与8 g氧气恰好完全反应,题中给出的10g氧气会剩余2g,而计算时只计算参加反应的物质之和,故仍为11g。
化学反应过程
六个不改变
两个一定改变
一个可能改变:分子总数可能改变
宏观
微观
反应物和生成物的总质量不变
元素种类不变
元素质量不变
原子种类不变
原子数目不变
原子质量不变
宏观:物质的种类一定改变
微观:分子的种类一定改变
课堂练习
新知讲解
复习回顾
课堂练习
课堂练习
1、化学反应前后一定没有发生变化的是______________________
①原子数目②原子种类 ③分子种类④物质总质量⑤物质种类 ⑥元素种类
2、动物脂肪通过呼吸作用生成二氧化碳和水,反应产生的热量是维持生命活动的能量,则动物脂肪中一定含有_________元素,可能含有____元素.
① ② ④ ⑥
碳、氢
氧
课堂练习
新知讲解
复习回顾
课堂练习
课堂练习
3、下列说法,你认为是否遵守质量守恒定律
A.打开盛酒精的瓶盖,酒精质量变小.( )
B.镁带燃烧后,固体的质量增加.( )
C.碳在氧气中燃烧后,产生的CO2的质量比参加反应的碳的质量大 ( )
D.蜡烛燃烧后,其质量变小. ( )
是
是
是
否
化学反应中的质量守恒
化学鲁教版 九年级上
课堂练习
新知讲解
新知导入
木炭燃烧
铁钉生锈
树木生长
葡萄酿酒
化学反应过程中,反应物和生成物的质量是否改变?
课堂练习
新知讲解
新知导入
过氧化氢分解了,分子变了,质量当然也就变了?
质量怎么会变呢?在化学反应中,分子虽然变了,但是原子没有改变,质量应该不变吧?
课堂练习
新知讲解
活动天地
如何用微观图解的形式表示该反应过程?
思考
这个反应前后都有哪些分子和原子?
01
02
课堂练习
新知讲解
活动天地
用图示表示过氧化氢分解生成水和氧气的反应。你认为哪个图示是正确的?为什么?
1.你选择了___,为什么做出这样的选择?
2.根据你的选择,请推测在化学反应前后,物质的总质量会发生怎样的变化?
(丙)
不变
课堂练习
实验探究
现在要做实验来验证自己的推测是否正确,有哪些问题必须思考呢?
1.容易发生的反应
2.如何测定反应前后质量
3.需要哪些仪器,药品
结论 :在化学反应前后,物质的总质量是______(变化的/不变的)。
实验名称 实验现象 化学反应前后物质的总质量
盐酸和大理石的反应
氢氧化钠溶液和硫酸铜溶液的反应
白磷的燃烧
大理石表面有气泡产生,气球鼓起
有蓝色沉淀生成
发黄光,放出热量,生成大量白烟
相等
相等
相等
不变的
课堂练习
实验探究
课堂练习
活动探究
1.在稀盐酸和大理石的反应中,如果锥形瓶上方位套有气球,天平会保持平衡吗?为什么?
不会,稀盐酸和大理石反应产生的气体逸出,天平指针向砝码一侧倾斜。
2.若果装置气密性良好,操作无误差,但发现反应后,天平指针仍旧向砝码一侧倾斜,可能的原因是什么?
气球变大,受到空气的浮力增大。
质量守恒定律
定义:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。
注意事项
1.指的是实际参与反应的各物质的质量。
2.所有化学反应都符合质量守恒定律。
3.强调质量的关系而不是其他的物理量。
课堂练习
新知讲解
复习回顾
课堂练习
课堂练习
讨论
说法一
10 g过氧化氢溶液完全分解后所得液体的质量小于10 g,所以在该实验中生成物质量减少。
说法二
镁条完全燃烧后生成物的质量大于反应前镁条的质量,所以在该实验中生成物质量增加。
以上两种说法正确吗?
不正确。因为参加反应的过氧化氢的质量,应该等于生成的水的质量和氧气的质量之和,题中漏掉了生成的氧气。
不正确。因为参加反应的镁条的质量和氧气的质量之和,应该等于生成的氧化镁的质量,题中漏掉了参加反应的氧气。
课堂练习
新知讲解
复习回顾
课堂练习
课堂练习
讨论
已知3 g碳可以与8 g氧气恰好完全反应,生成11 g二氧化碳。请你考虑:将3 g碳放在10 g氧气中充分燃烧后,能生成多少克二氧化碳?
生成11g二氧化碳。因为3 g碳可以与8 g氧气恰好完全反应,题中给出的10g氧气会剩余2g,而计算时只计算参加反应的物质之和,故仍为11g。
化学反应过程
六个不改变
两个一定改变
一个可能改变:分子总数可能改变
宏观
微观
反应物和生成物的总质量不变
元素种类不变
元素质量不变
原子种类不变
原子数目不变
原子质量不变
宏观:物质的种类一定改变
微观:分子的种类一定改变
课堂练习
新知讲解
复习回顾
课堂练习
课堂练习
1、化学反应前后一定没有发生变化的是______________________
①原子数目②原子种类 ③分子种类④物质总质量⑤物质种类 ⑥元素种类
2、动物脂肪通过呼吸作用生成二氧化碳和水,反应产生的热量是维持生命活动的能量,则动物脂肪中一定含有_________元素,可能含有____元素.
① ② ④ ⑥
碳、氢
氧
课堂练习
新知讲解
复习回顾
课堂练习
课堂练习
3、下列说法,你认为是否遵守质量守恒定律
A.打开盛酒精的瓶盖,酒精质量变小.( )
B.镁带燃烧后,固体的质量增加.( )
C.碳在氧气中燃烧后,产生的CO2的质量比参加反应的碳的质量大 ( )
D.蜡烛燃烧后,其质量变小. ( )
是
是
是
否
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
