2024福建中考一轮复习 人教版化学 教材基础复习 板块一 主题1 空气和氧气(共61张PPT)
文档属性
| 名称 | 2024福建中考一轮复习 人教版化学 教材基础复习 板块一 主题1 空气和氧气(共61张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 931.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-21 00:00:00 | ||
图片预览










文档简介
(共61张PPT)
教材基础复习篇
板块一 身边的化学物质
主题1 空气和氧气
知识清单·理脉络
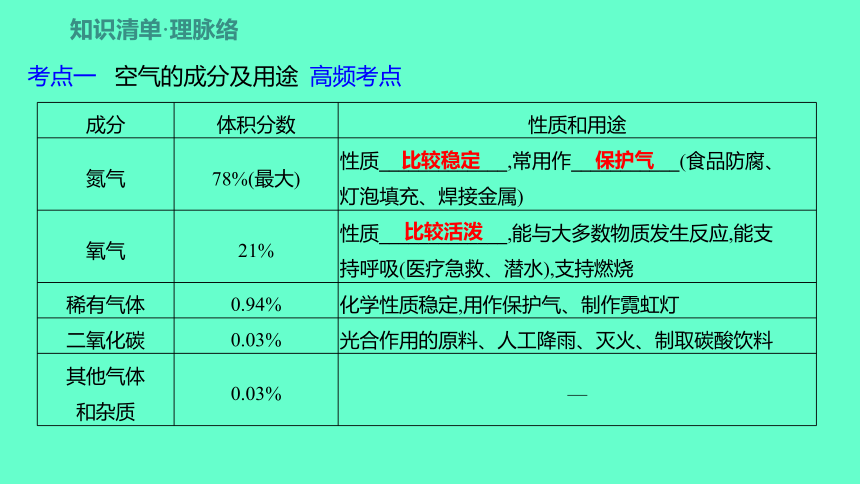
考点一 空气的成分及用途 高频考点
成分 体积分数 性质和用途
氮气 78%(最大) 性质_____________,常用作___________(食品防腐、
灯泡填充、焊接金属)
氧气 21% 性质_____________,能与大多数物质发生反应,能支
持呼吸(医疗急救、潜水),支持燃烧
稀有气体 0.94% 化学性质稳定,用作保护气、制作霓虹灯
二氧化碳 0.03% 光合作用的原料、人工降雨、灭火、制取碳酸饮料
其他气体 和杂质 0.03% —
比较稳定
保护气
比较活泼
考点二 空气的污染及防治
1.空气污染物:
【微点拨】CO2不属于空气污染物。
2.空气污染的来源及防治措施:
污染来源 防治措施
化石燃料的燃烧 改变能源结构,开发新能源
工业废气 工业废气处理达标后排放,减少有害物质的排放
植被被破坏引起的沙尘 植树、造林、种草等,提高空气的自净能力
考点三 氧气的性质
1.物理性质:
溶解性:不易溶于水;密度:比空气略大;
状态变化:降温时,变为淡蓝色液体和淡蓝色雪花状固体。
2.化学性质:
(1)氧气的助燃性。
带火星的木条在氧气中能够_________,说明氧气支持燃烧,常利用此性质来检验
某气体是否为氧气。
【微点拨】氧气虽然具有助燃性,但本身不能燃烧,不能用作燃料。
复燃
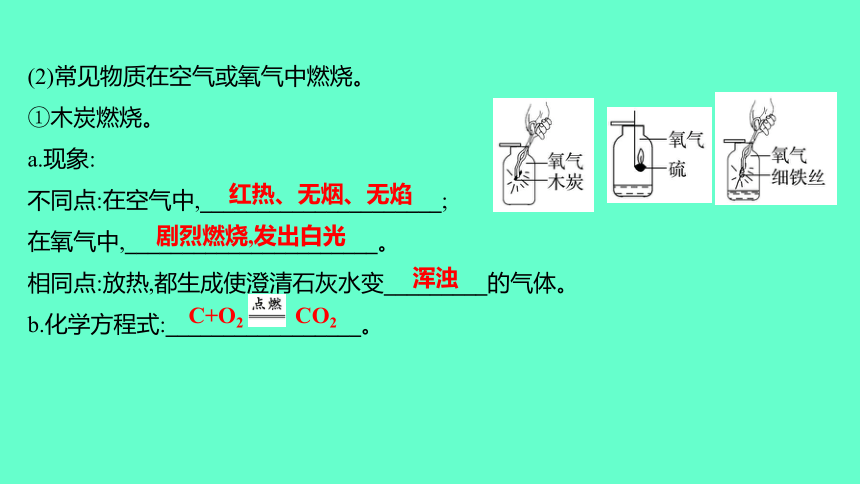
(2)常见物质在空气或氧气中燃烧。
①木炭燃烧。
a.现象:
不同点:在空气中,_____________________;
在氧气中,______________________。
相同点:放热,都生成使澄清石灰水变_________的气体。
b.化学方程式:_________________。
红热、无烟、无焰
剧烈燃烧,发出白光
浑浊
C+O2 CO2
②硫燃烧
a.不同点:在空气中发出_______________,在氧气中发出___________________。
相同点:_________________________________。
b.化学方程式:__________________。
③铁的燃烧。
a.现象:
不同点:在空气中,__________________________;在氧气中,____________________
_______________。
b.化学方程式:_______________________。
淡蓝色火焰
放热、生成一种刺激性气味气体
S+O2 SO2
发生红热现象,不能燃烧
剧烈燃烧,火星四射,
生成黑色固体
3Fe+2O2 Fe3O4
明亮蓝紫色火焰
【微点拨】硫粉在氧气中燃烧时,集气瓶瓶底放少量水或氢氧化钠溶液,目的是吸收二氧化硫,防止污染空气;做铁丝燃烧实验前,要预先在集气瓶中放少量水或铺一层细沙,目的是防止熔融物溅落下来炸裂瓶底。
④其他常见可燃物在空气或氧气中燃烧。
物质 现象 化学方程式
红磷 在空气中和氧气中燃烧都产生大量白烟、 放热 _____________________
镁条 发出_________的白光,生成_______色固体、 大量放热 ______________________
氢气 在氧气中燃烧,___________________, 火焰上方罩着的干冷烧杯内壁出现水雾、 放热 _____________________
4P+5O2 2P2O5
耀眼
白
2Mg+O2 2MgO
产生淡蓝色火焰
2H2+O2 2H2O
物质 现象 化学方程式
一氧 化碳 在空气或氧气中燃烧,发出_______________, 放热,生成能使澄清石灰水变浑浊的气体 _____________________
甲烷 在空气中燃烧,发出_______________, 火焰上方的烧杯中_______________, 取下烧杯正放,加入澄清石灰水振荡, 石灰水____________ ______________________
淡蓝色火焰
2CO+O2 2CO2
淡蓝色火焰
有水雾出现
变浑浊
CH4+2O2 CO2+2H2O
【微点拨】区分“光”与“火焰”及“烟”与“雾”的方法
(1)根据可燃物状态判定光和火焰。
光——高沸点的固体燃烧产生,如木炭
火焰——气体或固、液体的蒸气燃烧产生,如硫在空气中燃烧发出淡蓝色火焰
(2)根据燃烧产物的状态判定烟和雾。
烟——燃烧产物为固体小颗粒,如红磷
雾——燃烧产物为小液滴
(3)缓慢氧化。
①缓慢氧化与燃烧比较,共同点:都是氧化反应,都放热;不同点是反应剧烈程度不同。
②举例:动植物的呼吸、食物的腐烂变质、酒和醋的酿造等。
考点四 氧气的制取 高频考点
1.实验室制法:
(1)常温下,用过氧化氢溶液和二氧化锰混合。
化学方程式为_________________________。
(2)加热高锰酸钾或氯酸钾和二氧化锰的混合物。
化学方程式为__________________________________
__________________________。
2H2O2 2H2O+O2↑
2KMnO4 K2MnO4+MnO2+O2↑,
2KClO3 2KCl+3O2↑
2.工业制法:
(1)原理:利用液态氮和液态氧的_________不同,采用分离液态空气法,此变化为
_________变化。
(2)过程:
沸点
物理
考点五 自然界中的氧循环和碳循环
考点六 催化剂和催化作用
1.催化剂:在化学反应中,能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生改变的物质。
2.催化作用:催化剂在化学反应中所起的作用。
实验探究·培素养
实验一 空气中氧气含量的测定
1.必记基础知识:
(1)实验装置(用红磷作反应物)
(2)原理。
红磷燃烧消耗_________生成___________________,使容器中压强减小,水被压入
集气瓶,_____________体积即为氧气的体积。
(3)结论。
①氧气体积约占空气体积的________。
②氮气不能燃烧也不支持燃烧且难溶于水。
氧气
五氧化二磷固体
进入水的
1/5
2.突破关键点:
(1)实验成功的关键。
①药品:红磷_________。
②装置:气密性_________。
③操作:
a.导气管要关闭;
b.点燃红磷后将燃烧匙伸入集气瓶时要_________,并塞紧塞子;
c.待集气瓶_______________后再打开弹簧夹等。
足量
良好
迅速
冷却至室温
(2)药品选择应具备的条件。
①可燃物能够在空气中燃烧。不能选用铁丝代替红磷,因为铁丝在空气中不易燃烧。
②可燃物在空气中燃烧时只能与氧气反应,不能消耗其他的气体。不选用镁代替红磷,因为镁不仅与氧气反应,也可与空气中的二氧化碳、氮气反应,使集气瓶内减少的气体体积不全是氧气的体积。
③可燃物燃烧时只能生成固体,不能生成气体。不能用木炭、硫代替红磷,因为木炭、硫在空气中燃烧会生成气体。
注意:上述三个条件必须同时满足。
[特别提醒] 如果实验前先在集气瓶内放少量的浓氢氧化钠溶液,则可以使用硫粉作红磷的替代品,因为氢氧化钠溶液可以吸收生成的二氧化硫气体。
3.对实验误差的分析:
误差 原因及分析
测量结果 偏_______ 红磷不足,氧气不能耗尽
装置漏气会使装置外的空气进入
过早打开弹簧夹(或止水夹),由于装置内气体温度偏高,压强偏大,导致进入瓶中的水的体积偏小
测量结果 偏_______ 弹簧夹(或止水夹)没夹紧,红磷燃烧时集气瓶内气体受热顺着导管逸出
红磷伸入过慢会使装置内的气体受热逸出,导致进入瓶中的水的体积偏大
小
大
4.装置改进:
(1)各装置的作用及原理:
装置①:通过热水使温度达到白磷着火点而燃烧,从而使玻璃管内压强减小,活塞移动,活塞的移动量是氧气的体积;
装置②:利用放大镜将太阳光聚焦在集气瓶的白磷上,使温度达到白磷着火点燃烧,消耗氧气,瓶内压强减小,烧杯内的水被压进集气瓶;
装置③:铜丝在加热的条件下与管内氧气反应,使管内压强减小,管内外形成压强差,针管向前推进。
(2)改进后的优点:实验始终在密闭容器内进行,防止容器内空气逸散,减少实验误差。
【示范题1】(2023·福州三牧中学模拟)某兴趣小组用图1装置探究集气瓶内压强、
温度和O2体积分数的变化情况(集气瓶内气体的体积为100mL),得到实验数据如
图2,下列说法不正确的是( )
A.AB段下降原因主要是氧气被消耗了
B.EF段上升的原因是红磷燃烧放热
C.由Y曲线可知实验结束,进入瓶内水的体积
约为20.5 mL
D.CD段对应的操作是打开活塞,水进入集气瓶
C
实验二 氧气的实验室制法和性质
1.必记基础知识:
(1)实验室制取氧气的三种方法。
方法 过氧化氢制取氧气 氯酸钾制取氧气 高锰酸钾制取氧气
反应 原理 ______________ __________ ______________ ___________ _______________
___________________
2H2O2
2H2O+O2↑
2KClO3
2KCl+3O2↑
2KMnO4
K2MnO4+MnO2+O2↑
方法 过氧化氢制取氧气 氯酸钾制取氧气 高锰酸钾制取氧气
发生装 置的选 择依据 固液反应不加热 固固反应且需要加热 固体反应且需要加热
发生 装置
收集 装置
注意:选用C图所示装置收集氧气,应______导管进气(填字母,下同),
选用D图所示装置收集氧气,应______导管进气
a
c
(2)检验方法。
用_______________。
现象:_____________。
(3)验满方法。
①排水法:当集气瓶口_____________时,说明已满。
②向上排空气法:把带火星的木条放在_____________,木条_________,说明已满。
带火星木条
木条复燃
出现气泡
集气瓶口
复燃
(4)操作注意事项。
①用高锰酸钾或氯酸钾制取氧气的注意事项:
a.用KMnO4制取O2时,试管口要塞一团棉花,防止高锰酸钾粉末进入导管,堵塞导
管。
b.用高锰酸钾或氯酸钾制取氧气,试管口要_______________,以防止___________
______________________。
c.用排水法收集气体,实验结束后,应先_____________________,然后再_________
_______,防止_______________________。
略向下倾斜
水倒流回
试管底,引起试管炸裂
从水槽中取出导管
熄灭酒
精灯
水倒流引起试管炸裂
②用H2O2制取氧气,应注意长颈漏斗下端必须_________________。
③排水法收集气体时,当_____________________ 时才可以收集气体,否则会导致收集到的气体不纯。
伸到液面以下
气泡连续均匀冒出
2.突破关键点:
(1)上述三种制取氧气的方法中,哪种更符合绿色化学的特点 你的理由是_______
____________________________________________________________________
____________________________。
(2)用排水法和排空气法收集气体,各自的优缺点是_______________________
_____________________________________________________________________。
过氧
化氢与二氧化锰混合制氧气更符合绿色化学的特点。此反应装置简单,不需要
加热,不会产生粉尘等污染物
排空气法,利:操作简单,
弊:收集的气体纯度不高。排水集气法, 利:收集的气体纯度较高,弊:操作复杂
【示范题2】(2023·泉州实验中学模拟)兴趣小组用如图所示装置制备气体,并进行相关
实验。
(1)实验时固定A、B装置中试管的仪器名称是___________。
(2)用A装置制取氧气,取用氯酸钾的仪器名称是_________,试管中发生反应的化学方程
式为__________________________;根据A装置中的导管可推测该实验收集氧气的方法
是___________,实验过程中,若发现收集氧气速度迅速减慢,可采用______(填字母)操作
使反应继续进行。
A.试管向下移动
B.酒精灯稍左右移动
C.加少量二氧化锰
铁架台
药匙
2KClO3 2KCl+3O2↑
排水法
B
(3)用装置B也可制取氧气,与氯酸钾制氧气相比,该方法的优点是_______________
_______。
(4)为验证A装置中二氧化锰反应前后的质量没有变化,先分别称量滤纸、二氧化
锰的质量,制取氧气实验结束后,再进行如下操作:
过滤时,需要用蒸馏水不断冲洗滤渣和滤纸,其目的是______________________
_________________,连带滤纸一起称量的优点是_____________。
可以控制反应
速率
除去氯化钾,防止影响
二氧化锰的质量
减少误差
题组精练·提素能
【重温·福建中考】
命题点一 空气中氧气含量的测定
1.(2019·福建中考)某兴趣小组开展“测定密闭容器中某种气体的体积分数”的探究实验。
【实验1】按图1所示装置,用红磷燃烧的方法测定空气中氧气的体积分数。
【实验2】按图2所示装置,在集气瓶内壁用水均匀涂附铁粉除氧剂(其中辅助成分不干扰实验),利用铁锈蚀原理测定空气中氧气的体积分数。
(1)实验1中,红磷燃烧的主要现象是________________________________________
____________。红磷熄灭后,集气瓶冷却至室温,打开K,水能倒吸入集气瓶的原因
是__________________________________________。
(2)为提高实验的准确性,以上两个实验都需要注意的事项是___________________
__________________________________________(写一点)。
产生大量白烟(或“发出黄色火焰”“放热”等
合理答案)
氧气被消耗,集气瓶内气体压强小于大气压
装置的气密性良好
(或“红磷和铁粉除氧剂足量”等其他合理答案)
(3)实验过程中,连接数字传感器,测得实验1、实验2中氧气的体积分数随时间变
化的关系分别如图3、图4所示。依据图3、图4信息,__________(填“实验 1”或“实
验 2”) 的测定方法更准确,判断依据是_____________________________________
_________________________________________。
实验2
反应后,实验1集气瓶中剩余氧气的体积
分数为8.6%,而实验2集气瓶中氧气几乎耗尽
(4)结合你的学习经验,若要寻找红磷或铁粉除氧剂的替代物。用图1或图2装置测
定空气中氧气的体积分数,该替代物应满足的条件是__________________________
______________________________(写两点)。
能够和氧气反应;生成物不
影响测定结果(或其他合理答案)
【实验3】测定用排空气法收集到的集气瓶中二氧化碳的体积分数。
(5)甲同学设计图5所示装置进行测定。浓NaOH溶液的作用是______________
__________________(用化学方程式表示)。
(6)乙同学提出,仅利用图6所示装置,在不添加其他试剂的前提下,也能测得集气瓶
中二氧化碳的体积分数。为达到实验目的,操作方法是________________________
____________________。
2NaOH+CO2
===Na2CO3+H2O
用冰水冷却集气瓶,打开
K(或其他合理答案)
命题点二 氧气的实验室制法
2.(2023·福建中考)在“氧气的实验室制取与性质”实验中,下列装置或操作不正确
的是( )
C
3.(2019·福建中考)实验室制取氧气并模拟氢氧焰实验。
(1)用过氧化氢制取氧气(二氧化锰作催化剂)
①反应的化学方程式为___________________________。
②仪器A的名称为___________。现用下列仪器组装氧气的发生装置,应选用的
仪器有_________(填标号)。
③欲用浓硫酸干燥氧气,应从装置F的______(填“a”或“b”)处通入气体。
2H2O2 2H2O+O2↑
锥形瓶
ACD
a
(2)模拟氢氧焰实验:按图2所示装置进行实验。
①关闭K,通入氢气,点燃。为保证安全,点燃氢气之前应先_________。将铁丝网放
在火焰上灼烧,铁丝网只发红,不熔断。
②打开K,通入氧气,火焰更明亮,铁丝熔断,说明燃烧的剧烈程度与氧气的_________
有关。
验纯
浓度
4.(2022·福建中考)为做好实验室制取氧气的实验活动和评价,某班级师生讨论并确定如下评价标准。
评价标准
1.是否根据实验条件选择实验方案,并进行可行性论证
2.是否积极参与实验操作活动,并善于与同学合作
3.是否规范取用药品,节约药品,保持实验台整洁
4.是否客观准确记录实验现象,并交流实验成果
5.是否体验到实验探究活动的乐趣
你是某小组成员,参与完成下列实验活动。
(1)选择实验方案。实验室可提供三种制取氧气的方案。
A.加热高锰酸钾
B.加热混有二氧化锰的氯酸钾
C.催化分解过氧化氢
你所选方案对应反应的化学方程式为___________________________________。
小组讨论决定选用A方案。
2KMnO4 K2MnO4+MnO2+O2↑
(2)进行实验活动。小组同学分工协作完成如下任务:
①同学甲负责选择组装制取气体装置的仪器。她选择了铁架台、带有导管的橡
胶塞、水槽、试管,还应根据如图所提供的仪器,选择___________、___________
(填仪器名称)。
②同学乙负责取用药品。他先检查装置气密性,再用纸槽小心地把高锰酸钾粉末
送至试管_________(填“中部”或“底部”)后直立试管,抽出纸槽。
酒精灯
集气瓶
底部
③同学丙负责组装仪器。他按“从下到上、从左到右”的顺序组装制取装置,固定
试管时注意试管口应略_____________。
④你负责排水法收集氧气。开始收集的时机是_____________________________
_______________。收集到两瓶气体,均呈红色。
⑤实验结束,待试管冷却,将残余物倒入指定容器,用___________(填仪器名称)洗涤
试管;整理实验台,报告老师后离开实验室。
(3)评价与反思。小组同学都认为体验到了实验活动的乐趣,但因实验过程存在不
足,同意本次活动表现评价为“有待改进”。针对存在的不足,你提出的一条实验改
进意见是__________________________________。
向下倾斜
当导管口有连续均匀的气泡冒
出时开始收集
试管刷
装入药品后,在试管口放一团棉花
命题点三 催化剂和催化作用
5.(2018·福建中考节选)某研究小组对过氧化氢溶液制取氧气进行如下探究。
探究制取氧气的适宜催化剂
实验方案如下:
Ⅰ.用MnO2、CuO、Fe2O3、Cr2O3四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。Ⅱ.取30粒含MnO2的海藻酸钠微球,采用如图装置进行实验。改用其他三种微球,分别重复上述实验,得到如图的锥形瓶内压强随时间变化的曲线图。
(1)每次实验时,海藻酸钠微球数应相同的原因是____________________________
____________。
(2)用含MnO2的海藻酸钠微球进行实验,60 s时压强瞬间回落,其原因是_________
_________________________________________________。
(3)从实验曲线看,催化效果较好、反应温和的催化剂是_________。
确保催化剂用量一致(或其他
合理答案)
产气速
率过快,导致气压过大,橡胶塞被弹出(或其他合理答案)
CuO
【精练·福建模拟】
1.2022年11月30日,神十五航天员顺利进驻中国空间站,6名航天员首次实现太空
会师。空间站的“人造空气”与我们身边的空气成分含量基本相同,“人造空气”中
体积分数最大的是( )
A.氧气 B.氮气 C.二氧化碳 D.稀有气体
2.下列关于氖气的说法正确的是( )
A.化学式为Ne2 B.颜色呈红色
C.化学性质活泼 D.用于霓虹灯的电光源
B
D
3.(2023·福州四十中模拟)PM2.5是指大气中直径小于或等于2.5微米的颗粒物,它对
空气质量和能见度等有重要的影响,下列做法不利于改善空气质量的是( )
A.火力发电厂排放的废气必须处理达标后排放
B.大量发展轨道交通,鼓励市民绿色出行
C.建设环城河景观带,增大绿化面积
D.建筑工地车辆未经冲洗直接进入路面
D
4.(2023·福州文博中学模拟)有关氧气的下列说法,正确的是( )
A.鱼儿说:“我能在水中呼吸,因为氧气易溶于水。”
B.火箭说:“氧气是我的燃料,因为氧气具有可燃性。”
C.绿色植物说:“氧气是我进行光合作用的原料。”
D.铁钉说:“我讨厌氧气,它会让我生锈。”
D
5.(2023·宁德培文模拟)过氧化氢在催化剂作用下可迅速分解成水和氧气,按如图
所示进行实验,量筒中涌出柱状的泡沫,可形象地称为“大象牙膏”。下列说法正确
的是( )
A.该实验可以用洗洁精作发泡剂
B.产生的泡沫可用于灭火
C.反应前后催化剂的化学性质改变
D.没有催化剂过氧化氢不会分解
A
6.化学兴趣小组欲探究用不同物质在空气中燃烧测定氧气的体积分数。他们用
足量的蜡烛、红磷分别在相同体积与状态的空气中燃烧,用氧气探测器测定容器
中剩余氧气与时间的关系如图所示。下列说法正确的是( )
A.两个实验中均为氧气过量
B.若用这两种物质做实验,测定空气中氧气的
体积分数偏高
C.用蜡烛测定空气中氧气体积分数的效果比
红磷好
D.该实验证明氧气的浓度较低时,红磷还能与之发生反应
D
7.“富氧空气”是指氧气含量高于普通空气的气体,可用于航天、医疗、炼钢等。化学兴趣小组欲制取“富氧空气”并开展相关探究,进行以下实验:
实验一:制取“富氧空气”
(1)用高锰酸钾制取氧气
①写出反应的化学方程式:____________________________________。
②仪器C的名称为_________。
(2)混制“富氧空气”如图,用纯氮气及上述实验制取的氧气,混制一瓶氧气体积分数
为40%的“富氧空气”,气体应从装置中的管______(填“a”或“b”)通入,先通入氮气排
出120 mL水,再通入氧气排出_______mL水。
2KMnO4 K2MnO4+MnO2+O2↑
水槽
b
80
实验二:测定“富氧空气”中氧气的含量
用如图装置测定“富氧空气”中氧气的含量(集气瓶中“富氧空气”体积为100 mL,底部残留少量水,燃烧匙内有足量红磷)。操作如下:
Ⅰ.往量筒内加入适量水,读出量筒内水的体积为V1 mL;
Ⅱ.用电点火装置点燃红磷,充分反应;
Ⅲ.打开止水夹,待右侧量筒内液面不再变化时,排出气球中的气体,调节两边液面在同一水平面上,读出量筒内水的体积为V2 mL。
回答下列问题:
(3)实验前,检查装置气密性的方法:______________________________________
____________________________________________________________。
(4)操作Ⅱ中可观察到的现象:__________________________。
(5)本次实验测得“富氧空气”中氧气的含量为_____________(用含V1、V2的式子
表示)。
(6)若读取V1时仰视,读取V2时俯视,则测得实验结果_________(填“偏大”“偏小”或
“无影响”)。
系紧气球,打开止水夹,向右侧量筒内加水
超过支管,然后上下移动量筒,两边液面有液面差,则装置的气密性好
红磷燃烧,产生白烟,放热
(V1-V2)%
偏小
【感悟·全国真题】
1.(2023·益阳中考)空气是一种宝贵的自然资源,各成分都具有广泛的用途。下列
不属于氮气的用途的是( )
A.人工降雨 B.冷冻麻醉
C.食品防腐 D.制造氮肥
A
2.(2023·烟台中考改编)下列有关空气及其成分的说法错误的是( )
A.氧气具有助燃性,常用作燃料
B.二氧化碳是植物进行光合作用必需的物质
C.工业上可用分离液态空气制取氧气
D.空气质量指数越大,空气质量状况越差
A
3.(2023广东中考)[基础实验与学科实践]
(1)实验室制取O2及性质检验
i.图1中仪器a的名称是___________;
ii.用高锰酸钾制取O2,应选择图1中的发生装置______(填字母)。化学方程式为
___________________________________;
锥形瓶
A
2KMnO4 K2MnO4+MnO2+O2↑
iii.收集一瓶O2并进行性质检验。
操作 现象 结论
硫燃烧时,______(填字母),生成有刺激性 气味的气体 a.产生大量白烟 b.生成黑色固体 c.发出蓝紫色火焰 O2具有
氧化性
集气瓶中NaOH溶液的作用是__________________________________________ c
吸收反应生成的二氧化硫,防止其污染空气
(2)制作氧自救呼吸器
查阅资料,超氧化钾(KO2)为黄色固体,分别与CO2、H2O反应生成O2和白色固体,
产氧效率高,适合作生氧剂。
原理分析:4KO2+2CO2===2K2CO3+3O2、4KO2+2H2O===4X+3O3↑则X的化学式
为__________。
动手实践:设计并制作氧自救呼吸器,如图2所示,使用一段时间后,观察到生氧剂由
___________________(填颜色变化),则基本失效。
KOH
由黄色变为白色
教材基础复习篇
板块一 身边的化学物质
主题1 空气和氧气
知识清单·理脉络
考点一 空气的成分及用途 高频考点
成分 体积分数 性质和用途
氮气 78%(最大) 性质_____________,常用作___________(食品防腐、
灯泡填充、焊接金属)
氧气 21% 性质_____________,能与大多数物质发生反应,能支
持呼吸(医疗急救、潜水),支持燃烧
稀有气体 0.94% 化学性质稳定,用作保护气、制作霓虹灯
二氧化碳 0.03% 光合作用的原料、人工降雨、灭火、制取碳酸饮料
其他气体 和杂质 0.03% —
比较稳定
保护气
比较活泼
考点二 空气的污染及防治
1.空气污染物:
【微点拨】CO2不属于空气污染物。
2.空气污染的来源及防治措施:
污染来源 防治措施
化石燃料的燃烧 改变能源结构,开发新能源
工业废气 工业废气处理达标后排放,减少有害物质的排放
植被被破坏引起的沙尘 植树、造林、种草等,提高空气的自净能力
考点三 氧气的性质
1.物理性质:
溶解性:不易溶于水;密度:比空气略大;
状态变化:降温时,变为淡蓝色液体和淡蓝色雪花状固体。
2.化学性质:
(1)氧气的助燃性。
带火星的木条在氧气中能够_________,说明氧气支持燃烧,常利用此性质来检验
某气体是否为氧气。
【微点拨】氧气虽然具有助燃性,但本身不能燃烧,不能用作燃料。
复燃
(2)常见物质在空气或氧气中燃烧。
①木炭燃烧。
a.现象:
不同点:在空气中,_____________________;
在氧气中,______________________。
相同点:放热,都生成使澄清石灰水变_________的气体。
b.化学方程式:_________________。
红热、无烟、无焰
剧烈燃烧,发出白光
浑浊
C+O2 CO2
②硫燃烧
a.不同点:在空气中发出_______________,在氧气中发出___________________。
相同点:_________________________________。
b.化学方程式:__________________。
③铁的燃烧。
a.现象:
不同点:在空气中,__________________________;在氧气中,____________________
_______________。
b.化学方程式:_______________________。
淡蓝色火焰
放热、生成一种刺激性气味气体
S+O2 SO2
发生红热现象,不能燃烧
剧烈燃烧,火星四射,
生成黑色固体
3Fe+2O2 Fe3O4
明亮蓝紫色火焰
【微点拨】硫粉在氧气中燃烧时,集气瓶瓶底放少量水或氢氧化钠溶液,目的是吸收二氧化硫,防止污染空气;做铁丝燃烧实验前,要预先在集气瓶中放少量水或铺一层细沙,目的是防止熔融物溅落下来炸裂瓶底。
④其他常见可燃物在空气或氧气中燃烧。
物质 现象 化学方程式
红磷 在空气中和氧气中燃烧都产生大量白烟、 放热 _____________________
镁条 发出_________的白光,生成_______色固体、 大量放热 ______________________
氢气 在氧气中燃烧,___________________, 火焰上方罩着的干冷烧杯内壁出现水雾、 放热 _____________________
4P+5O2 2P2O5
耀眼
白
2Mg+O2 2MgO
产生淡蓝色火焰
2H2+O2 2H2O
物质 现象 化学方程式
一氧 化碳 在空气或氧气中燃烧,发出_______________, 放热,生成能使澄清石灰水变浑浊的气体 _____________________
甲烷 在空气中燃烧,发出_______________, 火焰上方的烧杯中_______________, 取下烧杯正放,加入澄清石灰水振荡, 石灰水____________ ______________________
淡蓝色火焰
2CO+O2 2CO2
淡蓝色火焰
有水雾出现
变浑浊
CH4+2O2 CO2+2H2O
【微点拨】区分“光”与“火焰”及“烟”与“雾”的方法
(1)根据可燃物状态判定光和火焰。
光——高沸点的固体燃烧产生,如木炭
火焰——气体或固、液体的蒸气燃烧产生,如硫在空气中燃烧发出淡蓝色火焰
(2)根据燃烧产物的状态判定烟和雾。
烟——燃烧产物为固体小颗粒,如红磷
雾——燃烧产物为小液滴
(3)缓慢氧化。
①缓慢氧化与燃烧比较,共同点:都是氧化反应,都放热;不同点是反应剧烈程度不同。
②举例:动植物的呼吸、食物的腐烂变质、酒和醋的酿造等。
考点四 氧气的制取 高频考点
1.实验室制法:
(1)常温下,用过氧化氢溶液和二氧化锰混合。
化学方程式为_________________________。
(2)加热高锰酸钾或氯酸钾和二氧化锰的混合物。
化学方程式为__________________________________
__________________________。
2H2O2 2H2O+O2↑
2KMnO4 K2MnO4+MnO2+O2↑,
2KClO3 2KCl+3O2↑
2.工业制法:
(1)原理:利用液态氮和液态氧的_________不同,采用分离液态空气法,此变化为
_________变化。
(2)过程:
沸点
物理
考点五 自然界中的氧循环和碳循环
考点六 催化剂和催化作用
1.催化剂:在化学反应中,能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生改变的物质。
2.催化作用:催化剂在化学反应中所起的作用。
实验探究·培素养
实验一 空气中氧气含量的测定
1.必记基础知识:
(1)实验装置(用红磷作反应物)
(2)原理。
红磷燃烧消耗_________生成___________________,使容器中压强减小,水被压入
集气瓶,_____________体积即为氧气的体积。
(3)结论。
①氧气体积约占空气体积的________。
②氮气不能燃烧也不支持燃烧且难溶于水。
氧气
五氧化二磷固体
进入水的
1/5
2.突破关键点:
(1)实验成功的关键。
①药品:红磷_________。
②装置:气密性_________。
③操作:
a.导气管要关闭;
b.点燃红磷后将燃烧匙伸入集气瓶时要_________,并塞紧塞子;
c.待集气瓶_______________后再打开弹簧夹等。
足量
良好
迅速
冷却至室温
(2)药品选择应具备的条件。
①可燃物能够在空气中燃烧。不能选用铁丝代替红磷,因为铁丝在空气中不易燃烧。
②可燃物在空气中燃烧时只能与氧气反应,不能消耗其他的气体。不选用镁代替红磷,因为镁不仅与氧气反应,也可与空气中的二氧化碳、氮气反应,使集气瓶内减少的气体体积不全是氧气的体积。
③可燃物燃烧时只能生成固体,不能生成气体。不能用木炭、硫代替红磷,因为木炭、硫在空气中燃烧会生成气体。
注意:上述三个条件必须同时满足。
[特别提醒] 如果实验前先在集气瓶内放少量的浓氢氧化钠溶液,则可以使用硫粉作红磷的替代品,因为氢氧化钠溶液可以吸收生成的二氧化硫气体。
3.对实验误差的分析:
误差 原因及分析
测量结果 偏_______ 红磷不足,氧气不能耗尽
装置漏气会使装置外的空气进入
过早打开弹簧夹(或止水夹),由于装置内气体温度偏高,压强偏大,导致进入瓶中的水的体积偏小
测量结果 偏_______ 弹簧夹(或止水夹)没夹紧,红磷燃烧时集气瓶内气体受热顺着导管逸出
红磷伸入过慢会使装置内的气体受热逸出,导致进入瓶中的水的体积偏大
小
大
4.装置改进:
(1)各装置的作用及原理:
装置①:通过热水使温度达到白磷着火点而燃烧,从而使玻璃管内压强减小,活塞移动,活塞的移动量是氧气的体积;
装置②:利用放大镜将太阳光聚焦在集气瓶的白磷上,使温度达到白磷着火点燃烧,消耗氧气,瓶内压强减小,烧杯内的水被压进集气瓶;
装置③:铜丝在加热的条件下与管内氧气反应,使管内压强减小,管内外形成压强差,针管向前推进。
(2)改进后的优点:实验始终在密闭容器内进行,防止容器内空气逸散,减少实验误差。
【示范题1】(2023·福州三牧中学模拟)某兴趣小组用图1装置探究集气瓶内压强、
温度和O2体积分数的变化情况(集气瓶内气体的体积为100mL),得到实验数据如
图2,下列说法不正确的是( )
A.AB段下降原因主要是氧气被消耗了
B.EF段上升的原因是红磷燃烧放热
C.由Y曲线可知实验结束,进入瓶内水的体积
约为20.5 mL
D.CD段对应的操作是打开活塞,水进入集气瓶
C
实验二 氧气的实验室制法和性质
1.必记基础知识:
(1)实验室制取氧气的三种方法。
方法 过氧化氢制取氧气 氯酸钾制取氧气 高锰酸钾制取氧气
反应 原理 ______________ __________ ______________ ___________ _______________
___________________
2H2O2
2H2O+O2↑
2KClO3
2KCl+3O2↑
2KMnO4
K2MnO4+MnO2+O2↑
方法 过氧化氢制取氧气 氯酸钾制取氧气 高锰酸钾制取氧气
发生装 置的选 择依据 固液反应不加热 固固反应且需要加热 固体反应且需要加热
发生 装置
收集 装置
注意:选用C图所示装置收集氧气,应______导管进气(填字母,下同),
选用D图所示装置收集氧气,应______导管进气
a
c
(2)检验方法。
用_______________。
现象:_____________。
(3)验满方法。
①排水法:当集气瓶口_____________时,说明已满。
②向上排空气法:把带火星的木条放在_____________,木条_________,说明已满。
带火星木条
木条复燃
出现气泡
集气瓶口
复燃
(4)操作注意事项。
①用高锰酸钾或氯酸钾制取氧气的注意事项:
a.用KMnO4制取O2时,试管口要塞一团棉花,防止高锰酸钾粉末进入导管,堵塞导
管。
b.用高锰酸钾或氯酸钾制取氧气,试管口要_______________,以防止___________
______________________。
c.用排水法收集气体,实验结束后,应先_____________________,然后再_________
_______,防止_______________________。
略向下倾斜
水倒流回
试管底,引起试管炸裂
从水槽中取出导管
熄灭酒
精灯
水倒流引起试管炸裂
②用H2O2制取氧气,应注意长颈漏斗下端必须_________________。
③排水法收集气体时,当_____________________ 时才可以收集气体,否则会导致收集到的气体不纯。
伸到液面以下
气泡连续均匀冒出
2.突破关键点:
(1)上述三种制取氧气的方法中,哪种更符合绿色化学的特点 你的理由是_______
____________________________________________________________________
____________________________。
(2)用排水法和排空气法收集气体,各自的优缺点是_______________________
_____________________________________________________________________。
过氧
化氢与二氧化锰混合制氧气更符合绿色化学的特点。此反应装置简单,不需要
加热,不会产生粉尘等污染物
排空气法,利:操作简单,
弊:收集的气体纯度不高。排水集气法, 利:收集的气体纯度较高,弊:操作复杂
【示范题2】(2023·泉州实验中学模拟)兴趣小组用如图所示装置制备气体,并进行相关
实验。
(1)实验时固定A、B装置中试管的仪器名称是___________。
(2)用A装置制取氧气,取用氯酸钾的仪器名称是_________,试管中发生反应的化学方程
式为__________________________;根据A装置中的导管可推测该实验收集氧气的方法
是___________,实验过程中,若发现收集氧气速度迅速减慢,可采用______(填字母)操作
使反应继续进行。
A.试管向下移动
B.酒精灯稍左右移动
C.加少量二氧化锰
铁架台
药匙
2KClO3 2KCl+3O2↑
排水法
B
(3)用装置B也可制取氧气,与氯酸钾制氧气相比,该方法的优点是_______________
_______。
(4)为验证A装置中二氧化锰反应前后的质量没有变化,先分别称量滤纸、二氧化
锰的质量,制取氧气实验结束后,再进行如下操作:
过滤时,需要用蒸馏水不断冲洗滤渣和滤纸,其目的是______________________
_________________,连带滤纸一起称量的优点是_____________。
可以控制反应
速率
除去氯化钾,防止影响
二氧化锰的质量
减少误差
题组精练·提素能
【重温·福建中考】
命题点一 空气中氧气含量的测定
1.(2019·福建中考)某兴趣小组开展“测定密闭容器中某种气体的体积分数”的探究实验。
【实验1】按图1所示装置,用红磷燃烧的方法测定空气中氧气的体积分数。
【实验2】按图2所示装置,在集气瓶内壁用水均匀涂附铁粉除氧剂(其中辅助成分不干扰实验),利用铁锈蚀原理测定空气中氧气的体积分数。
(1)实验1中,红磷燃烧的主要现象是________________________________________
____________。红磷熄灭后,集气瓶冷却至室温,打开K,水能倒吸入集气瓶的原因
是__________________________________________。
(2)为提高实验的准确性,以上两个实验都需要注意的事项是___________________
__________________________________________(写一点)。
产生大量白烟(或“发出黄色火焰”“放热”等
合理答案)
氧气被消耗,集气瓶内气体压强小于大气压
装置的气密性良好
(或“红磷和铁粉除氧剂足量”等其他合理答案)
(3)实验过程中,连接数字传感器,测得实验1、实验2中氧气的体积分数随时间变
化的关系分别如图3、图4所示。依据图3、图4信息,__________(填“实验 1”或“实
验 2”) 的测定方法更准确,判断依据是_____________________________________
_________________________________________。
实验2
反应后,实验1集气瓶中剩余氧气的体积
分数为8.6%,而实验2集气瓶中氧气几乎耗尽
(4)结合你的学习经验,若要寻找红磷或铁粉除氧剂的替代物。用图1或图2装置测
定空气中氧气的体积分数,该替代物应满足的条件是__________________________
______________________________(写两点)。
能够和氧气反应;生成物不
影响测定结果(或其他合理答案)
【实验3】测定用排空气法收集到的集气瓶中二氧化碳的体积分数。
(5)甲同学设计图5所示装置进行测定。浓NaOH溶液的作用是______________
__________________(用化学方程式表示)。
(6)乙同学提出,仅利用图6所示装置,在不添加其他试剂的前提下,也能测得集气瓶
中二氧化碳的体积分数。为达到实验目的,操作方法是________________________
____________________。
2NaOH+CO2
===Na2CO3+H2O
用冰水冷却集气瓶,打开
K(或其他合理答案)
命题点二 氧气的实验室制法
2.(2023·福建中考)在“氧气的实验室制取与性质”实验中,下列装置或操作不正确
的是( )
C
3.(2019·福建中考)实验室制取氧气并模拟氢氧焰实验。
(1)用过氧化氢制取氧气(二氧化锰作催化剂)
①反应的化学方程式为___________________________。
②仪器A的名称为___________。现用下列仪器组装氧气的发生装置,应选用的
仪器有_________(填标号)。
③欲用浓硫酸干燥氧气,应从装置F的______(填“a”或“b”)处通入气体。
2H2O2 2H2O+O2↑
锥形瓶
ACD
a
(2)模拟氢氧焰实验:按图2所示装置进行实验。
①关闭K,通入氢气,点燃。为保证安全,点燃氢气之前应先_________。将铁丝网放
在火焰上灼烧,铁丝网只发红,不熔断。
②打开K,通入氧气,火焰更明亮,铁丝熔断,说明燃烧的剧烈程度与氧气的_________
有关。
验纯
浓度
4.(2022·福建中考)为做好实验室制取氧气的实验活动和评价,某班级师生讨论并确定如下评价标准。
评价标准
1.是否根据实验条件选择实验方案,并进行可行性论证
2.是否积极参与实验操作活动,并善于与同学合作
3.是否规范取用药品,节约药品,保持实验台整洁
4.是否客观准确记录实验现象,并交流实验成果
5.是否体验到实验探究活动的乐趣
你是某小组成员,参与完成下列实验活动。
(1)选择实验方案。实验室可提供三种制取氧气的方案。
A.加热高锰酸钾
B.加热混有二氧化锰的氯酸钾
C.催化分解过氧化氢
你所选方案对应反应的化学方程式为___________________________________。
小组讨论决定选用A方案。
2KMnO4 K2MnO4+MnO2+O2↑
(2)进行实验活动。小组同学分工协作完成如下任务:
①同学甲负责选择组装制取气体装置的仪器。她选择了铁架台、带有导管的橡
胶塞、水槽、试管,还应根据如图所提供的仪器,选择___________、___________
(填仪器名称)。
②同学乙负责取用药品。他先检查装置气密性,再用纸槽小心地把高锰酸钾粉末
送至试管_________(填“中部”或“底部”)后直立试管,抽出纸槽。
酒精灯
集气瓶
底部
③同学丙负责组装仪器。他按“从下到上、从左到右”的顺序组装制取装置,固定
试管时注意试管口应略_____________。
④你负责排水法收集氧气。开始收集的时机是_____________________________
_______________。收集到两瓶气体,均呈红色。
⑤实验结束,待试管冷却,将残余物倒入指定容器,用___________(填仪器名称)洗涤
试管;整理实验台,报告老师后离开实验室。
(3)评价与反思。小组同学都认为体验到了实验活动的乐趣,但因实验过程存在不
足,同意本次活动表现评价为“有待改进”。针对存在的不足,你提出的一条实验改
进意见是__________________________________。
向下倾斜
当导管口有连续均匀的气泡冒
出时开始收集
试管刷
装入药品后,在试管口放一团棉花
命题点三 催化剂和催化作用
5.(2018·福建中考节选)某研究小组对过氧化氢溶液制取氧气进行如下探究。
探究制取氧气的适宜催化剂
实验方案如下:
Ⅰ.用MnO2、CuO、Fe2O3、Cr2O3四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。Ⅱ.取30粒含MnO2的海藻酸钠微球,采用如图装置进行实验。改用其他三种微球,分别重复上述实验,得到如图的锥形瓶内压强随时间变化的曲线图。
(1)每次实验时,海藻酸钠微球数应相同的原因是____________________________
____________。
(2)用含MnO2的海藻酸钠微球进行实验,60 s时压强瞬间回落,其原因是_________
_________________________________________________。
(3)从实验曲线看,催化效果较好、反应温和的催化剂是_________。
确保催化剂用量一致(或其他
合理答案)
产气速
率过快,导致气压过大,橡胶塞被弹出(或其他合理答案)
CuO
【精练·福建模拟】
1.2022年11月30日,神十五航天员顺利进驻中国空间站,6名航天员首次实现太空
会师。空间站的“人造空气”与我们身边的空气成分含量基本相同,“人造空气”中
体积分数最大的是( )
A.氧气 B.氮气 C.二氧化碳 D.稀有气体
2.下列关于氖气的说法正确的是( )
A.化学式为Ne2 B.颜色呈红色
C.化学性质活泼 D.用于霓虹灯的电光源
B
D
3.(2023·福州四十中模拟)PM2.5是指大气中直径小于或等于2.5微米的颗粒物,它对
空气质量和能见度等有重要的影响,下列做法不利于改善空气质量的是( )
A.火力发电厂排放的废气必须处理达标后排放
B.大量发展轨道交通,鼓励市民绿色出行
C.建设环城河景观带,增大绿化面积
D.建筑工地车辆未经冲洗直接进入路面
D
4.(2023·福州文博中学模拟)有关氧气的下列说法,正确的是( )
A.鱼儿说:“我能在水中呼吸,因为氧气易溶于水。”
B.火箭说:“氧气是我的燃料,因为氧气具有可燃性。”
C.绿色植物说:“氧气是我进行光合作用的原料。”
D.铁钉说:“我讨厌氧气,它会让我生锈。”
D
5.(2023·宁德培文模拟)过氧化氢在催化剂作用下可迅速分解成水和氧气,按如图
所示进行实验,量筒中涌出柱状的泡沫,可形象地称为“大象牙膏”。下列说法正确
的是( )
A.该实验可以用洗洁精作发泡剂
B.产生的泡沫可用于灭火
C.反应前后催化剂的化学性质改变
D.没有催化剂过氧化氢不会分解
A
6.化学兴趣小组欲探究用不同物质在空气中燃烧测定氧气的体积分数。他们用
足量的蜡烛、红磷分别在相同体积与状态的空气中燃烧,用氧气探测器测定容器
中剩余氧气与时间的关系如图所示。下列说法正确的是( )
A.两个实验中均为氧气过量
B.若用这两种物质做实验,测定空气中氧气的
体积分数偏高
C.用蜡烛测定空气中氧气体积分数的效果比
红磷好
D.该实验证明氧气的浓度较低时,红磷还能与之发生反应
D
7.“富氧空气”是指氧气含量高于普通空气的气体,可用于航天、医疗、炼钢等。化学兴趣小组欲制取“富氧空气”并开展相关探究,进行以下实验:
实验一:制取“富氧空气”
(1)用高锰酸钾制取氧气
①写出反应的化学方程式:____________________________________。
②仪器C的名称为_________。
(2)混制“富氧空气”如图,用纯氮气及上述实验制取的氧气,混制一瓶氧气体积分数
为40%的“富氧空气”,气体应从装置中的管______(填“a”或“b”)通入,先通入氮气排
出120 mL水,再通入氧气排出_______mL水。
2KMnO4 K2MnO4+MnO2+O2↑
水槽
b
80
实验二:测定“富氧空气”中氧气的含量
用如图装置测定“富氧空气”中氧气的含量(集气瓶中“富氧空气”体积为100 mL,底部残留少量水,燃烧匙内有足量红磷)。操作如下:
Ⅰ.往量筒内加入适量水,读出量筒内水的体积为V1 mL;
Ⅱ.用电点火装置点燃红磷,充分反应;
Ⅲ.打开止水夹,待右侧量筒内液面不再变化时,排出气球中的气体,调节两边液面在同一水平面上,读出量筒内水的体积为V2 mL。
回答下列问题:
(3)实验前,检查装置气密性的方法:______________________________________
____________________________________________________________。
(4)操作Ⅱ中可观察到的现象:__________________________。
(5)本次实验测得“富氧空气”中氧气的含量为_____________(用含V1、V2的式子
表示)。
(6)若读取V1时仰视,读取V2时俯视,则测得实验结果_________(填“偏大”“偏小”或
“无影响”)。
系紧气球,打开止水夹,向右侧量筒内加水
超过支管,然后上下移动量筒,两边液面有液面差,则装置的气密性好
红磷燃烧,产生白烟,放热
(V1-V2)%
偏小
【感悟·全国真题】
1.(2023·益阳中考)空气是一种宝贵的自然资源,各成分都具有广泛的用途。下列
不属于氮气的用途的是( )
A.人工降雨 B.冷冻麻醉
C.食品防腐 D.制造氮肥
A
2.(2023·烟台中考改编)下列有关空气及其成分的说法错误的是( )
A.氧气具有助燃性,常用作燃料
B.二氧化碳是植物进行光合作用必需的物质
C.工业上可用分离液态空气制取氧气
D.空气质量指数越大,空气质量状况越差
A
3.(2023广东中考)[基础实验与学科实践]
(1)实验室制取O2及性质检验
i.图1中仪器a的名称是___________;
ii.用高锰酸钾制取O2,应选择图1中的发生装置______(填字母)。化学方程式为
___________________________________;
锥形瓶
A
2KMnO4 K2MnO4+MnO2+O2↑
iii.收集一瓶O2并进行性质检验。
操作 现象 结论
硫燃烧时,______(填字母),生成有刺激性 气味的气体 a.产生大量白烟 b.生成黑色固体 c.发出蓝紫色火焰 O2具有
氧化性
集气瓶中NaOH溶液的作用是__________________________________________ c
吸收反应生成的二氧化硫,防止其污染空气
(2)制作氧自救呼吸器
查阅资料,超氧化钾(KO2)为黄色固体,分别与CO2、H2O反应生成O2和白色固体,
产氧效率高,适合作生氧剂。
原理分析:4KO2+2CO2===2K2CO3+3O2、4KO2+2H2O===4X+3O3↑则X的化学式
为__________。
动手实践:设计并制作氧自救呼吸器,如图2所示,使用一段时间后,观察到生氧剂由
___________________(填颜色变化),则基本失效。
KOH
由黄色变为白色
同课章节目录
