8.2金属的化学性质课时练习(含答案)人教版化学九年级下册
文档属性
| 名称 | 8.2金属的化学性质课时练习(含答案)人教版化学九年级下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 468.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-22 00:00:00 | ||
图片预览




文档简介
8.2 金属的化学性质 课时练习
一、多选题
1.下列有关做法正确的是
A.区别水和过氧化氢溶液,可以各取少量分别放入试管中,再加入等量的MnO2,并在瓶口放一个带火星的木条看是否复燃
B.除去铁粉中混入的镁粉,将混合物放入足量的稀硫酸中,充分反应后过滤
C.氧化钙和氢氧化钙可以通过取样加入水来进行鉴别
D.向某固体物质中加入盐酸,观察到有气泡产生,则该物质一定是较活泼金属
2.下列解释错误的是
A.铝制品不用涂任何保层来防腐,因为铝不与空气反应
B.铁丝在空气不能被点燃与空气中氧气的体积分数有关
C.生铁和钢的性能不同与它们的组成中含碳量不同有关
D.新轿车中常弥漫着皮革气味。从分子角度看,这是构成物质的分子大小不同的结果
3.向AgNO3和Cu(NO3)2的混合液中加入一定量的Fe、Cu的混合粉末,充分反应后过滤、洗涤,得到滤液和滤渣。下列说法正确的是( )
A.向滤液中加入KCl溶液,无明显现象,则滤液中一定有Fe(NO3)2、Cu(NO3)2,滤渣中可能有Fe、Cu
B.当滤液为蓝色时,滤渣中一定有Cu、Ag,一定没有Fe
C.向滤渣中加入盐酸,有气泡产生,则滤渣中一定有Fe、Cu、Ag
D.滤渣中一定有Ag,滤液中可能有Cu(NO3)2、AgNO3
4.下列图像能正确反映其对应操作中各量变化关系的是
A.加热高锰酸钾制氧气的实验,试管中固体的质量变化
B.向一定质量过氧化氢溶液中加入少量二氧化锰的实验,试管中水的质量变化
C.向一定质量的硫酸铜溶液中加入铁粉至过量的实验,试管中溶液的质量变化
D.分别向质量相等的镁和铁中加入相同的稀盐酸至过量的实验,生成H2的质量变化
5.除去下列物质中的杂质,所用试剂和方法均正确的是
物质 杂质 所用试剂或方法
A CO2 CO 点燃
B Cu Fe 足量的稀盐酸
C N2 O2 灼热的铜网
D 炭粉 MnO2 加水过滤
A.A B.B C.C D.D
二、选择题
6.下列说法符合客观事实的是
A.通常情况下铝制品耐腐蚀,原因是铝不易发生化学反应
B.氯酸钾中加入少量高锰酸钾加热,发现产生氧气的速率会加快
C.巴黎圣母院失火,消防队员用水灭火是为了降低可燃物的着火点
D.将燃着的木条伸入呼出气体中会熄灭,说明呼出气体中二氧化碳含量大于空气
7.将一定质量的铁粉放入硝酸锌和硝酸铜的混合溶液中,充分反应后过滤,得到滤液和滤渣。下列有关滤液和滤渣的说法正确的是
A.滤渣中一定有Cu,可能有Zn、Fe
B.滤渣中一定有Cu、Zn,可能有Fe
C.如果滤液中有Cu(NO3)2,则滤渣的成分可能是Cu,Fe
D.滤液中一定有Fe(NO3)2、Zn(NO3)2,可能有Cu(NO3)2
8.有X、Y、Z三种金属,把Y投入X(NO3)2溶液中,Y表面有X析出,溶液质量增大;把X投入Z(NO3)2溶液中,得到X(NO3)2,固体质量增大。下列判断错误的是
A.X、Y、Z可能依次是:Cu、Fe、Ag
B.元素的相对原子质量可能是:Z>Y>X
C.金属活动性顺序是:Y>X>Z
D.X、Y、Z可能依次是:Fe、Zn、Hg
9.有X、Y、Z三种金属,若将X、Y、Z分别放入一定质量的稀盐酸中,只有X表面产生气泡:若将Z放到Y(NO3)2溶液中,Z表面无现象,则X、Y、Z三种金属活动性顺序是
A.Y>Z>X B.X>Y>Z C.X >Z>Y D.Y>X>Z
10.有X、Y、Z三种金属,只有Y在自然界主要以单质形式存在,如果把X放入含Z的化合物溶液中,X表面有Z析出。据此判断这三种金属的活动性由强到弱的顺序为( )
A.Y、X、Z
B.Z、X、Y
C.Y、Z、X
D.X、Z、Y
11.为了验证“Fe,Cu,Ag三种金属的活动性由强到弱”,小明设计了如图所示的实验,其中可以达到实验目的组合是
A.②③④ B.①③⑤ C.①②③ D.①②⑥
12.某金属加工厂生产过程中的废液含有少量的硝酸银和硝酸铜,为回收利用资源和防止污染,该厂向废液中加入一定量的铁粉,反应停止后过滤,向滤渣中加入少量的稀盐酸,有气泡产生,则下列有关说法正确的是
A.滤出的固体中一定含有银,可能含有铜
B.滤出的固体中一定含有银和铜
C.滤液中一定含有硝酸亚铁,一定没有硝酸银,可能含有硝酸铜
D.滤液中一定含有硝酸亚铁,一定没有硝酸铜,可能含有硝酸银
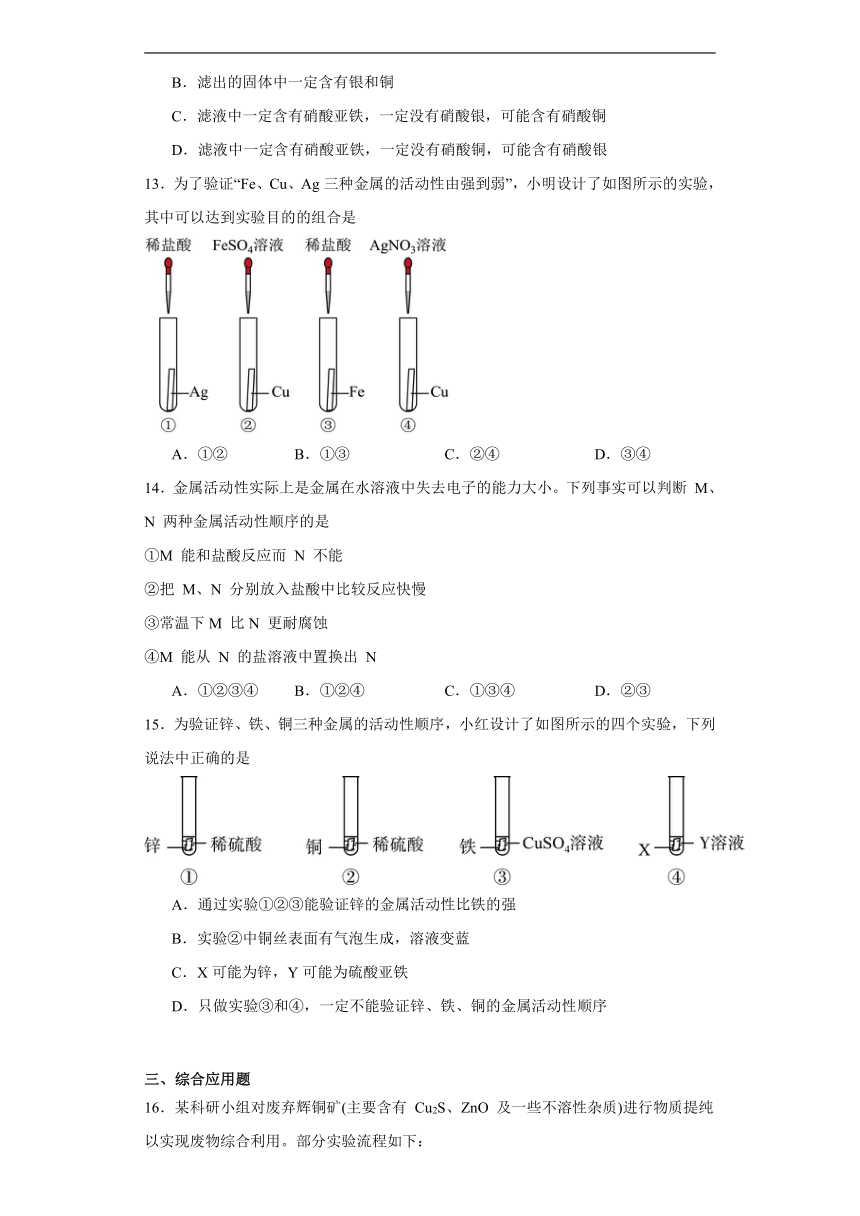
13.为了验证“Fe、Cu、Ag三种金属的活动性由强到弱”,小明设计了如图所示的实验,其中可以达到实验目的的组合是
A.①② B.①③ C.②④ D.③④
14.金属活动性实际上是金属在水溶液中失去电子的能力大小。下列事实可以判断 M、N 两种金属活动性顺序的是
①M 能和盐酸反应而 N 不能
②把 M、N 分别放入盐酸中比较反应快慢
③常温下M 比N 更耐腐蚀
④M 能从 N 的盐溶液中置换出 N
A.①②③④ B.①②④ C.①③④ D.②③
15.为验证锌、铁、铜三种金属的活动性顺序,小红设计了如图所示的四个实验,下列说法中正确的是
A.通过实验①②③能验证锌的金属活动性比铁的强
B.实验②中铜丝表面有气泡生成,溶液变蓝
C.X可能为锌,Y可能为硫酸亚铁
D.只做实验③和④,一定不能验证锌、铁、铜的金属活动性顺序
三、综合应用题
16.某科研小组对废弃辉铜矿(主要含有 Cu2S、ZnO 及一些不溶性杂质)进行物质提纯以实现废物综合利用。部分实验流程如下:
请根据上述实验流程回答下列问题:
⑴ “焙烧”(加热而又不使熔化)中生成CuO和SO2,该气体直接排放会使雨水pH小于 ,形成酸雨。
⑵ “酸浸”时发生的反应类型是 。
⑶ “置换”时反应的方程式为 (写出一个即可)。滤渣2的成分为 (填化学式)。
⑷ “氧化”时高锰酸钾溶液和双氧水(过氧化氢溶液)都能将Fe2+氧化为Fe3+,从绿色化学角度考虑物质A选用 较合适。
⑸ 聚合硫酸铁常用于净水,其化学式可表示为[Fea(OH)b(SO4)c]n。实验测得某聚合硫酸铁中铁离子与硫酸根离子的质量比为7∶15,则b∶a = 。
17.计算:
(1)硅钢是制变压器、充电器的核心材料,其主要成分是Fe和Si。取6.60g硅钢样品于烧杯中,将60.00g稀硫酸分6次加入样品中(其中稀硫酸与硅及其它杂质不反应)。实验测得相关数据如表:
第1次 第2次 第3次 第4次 第5次 第6次
稀硫酸的质量 10.00g 10.00g 10.00g 10.00g 10.00g 10.00g
剩余固体质量 5.48g Wg 3.24g 2.12g 1.00g 1.00g
①根据表中数据判断,稀硫酸加入到第 次,铁恰好反应完全。
②表中W= g;6.60g硅钢样品中含铁的质量为 g。
③计算该硅钢与稀硫酸充分反应后共产生多少g氢气。 (写出详细过程)
(2)运用手持技术探究金属与酸的反应。向烧瓶内注入等量等浓度的稀硫酸,分别剪取长约0.4cm、宽约0.4cm的镁、铁、铜金属条,打磨后投入烧瓶中,迅速塞紧带有压强传感器的橡皮塞(见图),点击采集得到如图所示的气压变化曲线。回答下列问题:
①金属Cu对应的曲线是 。
②曲线c在40s左右达到最高点后又略微下降的原因是 。
18.金属在人类生产中的应用十分广泛。
(1)三星堆遗址的Ⅱ号青铜神树引人注目,铸造铜树时,在铜中加入锡和铅会使材料的熔点 (选填“降低”、“升高”)。
(2)如图为锌与硫酸镍和硫酸锰混合溶液充分反应后粒子变化微观示意图。
①Ni、Zn、Mn三种金属活动性由强到弱的顺序 。
②反应后溶液的质量会 (填“增大”或“减小”)。
(3)化学小组的同学收集到一些含硝酸银、硝酸铜的混合废液,同学们向其中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色。则下列有关判断正确的是___________(填字母)。
A.滤渣中一定有银,没有铜和锌
B.滤渣中一定有银和锌,可能有铜
C.滤液中一定有硝酸锌、硝酸铜、硝酸银
D.滤液中一定有硝酸锌、硝酸铜,可能有硝酸银
(4)2022年全国钢铁产量高达10亿多万吨。铁的冶炼是化学研究的重要范畴。取12g Fe2O3粉末,小组同学用如下图装置模拟炼铁,并测定反应后固体的成分。
资料:CH4具有还原性,能与Fe2O3反应生成CO2、H2O和铁单质或铁的氧化物。
a.连接装置,先 ,再装入药品
b.反应中循环使用CH4的目的是 。
c.若生成物充分被B、C装置吸收,B、C装置增加的质量比为 。
d.控温加热一段时间后,继续通CH4至冷却,称得A中剩余固体为8.8g,若固体成分为Fe和FeO,则剩余固体中FeO的质量为 g。
(5)2023年4月24日是第八个“中国航天日”。神舟十五号飞船成功发射,实现了“格物致知,叩问苍穹”的航空主题。
a.飞船进入太空后,白天太阳能电池板打开给电池充电,储存能量,夜间利用电池能量运行,电池在该过程中的能量转化形式为:太阳能→ →电能。
b.飞船返回舱使用了钛合金等复合金属材料制成的“避火衣”,钛合金中的钛(Ti),一般用过量的镁在加热的条件下与TiCl4反应制得金属钛,发生反应的化学方程式为 。
参考答案:
1.AC
2.AD
3.CD
4.BD
5.BC
6.B
7.D
8.A
9.B
10.D
11.D
12.B
13.C
14.B
15.C
16. 5.6 复分解反应 Fe+H2SO4 ==FeSO4 +H2↑或Fe+CuSO4==Cu+FeSO4 Fe、Cu 双氧水 1:2(或0.5)
17.(1) 5 4.36 5.60 解:设该硅钢与稀硫酸充分反应后共产生氢气的质量为x
x=0.2g
答:该硅钢与稀硫酸充分反应后共产生氢气的质量为0.2g
(2) a 镁与稀硫酸反应放热,在约40s时反应结束,温度降低
18.(1)降低
(2) Mn、Zn、Ni 增大
(3)D
(4) 检查装置气密性 充分利用资源 9:11 1.8
(5) 化学能
一、多选题
1.下列有关做法正确的是
A.区别水和过氧化氢溶液,可以各取少量分别放入试管中,再加入等量的MnO2,并在瓶口放一个带火星的木条看是否复燃
B.除去铁粉中混入的镁粉,将混合物放入足量的稀硫酸中,充分反应后过滤
C.氧化钙和氢氧化钙可以通过取样加入水来进行鉴别
D.向某固体物质中加入盐酸,观察到有气泡产生,则该物质一定是较活泼金属
2.下列解释错误的是
A.铝制品不用涂任何保层来防腐,因为铝不与空气反应
B.铁丝在空气不能被点燃与空气中氧气的体积分数有关
C.生铁和钢的性能不同与它们的组成中含碳量不同有关
D.新轿车中常弥漫着皮革气味。从分子角度看,这是构成物质的分子大小不同的结果
3.向AgNO3和Cu(NO3)2的混合液中加入一定量的Fe、Cu的混合粉末,充分反应后过滤、洗涤,得到滤液和滤渣。下列说法正确的是( )
A.向滤液中加入KCl溶液,无明显现象,则滤液中一定有Fe(NO3)2、Cu(NO3)2,滤渣中可能有Fe、Cu
B.当滤液为蓝色时,滤渣中一定有Cu、Ag,一定没有Fe
C.向滤渣中加入盐酸,有气泡产生,则滤渣中一定有Fe、Cu、Ag
D.滤渣中一定有Ag,滤液中可能有Cu(NO3)2、AgNO3
4.下列图像能正确反映其对应操作中各量变化关系的是
A.加热高锰酸钾制氧气的实验,试管中固体的质量变化
B.向一定质量过氧化氢溶液中加入少量二氧化锰的实验,试管中水的质量变化
C.向一定质量的硫酸铜溶液中加入铁粉至过量的实验,试管中溶液的质量变化
D.分别向质量相等的镁和铁中加入相同的稀盐酸至过量的实验,生成H2的质量变化
5.除去下列物质中的杂质,所用试剂和方法均正确的是
物质 杂质 所用试剂或方法
A CO2 CO 点燃
B Cu Fe 足量的稀盐酸
C N2 O2 灼热的铜网
D 炭粉 MnO2 加水过滤
A.A B.B C.C D.D
二、选择题
6.下列说法符合客观事实的是
A.通常情况下铝制品耐腐蚀,原因是铝不易发生化学反应
B.氯酸钾中加入少量高锰酸钾加热,发现产生氧气的速率会加快
C.巴黎圣母院失火,消防队员用水灭火是为了降低可燃物的着火点
D.将燃着的木条伸入呼出气体中会熄灭,说明呼出气体中二氧化碳含量大于空气
7.将一定质量的铁粉放入硝酸锌和硝酸铜的混合溶液中,充分反应后过滤,得到滤液和滤渣。下列有关滤液和滤渣的说法正确的是
A.滤渣中一定有Cu,可能有Zn、Fe
B.滤渣中一定有Cu、Zn,可能有Fe
C.如果滤液中有Cu(NO3)2,则滤渣的成分可能是Cu,Fe
D.滤液中一定有Fe(NO3)2、Zn(NO3)2,可能有Cu(NO3)2
8.有X、Y、Z三种金属,把Y投入X(NO3)2溶液中,Y表面有X析出,溶液质量增大;把X投入Z(NO3)2溶液中,得到X(NO3)2,固体质量增大。下列判断错误的是
A.X、Y、Z可能依次是:Cu、Fe、Ag
B.元素的相对原子质量可能是:Z>Y>X
C.金属活动性顺序是:Y>X>Z
D.X、Y、Z可能依次是:Fe、Zn、Hg
9.有X、Y、Z三种金属,若将X、Y、Z分别放入一定质量的稀盐酸中,只有X表面产生气泡:若将Z放到Y(NO3)2溶液中,Z表面无现象,则X、Y、Z三种金属活动性顺序是
A.Y>Z>X B.X>Y>Z C.X >Z>Y D.Y>X>Z
10.有X、Y、Z三种金属,只有Y在自然界主要以单质形式存在,如果把X放入含Z的化合物溶液中,X表面有Z析出。据此判断这三种金属的活动性由强到弱的顺序为( )
A.Y、X、Z
B.Z、X、Y
C.Y、Z、X
D.X、Z、Y
11.为了验证“Fe,Cu,Ag三种金属的活动性由强到弱”,小明设计了如图所示的实验,其中可以达到实验目的组合是
A.②③④ B.①③⑤ C.①②③ D.①②⑥
12.某金属加工厂生产过程中的废液含有少量的硝酸银和硝酸铜,为回收利用资源和防止污染,该厂向废液中加入一定量的铁粉,反应停止后过滤,向滤渣中加入少量的稀盐酸,有气泡产生,则下列有关说法正确的是
A.滤出的固体中一定含有银,可能含有铜
B.滤出的固体中一定含有银和铜
C.滤液中一定含有硝酸亚铁,一定没有硝酸银,可能含有硝酸铜
D.滤液中一定含有硝酸亚铁,一定没有硝酸铜,可能含有硝酸银
13.为了验证“Fe、Cu、Ag三种金属的活动性由强到弱”,小明设计了如图所示的实验,其中可以达到实验目的的组合是
A.①② B.①③ C.②④ D.③④
14.金属活动性实际上是金属在水溶液中失去电子的能力大小。下列事实可以判断 M、N 两种金属活动性顺序的是
①M 能和盐酸反应而 N 不能
②把 M、N 分别放入盐酸中比较反应快慢
③常温下M 比N 更耐腐蚀
④M 能从 N 的盐溶液中置换出 N
A.①②③④ B.①②④ C.①③④ D.②③
15.为验证锌、铁、铜三种金属的活动性顺序,小红设计了如图所示的四个实验,下列说法中正确的是
A.通过实验①②③能验证锌的金属活动性比铁的强
B.实验②中铜丝表面有气泡生成,溶液变蓝
C.X可能为锌,Y可能为硫酸亚铁
D.只做实验③和④,一定不能验证锌、铁、铜的金属活动性顺序
三、综合应用题
16.某科研小组对废弃辉铜矿(主要含有 Cu2S、ZnO 及一些不溶性杂质)进行物质提纯以实现废物综合利用。部分实验流程如下:
请根据上述实验流程回答下列问题:
⑴ “焙烧”(加热而又不使熔化)中生成CuO和SO2,该气体直接排放会使雨水pH小于 ,形成酸雨。
⑵ “酸浸”时发生的反应类型是 。
⑶ “置换”时反应的方程式为 (写出一个即可)。滤渣2的成分为 (填化学式)。
⑷ “氧化”时高锰酸钾溶液和双氧水(过氧化氢溶液)都能将Fe2+氧化为Fe3+,从绿色化学角度考虑物质A选用 较合适。
⑸ 聚合硫酸铁常用于净水,其化学式可表示为[Fea(OH)b(SO4)c]n。实验测得某聚合硫酸铁中铁离子与硫酸根离子的质量比为7∶15,则b∶a = 。
17.计算:
(1)硅钢是制变压器、充电器的核心材料,其主要成分是Fe和Si。取6.60g硅钢样品于烧杯中,将60.00g稀硫酸分6次加入样品中(其中稀硫酸与硅及其它杂质不反应)。实验测得相关数据如表:
第1次 第2次 第3次 第4次 第5次 第6次
稀硫酸的质量 10.00g 10.00g 10.00g 10.00g 10.00g 10.00g
剩余固体质量 5.48g Wg 3.24g 2.12g 1.00g 1.00g
①根据表中数据判断,稀硫酸加入到第 次,铁恰好反应完全。
②表中W= g;6.60g硅钢样品中含铁的质量为 g。
③计算该硅钢与稀硫酸充分反应后共产生多少g氢气。 (写出详细过程)
(2)运用手持技术探究金属与酸的反应。向烧瓶内注入等量等浓度的稀硫酸,分别剪取长约0.4cm、宽约0.4cm的镁、铁、铜金属条,打磨后投入烧瓶中,迅速塞紧带有压强传感器的橡皮塞(见图),点击采集得到如图所示的气压变化曲线。回答下列问题:
①金属Cu对应的曲线是 。
②曲线c在40s左右达到最高点后又略微下降的原因是 。
18.金属在人类生产中的应用十分广泛。
(1)三星堆遗址的Ⅱ号青铜神树引人注目,铸造铜树时,在铜中加入锡和铅会使材料的熔点 (选填“降低”、“升高”)。
(2)如图为锌与硫酸镍和硫酸锰混合溶液充分反应后粒子变化微观示意图。
①Ni、Zn、Mn三种金属活动性由强到弱的顺序 。
②反应后溶液的质量会 (填“增大”或“减小”)。
(3)化学小组的同学收集到一些含硝酸银、硝酸铜的混合废液,同学们向其中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色。则下列有关判断正确的是___________(填字母)。
A.滤渣中一定有银,没有铜和锌
B.滤渣中一定有银和锌,可能有铜
C.滤液中一定有硝酸锌、硝酸铜、硝酸银
D.滤液中一定有硝酸锌、硝酸铜,可能有硝酸银
(4)2022年全国钢铁产量高达10亿多万吨。铁的冶炼是化学研究的重要范畴。取12g Fe2O3粉末,小组同学用如下图装置模拟炼铁,并测定反应后固体的成分。
资料:CH4具有还原性,能与Fe2O3反应生成CO2、H2O和铁单质或铁的氧化物。
a.连接装置,先 ,再装入药品
b.反应中循环使用CH4的目的是 。
c.若生成物充分被B、C装置吸收,B、C装置增加的质量比为 。
d.控温加热一段时间后,继续通CH4至冷却,称得A中剩余固体为8.8g,若固体成分为Fe和FeO,则剩余固体中FeO的质量为 g。
(5)2023年4月24日是第八个“中国航天日”。神舟十五号飞船成功发射,实现了“格物致知,叩问苍穹”的航空主题。
a.飞船进入太空后,白天太阳能电池板打开给电池充电,储存能量,夜间利用电池能量运行,电池在该过程中的能量转化形式为:太阳能→ →电能。
b.飞船返回舱使用了钛合金等复合金属材料制成的“避火衣”,钛合金中的钛(Ti),一般用过量的镁在加热的条件下与TiCl4反应制得金属钛,发生反应的化学方程式为 。
参考答案:
1.AC
2.AD
3.CD
4.BD
5.BC
6.B
7.D
8.A
9.B
10.D
11.D
12.B
13.C
14.B
15.C
16. 5.6 复分解反应 Fe+H2SO4 ==FeSO4 +H2↑或Fe+CuSO4==Cu+FeSO4 Fe、Cu 双氧水 1:2(或0.5)
17.(1) 5 4.36 5.60 解:设该硅钢与稀硫酸充分反应后共产生氢气的质量为x
x=0.2g
答:该硅钢与稀硫酸充分反应后共产生氢气的质量为0.2g
(2) a 镁与稀硫酸反应放热,在约40s时反应结束,温度降低
18.(1)降低
(2) Mn、Zn、Ni 增大
(3)D
(4) 检查装置气密性 充分利用资源 9:11 1.8
(5) 化学能
同课章节目录
