8.3金属资源的利用和保护课时练习(含答案)人教版化学九年级下册
文档属性
| 名称 | 8.3金属资源的利用和保护课时练习(含答案)人教版化学九年级下册 |
|
|
| 格式 | docx | ||
| 文件大小 | 754.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-22 00:00:00 | ||
图片预览




文档简介
8.3 金属资源的利用和保护 课时练习
一、多选题
1.下列有关资源、能源、环保方面叙述正确的是
A.今年春节期间,哈市居民燃放烟花、爆竹明显减少,向空气中排放的PM2.5也会减少
B.海洋是地球上巨大的资源宝库,海水中含80多种矿物
C.回收废旧金属可以节约金属资源,但不能节约能源
D.人们正在利用和开发的能源有,氢能、太阳能、风能、水能、生物质能等
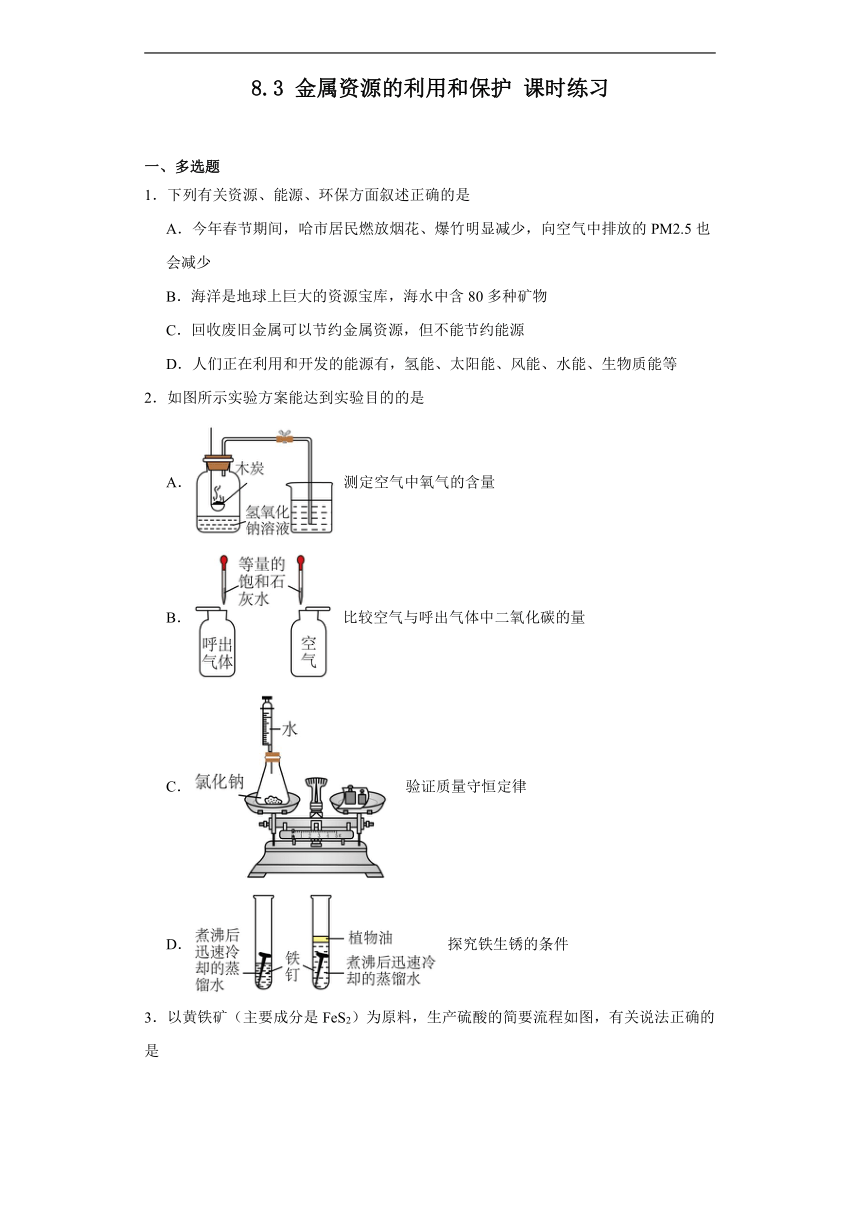
2.如图所示实验方案能达到实验目的的是
A. 测定空气中氧气的含量
B. 比较空气与呼出气体中二氧化碳的量
C. 验证质量守恒定律
D. 探究铁生锈的条件
3.以黄铁矿(主要成分是FeS2)为原料,生产硫酸的简要流程如图,有关说法正确的是
A.流程中SO2转化为SO3的化学方程式为2SO2 + O2=2SO3
B.炉渣(Fe2O3)在工业上可用来炼铁
C.该流程图中生成物都是氧化物,生成过程必须防止泄漏产生污染
D.将黄铁矿粉碎,目的是增大接触面积,加快反应速率
4.炼铁的主要原料是赤铁矿(主要成分是Fe2O3)、焦炭、空气、石灰石,转化过程如图所示:下列有关说法正确的是
A.制得的生铁是纯净物
B.②中焦炭表现出的化学性质是还原性
C.③中发生反应的化学方程式是
D.世界上每年因腐蚀而报废的金属设备和材料相当于其年产量的20%~40%,铁制品在干燥的环境中锈蚀的更快
5.下列说法正确的是
A.足量的Al和Mg分别与等质量等浓度稀硫酸充分反应,生成H2的质量相等
B.等质量的CO和CO2,CO和CO2中氧元素的质量比为14:11
C.等质量的NaHCO3和MgCO3分别与足量稀盐酸充分反应,生成CO2的质量相等
D.用含氧化铁85%的赤铁矿石160t,理论上可炼出含杂质3%的生铁80t
二、选择题
6.下列图示实验能达到实验目的的是
A.①探究可燃物燃烧的条件 B.②验证二氧化碳与氢氧化钠溶液反应
C.③验证质量守恒定律 D.④探究铁钉生锈的条件
7.如图是某化学兴趣小组设计的观察铁制品锈蚀的实验装置。下列相关叙述中正确的是( )
①一段时间后,铁丝会由下向上出现锈蚀现象
②一段时间后,水面处铁丝锈蚀严重
③一段时间后,塑料瓶会变膨胀,因为铁生锈要放热
④一段时间后,塑料瓶会变瘪,因为铁生锈与空气有关
A.①② B.②④ C.②③ D.③④
8.树立环保意识,践行环境友好生活方式。下列做法中,不利于环境保护的是
A.植树造林 B.加快煤的开采与使用
C.绿色出行 D.生活垃圾分类处理
9.《郑州市城市生活垃圾分类管理办法》自2019年12月1日起施行。你用过的废旧电池应放入下列哪种图标的垃圾桶中
A. B.
C. D.
10.足量的CO还原10.0g工业铁红(主要成分是Fe2O3,还含有少量的FeO、Fe3O4),将生成的气通入足量的Ca(OH)2溶液中,产生15.0g沉淀。则此铁红中铁元素的质量分数是
A.32% B.20% C.76% D.85%
11.下列做法不符合“绿色环保、节能减排”理念的是
A.废旧电池深埋处理 B.使用太阳能景观灯
C.乘坐公共交通出行 D.循环利用教科书
12.控制变量法是实验探究的重要方法.利用如下图所示的对比实验不能实现探究目的是( )
A.甲图中①②对比可探究铁的锈蚀与植物油是否有关
B.甲图中①③对比可探究铁的锈蚀与水是否有关
C.乙图中(Ⅱ)(Ⅳ)对比可探究水能否让紫色石蕊浸泡后的干纸花变红
D.乙图中(Ⅲ)(Ⅳ)对比可探究二氧化碳能否让紫色石蕊浸泡后的干纸花变红
13.下列叙述中,依次是物理变化,化学变化,化学性质的是
A.切削金属;钢锭轧成钢条;一氧化碳可用于冶炼金属
B.石蜡受热熔化;食物变馊;酒精易燃
C.风力发电;铁生锈;红磷燃烧
D.木柴劈成块;西瓜榨成汁;高粱酿成酒
14.生活中废弃的铁锅、铝制易拉罐、铜线等可以归为一类加以回收利用,它们属于( )
A.铁矿石 B.金属或合金 C.氧化物 D.非金属单质
15.下列实验是对铁钉锈蚀条件进行探究,四支试管里面均放有一颗铁钉,其中铁钉锈蚀最慢的是
A. B.
C. D.
三、综合应用题
16.(1)下图装置可做一氧化碳还原氧化铁的实验,并检验生成的气体产物。
①B装置玻璃管里可观察到的现象是 ;写出B装置内发生反应的化学方程式 。
②C装置中反应的化学方程式为 。
(2)实验室利用如图装置可制取干燥的氧气。
①A中发生反应的的化学方程式为 。
②试剂X为 。
③若用C装置收集氧气,请将C装置中导管补画完整 。
(3)取12.5g石灰石于装置A中,向其中加入100g足量的稀盐酸,充分反应后(杂质不参加反应),A中固液混合物的质量为108.1g,请计算该石灰石中碳酸钙的质量分数 。
17.金属与人类的生产、生活密切相关,牢固掌握金属的知识非常重要。
(1)铝和铁都是我们生活中常见的金属,铝耐腐蚀性能比铁好的原因是 。
(2)如图是一氧化碳还原氧化铁的实验装置,请回答下列问题。
①玻璃管A中的实验现象是 。
②实验开始时,先通入一氧化碳的原因是 。
③从环保角度考虑,还需对以上装置进行改进,请简述改进措施 。
(3)为了验证Fe、Cu、Ag三种金属的活动性顺序,请你写出两种可行方案所需的物质。
方案一:
方案二:
(4)若除去FeCl2溶液中杂质CuCl2,请写出有关的化学方程式。
(5)实验室在高温条件下,用足量一氧化碳还原10g赤铁矿,充分反应后,测得生成的纯铁的质量为5.6g。则该赤铁矿中氧化铁的质量分数是 。
18.早在春秋战国时期,我国就开始生产和使用铁器。工业上炼铁的原理是利用CO和氧化铁的反应。某化学兴趣小组利用下图装置进行实验探究,请按要求填空:
(1)硬质玻璃管A中反应的现象为 ;实验中看到B中澄清石灰水变浑浊的化学方程式 ;
(2)实验开始时要先通入CO的目的是 ;反应结束后继续通入CO的目的是 ;
(3)盛满石灰水的B装置在此实验中的作用有如下说法:①收集多余的一氧化碳 ②检验并吸收反应生成的二氧化碳,上述说法中正确的是 。
A 只有① B 只有② C 是①和②
(4)以硫铁矿(主要成分是二硫化亚铁(FeS2)为原料可生产硫酸,炉渣回收可炼铁。其主要流程如图所示(反应条件已略去):
上述流程出现的物质中,硫元素显+6价的物质的氧化物是 。
(5)现有Fe2O3、CuO的混合粉末共8g于硬质玻璃管中,高温下与足量CO充分反应后,得到干燥固体的质量可能为 。(填字母)
A 5g B 6g C 7g
参考答案:
1.AD
2.AB
3.BD
4.BC
5.AC
6.B
7.B
8.B
9.C
10.C
11.A
12.A
13.B
14.B
15.A
16. 固体由红棕色逐渐变为黑色 浓硫酸 解:根据质量守恒定律
设石灰石中碳酸钙的质量分数为x
x=80%
答:石灰石中碳酸钙的质量分数为80%。
17. 铝和氧气反应生成一层致密的氧化铝保护膜,阻止了内部的铝被氧化 红色物质变成黑色 一氧化碳气体是可燃性气体,所以在点燃前要先通入一氧化碳气体使装置中的空气排净,然后再加热,防止气体不纯,加热时发生爆炸 一氧化碳能毒不能直接排放到空气中,在装置的最右端放一燃着的酒精灯 把铁丝、银丝分别伸入硫酸铜溶液中时,铁丝表面析出红色固体,是因为铁和硫酸铜反应生成硫酸亚铁和铜,说明铁比铜活泼,银丝表面无明显现象,说明铜比银活泼,可选用Fe、CuSO4溶液、Ag 把铜丝分别伸入FeSO4溶液、AgNO3溶液中时,伸入硫酸亚铁溶液的铜丝表面无明显现象,说明铁比铜活泼,伸入硝酸银溶液中的铜丝表面析出银白色固体,说明铜比银活泼,可选用FeSO4溶液、Cu、AgNO3溶液 Fe+CuCl2=FeCl2+Cu 80%
18. 红色粉末变为黑色 CO2+Ca(OH)2=CaCO3↓+H2O 排尽空气,防止发生爆炸 保护铁,防止生成的铁被空气中的氧气氧化 C SO3 B
一、多选题
1.下列有关资源、能源、环保方面叙述正确的是
A.今年春节期间,哈市居民燃放烟花、爆竹明显减少,向空气中排放的PM2.5也会减少
B.海洋是地球上巨大的资源宝库,海水中含80多种矿物
C.回收废旧金属可以节约金属资源,但不能节约能源
D.人们正在利用和开发的能源有,氢能、太阳能、风能、水能、生物质能等
2.如图所示实验方案能达到实验目的的是
A. 测定空气中氧气的含量
B. 比较空气与呼出气体中二氧化碳的量
C. 验证质量守恒定律
D. 探究铁生锈的条件
3.以黄铁矿(主要成分是FeS2)为原料,生产硫酸的简要流程如图,有关说法正确的是
A.流程中SO2转化为SO3的化学方程式为2SO2 + O2=2SO3
B.炉渣(Fe2O3)在工业上可用来炼铁
C.该流程图中生成物都是氧化物,生成过程必须防止泄漏产生污染
D.将黄铁矿粉碎,目的是增大接触面积,加快反应速率
4.炼铁的主要原料是赤铁矿(主要成分是Fe2O3)、焦炭、空气、石灰石,转化过程如图所示:下列有关说法正确的是
A.制得的生铁是纯净物
B.②中焦炭表现出的化学性质是还原性
C.③中发生反应的化学方程式是
D.世界上每年因腐蚀而报废的金属设备和材料相当于其年产量的20%~40%,铁制品在干燥的环境中锈蚀的更快
5.下列说法正确的是
A.足量的Al和Mg分别与等质量等浓度稀硫酸充分反应,生成H2的质量相等
B.等质量的CO和CO2,CO和CO2中氧元素的质量比为14:11
C.等质量的NaHCO3和MgCO3分别与足量稀盐酸充分反应,生成CO2的质量相等
D.用含氧化铁85%的赤铁矿石160t,理论上可炼出含杂质3%的生铁80t
二、选择题
6.下列图示实验能达到实验目的的是
A.①探究可燃物燃烧的条件 B.②验证二氧化碳与氢氧化钠溶液反应
C.③验证质量守恒定律 D.④探究铁钉生锈的条件
7.如图是某化学兴趣小组设计的观察铁制品锈蚀的实验装置。下列相关叙述中正确的是( )
①一段时间后,铁丝会由下向上出现锈蚀现象
②一段时间后,水面处铁丝锈蚀严重
③一段时间后,塑料瓶会变膨胀,因为铁生锈要放热
④一段时间后,塑料瓶会变瘪,因为铁生锈与空气有关
A.①② B.②④ C.②③ D.③④
8.树立环保意识,践行环境友好生活方式。下列做法中,不利于环境保护的是
A.植树造林 B.加快煤的开采与使用
C.绿色出行 D.生活垃圾分类处理
9.《郑州市城市生活垃圾分类管理办法》自2019年12月1日起施行。你用过的废旧电池应放入下列哪种图标的垃圾桶中
A. B.
C. D.
10.足量的CO还原10.0g工业铁红(主要成分是Fe2O3,还含有少量的FeO、Fe3O4),将生成的气通入足量的Ca(OH)2溶液中,产生15.0g沉淀。则此铁红中铁元素的质量分数是
A.32% B.20% C.76% D.85%
11.下列做法不符合“绿色环保、节能减排”理念的是
A.废旧电池深埋处理 B.使用太阳能景观灯
C.乘坐公共交通出行 D.循环利用教科书
12.控制变量法是实验探究的重要方法.利用如下图所示的对比实验不能实现探究目的是( )
A.甲图中①②对比可探究铁的锈蚀与植物油是否有关
B.甲图中①③对比可探究铁的锈蚀与水是否有关
C.乙图中(Ⅱ)(Ⅳ)对比可探究水能否让紫色石蕊浸泡后的干纸花变红
D.乙图中(Ⅲ)(Ⅳ)对比可探究二氧化碳能否让紫色石蕊浸泡后的干纸花变红
13.下列叙述中,依次是物理变化,化学变化,化学性质的是
A.切削金属;钢锭轧成钢条;一氧化碳可用于冶炼金属
B.石蜡受热熔化;食物变馊;酒精易燃
C.风力发电;铁生锈;红磷燃烧
D.木柴劈成块;西瓜榨成汁;高粱酿成酒
14.生活中废弃的铁锅、铝制易拉罐、铜线等可以归为一类加以回收利用,它们属于( )
A.铁矿石 B.金属或合金 C.氧化物 D.非金属单质
15.下列实验是对铁钉锈蚀条件进行探究,四支试管里面均放有一颗铁钉,其中铁钉锈蚀最慢的是
A. B.
C. D.
三、综合应用题
16.(1)下图装置可做一氧化碳还原氧化铁的实验,并检验生成的气体产物。
①B装置玻璃管里可观察到的现象是 ;写出B装置内发生反应的化学方程式 。
②C装置中反应的化学方程式为 。
(2)实验室利用如图装置可制取干燥的氧气。
①A中发生反应的的化学方程式为 。
②试剂X为 。
③若用C装置收集氧气,请将C装置中导管补画完整 。
(3)取12.5g石灰石于装置A中,向其中加入100g足量的稀盐酸,充分反应后(杂质不参加反应),A中固液混合物的质量为108.1g,请计算该石灰石中碳酸钙的质量分数 。
17.金属与人类的生产、生活密切相关,牢固掌握金属的知识非常重要。
(1)铝和铁都是我们生活中常见的金属,铝耐腐蚀性能比铁好的原因是 。
(2)如图是一氧化碳还原氧化铁的实验装置,请回答下列问题。
①玻璃管A中的实验现象是 。
②实验开始时,先通入一氧化碳的原因是 。
③从环保角度考虑,还需对以上装置进行改进,请简述改进措施 。
(3)为了验证Fe、Cu、Ag三种金属的活动性顺序,请你写出两种可行方案所需的物质。
方案一:
方案二:
(4)若除去FeCl2溶液中杂质CuCl2,请写出有关的化学方程式。
(5)实验室在高温条件下,用足量一氧化碳还原10g赤铁矿,充分反应后,测得生成的纯铁的质量为5.6g。则该赤铁矿中氧化铁的质量分数是 。
18.早在春秋战国时期,我国就开始生产和使用铁器。工业上炼铁的原理是利用CO和氧化铁的反应。某化学兴趣小组利用下图装置进行实验探究,请按要求填空:
(1)硬质玻璃管A中反应的现象为 ;实验中看到B中澄清石灰水变浑浊的化学方程式 ;
(2)实验开始时要先通入CO的目的是 ;反应结束后继续通入CO的目的是 ;
(3)盛满石灰水的B装置在此实验中的作用有如下说法:①收集多余的一氧化碳 ②检验并吸收反应生成的二氧化碳,上述说法中正确的是 。
A 只有① B 只有② C 是①和②
(4)以硫铁矿(主要成分是二硫化亚铁(FeS2)为原料可生产硫酸,炉渣回收可炼铁。其主要流程如图所示(反应条件已略去):
上述流程出现的物质中,硫元素显+6价的物质的氧化物是 。
(5)现有Fe2O3、CuO的混合粉末共8g于硬质玻璃管中,高温下与足量CO充分反应后,得到干燥固体的质量可能为 。(填字母)
A 5g B 6g C 7g
参考答案:
1.AD
2.AB
3.BD
4.BC
5.AC
6.B
7.B
8.B
9.C
10.C
11.A
12.A
13.B
14.B
15.A
16. 固体由红棕色逐渐变为黑色 浓硫酸 解:根据质量守恒定律
设石灰石中碳酸钙的质量分数为x
x=80%
答:石灰石中碳酸钙的质量分数为80%。
17. 铝和氧气反应生成一层致密的氧化铝保护膜,阻止了内部的铝被氧化 红色物质变成黑色 一氧化碳气体是可燃性气体,所以在点燃前要先通入一氧化碳气体使装置中的空气排净,然后再加热,防止气体不纯,加热时发生爆炸 一氧化碳能毒不能直接排放到空气中,在装置的最右端放一燃着的酒精灯 把铁丝、银丝分别伸入硫酸铜溶液中时,铁丝表面析出红色固体,是因为铁和硫酸铜反应生成硫酸亚铁和铜,说明铁比铜活泼,银丝表面无明显现象,说明铜比银活泼,可选用Fe、CuSO4溶液、Ag 把铜丝分别伸入FeSO4溶液、AgNO3溶液中时,伸入硫酸亚铁溶液的铜丝表面无明显现象,说明铁比铜活泼,伸入硝酸银溶液中的铜丝表面析出银白色固体,说明铜比银活泼,可选用FeSO4溶液、Cu、AgNO3溶液 Fe+CuCl2=FeCl2+Cu 80%
18. 红色粉末变为黑色 CO2+Ca(OH)2=CaCO3↓+H2O 排尽空气,防止发生爆炸 保护铁,防止生成的铁被空气中的氧气氧化 C SO3 B
同课章节目录
