化学人教版(2019)必修第一册3.1.1铁及其化合物(共24张PPT)
文档属性
| 名称 | 化学人教版(2019)必修第一册3.1.1铁及其化合物(共24张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 26.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-23 00:00:00 | ||
图片预览





文档简介
(共24张PPT)
人教版高中化学必修1第三章 铁 金属材料铁及其化合物创设情境----人类是如何进入铁器时代的?
感受铁的存在
陨铁是陨石的一种,
含铁80%以上,常含镍。
其中铁以单质形式存在
创设情境----人类是如何进入铁器时代的?
感受铁的存在
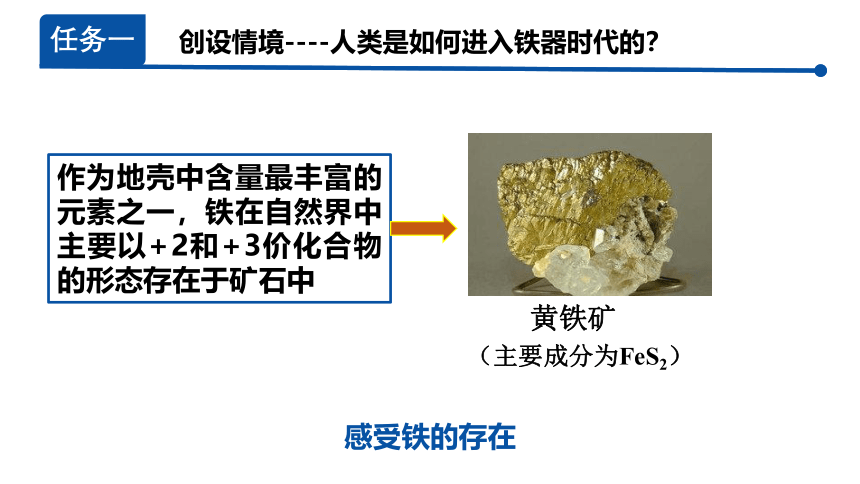
作为地壳中含量最丰富的元素之一,铁在自然界中主要以+2和+3价化合物的形态存在于矿石中
创设情境----人类是如何进入铁器时代的?
感受铁的存在
作为地壳中含量最丰富的元素之一,铁在自然界中主要以+2和+3价化合物的形态存在于矿石中
黄铁矿
(主要成分为FeS2)
创设情境----人类是如何进入铁器时代的?
感受铁的存在
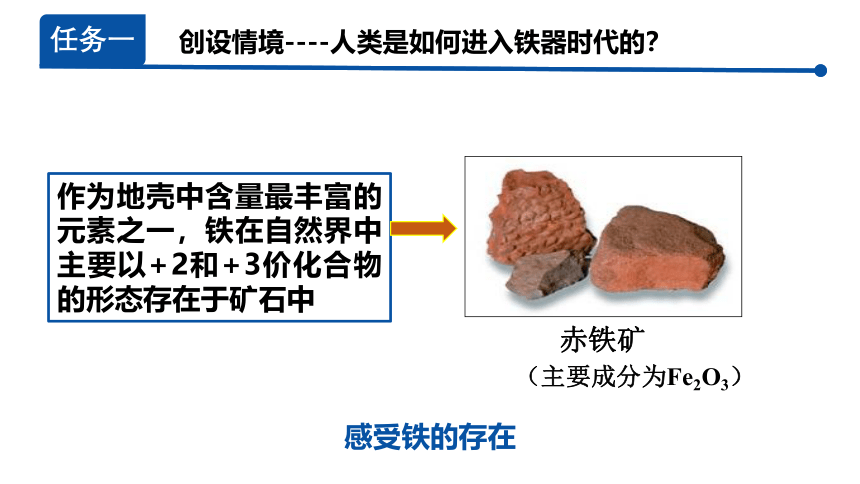
作为地壳中含量最丰富的元素之一,铁在自然界中主要以+2和+3价化合物的形态存在于矿石中
赤铁矿
(主要成分为Fe2O3)
创设情境----人类是如何进入铁器时代的?
感受铁的存在
作为地壳中含量最丰富的元素之一,铁在自然界中主要以+2和+3价化合物的形态存在于矿石中
磁铁矿
(主要成分为Fe3O4 )
创设情境----人类是如何进入铁器时代的?
感受铁的存在
作为地壳中含量最丰富的元素之一,铁在自然界中主要以+2和+3价化合物的形态存在于矿石中
菱铁矿( FeCO3 )
创设情境----人类是如何进入铁器时代的?
感受铁的存在
铁的存在形态
游离态
化合态
创设情境----人类是如何进入铁器时代的?
感受铁的存在
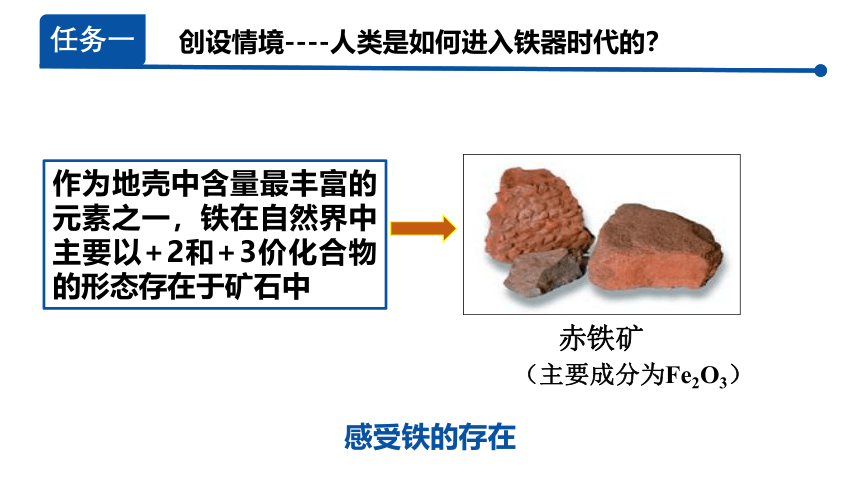
作为地壳中含量最丰富的元素之一,铁在自然界中主要以+2和+3价化合物的形态存在于矿石中
赤铁矿
(主要成分为Fe2O3)
创设情境----人类是如何进入铁器时代的?
工业高炉炼铁原理:高温条件下将铁从铁矿石中提炼出来
解密铁的单质
【资料卡片】铁是活泼的过渡元素,是一种光亮的银白色金属。纯铁相对较软,有良好的延展性和导热性,能导电,能被磁化,又可去磁。铁是生命过程中必须的元素,是血红蛋白的主要成分。
【问题】你能得出哪些铁的物理性质?
颜色 光泽 熔点 沸点 密度 导电性 导热性 延展性 特性 地壳含量
银白色 金属光泽 1535 ℃ 2750 ℃ 大 (7.86 g·cm-3) 良好 能被磁铁吸引 占第四位
解密铁的单质
【追问】铁的化学性质比较活泼,你可以尝试写出所学过的铁与一些物质的反应吗?铁的化合价发生了什么变化?体现了铁的什么化学性质?
铁的还原性
非金属单质 现象 化学方程式
O2
Cl2
3Fe+2O2 Fe3O4
点燃
2Fe+3Cl2 2FeCl3
点燃
铁生锈
剧烈燃烧,火星四射,生成黑色固体
剧烈燃烧,产生红棕色烟
铁丝在氯气中燃烧
铁丝在氧气中燃烧
解密铁的单质
(2)铁与非氧化性酸反应
(3)铁与盐反应
Fe+2H+=Fe2+ +H2↑
Fe+Cu2+=Fe2+ +Cu
铁丝与硫酸铜反应
铁丝与稀硫酸反应
Fe+S FeS
铁与非金属单质硫反应
铁丝与硫磺的反应
解密铁的单质
【问题探究】通过钠和水的反应,可知水是一种较弱的氧化剂。结合生活常识以及以下材料,预测水能氧化铁吗
【材料】在钢铁厂的生产中,炽热的铁水或钢水注入模具之前,模具必须进行充分的干燥处理,不得留有水(如图3 4)。
(4)铁与水蒸气的反应
3Fe+4H2O(g) ====Fe3O4+4H2
高温
解密铁的重要化合物——铁的氧化物
化学式 FeO Fe2O3 Fe3O4(FeO·Fe2O3)
俗名 \
颜色 状态
溶解性 物理性质对比
黑色粉末
红棕色粉末
黑色晶体
铁红
磁性氧化铁
均不溶于水
解密铁的重要化合物——铁的氧化物
物理性质对比
均不溶于水
丹霞地貌的岩层因含Fe2O3而呈红色
Fe2O3可作墙外涂料
价态观
解密铁的重要化合物——铁的氧化物
化学性质对比
价态未变
碱性氧化物
FeO+2H+=Fe2++H2O
Fe2O3+6H+=2Fe3++3H2O
与某些还原剂反应
还原性
价态改变
氧化性
C、H2、CO、HI
与某些氧化剂反应
Fe2O3+3CO 2Fe+3CO2
高温
分类观
价态观
Fe2O3+6H+ +2I- =2Fe2+ +I2+3H2O
分类观
Fe3O4+8H+=Fe2++2Fe3++4H2O
FeO+2H+=Fe2++H2O
Fe2O3+6H+=2Fe3++3H2O
Fe3O4+8H+=Fe2++2Fe3++4H2O
6FeO+O2 2Fe3O4
解密铁的重要化合物——铁的氢氧化物
【实验3-1】在两支试管中分别加入少量的FeCl3溶液和FeSO4溶液,然后各滴入NaOH溶液。观察并描述发生的现象。
4Fe(OH)2+O2 +2H2O =4Fe(OH)3
FeSO4+2NaOH =Fe(OH)2 +Na2SO4
2Fe(OH)3 Fe2O3+2H2O
解密铁的重要化合物——铁的氢氧化物
氧化性
1
2
四 性
4Fe(OH)2+O2+2H2O =4Fe(OH)3
分类观
碱性
Fe(OH)3+3H+=Fe3++3H2O
价态观
Fe(OH)2+2H+=Fe2++2H2O
还原性
Fe(OH)3+H++I-→Fe2++ I2+ H2O
3
热稳定性
2Fe(OH)3 Fe2O3+3H2O
Fe(OH)2 FeO+H2O(隔绝氧气)
4Fe(OH)2+O2 Fe2O3+4H2O
1.有关铁的叙述中不正确的是( )
A.铁能被磁铁吸引 B.人体的血红蛋白中含有铁元素
C.在空气中能剧烈燃烧 D.铁能与水蒸气反应
【解析】A.铁能被磁铁吸引,A项说法正确;B.人体的血红蛋白中含有铁元素,B项说法正确;C.铁在氧气中能剧烈燃烧,在空气中不燃烧。故C项错误;D.铁能与水蒸气在高温条件下反应生成四氧化三铁和氢气,故D说法正确;故答案为C。
C
2、某学生以铁丝和Cl2为原料进行下列三个实验。从分类角度分析,下列说法正确的是( )
A.实验①②所涉及的物质均为电解质
B.实验①③发生的均为离子反应
C.实验②③均未发生氧化还原反应
D.实验①③反应制得的物质均为纯净物
C
存在形态
物理性质
化学性质
用途
化合态
游离态
熔沸点高、导热、导电、延展性、可以被磁铁吸引
与O2、Cl2、S反应;与H2O反应;与酸反应;与盐反应
还原剂
脱氧剂
人教版高中化学必修1第三章 铁 金属材料铁及其化合物创设情境----人类是如何进入铁器时代的?
感受铁的存在
陨铁是陨石的一种,
含铁80%以上,常含镍。
其中铁以单质形式存在
创设情境----人类是如何进入铁器时代的?
感受铁的存在
作为地壳中含量最丰富的元素之一,铁在自然界中主要以+2和+3价化合物的形态存在于矿石中
创设情境----人类是如何进入铁器时代的?
感受铁的存在
作为地壳中含量最丰富的元素之一,铁在自然界中主要以+2和+3价化合物的形态存在于矿石中
黄铁矿
(主要成分为FeS2)
创设情境----人类是如何进入铁器时代的?
感受铁的存在
作为地壳中含量最丰富的元素之一,铁在自然界中主要以+2和+3价化合物的形态存在于矿石中
赤铁矿
(主要成分为Fe2O3)
创设情境----人类是如何进入铁器时代的?
感受铁的存在
作为地壳中含量最丰富的元素之一,铁在自然界中主要以+2和+3价化合物的形态存在于矿石中
磁铁矿
(主要成分为Fe3O4 )
创设情境----人类是如何进入铁器时代的?
感受铁的存在
作为地壳中含量最丰富的元素之一,铁在自然界中主要以+2和+3价化合物的形态存在于矿石中
菱铁矿( FeCO3 )
创设情境----人类是如何进入铁器时代的?
感受铁的存在
铁的存在形态
游离态
化合态
创设情境----人类是如何进入铁器时代的?
感受铁的存在
作为地壳中含量最丰富的元素之一,铁在自然界中主要以+2和+3价化合物的形态存在于矿石中
赤铁矿
(主要成分为Fe2O3)
创设情境----人类是如何进入铁器时代的?
工业高炉炼铁原理:高温条件下将铁从铁矿石中提炼出来
解密铁的单质
【资料卡片】铁是活泼的过渡元素,是一种光亮的银白色金属。纯铁相对较软,有良好的延展性和导热性,能导电,能被磁化,又可去磁。铁是生命过程中必须的元素,是血红蛋白的主要成分。
【问题】你能得出哪些铁的物理性质?
颜色 光泽 熔点 沸点 密度 导电性 导热性 延展性 特性 地壳含量
银白色 金属光泽 1535 ℃ 2750 ℃ 大 (7.86 g·cm-3) 良好 能被磁铁吸引 占第四位
解密铁的单质
【追问】铁的化学性质比较活泼,你可以尝试写出所学过的铁与一些物质的反应吗?铁的化合价发生了什么变化?体现了铁的什么化学性质?
铁的还原性
非金属单质 现象 化学方程式
O2
Cl2
3Fe+2O2 Fe3O4
点燃
2Fe+3Cl2 2FeCl3
点燃
铁生锈
剧烈燃烧,火星四射,生成黑色固体
剧烈燃烧,产生红棕色烟
铁丝在氯气中燃烧
铁丝在氧气中燃烧
解密铁的单质
(2)铁与非氧化性酸反应
(3)铁与盐反应
Fe+2H+=Fe2+ +H2↑
Fe+Cu2+=Fe2+ +Cu
铁丝与硫酸铜反应
铁丝与稀硫酸反应
Fe+S FeS
铁与非金属单质硫反应
铁丝与硫磺的反应
解密铁的单质
【问题探究】通过钠和水的反应,可知水是一种较弱的氧化剂。结合生活常识以及以下材料,预测水能氧化铁吗
【材料】在钢铁厂的生产中,炽热的铁水或钢水注入模具之前,模具必须进行充分的干燥处理,不得留有水(如图3 4)。
(4)铁与水蒸气的反应
3Fe+4H2O(g) ====Fe3O4+4H2
高温
解密铁的重要化合物——铁的氧化物
化学式 FeO Fe2O3 Fe3O4(FeO·Fe2O3)
俗名 \
颜色 状态
溶解性 物理性质对比
黑色粉末
红棕色粉末
黑色晶体
铁红
磁性氧化铁
均不溶于水
解密铁的重要化合物——铁的氧化物
物理性质对比
均不溶于水
丹霞地貌的岩层因含Fe2O3而呈红色
Fe2O3可作墙外涂料
价态观
解密铁的重要化合物——铁的氧化物
化学性质对比
价态未变
碱性氧化物
FeO+2H+=Fe2++H2O
Fe2O3+6H+=2Fe3++3H2O
与某些还原剂反应
还原性
价态改变
氧化性
C、H2、CO、HI
与某些氧化剂反应
Fe2O3+3CO 2Fe+3CO2
高温
分类观
价态观
Fe2O3+6H+ +2I- =2Fe2+ +I2+3H2O
分类观
Fe3O4+8H+=Fe2++2Fe3++4H2O
FeO+2H+=Fe2++H2O
Fe2O3+6H+=2Fe3++3H2O
Fe3O4+8H+=Fe2++2Fe3++4H2O
6FeO+O2 2Fe3O4
解密铁的重要化合物——铁的氢氧化物
【实验3-1】在两支试管中分别加入少量的FeCl3溶液和FeSO4溶液,然后各滴入NaOH溶液。观察并描述发生的现象。
4Fe(OH)2+O2 +2H2O =4Fe(OH)3
FeSO4+2NaOH =Fe(OH)2 +Na2SO4
2Fe(OH)3 Fe2O3+2H2O
解密铁的重要化合物——铁的氢氧化物
氧化性
1
2
四 性
4Fe(OH)2+O2+2H2O =4Fe(OH)3
分类观
碱性
Fe(OH)3+3H+=Fe3++3H2O
价态观
Fe(OH)2+2H+=Fe2++2H2O
还原性
Fe(OH)3+H++I-→Fe2++ I2+ H2O
3
热稳定性
2Fe(OH)3 Fe2O3+3H2O
Fe(OH)2 FeO+H2O(隔绝氧气)
4Fe(OH)2+O2 Fe2O3+4H2O
1.有关铁的叙述中不正确的是( )
A.铁能被磁铁吸引 B.人体的血红蛋白中含有铁元素
C.在空气中能剧烈燃烧 D.铁能与水蒸气反应
【解析】A.铁能被磁铁吸引,A项说法正确;B.人体的血红蛋白中含有铁元素,B项说法正确;C.铁在氧气中能剧烈燃烧,在空气中不燃烧。故C项错误;D.铁能与水蒸气在高温条件下反应生成四氧化三铁和氢气,故D说法正确;故答案为C。
C
2、某学生以铁丝和Cl2为原料进行下列三个实验。从分类角度分析,下列说法正确的是( )
A.实验①②所涉及的物质均为电解质
B.实验①③发生的均为离子反应
C.实验②③均未发生氧化还原反应
D.实验①③反应制得的物质均为纯净物
C
存在形态
物理性质
化学性质
用途
化合态
游离态
熔沸点高、导热、导电、延展性、可以被磁铁吸引
与O2、Cl2、S反应;与H2O反应;与酸反应;与盐反应
还原剂
脱氧剂
