3.4 分子间作用力 分子晶体 同步练习 (含解析) 2023-2024学年高二下学期化学苏教版(2019)选择性必修2
文档属性
| 名称 | 3.4 分子间作用力 分子晶体 同步练习 (含解析) 2023-2024学年高二下学期化学苏教版(2019)选择性必修2 |

|
|
| 格式 | docx | ||
| 文件大小 | 390.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-23 00:00:00 | ||
图片预览




文档简介
3.4 分子间作用力 分子晶体 同步练习 2023-2024学年高二下学期化学苏教版(2019)选择性必修2
一、单选题
1.下列物质中含有电子的是
A.铝粉 B.金刚石 C.液态氯化氢 D.冰醋酸
2.下列说法不正确的是
A.液晶是物质的一种聚集状态
B.“杯酚”分离和这个案例体现了超分子具有分子识别这个重要特征
C.等离子体具有良好的导电性和流动性是因为其含有带电粒子且能自由运动
D.人工合成反应:,所得X的中子数为2,此反应是化学变化
3.下列说法不正确的是
A.NaCl和晶体所含化学键的类型相同
B.和是同素异形体
C.干冰、二氧化硅均属于原子晶体
D.合成纤维是一类高分子化合物
4.下列晶体的熔点最低的是
A.干冰 B.冰 C.晶体硅 D.冰醋酸
5.分子晶体具有的本质特征是
A.晶体硬度小 B.熔融时不导电
C.晶体内微粒间以分子间作用力相结合 D.熔点一般比共价晶体低
6.短周期主族元素W、X、Y、Z的原子序数依次增大,其中X、Y、Z同周期,X原子的电子数等于Y原子的最外层电子数。W、X、Y形成的分子的结构如图所示。下列说法正确的是
A.电负性:W<X<Y<Z
B.W、Y、Z可形成离子晶体
C.Y与Z形成的化合物均可被强碱溶液吸收
D.W分别与Y、Z形成简单化合物的沸点:Y>Z
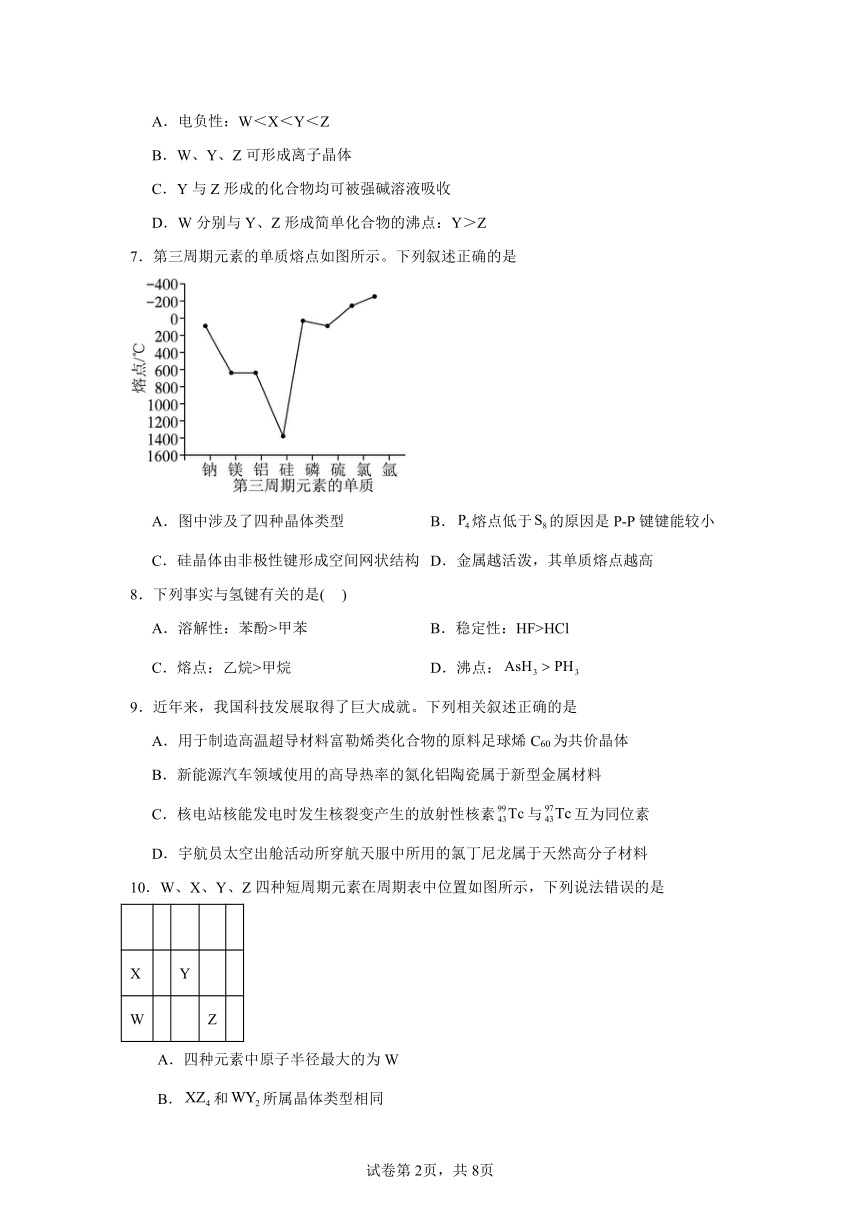
7.第三周期元素的单质熔点如图所示。下列叙述正确的是
A.图中涉及了四种晶体类型 B.熔点低于的原因是P-P键键能较小
C.硅晶体由非极性键形成空间网状结构 D.金属越活泼,其单质熔点越高
8.下列事实与氢键有关的是( )
A.溶解性:苯酚>甲苯 B.稳定性:HF>HCl
C.熔点:乙烷>甲烷 D.沸点:
9.近年来,我国科技发展取得了巨大成就。下列相关叙述正确的是
A.用于制造高温超导材料富勒烯类化合物的原料足球烯C60为共价晶体
B.新能源汽车领域使用的高导热率的氮化铝陶瓷属于新型金属材料
C.核电站核能发电时发生核裂变产生的放射性核素与互为同位素
D.宇航员太空出舱活动所穿航天服中所用的氯丁尼龙属于天然高分子材料
10.W、X、Y、Z四种短周期元素在周期表中位置如图所示,下列说法错误的是
X Y
W Z
A.四种元素中原子半径最大的为W
B.和所属晶体类型相同
C.X和W的氧化物都可以与NaOH溶液反应
D.W单质是重要的半导体材料
11.表中所列数据是对应物质的熔点,据此判断下列选项正确的是
物质 Na2O Na AlF3 AlCl3 Al2O3 BCl3 CO2 SiO2
熔点(℃) 920 97.8 1291 190 2073 -107 -57 1723
A.含有金属元素的晶体一定是离子晶体
B.AlF3和AlCl3晶体熔化时,克服的微粒间作用力类型相同
C.同族元素的氧化物不可能形成不同类型的晶体
D.金属晶体的熔点不一定比分子晶体的高
12.下列说法中正确的是
A.任何晶体中,若含有阳离子就一定有阴离子
B.方形容器中结出的冰是方形的,体现了晶体的自范性
C.气态物质不一定都是由分子组成的
D.接近水的沸点的水蒸气的相对分子质量测定值比按化学式计算出的要大一些,可以用范德华力解释这种异常性
13.下列说法正确的组合是
①晶体在不同方向上的硬度、导热性、导电性相同
②离子晶体都是化合物
③共价晶体中,共价键越强,熔点越高
④分子晶体中,分子间作用力越大,对应的物质越稳定
⑤金属晶体能导电的原因是在外加电场作用下可失去电子
⑥分子识别是超分子的重要特征之一
A.①②③ B.①④⑤ C.②③⑥ D.②④⑥
14.设NA为阿伏加德罗常数的值,下列叙述错误的是
A.含16 g氧原子的二氧化硅晶体中含有的键数目为2NA
B.58.5 gNaCl晶体中含有0.25NA个如图所示的结构单元
C.常温常压下,18 gH2O含有氢键数为2NA
D.标准状况下,22.4 LHF的分子数大于NA
15.判断有关说法正确的是
A.NaCl晶体熔化时,既要克服离子间作用力,又要克服分子间作用力
B.C60分子是有60个碳原子构成,所以C60属于原子晶体
C.CCl4中所有原子最外层都形成了8个电子的结构
D.MgCl2和NaOH所含有的化学键完全相同
16.下 列晶体性质的比较中不正确的是
A.熔点:金刚石>碳化硅>晶体硅
B.沸点: NH3>PH3
C.硬度: K>Na>Li
D.熔点: SiI4>SiBr4>SiCl4
17.根据下表中的有关数据分析,下列说法错误的是
AlCl3 SiCl4 晶体硼 金刚石 晶体硅
熔点/℃ 194 -70 2180 >3500 1410
沸点/℃ 181 57 3650 4827 2355
A.SiCl4、AlCl3是分子晶体
B.晶体硼是共价晶体
C.晶体硅是共价晶体
D.金刚石中的C-C键比晶体硅中的Si-Si键弱
18.下列类比或推理合理的是
已知 方法 结论
A 沸点:HBr>HCl 类比 沸点:HCl>HF
B 少量Cl2通入足量FeBr2溶液里,Fe2+先反应 类比 少量Cl2通入足量FeI2溶液里,Fe2+先反应
C 将盐酸与NaHCO3混合产生的气体直接通入硅酸钠溶液 推理 酸性:H2CO3>H2SiO3
D 曾青得铁化为铜 推理 金属性:Fe>Cu
A.A B.B C.C D.D
19.下列各物质中,按熔点由高到低的顺序排列正确的是
A.CH4>SiH4>GeH4>SnH4 B.KCl>NaCl>MgCl2>MgO
C.MgBr2<SiCl4<BN D.金刚石>晶体硅>钠
20.有关晶体的结构如图所示,下列说法中正确的是
A.在NaCl晶体中,距Cl-最近的Na有6个,距Na+最近且等距的Na+共6个
B.在CaF2晶体中,每个晶胞平均占有4个Ca2+,F-的配位数是4
C.在金刚石晶体中,每个碳原子被6个六元环共同占有,每个六元环最多有4个碳原子共面
D.该气态团簇分子的分子式为EF或FE
21.科学家在20℃时,将水置于足够强的电场中,水分子瞬间凝固成“暖冰”。对“暖冰”与其它物质比较正确的是
A.与Na2O晶体类型相同 B.与SiO2晶体类型相同
C.与CO2化学键类型相同 D.与普通的冰化学性质不同
22.目前,科学界拟合成一种“二重构造”的球形分子,即把“足球形”的C60熔进“足球形”的Si60分子中,外面的硅原子与里面的碳原子以共价键结合。下列关于这种分子的说法中不正确的是( )
A.是一种新型化合物 B.晶体属于分子晶体
C.是两种单质组成的混合物 D.相对分子质量为2400
23.钛有“二十一世纪的金属”、“全能金属”、“现代金属”的美称。镁与熔融的四氯化钛反应可制取钛:2Mg+TiCl42MgCl2+Ti。下列说法正确的是
A.基态Ti原子的价层电子排布式:3d4
B.Cl-结构示意图:
C.MgCl2的电子:
D.TiCl4熔点是-25℃,沸点是136.4℃,可溶于苯和CCl4,该晶体属于共价晶体
24.下列关于物质熔、沸点高低说法错误的是
A.的熔、沸点依次降低
B.分子晶体中共价键的键能越大,分子晶体的熔、沸点越高
C.的熔、沸点依次升高
D.比熔点高
25.某抗癌药物的结构简式如图所示,其中W、X、Y、Z是原子序数依次增大的短周期主族元素,W、Y同主族,Y、Z的最外层电子数之和是X的最外层电子数的2倍。下列叙述正确的是
A.W的最简单氢化物与Z的单质混合后可产生白烟
B.最高价氧化物对应的水化物酸性强弱Y>Z
C.简单氢化物的沸点:WD.Y、Z形成的化合物中,每个原子均满足8电子结构
二、填空题
26.晶体的个性
(1)绝大多数金属晶体是 的良导体, 性好。
(2)食盐为 晶体,质脆,熔融状态下 导电。
(3)金刚石为 晶体,无色透明、坚硬、质脆,常温下不导电。
(4)干冰属于 晶体,只能在低温下存在。
27.分子晶体与共价晶体
晶体类型 分子晶体 共价晶体
概念 分子间以 结合形成的晶体 相邻原子间以 相结合而形成空间网状结构
组成微粒 分子 原子
作用力 分子间作用力 共价键
常见的物质类型 大多数非金属单质 大多数共价化合物 少量非金属单质:金刚石、晶体硅;少量共价化合物:SiO2、SiC等
熔沸点 很大
硬度 很大
溶解性 部分溶于水 不溶于任何溶剂
导电性 固体和熔化状态都 ,部分溶于水导电 不导电,个别为半导体
影响作用力的因素 1.结构与组成相似的分子:分子量大→范德华力大→分子晶体的 就高 2.分子间有氢键的 升高,分子内有氢键的熔沸点 原子半径小→共价键长短→共价键能大→原子晶体的熔沸点高
28.(1)已知:碳化硅()是一种具有类似金刚石结构的晶体,其中碳原子和硅原子是交替排列的。在下列晶体:①晶体硅、②金刚石、③碳化硅、④干冰、⑤冰中,它们的熔点由高到低的顺序是 (填序号)。
(2)继后,科学家又合成了、。已知熔点:,而破坏分子所需要的能量:,其原因是 。
试卷第1页,共3页
参考答案:
1.A
【详解】A.铝是金属晶体,由铝离子和自由电子构成,A符合题意;
B.金刚石为共价(原子)晶体,不含电子,B不符合题意;
C.液态氯化氢由分子构成,C不符合题意;
D.冰醋酸为乙酸,由分子构成,D不符合题意;
故选A。
2.D
【详解】A.液晶是一种介于液态与结晶态之间的一种物质聚集状态,A正确;
B.“杯酚”分离C60和C70,是利用超分子的分子识别特征,B正确;
C.等离子体中含有大量能自由运动的带电粒子,具有良好的导电性和流动性,C正确;
D.反应过程遵循电荷数守恒、质量数守恒得为,所以X的中子数为4,且该反应是核反应不是化学反应,D错误;
故选D。
【点睛】
3.C
【详解】A.NaCl、MgCl2均为离子化合物,只含离子键,A正确;
B.C60、C70为碳元素的不同单质,互为同素异形体,B正确;
C.干冰(CO2)由分子构成,属于分子晶体,SiO2由原子构成,属于原子晶体,C错误;
D.合成纤维、合成树脂、合成橡胶属于三大合成高分子材料,D正确;
故答案选C。
4.A
【详解】干冰常温时为气体,冰常温时为液态,晶体硅为共价晶体,常温为固体,冰醋酸常温为液体,综合分析可知,干冰的熔点最低;
故选A。
5.C
【详解】分子晶体的熔、沸点较低,硬度较小,导致这些性质特征的本质原因是其构成微粒间的相互作用——分子间作用力,它相对于化学键来说是极其微弱的,C项符合题意。
6.B
【分析】X、Y、Z位于同周期,X原子的电子数等于Y原子的最外层电子数,说明X位于第二周期,即X、Y、Z位于第二周期,四种元素原子序数依次增大,以及根据结构图可知,W、X、Y、Z分别为H、B、N、O或F,据此分析;
【详解】A.根据上述分析,电负性:B<H<N<O或F,故A错误;
B.H、N、O或F可形成硝酸铵、氟化铵等离子晶体,故B正确;
C.NO为不成盐氧化物,不能被强碱溶液吸收,故C错误;
D.H2O或HF的沸点高于NH3,故D错误;
答案为B。
7.C
【详解】A.由图像可知,第三周期元素形成的单质中,钠、镁、铝是金属晶体,硅是共价晶体,磷、硫、氯、氩固体单质是分子晶体,共3种晶体类型,A错误;
B.分子晶体的熔点与共价键键能无关,与分子间作用力大小有关的相对分子质量大于,B错误;
C.硅晶体由硅硅键形成空间网状结构,C正确;
D.金属晶体熔点与金属键强弱有关,金属键强弱与金属离子带电荷数、离子半径有关。钠、镁、铝离子所带电荷数依次为1、2、3,离子半径依次减小,故金属键依次增强,熔点升高,D错误;
故选C。
8.A
【详解】A.苯酚与水分子之间存在氢键,而甲苯与水分子之间不存在氢键,所以溶解性:苯酚>甲苯,A正确;
B.稳定性与化学键强弱有关,与氢键无关,B错误;
C.分子间氢键可以使物质熔点升高,但乙烷和甲烷均不能形成分子间氢键,则两者熔点高低与氢键无关,C错误;
D.分子间氢键可以使物质沸点升高,但均不能形成分子间氢键,则两者沸点高低与氢键无关,D错误;
故答案为A。
9.C
【详解】A.足球烯C60是由C60分子通过分子间作用力形成的分子晶体,而不是共价晶体,A错误;
B.氮化铝陶瓷属于新型无机非金属材料,而不是金属材料,B错误;
C.同位素是指质子数相同而中子数不同的同一元素的不同原子间的关系,故与互为同位素,C正确;
D.氯丁尼龙属于合成纤维,属于合成高分子材料,而不是天然高分子材料,D错误;
故答案为:C。
10.B
【分析】根据元素在周期表中的位置可知, X为C元素,Y为O元素,W为Si元素,Z为Cl元素。
【详解】A.同周期元素从左到右半径依次减小,同主族元素从上到下半径依次增大,四种元素中原子半径最大的是Si,即W,A正确;
B.CCl4是分子晶体,SiO2是共价晶体,晶体类型不同,B错误;
C.CO2和SiO2都能与NaOH反应,CO2+2NaOH = Na2CO3+H2O、SiO2+2NaOH = Na2SiO3+H2O,C正确;
D.Si是重要的半导体材料,用于计算机芯片、太阳能电池等多项领域,D正确;
故选B。
11.D
【详解】A.金属晶体中含有金属元素,AlCl3是分子晶体,其也含有金属元素,所以含有金属元素的晶体不一定是离子晶体,故A错误;
B.属于分子晶体,熔点较低,熔化时破坏分子间作用力,属于离子晶体,熔点较高,熔化时破坏离子键,故B错误;
C.C和同主族,但其最高价氧化物的晶体类型不同,晶体和晶体分别属于分子晶体和共价晶体,所以同族元素的最高价氧化物可能形成不同类型的晶体,故C错误;
D.金属晶体的熔点有的很高,有的很低,如常温下汞呈液态,所以金属晶体的熔点不一定比分子晶体的高,故D正确;
答案D。
12.C
【详解】A.金属晶体中有阳离子和自由电子,没有阴离子,A错误;
B.在方形容器中结冰得到的方形外观并不是自发形成的,而是受限于容器形状形成的,所以没有体现自范性,B错误;
C.由阳离子、电子和电中性粒子组成的等离子体气态物质没有分子,C正确;
D.接近水的沸点的水蒸气中存在相当量的水分子因氢键而相互缔合形成所谓的缔合分子,所以相对分子质量测定值比按化学式计算出的要大一些,D错误;
故选C。
13.C
【详解】①晶体具有各向异性,所以晶体在不同方向上的硬度、导热性、导电性不同,①错误;
②离子晶体由常见的离子化合物形成的晶体,所以都是化合物,②正确;
③共价晶体熔化时需要破坏共价键,所以共价键越强,熔点越高,③正确;
④分子晶体中,分子间作用力越大,物质熔沸点越高,④错误;
⑤金属晶体能导电的原因是在外加电场作用下电子形成电子气,发生定向移动,⑤错误;
⑥分子识别是超分子的重要特征之一,⑥正确;
答案为:C。
14.C
【详解】A.16 g氧原子的物质的量为1 mol,由于1 mol二氧化硅中含2 mol氧原子,故含1 mol氧原子的二氧化硅的物质的量为0.5 mol,而二氧化硅中每个硅原子含4条σ键,故0.5 mol二氧化硅中含2NA条σ键,A正确;
B.在一个结构单元含有Na+:,含有Cl-: ,即1个结构单元中含有4个钠离子和4个氯离子。58.5 gNaCl的物质的量是1 mol,,所以含0.25NA个结构单元,B正确;
C.在冰晶体中,每个水分子与相邻的4个水分子形成氢键,每1个水分子平均形成2个氢键。18 gH2O的物质的量是1 mol,因此在1 mol冰中含有2NA个氢键。但在常温、常压下温度升高,冰变为液态水,部分氢键被破坏,故1 mol液体水的氢键数目小于2NA,C错误;
D.标准状况下HF是液体,22.4 LHF的物质的量大于1 mol,因此所含HF的分子数大于NA,D正确;
故合理选项是C。
15.C
【详解】A.氯化钠是离子晶体,晶体中只含有离子键,熔化时只需要克服离子键,故A错误;
B.碳60是由分子组成的分子晶体,故B错误;
C.四氯化碳分子中碳原子和氯原子的最外层都形成了8个电子的稳定结构,故C正确;
D.氯化镁和氢氧化钠都是离子晶体,氯化镁晶体中只含有离子键,氢氧化钠晶体中含有离子键和共价键,化学键类型不完全相同,故D错误;
故选C。
16.C
【详解】A.三种物质都是共价晶体,因为C的原子半径小于Si的,所以键长:C—C键C—Si键>Si—Si键,键能越大,共价晶体的熔点越高,A正确;
B.NH3和PH3都是分子晶体,但NH3分子间存在氢键,故NH3的沸点较高,B正确;
C.Li 、Na、 K位于同一主族,从上到下核电荷数递增、原子半径与离子半径递增,金属键的强度递减,则硬度:Li >Na> K,C错误;
D.卤化硅为分子晶体,它们的组成和结构相似,分子间不存在氢键,故相对分子质量越大,分子间作用力越大,熔点越高,D正确;
故答案选C。
17.D
【详解】A.根据表格数据可知SiCl4、AlCl3的熔沸点低,说明在晶体中构成微粒间的作用力十分微弱,由于分子间作用力比化学键弱得多,因此SiCl4、AlCl3都是分子晶体,A正确;
B.根据表格数据可知晶体硼熔沸点高,说明构成微粒的作用力很强,该物质属于共价晶体,B正确;
C.根据表格数据可知晶体硅熔沸点高,说明构成微粒的作用力很强,该物质属于共价晶体,C正确;
D.金刚石、晶体硅的熔沸点高,由于原子半径:C<Si,键长:C-C<Si-Si。键长越长,原子之间的共价键结合力就越弱,就越不牢固,越容易断裂,该化学键的键能就越小,故金刚石中的C-C键比晶体硅中的Si-Si键强,D错误;
故合理选项是D。
18.D
【详解】A.对于分子结构相似的物质,相对分子质量越大,分子间作用力就越强,物质的熔沸点就越高,沸点:HBr>HCl,但由于HF分子之间还存在氢键,增加了分子之间的吸引作用,导致HF的熔沸点比只有分子间作用力的HCl大,故沸点:HF>HCl,推理不符合事实,A错误;
B.由于还原性:Fe2+>Br->Cl-,所以少量Cl2通入足量FeBr2溶液里,Fe2+先反应,2Fe2++Cl2=2Fe3++2Cl-;但由于还原剂I->Fe2+,所以向足量FeI2溶液里通入少量Cl2,先发生反应:2I-+Cl2=I2+2Cl-,推理不符合事实,B错误;
C.由于酸性:HCl>H2CO3,所以将盐酸与NaHCO3混合,会发生反应:HCl+NaHCO3=NaCl+H2O+CO2↑,反应产生的气体CO2与Na2SiO3溶液发生反应:CO2+H2O+Na2SiO3=Na2CO3+H2SiO3↓,但盐酸具有挥发性,挥发的HCl也会与硅酸钠溶液发生反应:2HCl+Na2SiO3=2NaCl+H2SiO3↓,因此不能据此证明酸性:H2CO3>H2SiO3,C错误;
D.曾青主要成分是CuSO4,向其水溶液中加入Fe会发生反应:CuSO4+Fe=FeSO4+Cu,根据置换反应的规律可知元素的金属性:Fe>Cu,D正确;
故合理选项是D。
19.D
【详解】A.该组物质均为结构相似的分子晶体,其熔点取决于分子间作用力的大小,一般来说,结构相似的分子晶体,相对分子质量越大,分子间作用力也越大,故该组各物质熔点应为逐渐升高的顺序,A错误;
B.该组物质均为离子晶体,离子晶体熔点高低取决于离子键键能的大小,一般来说,离子的半径越小,电荷越多,离子键的键能就越大,故该组各物质熔点应为升高顺序,B错误;
C.SiCl4为分子晶体,MgBr2为离子晶体,BN为原子晶体,故熔点: SiCl4<MgBr2<BN,C错误;
D.金刚石和晶体硅属于原子晶体,钠属于离子晶体;原子晶体的熔点取决于共价键的键能,键能与键长成反比;金刚石C-C键的键长更短些,所以金刚石的熔点比晶体硅高,原子晶体的熔点一般比金属晶体的熔点高,则金刚石和晶体硅的熔点比钠的高;D正确;
故选D。
20.B
【详解】A.氯化钠晶体中,距Na+最近且等距的Cl-是6个,即钠离子的配位数是6;以底面左下角的钠离子为例,距Na+最近且相等的Na+位于面心处,共有=12个,选项A错误;
B.Ca2+位于晶胞顶点和面心,数目为8×+6×=4,即每个晶胞平均占有4个Ca2+;距离F-最近且等距的Ca2+有4个,即F-的配位数为4,选项B正确;
C.在金刚石的晶体结构中每个碳原子与周围的4个碳原子形成四个碳碳单键,最小的环为6元环,每个单键为3个环共有,则每个C原子连接4×3=12个六元环,晶胞中共平面的原子如图 ,共4个,选项C错误;
D.该气态团簇分子的分子含有4个E和4个F原子,则该气态团簇分子的分子式为E4F4或F4E4,选项D错误;
答案选B。
21.C
【详解】A.根据题意:在电场作用下,水分子瞬间凝固成“暖冰”,可知水分子间更易形成氢键,不存在离子键,是分子晶体,而Na2O晶体属于离子晶体,故A错误;
B.“暖冰”应该是分子晶体,而SiO2是共价晶体,故B错误;
C.“暖冰”中水分子的O-H是极性共价键,CO2分子内也只存在极性共价键,故C正确;
D.“暖冰”与普通冰的成分均为水分子,化学性质相同,故D错误;
故答案为C。
22.C
【详解】A.根据题意可知硅原子和碳原子之间形成了碳硅键,也就是形成了一种新的化合物,A正确;
B.根据题意“二重构造”的球形分子,说明该化合物为分子晶体,B正确;
C.该分子为两种元素形成的化合物而非混合物,C错误;
D.该物质的分子式为Si60C60,相对分子质量为2400,D正确;
正确选项C。
23.C
【详解】A.已知Ti是24号元素,故基态Ti原子的价层电子排布式:3d24s2,A错误;
B.Cl-的最外层上有8个电子,则Cl-结构示意图为:,B错误;
C.已知MgCl2是由Mg2+和Cl-通过离子键形成的离子化合物,则MgCl2的电子为:,C正确;
D.TiCl4熔点是-25℃,沸点是136.4℃,即熔沸点较低,可溶于苯和CCl4,该晶体属于分子晶体,共价晶体的熔沸点很高,一般不溶于任何溶剂中,D错误;
故答案为:C。
24.B
【详解】A.的熔、沸点随着原子序数的递增依次降低,A正确;
B.分子晶体的熔、沸点与分子间作用力和氢键有关,与化学键的键能无关,B错误;
C.分子间都不能形成氢键,分子间作用力依次增大,故它们的熔、沸点依次升高,C正确;
D.氧化镁和氯化钠都属于离子晶体,r(O2-)故选B。
25.A
【分析】由分子结构可知Y形成5个共价键,则Y原子最外层有5个电子,由于W、X、Y、Z是原子序数依次增大的短周期主族元素,W、Y同主族,则W是氮元素,Y是磷元素,Y、Z的最外层电子数之和是X的最外层电子数的2倍,磷的最外层有5个电子,Z最外层电子数也是奇数,X最外层电子数为偶数,结合都是短周期元素,则Z是氯元素,最外层有7个电子,所以X最外层电子数为(5+7)/2=6,原子序数比磷小,则X是氧元素。根据上述分析知:W是氮元素,X是氧元素,Y是磷元素,Z是氯元素。
【详解】A.W是氮元素,Z是氯元素,W的最简单氢化物NH3与Z的单质Cl2混合后会发生氧化还原反应(8NH3+3Cl2=6NH4Cl+N2),反应产生的NH4Cl在室温下呈固态,可以看到白烟现象,A项符合题意;
B.Y的最高价氧化物对应水化物为H3PO4,其为中强酸;Z的最高价氧化物对应水化物为HClO4,其为强酸,所以Z>Y,B项不符合题意;
C.对应的简单氢化物分别为W—NH3,Y—PH3,X—H2O,氨气和水的分子间均都有氢键,沸点较高,水在常温下呈液态而氨在常温下为气态,所以沸点顺序为H2O>NH3>PH3,即X>W>Y,C项不符合题意;
D.Y为P元素,可与氯形成PCl5,其中P不能满足8电子结构,D项不符合题意;
故正确选项为A
26. 电和热 延展 离子 能 共价 分子
【详解】不同类型的晶体因构成微粒及其粒子间的相互作用力的不同,常常表现出各自的特性。
(1)绝大多数的金属晶体是电和热的良导体,延展性好;
(2)食盐为离子晶体,质脆,熔融状态下能导电;
(3)金刚石为共价晶体 (原子晶体),无色透明,坚硬、质脆,常温下不导电;
(4)干冰属于分子晶体,只能在低温下存在。
27. 分子作用力 共价键 较小 较小 不导电 熔沸点 熔沸点 降低
【详解】分子晶体是只含有分子的晶体,分子间以分子间作用力结合形成的晶体,组成晶体的微粒是分子,分子与分子之间的作用力是分子间作用力,分子晶体的熔沸点一般都较低,硬度也较小,这是因为分子晶体熔沸点及硬度是由分子间作用力决定的,分子间作用力包括范德华力和氢键,分子间作用力很弱,约比化学键的键能小个数量级,结构与组成相似的分子,相对分子质量越大,范德华力大,分子晶体的熔沸点就高,氢键比范德华力要强的一种分子间作用力,能形成分子间氢键的分子晶体熔沸点升高,氢键有时也存在于分子内,形成分子内氢键的分子晶体熔沸点降低,属于分子晶体的物质类型包括大多数非金属单质、大多数共价化合物,有的分子晶体能溶于水,有的分子晶体不能溶于水,由于组成微粒是分子,所以固体和熔化状态都不导电,部分溶于水后导电;共价晶体中不存在分子,是相邻原子间以共价键相结合而形成空间网状结构的晶体。
28. ②③①⑤④ 一般情况下,对于组成与结构相似的分了晶体,分子晶体的相对分子质量越大,分子间作用力越强,熔化所需的能量越多,故熔点:;而破坏分子需断开化学键,元素电负性越强其形成的化学键越稳定,断键时所需能量越多,故破坏分子所需要的能量:
【详解】(1)题述晶体中属于共价晶体的是①②③,属于分子晶体的是④⑤。一般来说,共价晶体的熔点>分子晶体的熔点;对于共价晶体,键长:键>键键,相应键能:键键键,故熔点:金刚石>碳化硅>晶体硅。故答案为:②③①⑤④;
(2)分子晶体熔点与分子间作用力有关,而破坏分子则是破坏分子内的共价键。故答案为:一般情况下,对于组成与结构相似的分了晶体,分子晶体的相对分子质量越大,分子间作用力越强,熔化所需的能量越多,故熔点:;而破坏分子需断开化学键,元素电负性越强其形成的化学键越稳定,断键时所需能量越多,故破坏分子所需要的能量:。
答案第1页,共2页
一、单选题
1.下列物质中含有电子的是
A.铝粉 B.金刚石 C.液态氯化氢 D.冰醋酸
2.下列说法不正确的是
A.液晶是物质的一种聚集状态
B.“杯酚”分离和这个案例体现了超分子具有分子识别这个重要特征
C.等离子体具有良好的导电性和流动性是因为其含有带电粒子且能自由运动
D.人工合成反应:,所得X的中子数为2,此反应是化学变化
3.下列说法不正确的是
A.NaCl和晶体所含化学键的类型相同
B.和是同素异形体
C.干冰、二氧化硅均属于原子晶体
D.合成纤维是一类高分子化合物
4.下列晶体的熔点最低的是
A.干冰 B.冰 C.晶体硅 D.冰醋酸
5.分子晶体具有的本质特征是
A.晶体硬度小 B.熔融时不导电
C.晶体内微粒间以分子间作用力相结合 D.熔点一般比共价晶体低
6.短周期主族元素W、X、Y、Z的原子序数依次增大,其中X、Y、Z同周期,X原子的电子数等于Y原子的最外层电子数。W、X、Y形成的分子的结构如图所示。下列说法正确的是
A.电负性:W<X<Y<Z
B.W、Y、Z可形成离子晶体
C.Y与Z形成的化合物均可被强碱溶液吸收
D.W分别与Y、Z形成简单化合物的沸点:Y>Z
7.第三周期元素的单质熔点如图所示。下列叙述正确的是
A.图中涉及了四种晶体类型 B.熔点低于的原因是P-P键键能较小
C.硅晶体由非极性键形成空间网状结构 D.金属越活泼,其单质熔点越高
8.下列事实与氢键有关的是( )
A.溶解性:苯酚>甲苯 B.稳定性:HF>HCl
C.熔点:乙烷>甲烷 D.沸点:
9.近年来,我国科技发展取得了巨大成就。下列相关叙述正确的是
A.用于制造高温超导材料富勒烯类化合物的原料足球烯C60为共价晶体
B.新能源汽车领域使用的高导热率的氮化铝陶瓷属于新型金属材料
C.核电站核能发电时发生核裂变产生的放射性核素与互为同位素
D.宇航员太空出舱活动所穿航天服中所用的氯丁尼龙属于天然高分子材料
10.W、X、Y、Z四种短周期元素在周期表中位置如图所示,下列说法错误的是
X Y
W Z
A.四种元素中原子半径最大的为W
B.和所属晶体类型相同
C.X和W的氧化物都可以与NaOH溶液反应
D.W单质是重要的半导体材料
11.表中所列数据是对应物质的熔点,据此判断下列选项正确的是
物质 Na2O Na AlF3 AlCl3 Al2O3 BCl3 CO2 SiO2
熔点(℃) 920 97.8 1291 190 2073 -107 -57 1723
A.含有金属元素的晶体一定是离子晶体
B.AlF3和AlCl3晶体熔化时,克服的微粒间作用力类型相同
C.同族元素的氧化物不可能形成不同类型的晶体
D.金属晶体的熔点不一定比分子晶体的高
12.下列说法中正确的是
A.任何晶体中,若含有阳离子就一定有阴离子
B.方形容器中结出的冰是方形的,体现了晶体的自范性
C.气态物质不一定都是由分子组成的
D.接近水的沸点的水蒸气的相对分子质量测定值比按化学式计算出的要大一些,可以用范德华力解释这种异常性
13.下列说法正确的组合是
①晶体在不同方向上的硬度、导热性、导电性相同
②离子晶体都是化合物
③共价晶体中,共价键越强,熔点越高
④分子晶体中,分子间作用力越大,对应的物质越稳定
⑤金属晶体能导电的原因是在外加电场作用下可失去电子
⑥分子识别是超分子的重要特征之一
A.①②③ B.①④⑤ C.②③⑥ D.②④⑥
14.设NA为阿伏加德罗常数的值,下列叙述错误的是
A.含16 g氧原子的二氧化硅晶体中含有的键数目为2NA
B.58.5 gNaCl晶体中含有0.25NA个如图所示的结构单元
C.常温常压下,18 gH2O含有氢键数为2NA
D.标准状况下,22.4 LHF的分子数大于NA
15.判断有关说法正确的是
A.NaCl晶体熔化时,既要克服离子间作用力,又要克服分子间作用力
B.C60分子是有60个碳原子构成,所以C60属于原子晶体
C.CCl4中所有原子最外层都形成了8个电子的结构
D.MgCl2和NaOH所含有的化学键完全相同
16.下 列晶体性质的比较中不正确的是
A.熔点:金刚石>碳化硅>晶体硅
B.沸点: NH3>PH3
C.硬度: K>Na>Li
D.熔点: SiI4>SiBr4>SiCl4
17.根据下表中的有关数据分析,下列说法错误的是
AlCl3 SiCl4 晶体硼 金刚石 晶体硅
熔点/℃ 194 -70 2180 >3500 1410
沸点/℃ 181 57 3650 4827 2355
A.SiCl4、AlCl3是分子晶体
B.晶体硼是共价晶体
C.晶体硅是共价晶体
D.金刚石中的C-C键比晶体硅中的Si-Si键弱
18.下列类比或推理合理的是
已知 方法 结论
A 沸点:HBr>HCl 类比 沸点:HCl>HF
B 少量Cl2通入足量FeBr2溶液里,Fe2+先反应 类比 少量Cl2通入足量FeI2溶液里,Fe2+先反应
C 将盐酸与NaHCO3混合产生的气体直接通入硅酸钠溶液 推理 酸性:H2CO3>H2SiO3
D 曾青得铁化为铜 推理 金属性:Fe>Cu
A.A B.B C.C D.D
19.下列各物质中,按熔点由高到低的顺序排列正确的是
A.CH4>SiH4>GeH4>SnH4 B.KCl>NaCl>MgCl2>MgO
C.MgBr2<SiCl4<BN D.金刚石>晶体硅>钠
20.有关晶体的结构如图所示,下列说法中正确的是
A.在NaCl晶体中,距Cl-最近的Na有6个,距Na+最近且等距的Na+共6个
B.在CaF2晶体中,每个晶胞平均占有4个Ca2+,F-的配位数是4
C.在金刚石晶体中,每个碳原子被6个六元环共同占有,每个六元环最多有4个碳原子共面
D.该气态团簇分子的分子式为EF或FE
21.科学家在20℃时,将水置于足够强的电场中,水分子瞬间凝固成“暖冰”。对“暖冰”与其它物质比较正确的是
A.与Na2O晶体类型相同 B.与SiO2晶体类型相同
C.与CO2化学键类型相同 D.与普通的冰化学性质不同
22.目前,科学界拟合成一种“二重构造”的球形分子,即把“足球形”的C60熔进“足球形”的Si60分子中,外面的硅原子与里面的碳原子以共价键结合。下列关于这种分子的说法中不正确的是( )
A.是一种新型化合物 B.晶体属于分子晶体
C.是两种单质组成的混合物 D.相对分子质量为2400
23.钛有“二十一世纪的金属”、“全能金属”、“现代金属”的美称。镁与熔融的四氯化钛反应可制取钛:2Mg+TiCl42MgCl2+Ti。下列说法正确的是
A.基态Ti原子的价层电子排布式:3d4
B.Cl-结构示意图:
C.MgCl2的电子:
D.TiCl4熔点是-25℃,沸点是136.4℃,可溶于苯和CCl4,该晶体属于共价晶体
24.下列关于物质熔、沸点高低说法错误的是
A.的熔、沸点依次降低
B.分子晶体中共价键的键能越大,分子晶体的熔、沸点越高
C.的熔、沸点依次升高
D.比熔点高
25.某抗癌药物的结构简式如图所示,其中W、X、Y、Z是原子序数依次增大的短周期主族元素,W、Y同主族,Y、Z的最外层电子数之和是X的最外层电子数的2倍。下列叙述正确的是
A.W的最简单氢化物与Z的单质混合后可产生白烟
B.最高价氧化物对应的水化物酸性强弱Y>Z
C.简单氢化物的沸点:W
二、填空题
26.晶体的个性
(1)绝大多数金属晶体是 的良导体, 性好。
(2)食盐为 晶体,质脆,熔融状态下 导电。
(3)金刚石为 晶体,无色透明、坚硬、质脆,常温下不导电。
(4)干冰属于 晶体,只能在低温下存在。
27.分子晶体与共价晶体
晶体类型 分子晶体 共价晶体
概念 分子间以 结合形成的晶体 相邻原子间以 相结合而形成空间网状结构
组成微粒 分子 原子
作用力 分子间作用力 共价键
常见的物质类型 大多数非金属单质 大多数共价化合物 少量非金属单质:金刚石、晶体硅;少量共价化合物:SiO2、SiC等
熔沸点 很大
硬度 很大
溶解性 部分溶于水 不溶于任何溶剂
导电性 固体和熔化状态都 ,部分溶于水导电 不导电,个别为半导体
影响作用力的因素 1.结构与组成相似的分子:分子量大→范德华力大→分子晶体的 就高 2.分子间有氢键的 升高,分子内有氢键的熔沸点 原子半径小→共价键长短→共价键能大→原子晶体的熔沸点高
28.(1)已知:碳化硅()是一种具有类似金刚石结构的晶体,其中碳原子和硅原子是交替排列的。在下列晶体:①晶体硅、②金刚石、③碳化硅、④干冰、⑤冰中,它们的熔点由高到低的顺序是 (填序号)。
(2)继后,科学家又合成了、。已知熔点:,而破坏分子所需要的能量:,其原因是 。
试卷第1页,共3页
参考答案:
1.A
【详解】A.铝是金属晶体,由铝离子和自由电子构成,A符合题意;
B.金刚石为共价(原子)晶体,不含电子,B不符合题意;
C.液态氯化氢由分子构成,C不符合题意;
D.冰醋酸为乙酸,由分子构成,D不符合题意;
故选A。
2.D
【详解】A.液晶是一种介于液态与结晶态之间的一种物质聚集状态,A正确;
B.“杯酚”分离C60和C70,是利用超分子的分子识别特征,B正确;
C.等离子体中含有大量能自由运动的带电粒子,具有良好的导电性和流动性,C正确;
D.反应过程遵循电荷数守恒、质量数守恒得为,所以X的中子数为4,且该反应是核反应不是化学反应,D错误;
故选D。
【点睛】
3.C
【详解】A.NaCl、MgCl2均为离子化合物,只含离子键,A正确;
B.C60、C70为碳元素的不同单质,互为同素异形体,B正确;
C.干冰(CO2)由分子构成,属于分子晶体,SiO2由原子构成,属于原子晶体,C错误;
D.合成纤维、合成树脂、合成橡胶属于三大合成高分子材料,D正确;
故答案选C。
4.A
【详解】干冰常温时为气体,冰常温时为液态,晶体硅为共价晶体,常温为固体,冰醋酸常温为液体,综合分析可知,干冰的熔点最低;
故选A。
5.C
【详解】分子晶体的熔、沸点较低,硬度较小,导致这些性质特征的本质原因是其构成微粒间的相互作用——分子间作用力,它相对于化学键来说是极其微弱的,C项符合题意。
6.B
【分析】X、Y、Z位于同周期,X原子的电子数等于Y原子的最外层电子数,说明X位于第二周期,即X、Y、Z位于第二周期,四种元素原子序数依次增大,以及根据结构图可知,W、X、Y、Z分别为H、B、N、O或F,据此分析;
【详解】A.根据上述分析,电负性:B<H<N<O或F,故A错误;
B.H、N、O或F可形成硝酸铵、氟化铵等离子晶体,故B正确;
C.NO为不成盐氧化物,不能被强碱溶液吸收,故C错误;
D.H2O或HF的沸点高于NH3,故D错误;
答案为B。
7.C
【详解】A.由图像可知,第三周期元素形成的单质中,钠、镁、铝是金属晶体,硅是共价晶体,磷、硫、氯、氩固体单质是分子晶体,共3种晶体类型,A错误;
B.分子晶体的熔点与共价键键能无关,与分子间作用力大小有关的相对分子质量大于,B错误;
C.硅晶体由硅硅键形成空间网状结构,C正确;
D.金属晶体熔点与金属键强弱有关,金属键强弱与金属离子带电荷数、离子半径有关。钠、镁、铝离子所带电荷数依次为1、2、3,离子半径依次减小,故金属键依次增强,熔点升高,D错误;
故选C。
8.A
【详解】A.苯酚与水分子之间存在氢键,而甲苯与水分子之间不存在氢键,所以溶解性:苯酚>甲苯,A正确;
B.稳定性与化学键强弱有关,与氢键无关,B错误;
C.分子间氢键可以使物质熔点升高,但乙烷和甲烷均不能形成分子间氢键,则两者熔点高低与氢键无关,C错误;
D.分子间氢键可以使物质沸点升高,但均不能形成分子间氢键,则两者沸点高低与氢键无关,D错误;
故答案为A。
9.C
【详解】A.足球烯C60是由C60分子通过分子间作用力形成的分子晶体,而不是共价晶体,A错误;
B.氮化铝陶瓷属于新型无机非金属材料,而不是金属材料,B错误;
C.同位素是指质子数相同而中子数不同的同一元素的不同原子间的关系,故与互为同位素,C正确;
D.氯丁尼龙属于合成纤维,属于合成高分子材料,而不是天然高分子材料,D错误;
故答案为:C。
10.B
【分析】根据元素在周期表中的位置可知, X为C元素,Y为O元素,W为Si元素,Z为Cl元素。
【详解】A.同周期元素从左到右半径依次减小,同主族元素从上到下半径依次增大,四种元素中原子半径最大的是Si,即W,A正确;
B.CCl4是分子晶体,SiO2是共价晶体,晶体类型不同,B错误;
C.CO2和SiO2都能与NaOH反应,CO2+2NaOH = Na2CO3+H2O、SiO2+2NaOH = Na2SiO3+H2O,C正确;
D.Si是重要的半导体材料,用于计算机芯片、太阳能电池等多项领域,D正确;
故选B。
11.D
【详解】A.金属晶体中含有金属元素,AlCl3是分子晶体,其也含有金属元素,所以含有金属元素的晶体不一定是离子晶体,故A错误;
B.属于分子晶体,熔点较低,熔化时破坏分子间作用力,属于离子晶体,熔点较高,熔化时破坏离子键,故B错误;
C.C和同主族,但其最高价氧化物的晶体类型不同,晶体和晶体分别属于分子晶体和共价晶体,所以同族元素的最高价氧化物可能形成不同类型的晶体,故C错误;
D.金属晶体的熔点有的很高,有的很低,如常温下汞呈液态,所以金属晶体的熔点不一定比分子晶体的高,故D正确;
答案D。
12.C
【详解】A.金属晶体中有阳离子和自由电子,没有阴离子,A错误;
B.在方形容器中结冰得到的方形外观并不是自发形成的,而是受限于容器形状形成的,所以没有体现自范性,B错误;
C.由阳离子、电子和电中性粒子组成的等离子体气态物质没有分子,C正确;
D.接近水的沸点的水蒸气中存在相当量的水分子因氢键而相互缔合形成所谓的缔合分子,所以相对分子质量测定值比按化学式计算出的要大一些,D错误;
故选C。
13.C
【详解】①晶体具有各向异性,所以晶体在不同方向上的硬度、导热性、导电性不同,①错误;
②离子晶体由常见的离子化合物形成的晶体,所以都是化合物,②正确;
③共价晶体熔化时需要破坏共价键,所以共价键越强,熔点越高,③正确;
④分子晶体中,分子间作用力越大,物质熔沸点越高,④错误;
⑤金属晶体能导电的原因是在外加电场作用下电子形成电子气,发生定向移动,⑤错误;
⑥分子识别是超分子的重要特征之一,⑥正确;
答案为:C。
14.C
【详解】A.16 g氧原子的物质的量为1 mol,由于1 mol二氧化硅中含2 mol氧原子,故含1 mol氧原子的二氧化硅的物质的量为0.5 mol,而二氧化硅中每个硅原子含4条σ键,故0.5 mol二氧化硅中含2NA条σ键,A正确;
B.在一个结构单元含有Na+:,含有Cl-: ,即1个结构单元中含有4个钠离子和4个氯离子。58.5 gNaCl的物质的量是1 mol,,所以含0.25NA个结构单元,B正确;
C.在冰晶体中,每个水分子与相邻的4个水分子形成氢键,每1个水分子平均形成2个氢键。18 gH2O的物质的量是1 mol,因此在1 mol冰中含有2NA个氢键。但在常温、常压下温度升高,冰变为液态水,部分氢键被破坏,故1 mol液体水的氢键数目小于2NA,C错误;
D.标准状况下HF是液体,22.4 LHF的物质的量大于1 mol,因此所含HF的分子数大于NA,D正确;
故合理选项是C。
15.C
【详解】A.氯化钠是离子晶体,晶体中只含有离子键,熔化时只需要克服离子键,故A错误;
B.碳60是由分子组成的分子晶体,故B错误;
C.四氯化碳分子中碳原子和氯原子的最外层都形成了8个电子的稳定结构,故C正确;
D.氯化镁和氢氧化钠都是离子晶体,氯化镁晶体中只含有离子键,氢氧化钠晶体中含有离子键和共价键,化学键类型不完全相同,故D错误;
故选C。
16.C
【详解】A.三种物质都是共价晶体,因为C的原子半径小于Si的,所以键长:C—C键
B.NH3和PH3都是分子晶体,但NH3分子间存在氢键,故NH3的沸点较高,B正确;
C.Li 、Na、 K位于同一主族,从上到下核电荷数递增、原子半径与离子半径递增,金属键的强度递减,则硬度:Li >Na> K,C错误;
D.卤化硅为分子晶体,它们的组成和结构相似,分子间不存在氢键,故相对分子质量越大,分子间作用力越大,熔点越高,D正确;
故答案选C。
17.D
【详解】A.根据表格数据可知SiCl4、AlCl3的熔沸点低,说明在晶体中构成微粒间的作用力十分微弱,由于分子间作用力比化学键弱得多,因此SiCl4、AlCl3都是分子晶体,A正确;
B.根据表格数据可知晶体硼熔沸点高,说明构成微粒的作用力很强,该物质属于共价晶体,B正确;
C.根据表格数据可知晶体硅熔沸点高,说明构成微粒的作用力很强,该物质属于共价晶体,C正确;
D.金刚石、晶体硅的熔沸点高,由于原子半径:C<Si,键长:C-C<Si-Si。键长越长,原子之间的共价键结合力就越弱,就越不牢固,越容易断裂,该化学键的键能就越小,故金刚石中的C-C键比晶体硅中的Si-Si键强,D错误;
故合理选项是D。
18.D
【详解】A.对于分子结构相似的物质,相对分子质量越大,分子间作用力就越强,物质的熔沸点就越高,沸点:HBr>HCl,但由于HF分子之间还存在氢键,增加了分子之间的吸引作用,导致HF的熔沸点比只有分子间作用力的HCl大,故沸点:HF>HCl,推理不符合事实,A错误;
B.由于还原性:Fe2+>Br->Cl-,所以少量Cl2通入足量FeBr2溶液里,Fe2+先反应,2Fe2++Cl2=2Fe3++2Cl-;但由于还原剂I->Fe2+,所以向足量FeI2溶液里通入少量Cl2,先发生反应:2I-+Cl2=I2+2Cl-,推理不符合事实,B错误;
C.由于酸性:HCl>H2CO3,所以将盐酸与NaHCO3混合,会发生反应:HCl+NaHCO3=NaCl+H2O+CO2↑,反应产生的气体CO2与Na2SiO3溶液发生反应:CO2+H2O+Na2SiO3=Na2CO3+H2SiO3↓,但盐酸具有挥发性,挥发的HCl也会与硅酸钠溶液发生反应:2HCl+Na2SiO3=2NaCl+H2SiO3↓,因此不能据此证明酸性:H2CO3>H2SiO3,C错误;
D.曾青主要成分是CuSO4,向其水溶液中加入Fe会发生反应:CuSO4+Fe=FeSO4+Cu,根据置换反应的规律可知元素的金属性:Fe>Cu,D正确;
故合理选项是D。
19.D
【详解】A.该组物质均为结构相似的分子晶体,其熔点取决于分子间作用力的大小,一般来说,结构相似的分子晶体,相对分子质量越大,分子间作用力也越大,故该组各物质熔点应为逐渐升高的顺序,A错误;
B.该组物质均为离子晶体,离子晶体熔点高低取决于离子键键能的大小,一般来说,离子的半径越小,电荷越多,离子键的键能就越大,故该组各物质熔点应为升高顺序,B错误;
C.SiCl4为分子晶体,MgBr2为离子晶体,BN为原子晶体,故熔点: SiCl4<MgBr2<BN,C错误;
D.金刚石和晶体硅属于原子晶体,钠属于离子晶体;原子晶体的熔点取决于共价键的键能,键能与键长成反比;金刚石C-C键的键长更短些,所以金刚石的熔点比晶体硅高,原子晶体的熔点一般比金属晶体的熔点高,则金刚石和晶体硅的熔点比钠的高;D正确;
故选D。
20.B
【详解】A.氯化钠晶体中,距Na+最近且等距的Cl-是6个,即钠离子的配位数是6;以底面左下角的钠离子为例,距Na+最近且相等的Na+位于面心处,共有=12个,选项A错误;
B.Ca2+位于晶胞顶点和面心,数目为8×+6×=4,即每个晶胞平均占有4个Ca2+;距离F-最近且等距的Ca2+有4个,即F-的配位数为4,选项B正确;
C.在金刚石的晶体结构中每个碳原子与周围的4个碳原子形成四个碳碳单键,最小的环为6元环,每个单键为3个环共有,则每个C原子连接4×3=12个六元环,晶胞中共平面的原子如图 ,共4个,选项C错误;
D.该气态团簇分子的分子含有4个E和4个F原子,则该气态团簇分子的分子式为E4F4或F4E4,选项D错误;
答案选B。
21.C
【详解】A.根据题意:在电场作用下,水分子瞬间凝固成“暖冰”,可知水分子间更易形成氢键,不存在离子键,是分子晶体,而Na2O晶体属于离子晶体,故A错误;
B.“暖冰”应该是分子晶体,而SiO2是共价晶体,故B错误;
C.“暖冰”中水分子的O-H是极性共价键,CO2分子内也只存在极性共价键,故C正确;
D.“暖冰”与普通冰的成分均为水分子,化学性质相同,故D错误;
故答案为C。
22.C
【详解】A.根据题意可知硅原子和碳原子之间形成了碳硅键,也就是形成了一种新的化合物,A正确;
B.根据题意“二重构造”的球形分子,说明该化合物为分子晶体,B正确;
C.该分子为两种元素形成的化合物而非混合物,C错误;
D.该物质的分子式为Si60C60,相对分子质量为2400,D正确;
正确选项C。
23.C
【详解】A.已知Ti是24号元素,故基态Ti原子的价层电子排布式:3d24s2,A错误;
B.Cl-的最外层上有8个电子,则Cl-结构示意图为:,B错误;
C.已知MgCl2是由Mg2+和Cl-通过离子键形成的离子化合物,则MgCl2的电子为:,C正确;
D.TiCl4熔点是-25℃,沸点是136.4℃,即熔沸点较低,可溶于苯和CCl4,该晶体属于分子晶体,共价晶体的熔沸点很高,一般不溶于任何溶剂中,D错误;
故答案为:C。
24.B
【详解】A.的熔、沸点随着原子序数的递增依次降低,A正确;
B.分子晶体的熔、沸点与分子间作用力和氢键有关,与化学键的键能无关,B错误;
C.分子间都不能形成氢键,分子间作用力依次增大,故它们的熔、沸点依次升高,C正确;
D.氧化镁和氯化钠都属于离子晶体,r(O2-)
25.A
【分析】由分子结构可知Y形成5个共价键,则Y原子最外层有5个电子,由于W、X、Y、Z是原子序数依次增大的短周期主族元素,W、Y同主族,则W是氮元素,Y是磷元素,Y、Z的最外层电子数之和是X的最外层电子数的2倍,磷的最外层有5个电子,Z最外层电子数也是奇数,X最外层电子数为偶数,结合都是短周期元素,则Z是氯元素,最外层有7个电子,所以X最外层电子数为(5+7)/2=6,原子序数比磷小,则X是氧元素。根据上述分析知:W是氮元素,X是氧元素,Y是磷元素,Z是氯元素。
【详解】A.W是氮元素,Z是氯元素,W的最简单氢化物NH3与Z的单质Cl2混合后会发生氧化还原反应(8NH3+3Cl2=6NH4Cl+N2),反应产生的NH4Cl在室温下呈固态,可以看到白烟现象,A项符合题意;
B.Y的最高价氧化物对应水化物为H3PO4,其为中强酸;Z的最高价氧化物对应水化物为HClO4,其为强酸,所以Z>Y,B项不符合题意;
C.对应的简单氢化物分别为W—NH3,Y—PH3,X—H2O,氨气和水的分子间均都有氢键,沸点较高,水在常温下呈液态而氨在常温下为气态,所以沸点顺序为H2O>NH3>PH3,即X>W>Y,C项不符合题意;
D.Y为P元素,可与氯形成PCl5,其中P不能满足8电子结构,D项不符合题意;
故正确选项为A
26. 电和热 延展 离子 能 共价 分子
【详解】不同类型的晶体因构成微粒及其粒子间的相互作用力的不同,常常表现出各自的特性。
(1)绝大多数的金属晶体是电和热的良导体,延展性好;
(2)食盐为离子晶体,质脆,熔融状态下能导电;
(3)金刚石为共价晶体 (原子晶体),无色透明,坚硬、质脆,常温下不导电;
(4)干冰属于分子晶体,只能在低温下存在。
27. 分子作用力 共价键 较小 较小 不导电 熔沸点 熔沸点 降低
【详解】分子晶体是只含有分子的晶体,分子间以分子间作用力结合形成的晶体,组成晶体的微粒是分子,分子与分子之间的作用力是分子间作用力,分子晶体的熔沸点一般都较低,硬度也较小,这是因为分子晶体熔沸点及硬度是由分子间作用力决定的,分子间作用力包括范德华力和氢键,分子间作用力很弱,约比化学键的键能小个数量级,结构与组成相似的分子,相对分子质量越大,范德华力大,分子晶体的熔沸点就高,氢键比范德华力要强的一种分子间作用力,能形成分子间氢键的分子晶体熔沸点升高,氢键有时也存在于分子内,形成分子内氢键的分子晶体熔沸点降低,属于分子晶体的物质类型包括大多数非金属单质、大多数共价化合物,有的分子晶体能溶于水,有的分子晶体不能溶于水,由于组成微粒是分子,所以固体和熔化状态都不导电,部分溶于水后导电;共价晶体中不存在分子,是相邻原子间以共价键相结合而形成空间网状结构的晶体。
28. ②③①⑤④ 一般情况下,对于组成与结构相似的分了晶体,分子晶体的相对分子质量越大,分子间作用力越强,熔化所需的能量越多,故熔点:;而破坏分子需断开化学键,元素电负性越强其形成的化学键越稳定,断键时所需能量越多,故破坏分子所需要的能量:
【详解】(1)题述晶体中属于共价晶体的是①②③,属于分子晶体的是④⑤。一般来说,共价晶体的熔点>分子晶体的熔点;对于共价晶体,键长:键>键键,相应键能:键键键,故熔点:金刚石>碳化硅>晶体硅。故答案为:②③①⑤④;
(2)分子晶体熔点与分子间作用力有关,而破坏分子则是破坏分子内的共价键。故答案为:一般情况下,对于组成与结构相似的分了晶体,分子晶体的相对分子质量越大,分子间作用力越强,熔化所需的能量越多,故熔点:;而破坏分子需断开化学键,元素电负性越强其形成的化学键越稳定,断键时所需能量越多,故破坏分子所需要的能量:。
答案第1页,共2页
