2024中考一轮复习 鲁教版化学 教材基础复习 第三单元 第一节 构成物质的微粒 元素 课件(共54张PPT)
文档属性
| 名称 | 2024中考一轮复习 鲁教版化学 教材基础复习 第三单元 第一节 构成物质的微粒 元素 课件(共54张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-24 00:00:00 | ||
图片预览








文档简介
(共54张PPT)
第三单元
物质构成的奥秘
第一节
构成物质的微粒 元素
知识清单·理脉络
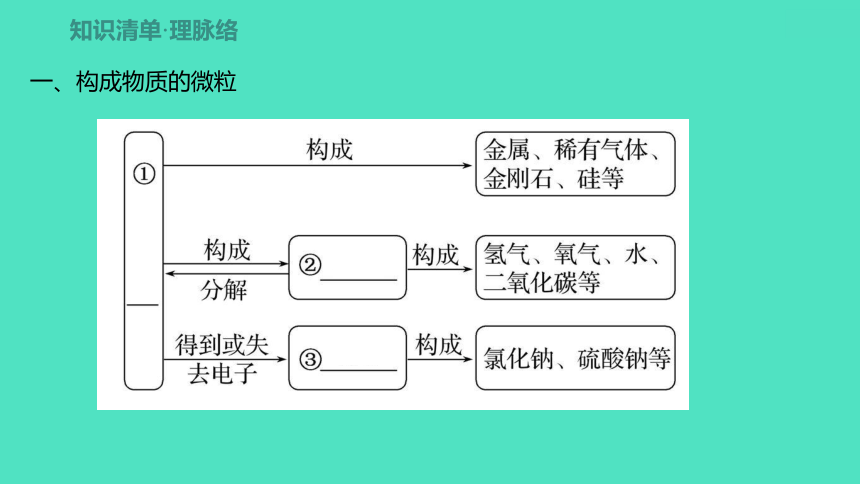
一、构成物质的微粒
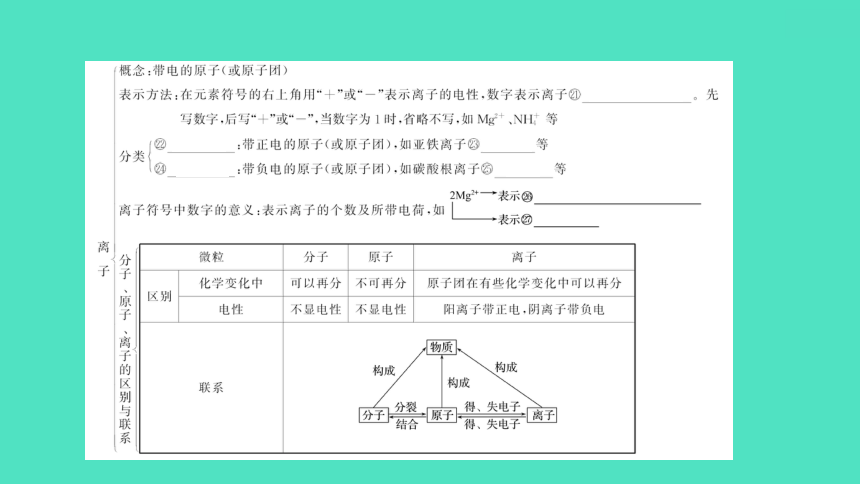
二、元素
易错辨析
判断下列说法是否正确。
(1)原子不能直接构成物质。 ( )
(2)分子由原子构成,所以分子一定比原子大。 ( )
(3)原子的质量主要集中在原子核上,电子质量可以忽略不计。 ( )
(4)2Fe2+表示两个铁离子。 ( )
(5)一氧化碳、二氧化碳二者化学性质不同,原因是分子不同。 ( )
(6)保持水的化学性质的粒子是氢原子和氧原子。 ( )
(7)水银体温计可以测定体温是因为汞分子之间的间隔发生变化。 ( )
(8)同种元素的原子核内质子数和中子数一定相等。 ( )
(9)镁的相对原子质量为24 g。 ( )
×
×
√
×
√
×
×
×
×
追根溯源(教材习题变式)
1.下列叙述错误的是 ( )
A.分子、原子、离子都可以直接构成物质
B.任何原子都是由质子、中子、电子构成的
C.化学反应中,分子可分,原子不能再分
D.原子的质量主要集中在原子核上
B
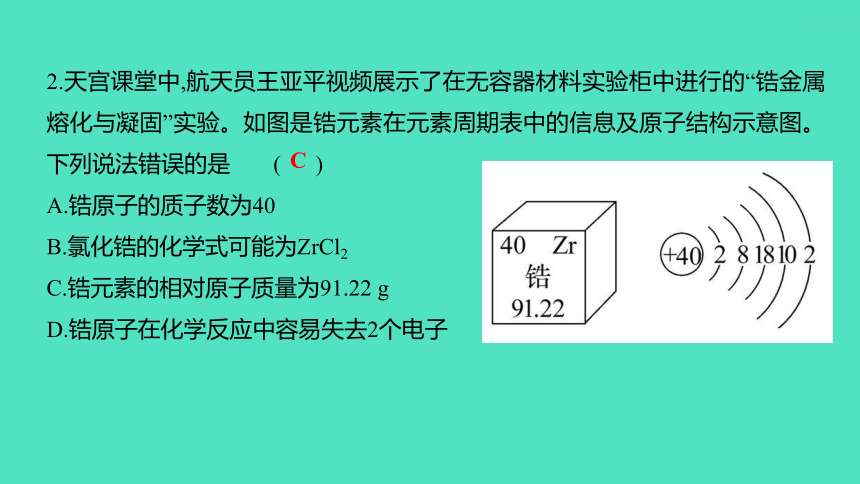
2.天宫课堂中,航天员王亚平视频展示了在无容器材料实验柜中进行的“锆金属熔化与凝固”实验。如图是锆元素在元素周期表中的信息及原子结构示意图。下列说法错误的是 ( )
A.锆原子的质子数为40
B.氯化锆的化学式可能为ZrCl2
C.锆元素的相对原子质量为91.22 g
D.锆原子在化学反应中容易失去2个电子
C
3.化学家张青莲主持测定了铟、铱、锌等元素相对原子质量的新值。碳-12原
子的质量为1.993×10-26 kg,一种锌原子的质量为1.096×10-25kg,该锌原子的相对
原子质量是( )
A.12 B.64
C.66 D.1.096×10-25 kg
C
4.如图是元素周期表的一部分信息,下列说法错误的是 ( )
A.氟原子的相对原子质量为19.00
B.硫原子的核电荷数是16
C.氟、硫、氯三种元素都属于非金属元素
D.氟元素和氯元素位于元素周期表的同一周期
D
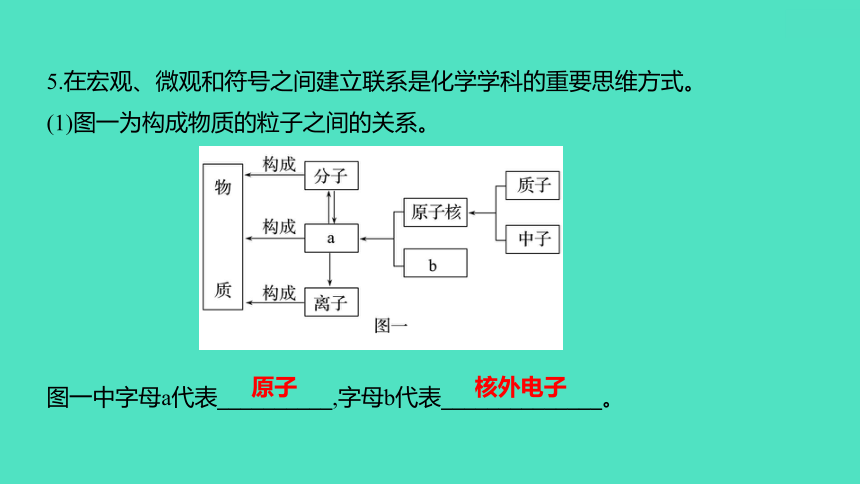
5.在宏观、微观和符号之间建立联系是化学学科的重要思维方式。
(1)图一为构成物质的粒子之间的关系。
图一中字母a代表__________,字母b代表______________。
原子
核外电子
(2)结构决定性质,请根据下列粒子结构示意图给出的信息回答:
其中属于同种元素是________(填序号),属于阴离子是_______(填序号),化学性
质相似的是________(填序号)。
BC
C
BD
6.一些粒子的结构都可用示意图 来表示。请回答下列问题:
(1)图中x表示的是_______________________。
(2)若x=12,则对应的元素符号为________。
(3)若x-y=3,则该粒子的符号为_________。
(4)若x=8,则y的值可能为__________。
质子数(或核电荷数)
Mg
Na+
6或8
考点一 构成物质的微粒
【示范题1】(2023·岳阳中考)推理是化学学习的一种常用思维方法。下列推理正确的是 ( )
A.分子能构成物质,所以物质都是由分子构成的
B.离子是带电的微观粒子,所以带电的微观粒子都是离子
C.由同种元素组成的纯净物是单质,所以单质只含有一种元素
D.碳酸钙能与稀盐酸反应生成气体,所以与稀盐酸反应产生气体的物质一定是碳酸钙
考点突破·释疑难
C
考点二 粒子结构示意图
【示范题2】(2023·株洲中考)如图为某元素原子的结构示意图。下列有关叙述不正确的是 ( )
A.该原子的结构示意图中x=1
B.该元素属于活泼的非金属元素
C.该元素的原子在化学反应中容易失去电子
D.该元素形成的单质容易与氧气反应
B
【方法点拨】 根据结构示意图判断粒子的种类
考点三 元素周期表
【示范题3】(2023·邵阳中考)中国承建的阿尔卡萨光伏电站是卡塔尔首座太阳能发电站。硅太阳能电池主要材料是高纯硅,如图是硅元素的相关信息和硅原子的结构示意图,下列关于硅的说法错误的是 ( )
A.x的数值为4
B.硅元素属于非金属元素
C.硅元素的相对原子质量为28.09 g
D.硅元素位于元素周期表的第三周期
C
命题点一 构成物质的微粒
1.(2019·淄博中考)公共场所禁止吸烟。香烟的烟雾中含有四千多种化学物质,
大多属于有害物质。吸烟者吸烟会造成非吸烟者被动吸烟的主要原因是( )
A.分子的质量很小 B.分子之间有间隔
C.分子的体积很小 D.分子不断地运动
2.(2022·泰安中考)下列物质是由分子构成的是 ( )
A.氢氧化钾 B.铝
C.金刚石 D.甲烷
五四制地区5年真题
D
D
3.(2022·烟台中考)下列有关化学史的叙述错误的是 ( )
A.汤姆森发现电子
B.卢瑟福发现原子核
C.门捷列夫编制了元素周期表
D.拉瓦锡发现酸碱指示剂
D
4.(2022·威海中考)下列认识不正确的是( )
A.微粒的运动和变化是导致物质发生变化的原因
B.原子虽小,既有质量又有能量
C.繁多复杂的物质是由种类有限的元素组成的
D.离子带电,所以不能构成物质
D
5.(2022·威海中考)下列对宏观现象的微观解释不正确的是 ( )
A.金刚石的硬度比石墨大——碳原子的内部结构不同
B.稀盐酸和稀硫酸都能使紫色石蕊试液变红——稀盐酸和稀硫酸中都含有氢离子
C.5 mL水与5 mL酒精混合后总体积小于10 mL——分子之间有间隔
D.氧气能支持燃烧,二氧化碳不能支持燃烧——不同种分子的化学性质不同
A
6.(2022·淄博中考)科学思维是从宏观、微观相结合的视角探究物质及其变化规律的认识方式。下列对宏观事实的微观解释错误的是 ( )
选项 宏观事实 微观解释
A 氢氧化钠溶液和氢氧化钾溶液具有相似的化学性质 两种溶液中都含有OH-
B 加热氧化汞得到汞和氧气 化学反应前后分子改变,原子不变
C 结成冰的水不能流动 温度降到零度以下后,水分子不再运动
D 把食盐颗粒放入水中充分搅拌后,食盐颗粒很快消失 在水分子作用下,氯化钠解离成钠离子和氯离子,扩散到水中,形成了氯化钠溶液
C
7.(2021·淄博中考)化学是在原子、分子水平上研究物质及其变化规律的一门基础自然科学。从原子、分子的角度分析,下列解释错误的是 ( )
A.一滴水中含有约1021个水分子——说明水分子很小
B.品红加入水中,整杯液体变为红色——说明分子在不断运动
C.原子的质量主要集中在原子核上——说明原子核是不可分割的实心球体
D.过氧化氢分解生成氧气和水——说明分子可以分成原子,原子可重新组合成新分子
C
8.(2023·威海中考)下列关于分子、原子、离子的认识不正确的是 ( )
A.在化学变化中,分子可以被创造也可以被消灭
B.原子得失电子变成离子后,质量几乎不变,化学性质差别很大
C.同种原子通过不同方式结合成的分子化学性质不同
D.同种分子排列方式不同,则化学性质不同
D
9.(2020·淄博中考)化学是在原子、分子水平上研究物质及其变化规律的一门学科,它能指导我们更好地认识、改造和应用物质。以下说法正确的是 ( )
A.质子、中子、电子都可以直接构成物质
B.原子、分子、离子都可以直接构成物质
C.分子是由原子构成的,水由氢原子和氧原子构成
D.分子是构成物质的基本粒子,空气由空气分子构成
B
10.(2019·淄博中考)世界万物都是由极其微小的粒子构成的,下列说法正确的
是( )
A.海水是由海水分子构成的
B.分子、原子、离子都能直接构成物质
C.二氧化碳是由碳原子和氧原子构成的
D.自然界中的物质都是由质子、中子、电子等粒子构成的
B
11.(2023·烟台中考)下列对宏观事实的微观解释错误的是 ( )
A.自然界中水的天然循环——水分子不断运动且间隔发生改变
B.氧气经压缩储存在钢瓶中——氧气分子体积变小
C.稀盐酸和稀硫酸具有相似的化学性质——酸溶液中都含有氢离子
D.一氧化碳和二氧化碳化学性质不同——构成二者的分子不同
B
12.(2020·济宁中考)对下列物质构成的说法中,不正确的是 ( )
A.铜是由铜原子构成的金属单质
B.氧气是由氧分子构成的气体单质
C.水是由水分子构成的化合物
D.氯化钠是由氯化钠分子构成的化合物
13.(2021·东营中考)下列观点不正确的是 ( )
A.化学改变世界的途径是使物质发生化学变化,实现物质与能量的互相转化
B.物质都是由极其微小的粒子构成的,原子是构成一切化学物质的基本单元
C.溶解就是溶质分子或离子通过自身不断运动分散到溶剂中的过程
D.过滤是分离颗粒大小不同的混合物的方法
D
C
14.(2021·淄博中考)原子结构示意图能简明地表示原子核外电子的排布。
小云从如图微粒结构示意图中获得相关信息,你认为正确的是 ( )
A.②③属于同一种原子
B.①②属于同一种元素
C.①③表示的都是原子
D.②③表示质子数相同
B
15.(2023·威海中考)从原子论到分子学说原子-分子论的创立,奠定了近代化学的基础,阅读下列材料回答问题:
材料一:1803年,道尔顿提出原子论,认为所有物质都是由原子构成的。单质由原子直接构成,同种原子相互排斥不能结合;化合物由“复杂原子”构成,“复杂原子”由不同原子按一定整数比例简单构成。
材料二:1811年,阿伏加德罗引入新的概念——分子,提出了分子学说。对于化合物而言,分子相当于道尔顿所谓的“复杂原子”;对于单质而言,同种原子可以结合成单质分子。
(1)完成下列表格
(2)上表微粒中符合道尔顿“复杂原子”的是__________________(写化学式)。
物质 葡萄糖 氢气 二氧化硫 氦气
构成物质的微粒 (写微粒符号) ________ ___ ____ ___
C6H12O6
H2
SO2
He
C6H12O6、SO2
(3)你同意材料一中加点部分的观点吗 ____________,请选用(1)表中的物质说
明理由:______________________________________________________。
(4)从原子论的创立到分子学说的提出,谈谈你对科学理论的发展有何感想:
_________________________________________________________________。
不同意
氢气由氢分子构成,每个氢分子由两个相同的氢原子构成
科学理论的发展需要大胆创新(或科学理论是不断传承和发展的,合理即可)
命题点二 元素与元素周期表
1.(2022·泰安中考)我们在商场常看到“补锌”“补铁”等字样的食品,其中“锌”“铁”是指( )
A.元素 B.原子 C.分子 D.单质
2.(2023·东营中考)元素周期表是学习和研究化学的工具之一。如图是元素周期表中某元素的信息,下列说法正确的是 ( )
A.该元素的名称是磷
B.该元素原子核外有14个电子
C.该元素的相对原子质量是28.09 g
D.该元素属于金属元素
A
B
3.(2019·淄博中考)今年是元素周期表诞生150周年,联合国宣布2019年为“国际化学元素周期表年”。元素周期表是学习和研究化学的重要工具,对于元素周期表的认识不正确的是 ( )
A.利用元素周期表预测新元素的化学性质
B.利用元素周期表预测新元素的原子结构
C.利用元素周期表查找某元素在自然界中的含量
D.利用元素周期表可查找某原子的相对原子质量
4.(2019·淄博中考)氧气、氮气、甲烷、乙炔、葡萄糖、淀粉、生理盐水都是生活中常用的物质,这些物质中所包含的元素种类有 ( )
A.2种 B.4种 C.6种 D.8种
C
C
5.(2022·烟台中考节选)2022年第二十四届冬季奥林匹克运动会在北京圆满举行,
本届冬奥会处处体现“低碳环保”理念,科技感十足。
场馆:“冰丝带”是由3360块发电玻璃拼成。发电玻璃是在普通玻璃上覆盖一层
碲化镉(化学式CdTe)。碲化镉在弱光照射下也能持续发电,为冬奥场馆提供电
力支持。根据如图信息:Te的相对原子质量是__________,Cd的质子数是
________,CdTe中Te的化合价是_______。
127.6
48
-2
6.(2022·淄博中考)元素周期表是学习和研究化学的重要工具。如图是钙原子的
结构示意图及钙元素在元素周期表中的相关信息。
(1)钙元素的原子序数是________,它属于______________(填写“金属元素”或
“非金属元素”)。
(2)钙原子在化学反应中容易失去电子形成离子,钙离子的符号是_________,
氧化钙中钙元素的化合价是________。
(3)人体缺乏钙元素就会导致_______(填字母)。
a.甲状腺肿大 b.骨质疏松症
c.贫血症
20
金属元素
Ca2+
+2
b
7.(2023·烟台中考)2022年8月9日,国内首条磁浮空轨列车“兴国号”在赣州兴国县首发,该列车
使用了钕铁硼稀土类永磁体,这种永磁体因其优异的磁性而被称为“磁王”。
(1)稀土元素是钪、钇等十七种元素的总称,这些不同种元素之间的本质区别是
________________。
(2)“兴国号”攻克了薄壁铝合金车体焊接技术,焊接时用氩气作保护气是因为氩气的化学性质
__________,铝具有抗腐蚀性的原因是常温下能跟氧气反应生成致密而坚固的氧化铝薄膜,
该反应的化学方程式是______________________。
(3)钕元素在元素周期表中的部分信息如图所示,钕原子的质子数是________。
已知氯化钕的化学式为NdCl3,则相同价态钕的氧化物的化学式是_______。
质子数不同
稳定
4Al+3O2===2Al2O3
60
Nd2O3
基础达标
1.(2023·烟台模拟)“等一帘烟雨,候十里春风”,是对二十四节气中“雨水”的形象描述。随着“雨水”之后雨量的增多,空气湿度逐渐增大的原因是 ( )
A.每个水分子体积变大
B.水分子分解加快
C.每个水分子质量增大
D.水分子数目增多
2.(2023·株洲中考)地壳中含量最多的金属元素是 ( )
A.Si B.Fe C.Al D.O
梯级训练·提素能
D
C
3.(2023·扬州中考)构成物质的微粒有分子、原子、离子等。下列物质由离子构成的是 ( )
C
4.(2023·荆州中考)对下列事实的微观解释错误的是 ( )
A.气体可压缩存储于钢瓶中——分子之间有间隔
B.花园里百花盛开,香气四溢——分子在不停运动
C.一氧化碳和二氧化碳的化学性质不同——分子的大小不同
D.金刚石与石墨的物理性质差异很大——碳原子排列方式不同
C
5.(2023·济南中考)如图分别为某微观粒子的结构示意图(图1)和元素周期表部
分内容(图2),结合图示信息判断,下列有关图1所示微观粒子的说法,合理的是
( )
A.该粒子是阳离子
B.该粒子最外层有8个电子
C.该粒子的相对原子质量为16.00
D.该粒子在化学反应中易失去电子
C
6.(2023·济宁任城模拟)同学们在化学实验室中用浓盐酸与浓氨水进行了以下实验,下列有关分析正确的是 ( )
A.①中的X溶液是酚酞溶液
B.①中的现象说明浓盐酸有挥发性
C.②中将Y溶液换成X溶液后无现象
D.③中的现象可证明分子在不断运动
D
7.化学是在原子、分子水平上研究物质及其变化规律的基础学科,以下说法正确的是 ( )
A.原子得失电子变成离子后,元素种类发生改变
B.原子、分子、离子都可以直接构成物质
C.保持水的化学性质的最小粒子是氢原子和氧原子
D.分子是构成物质的基本粒子,空气由空气分子构成
B
8. (2023·内江中考)如图为铝原子结构示意图。下列有关铝原子的说法正确的是 ( )
A.图中“+”表示铝原子带正电
B.铝原子的质量主要集中在核外13个电子上
C.铝原子在化学反应中易得到电子
D.铝原子核外有3个电子层
D
9.(2023·安徽中考)钠与氯气反应生成氯化钠的示意图如下。下列有关说法正确的是 ( )
A.氯化钠固体由分子构成
B.反应中一个钠原子失去一个电子,形成相对稳定结构
C.氯原子核外有两个电子层
D.反应中Cl变成Cl-,证明化学反应中元素种类发生改变
B
10.(2023·滨州中考)元素周期表是学习和研究化学的重要工具。如图中①、②为氧元素、铝元素在元素周期表中的信息示意图,A、B、C、D是四种粒子的结构示意图。试分析如图并回答问题:
(1)氧元素位于元素周期表的第________周期,铝元素属于__________(填“金属”
或“非金属”)元素;
(2)C粒子是____________(填“原子”“阴离子”或“阳离子”);若D是原子,
则X=_______;
(3)A、B、C、D中属于同种元素的是________(填字母,下同);
(4)A粒子的化学性质与图中_______粒子的化学性质相似。
二
金属
阴离子
8
BC
B
能力提升
1.(2023·泰安中考)对下列事实的解释不合理的是 ( )
A.通过气味区别氮气和氨气——分子是运动的,不同分子的性质不同
B.干冰升华为二氧化碳气体——状态变化,分子大小随之变化
C.氧气经压缩储存在钢瓶中——压强增大,分子之间的间隔变小
D.蔗糖在热水中溶解更快——温度升高,分子的运动速率加快
B
2.(2023·淄博淄川模拟)认识物质的微观世界是化学学科的重要内容之一,关于
下列微粒说法错误的是 ( )
A.①④属于相对稳定结构
B.它们表示四种不同的元素
C.③表示是阳离子
D.②表示的元素在化合物中通常显-2价
C
3.“宏观—微观—符号”三重表征,是化学学科知识的表征方式和特有的思维方式。
(1)从微观的角度研究物质的结构,如图1是氯元素在元素周期表中的信息,其中
氯原子的相对原子质量是__________,其核电荷数是________,氯元素的元素符
号为________,氯化钠中氯元素的化合价为_________。
(2)如图2,请写出臭氧化学式:________。
35.45
17
Cl
-1价
O3
(3)从微观知变化及本质:请从微观角度阐述氧气在紫外线照射的条件下转化为
臭氧的过程:________________________________________________________
_______________。
(4)图3是锶元素的结构示意图,图4中的三种元素,与锶元素化学性质相似的是
________(填元素符号);氯化锶是常用的牙膏脱敏剂,易溶于水,可由氢氧化锶与
盐酸反应制备,该反应的化学方程式为________________________________。
在紫外线照射的条件下,氧分子分解为氧原子,每3个氧原子结合
成1个臭氧分子
Mg
Sr(OH)2+2HCl===SrCl2+2H2O
4.(2023·岳阳中考)元素周期表是学习和研究化学的重要工具,下面是元素周期
表的部分内容,请根据下表回答问题:
(1)发现了元素周期律并编制出元素周期表的化学家是_______(填字母)。
A.门捷列夫 B.拉瓦锡
C.道尔顿 D.阿伏加德罗
(2)氟元素是人体必需微量元素之一,能防治龋齿。氟元素的相对原子质量为
__________。
A
19.00
(3)已知某微粒的结构示意图为 ,请写出该微粒的符号:________。
(4)地壳中含量最多的金属元素和最多的非金属元素组成的化合物的化学式
为__________。
(5)表中Ne和Ar的化学性质相似的原因是____________________________。
O2-
Al2O3
原子的最外层电子数相同
第三单元
物质构成的奥秘
第一节
构成物质的微粒 元素
知识清单·理脉络
一、构成物质的微粒
二、元素
易错辨析
判断下列说法是否正确。
(1)原子不能直接构成物质。 ( )
(2)分子由原子构成,所以分子一定比原子大。 ( )
(3)原子的质量主要集中在原子核上,电子质量可以忽略不计。 ( )
(4)2Fe2+表示两个铁离子。 ( )
(5)一氧化碳、二氧化碳二者化学性质不同,原因是分子不同。 ( )
(6)保持水的化学性质的粒子是氢原子和氧原子。 ( )
(7)水银体温计可以测定体温是因为汞分子之间的间隔发生变化。 ( )
(8)同种元素的原子核内质子数和中子数一定相等。 ( )
(9)镁的相对原子质量为24 g。 ( )
×
×
√
×
√
×
×
×
×
追根溯源(教材习题变式)
1.下列叙述错误的是 ( )
A.分子、原子、离子都可以直接构成物质
B.任何原子都是由质子、中子、电子构成的
C.化学反应中,分子可分,原子不能再分
D.原子的质量主要集中在原子核上
B
2.天宫课堂中,航天员王亚平视频展示了在无容器材料实验柜中进行的“锆金属熔化与凝固”实验。如图是锆元素在元素周期表中的信息及原子结构示意图。下列说法错误的是 ( )
A.锆原子的质子数为40
B.氯化锆的化学式可能为ZrCl2
C.锆元素的相对原子质量为91.22 g
D.锆原子在化学反应中容易失去2个电子
C
3.化学家张青莲主持测定了铟、铱、锌等元素相对原子质量的新值。碳-12原
子的质量为1.993×10-26 kg,一种锌原子的质量为1.096×10-25kg,该锌原子的相对
原子质量是( )
A.12 B.64
C.66 D.1.096×10-25 kg
C
4.如图是元素周期表的一部分信息,下列说法错误的是 ( )
A.氟原子的相对原子质量为19.00
B.硫原子的核电荷数是16
C.氟、硫、氯三种元素都属于非金属元素
D.氟元素和氯元素位于元素周期表的同一周期
D
5.在宏观、微观和符号之间建立联系是化学学科的重要思维方式。
(1)图一为构成物质的粒子之间的关系。
图一中字母a代表__________,字母b代表______________。
原子
核外电子
(2)结构决定性质,请根据下列粒子结构示意图给出的信息回答:
其中属于同种元素是________(填序号),属于阴离子是_______(填序号),化学性
质相似的是________(填序号)。
BC
C
BD
6.一些粒子的结构都可用示意图 来表示。请回答下列问题:
(1)图中x表示的是_______________________。
(2)若x=12,则对应的元素符号为________。
(3)若x-y=3,则该粒子的符号为_________。
(4)若x=8,则y的值可能为__________。
质子数(或核电荷数)
Mg
Na+
6或8
考点一 构成物质的微粒
【示范题1】(2023·岳阳中考)推理是化学学习的一种常用思维方法。下列推理正确的是 ( )
A.分子能构成物质,所以物质都是由分子构成的
B.离子是带电的微观粒子,所以带电的微观粒子都是离子
C.由同种元素组成的纯净物是单质,所以单质只含有一种元素
D.碳酸钙能与稀盐酸反应生成气体,所以与稀盐酸反应产生气体的物质一定是碳酸钙
考点突破·释疑难
C
考点二 粒子结构示意图
【示范题2】(2023·株洲中考)如图为某元素原子的结构示意图。下列有关叙述不正确的是 ( )
A.该原子的结构示意图中x=1
B.该元素属于活泼的非金属元素
C.该元素的原子在化学反应中容易失去电子
D.该元素形成的单质容易与氧气反应
B
【方法点拨】 根据结构示意图判断粒子的种类
考点三 元素周期表
【示范题3】(2023·邵阳中考)中国承建的阿尔卡萨光伏电站是卡塔尔首座太阳能发电站。硅太阳能电池主要材料是高纯硅,如图是硅元素的相关信息和硅原子的结构示意图,下列关于硅的说法错误的是 ( )
A.x的数值为4
B.硅元素属于非金属元素
C.硅元素的相对原子质量为28.09 g
D.硅元素位于元素周期表的第三周期
C
命题点一 构成物质的微粒
1.(2019·淄博中考)公共场所禁止吸烟。香烟的烟雾中含有四千多种化学物质,
大多属于有害物质。吸烟者吸烟会造成非吸烟者被动吸烟的主要原因是( )
A.分子的质量很小 B.分子之间有间隔
C.分子的体积很小 D.分子不断地运动
2.(2022·泰安中考)下列物质是由分子构成的是 ( )
A.氢氧化钾 B.铝
C.金刚石 D.甲烷
五四制地区5年真题
D
D
3.(2022·烟台中考)下列有关化学史的叙述错误的是 ( )
A.汤姆森发现电子
B.卢瑟福发现原子核
C.门捷列夫编制了元素周期表
D.拉瓦锡发现酸碱指示剂
D
4.(2022·威海中考)下列认识不正确的是( )
A.微粒的运动和变化是导致物质发生变化的原因
B.原子虽小,既有质量又有能量
C.繁多复杂的物质是由种类有限的元素组成的
D.离子带电,所以不能构成物质
D
5.(2022·威海中考)下列对宏观现象的微观解释不正确的是 ( )
A.金刚石的硬度比石墨大——碳原子的内部结构不同
B.稀盐酸和稀硫酸都能使紫色石蕊试液变红——稀盐酸和稀硫酸中都含有氢离子
C.5 mL水与5 mL酒精混合后总体积小于10 mL——分子之间有间隔
D.氧气能支持燃烧,二氧化碳不能支持燃烧——不同种分子的化学性质不同
A
6.(2022·淄博中考)科学思维是从宏观、微观相结合的视角探究物质及其变化规律的认识方式。下列对宏观事实的微观解释错误的是 ( )
选项 宏观事实 微观解释
A 氢氧化钠溶液和氢氧化钾溶液具有相似的化学性质 两种溶液中都含有OH-
B 加热氧化汞得到汞和氧气 化学反应前后分子改变,原子不变
C 结成冰的水不能流动 温度降到零度以下后,水分子不再运动
D 把食盐颗粒放入水中充分搅拌后,食盐颗粒很快消失 在水分子作用下,氯化钠解离成钠离子和氯离子,扩散到水中,形成了氯化钠溶液
C
7.(2021·淄博中考)化学是在原子、分子水平上研究物质及其变化规律的一门基础自然科学。从原子、分子的角度分析,下列解释错误的是 ( )
A.一滴水中含有约1021个水分子——说明水分子很小
B.品红加入水中,整杯液体变为红色——说明分子在不断运动
C.原子的质量主要集中在原子核上——说明原子核是不可分割的实心球体
D.过氧化氢分解生成氧气和水——说明分子可以分成原子,原子可重新组合成新分子
C
8.(2023·威海中考)下列关于分子、原子、离子的认识不正确的是 ( )
A.在化学变化中,分子可以被创造也可以被消灭
B.原子得失电子变成离子后,质量几乎不变,化学性质差别很大
C.同种原子通过不同方式结合成的分子化学性质不同
D.同种分子排列方式不同,则化学性质不同
D
9.(2020·淄博中考)化学是在原子、分子水平上研究物质及其变化规律的一门学科,它能指导我们更好地认识、改造和应用物质。以下说法正确的是 ( )
A.质子、中子、电子都可以直接构成物质
B.原子、分子、离子都可以直接构成物质
C.分子是由原子构成的,水由氢原子和氧原子构成
D.分子是构成物质的基本粒子,空气由空气分子构成
B
10.(2019·淄博中考)世界万物都是由极其微小的粒子构成的,下列说法正确的
是( )
A.海水是由海水分子构成的
B.分子、原子、离子都能直接构成物质
C.二氧化碳是由碳原子和氧原子构成的
D.自然界中的物质都是由质子、中子、电子等粒子构成的
B
11.(2023·烟台中考)下列对宏观事实的微观解释错误的是 ( )
A.自然界中水的天然循环——水分子不断运动且间隔发生改变
B.氧气经压缩储存在钢瓶中——氧气分子体积变小
C.稀盐酸和稀硫酸具有相似的化学性质——酸溶液中都含有氢离子
D.一氧化碳和二氧化碳化学性质不同——构成二者的分子不同
B
12.(2020·济宁中考)对下列物质构成的说法中,不正确的是 ( )
A.铜是由铜原子构成的金属单质
B.氧气是由氧分子构成的气体单质
C.水是由水分子构成的化合物
D.氯化钠是由氯化钠分子构成的化合物
13.(2021·东营中考)下列观点不正确的是 ( )
A.化学改变世界的途径是使物质发生化学变化,实现物质与能量的互相转化
B.物质都是由极其微小的粒子构成的,原子是构成一切化学物质的基本单元
C.溶解就是溶质分子或离子通过自身不断运动分散到溶剂中的过程
D.过滤是分离颗粒大小不同的混合物的方法
D
C
14.(2021·淄博中考)原子结构示意图能简明地表示原子核外电子的排布。
小云从如图微粒结构示意图中获得相关信息,你认为正确的是 ( )
A.②③属于同一种原子
B.①②属于同一种元素
C.①③表示的都是原子
D.②③表示质子数相同
B
15.(2023·威海中考)从原子论到分子学说原子-分子论的创立,奠定了近代化学的基础,阅读下列材料回答问题:
材料一:1803年,道尔顿提出原子论,认为所有物质都是由原子构成的。单质由原子直接构成,同种原子相互排斥不能结合;化合物由“复杂原子”构成,“复杂原子”由不同原子按一定整数比例简单构成。
材料二:1811年,阿伏加德罗引入新的概念——分子,提出了分子学说。对于化合物而言,分子相当于道尔顿所谓的“复杂原子”;对于单质而言,同种原子可以结合成单质分子。
(1)完成下列表格
(2)上表微粒中符合道尔顿“复杂原子”的是__________________(写化学式)。
物质 葡萄糖 氢气 二氧化硫 氦气
构成物质的微粒 (写微粒符号) ________ ___ ____ ___
C6H12O6
H2
SO2
He
C6H12O6、SO2
(3)你同意材料一中加点部分的观点吗 ____________,请选用(1)表中的物质说
明理由:______________________________________________________。
(4)从原子论的创立到分子学说的提出,谈谈你对科学理论的发展有何感想:
_________________________________________________________________。
不同意
氢气由氢分子构成,每个氢分子由两个相同的氢原子构成
科学理论的发展需要大胆创新(或科学理论是不断传承和发展的,合理即可)
命题点二 元素与元素周期表
1.(2022·泰安中考)我们在商场常看到“补锌”“补铁”等字样的食品,其中“锌”“铁”是指( )
A.元素 B.原子 C.分子 D.单质
2.(2023·东营中考)元素周期表是学习和研究化学的工具之一。如图是元素周期表中某元素的信息,下列说法正确的是 ( )
A.该元素的名称是磷
B.该元素原子核外有14个电子
C.该元素的相对原子质量是28.09 g
D.该元素属于金属元素
A
B
3.(2019·淄博中考)今年是元素周期表诞生150周年,联合国宣布2019年为“国际化学元素周期表年”。元素周期表是学习和研究化学的重要工具,对于元素周期表的认识不正确的是 ( )
A.利用元素周期表预测新元素的化学性质
B.利用元素周期表预测新元素的原子结构
C.利用元素周期表查找某元素在自然界中的含量
D.利用元素周期表可查找某原子的相对原子质量
4.(2019·淄博中考)氧气、氮气、甲烷、乙炔、葡萄糖、淀粉、生理盐水都是生活中常用的物质,这些物质中所包含的元素种类有 ( )
A.2种 B.4种 C.6种 D.8种
C
C
5.(2022·烟台中考节选)2022年第二十四届冬季奥林匹克运动会在北京圆满举行,
本届冬奥会处处体现“低碳环保”理念,科技感十足。
场馆:“冰丝带”是由3360块发电玻璃拼成。发电玻璃是在普通玻璃上覆盖一层
碲化镉(化学式CdTe)。碲化镉在弱光照射下也能持续发电,为冬奥场馆提供电
力支持。根据如图信息:Te的相对原子质量是__________,Cd的质子数是
________,CdTe中Te的化合价是_______。
127.6
48
-2
6.(2022·淄博中考)元素周期表是学习和研究化学的重要工具。如图是钙原子的
结构示意图及钙元素在元素周期表中的相关信息。
(1)钙元素的原子序数是________,它属于______________(填写“金属元素”或
“非金属元素”)。
(2)钙原子在化学反应中容易失去电子形成离子,钙离子的符号是_________,
氧化钙中钙元素的化合价是________。
(3)人体缺乏钙元素就会导致_______(填字母)。
a.甲状腺肿大 b.骨质疏松症
c.贫血症
20
金属元素
Ca2+
+2
b
7.(2023·烟台中考)2022年8月9日,国内首条磁浮空轨列车“兴国号”在赣州兴国县首发,该列车
使用了钕铁硼稀土类永磁体,这种永磁体因其优异的磁性而被称为“磁王”。
(1)稀土元素是钪、钇等十七种元素的总称,这些不同种元素之间的本质区别是
________________。
(2)“兴国号”攻克了薄壁铝合金车体焊接技术,焊接时用氩气作保护气是因为氩气的化学性质
__________,铝具有抗腐蚀性的原因是常温下能跟氧气反应生成致密而坚固的氧化铝薄膜,
该反应的化学方程式是______________________。
(3)钕元素在元素周期表中的部分信息如图所示,钕原子的质子数是________。
已知氯化钕的化学式为NdCl3,则相同价态钕的氧化物的化学式是_______。
质子数不同
稳定
4Al+3O2===2Al2O3
60
Nd2O3
基础达标
1.(2023·烟台模拟)“等一帘烟雨,候十里春风”,是对二十四节气中“雨水”的形象描述。随着“雨水”之后雨量的增多,空气湿度逐渐增大的原因是 ( )
A.每个水分子体积变大
B.水分子分解加快
C.每个水分子质量增大
D.水分子数目增多
2.(2023·株洲中考)地壳中含量最多的金属元素是 ( )
A.Si B.Fe C.Al D.O
梯级训练·提素能
D
C
3.(2023·扬州中考)构成物质的微粒有分子、原子、离子等。下列物质由离子构成的是 ( )
C
4.(2023·荆州中考)对下列事实的微观解释错误的是 ( )
A.气体可压缩存储于钢瓶中——分子之间有间隔
B.花园里百花盛开,香气四溢——分子在不停运动
C.一氧化碳和二氧化碳的化学性质不同——分子的大小不同
D.金刚石与石墨的物理性质差异很大——碳原子排列方式不同
C
5.(2023·济南中考)如图分别为某微观粒子的结构示意图(图1)和元素周期表部
分内容(图2),结合图示信息判断,下列有关图1所示微观粒子的说法,合理的是
( )
A.该粒子是阳离子
B.该粒子最外层有8个电子
C.该粒子的相对原子质量为16.00
D.该粒子在化学反应中易失去电子
C
6.(2023·济宁任城模拟)同学们在化学实验室中用浓盐酸与浓氨水进行了以下实验,下列有关分析正确的是 ( )
A.①中的X溶液是酚酞溶液
B.①中的现象说明浓盐酸有挥发性
C.②中将Y溶液换成X溶液后无现象
D.③中的现象可证明分子在不断运动
D
7.化学是在原子、分子水平上研究物质及其变化规律的基础学科,以下说法正确的是 ( )
A.原子得失电子变成离子后,元素种类发生改变
B.原子、分子、离子都可以直接构成物质
C.保持水的化学性质的最小粒子是氢原子和氧原子
D.分子是构成物质的基本粒子,空气由空气分子构成
B
8. (2023·内江中考)如图为铝原子结构示意图。下列有关铝原子的说法正确的是 ( )
A.图中“+”表示铝原子带正电
B.铝原子的质量主要集中在核外13个电子上
C.铝原子在化学反应中易得到电子
D.铝原子核外有3个电子层
D
9.(2023·安徽中考)钠与氯气反应生成氯化钠的示意图如下。下列有关说法正确的是 ( )
A.氯化钠固体由分子构成
B.反应中一个钠原子失去一个电子,形成相对稳定结构
C.氯原子核外有两个电子层
D.反应中Cl变成Cl-,证明化学反应中元素种类发生改变
B
10.(2023·滨州中考)元素周期表是学习和研究化学的重要工具。如图中①、②为氧元素、铝元素在元素周期表中的信息示意图,A、B、C、D是四种粒子的结构示意图。试分析如图并回答问题:
(1)氧元素位于元素周期表的第________周期,铝元素属于__________(填“金属”
或“非金属”)元素;
(2)C粒子是____________(填“原子”“阴离子”或“阳离子”);若D是原子,
则X=_______;
(3)A、B、C、D中属于同种元素的是________(填字母,下同);
(4)A粒子的化学性质与图中_______粒子的化学性质相似。
二
金属
阴离子
8
BC
B
能力提升
1.(2023·泰安中考)对下列事实的解释不合理的是 ( )
A.通过气味区别氮气和氨气——分子是运动的,不同分子的性质不同
B.干冰升华为二氧化碳气体——状态变化,分子大小随之变化
C.氧气经压缩储存在钢瓶中——压强增大,分子之间的间隔变小
D.蔗糖在热水中溶解更快——温度升高,分子的运动速率加快
B
2.(2023·淄博淄川模拟)认识物质的微观世界是化学学科的重要内容之一,关于
下列微粒说法错误的是 ( )
A.①④属于相对稳定结构
B.它们表示四种不同的元素
C.③表示是阳离子
D.②表示的元素在化合物中通常显-2价
C
3.“宏观—微观—符号”三重表征,是化学学科知识的表征方式和特有的思维方式。
(1)从微观的角度研究物质的结构,如图1是氯元素在元素周期表中的信息,其中
氯原子的相对原子质量是__________,其核电荷数是________,氯元素的元素符
号为________,氯化钠中氯元素的化合价为_________。
(2)如图2,请写出臭氧化学式:________。
35.45
17
Cl
-1价
O3
(3)从微观知变化及本质:请从微观角度阐述氧气在紫外线照射的条件下转化为
臭氧的过程:________________________________________________________
_______________。
(4)图3是锶元素的结构示意图,图4中的三种元素,与锶元素化学性质相似的是
________(填元素符号);氯化锶是常用的牙膏脱敏剂,易溶于水,可由氢氧化锶与
盐酸反应制备,该反应的化学方程式为________________________________。
在紫外线照射的条件下,氧分子分解为氧原子,每3个氧原子结合
成1个臭氧分子
Mg
Sr(OH)2+2HCl===SrCl2+2H2O
4.(2023·岳阳中考)元素周期表是学习和研究化学的重要工具,下面是元素周期
表的部分内容,请根据下表回答问题:
(1)发现了元素周期律并编制出元素周期表的化学家是_______(填字母)。
A.门捷列夫 B.拉瓦锡
C.道尔顿 D.阿伏加德罗
(2)氟元素是人体必需微量元素之一,能防治龋齿。氟元素的相对原子质量为
__________。
A
19.00
(3)已知某微粒的结构示意图为 ,请写出该微粒的符号:________。
(4)地壳中含量最多的金属元素和最多的非金属元素组成的化合物的化学式
为__________。
(5)表中Ne和Ar的化学性质相似的原因是____________________________。
O2-
Al2O3
原子的最外层电子数相同
同课章节目录
