2024中考一轮复习 鲁教版化学 教材基础复习 第七单元 第二节 物质的溶解性 课件(共53张PPT)
文档属性
| 名称 | 2024中考一轮复习 鲁教版化学 教材基础复习 第七单元 第二节 物质的溶解性 课件(共53张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-25 00:00:00 | ||
图片预览








文档简介
(共53张PPT)
第二节
物质的溶解性
知识清单·理脉络
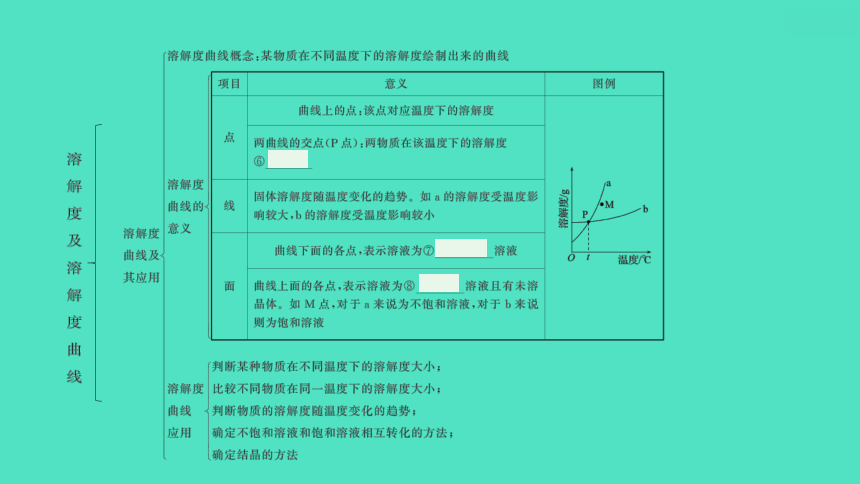
溶解度及溶解度曲线
易错辨析
判断下列说法是否正确。
(1)20 ℃时,10 g食盐溶解在100 g水中,所以20 ℃时,食盐的溶解度是10 g。( )
(2)100 g水中溶解了36 g食盐刚好达到饱和,所以食盐的溶解度是36 g。( )
(3)20 ℃时,100 g水里最多溶解了33.3 g氯化铵,则20 ℃时氯化铵的溶解度是33.3。( )
(4)20 ℃时,100 g硝酸钾的饱和溶液含硝酸钾24 g,则20 ℃时硝酸钾的溶解度是
24 g。 ( )
(5)两种物质溶解度曲线的交点表示该温度下两种物质的溶液溶质质量分数
一定相同。( )
(6)氢氧化钙的饱和溶液降温会析出固体。 ( )
×
×
×
×
×
×
追根溯源(教材习题变式)
1.与固体溶解度大小无关的因素是 ( )
A.温度 B.溶剂的多少
C.溶质的种类 D.溶剂的种类
2.夏季下雨之前,天气闷热,水中的含氧量降低,养鱼池中的鱼往往会浮出
水面。下列有关说法错误的是 ( )
A.氧气的溶解度会随压强的减小而减小
B.氧气的溶解度会随温度的升高而增大
C.为了增加养鱼池中的含氧量,可以向养鱼池中通入空气
D.为了增加养鱼池中的含氧量,可以把养鱼池的水喷向空中
B
B
3.下列说法正确的是 ( )
A.氯化钠的溶解度为36克
B.饱和溶液的质量分数一定比不饱和溶液的质量分数大
C.在一定温度下,搅拌不能改变硝酸钾的溶解度
D.固体物质的溶解度都是随着温度的升高而增大
C
4.溶解度曲线所表示的意义是 ( )
①同一种物质在不同温度下溶解度的大小
②不同种物质在同一温度下溶解度的大小
③物质溶解度受温度变化影响的大小
④比较不同物质的溶解度
A.仅①②③ B.①②
C.①②③④ D.①③④
C
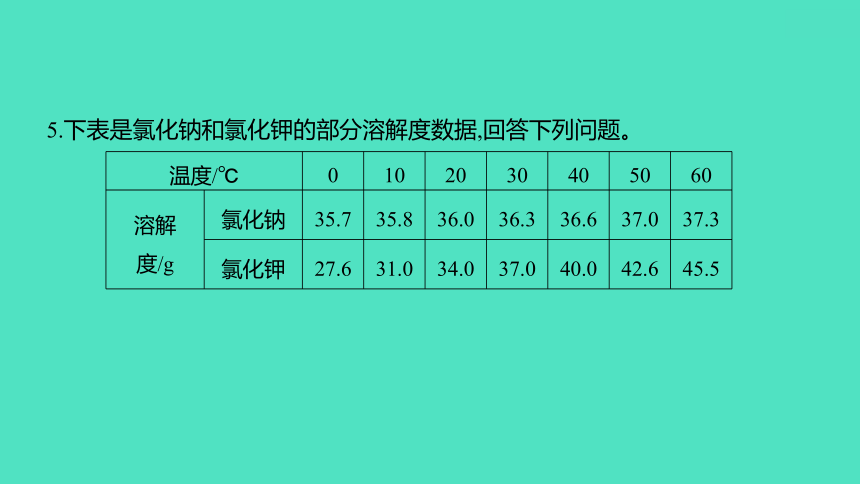
5.下表是氯化钠和氯化钾的部分溶解度数据,回答下列问题。
温度/℃ 0 10 20 30 40 50 60
溶解 度/g 氯化钠 35.7 35.8 36.0 36.3 36.6 37.0 37.3
氯化钾 27.6 31.0 34.0 37.0 40.0 42.6 45.5
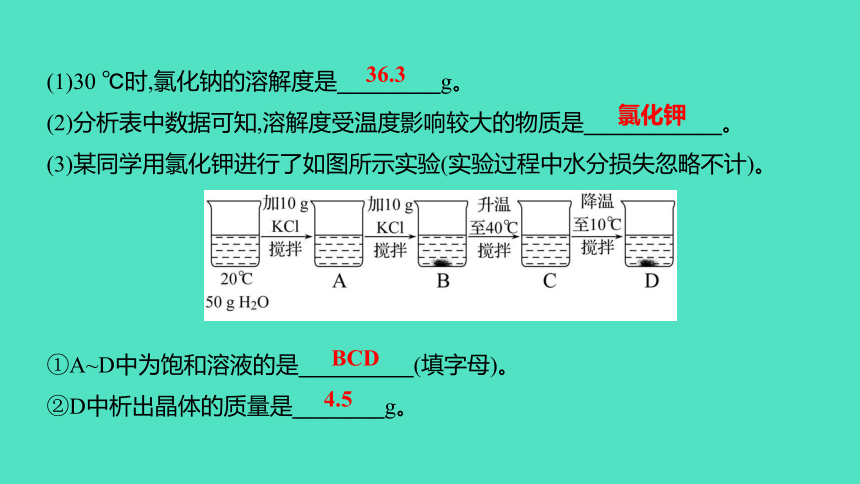
(1)30 ℃时,氯化钠的溶解度是_________g。
(2)分析表中数据可知,溶解度受温度影响较大的物质是____________。
(3)某同学用氯化钾进行了如图所示实验(实验过程中水分损失忽略不计)。
①A~D中为饱和溶液的是__________(填字母)。
②D中析出晶体的质量是________g。
36.3
氯化钾
BCD
4.5
考点 溶解度曲线及其应用
【示范题1】(2023·永州中考)甲、乙两种物质的溶解度曲线如图所示。
下列说法正确的是 ( )
A.阴影部分的任意点表明甲、乙两种溶液都是饱和溶液
B.P点时,甲、乙两种溶液的溶质质量分数相等
C.t2 ℃时,在100 g水中加入60 g甲,形成不饱和溶液
D.t1 ℃时,甲、乙的饱和溶液升温至t2 ℃,溶液的溶质质
量分数:甲>乙
考点突破·释疑难
B
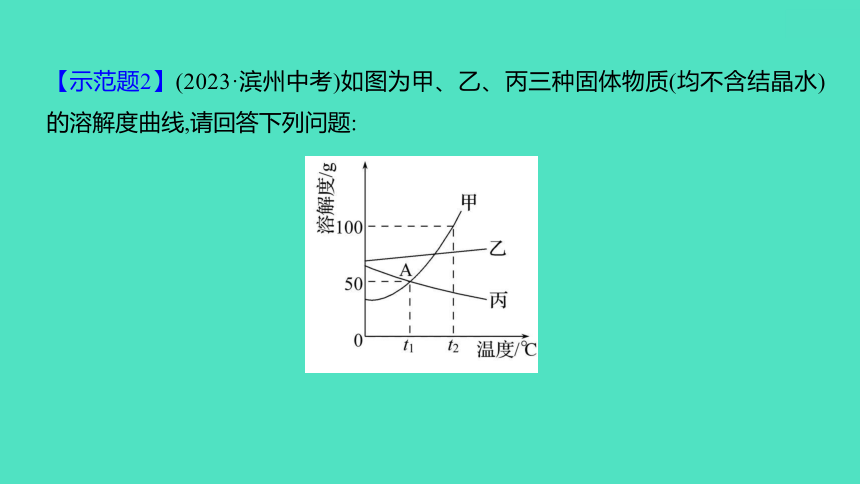
【示范题2】(2023·滨州中考)如图为甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,请回答下列问题:
(1)当温度为_______℃时;甲物质的溶解度等于丙物质的溶解度;
(2)图中A点表示乙物质在t1 ℃时的____________(填“饱和”或“不饱和”)溶液;
(3)若甲中含有少量乙时,可以采用______________(填“降温结晶”或“蒸发结晶”)
的方法提纯甲;
(4)将t2 ℃时接近饱和的丙溶液变成饱和溶液,下列方法不能达到目的的
是_______;
A.蒸发溶剂 B.降低温度 C.增加溶质 D.升高温度
(5)将t2 ℃时100 g甲的饱和溶液稀释成溶质质量分数为25%的溶液,需加水的
质量为_________g。
t1
不饱和
降温结晶
B
100
【方法点拨】
1.熟悉溶解度曲线中点、线、面的意义:
(1)点:曲线上的点叫饱和点。曲线上任一点表示对应温度下(横坐标)该物质的溶解度(纵坐标);两曲线的交点表示两物质在交点的温度下溶解度相等。
(2)线:溶解度曲线表示物质的溶解度随温度变化的趋势。
(3)面:溶解度曲线下方的面表示不同温度下该物质的不饱和溶液;溶解度曲线上方的面表示相应温度下的饱和溶液且有未溶解的溶质。
2.明确根据溶解度曲线确定分离混合物的方法:
(1)陡升型的物质中混有少量缓升型或缓降型的物质时,可采用降温结晶的方法进行提纯。
(2)缓升型的物质中含有少量陡升型物质时,可采用蒸发结晶的方法进行提纯。
命题点一 溶解性与溶解度
1.( 2019·东营中考 )夏季,鱼虾养殖池内常设置一些水泵,把水喷向空中,
从化学角度分析,喷水的目的是 ( )
A.降低养殖池内水的温度
B.增大与空气的接触面积,便于氧气溶解
C.增加观赏性
D.便于太阳照射,杀灭水中的病菌
五四制地区5年真题
B
2.(2022·济宁中考)利用20 ℃时KNO3溶液(有少量未溶解的KNO3晶体)见图Ⅰ,进行下面实验:
①加入NH4NO3固体后,实验结果见图Ⅱ;
②加入NaOH固体后,实验结果见图Ⅲ。
分析实验过程判断,以下说法错误的是( )
A.硝酸铵溶于水时,吸收热量
B.随温度升高,硝酸钾的溶解度增大
C.图Ⅰ、图Ⅱ中,硝酸钾溶液都是饱和溶液
D.图Ⅲ中,硝酸钾溶液一定是不饱和溶液
D
命题点二 溶解度曲线及其应用
1.(2022·淄博中考)如图为硝酸钾和氯化钠在水中的
溶解度曲线,下列说法错误的是 ( )
A.24 ℃时,硝酸钾和氯化钠的溶解度相等
B.硝酸钾中混有少量氯化钠,可用降温结晶的方法提纯硝酸钾
C.10 ℃时,将20 g硝酸钾放入50 g水中,充分搅拌,得到60 g硝酸钾溶液
D.30 ℃时,硝酸钾溶液中溶质的质量分数一定大于氯化钠溶液中溶质的质量分数
D
2.(2022·威海中考)如图为硝酸钾和氯化钠的溶解度曲线,
下列说法正确的是 ( )
A.氯化钠和硝酸钾的溶解度相等
B.20 ℃时,氯化钠饱和溶液中溶质和溶剂的质量比为36∶100
C.将24 ℃时两种物质的饱和溶液升温至40 ℃,硝酸钾溶液的溶质质量分数大于氯化钠溶液的溶质质量分数
D.10 ℃时,分别将硝酸钾和氯化钠的饱和溶液恒温蒸发等质量的水,析出晶体的质量:硝酸钾>氯化钠
B
3.(2019·淄博中考)如图是A、B、C三种固体物质的溶解度曲线,下列说法
正确的是 ( )
A.t1℃时,三种物质的溶解度为B>A>C
B.t2℃时,三种物质的饱和溶液溶质质量分数为A=B>C
C.t3℃时,三种物质的饱和溶液降温至t1℃,仍为饱和溶液
D.t3℃时,三种物质各b g分别放入100 g水中,所得溶液质量相等
B
4.(双选)(2023·烟台中考)KNO3和NaCl的溶解度曲线如图所示,下列叙述正确
的是 ( )
A.KNO3和NaCl都属于易溶物质
B.20 ℃时,100 g KNO3饱和溶液中溶解了32 g KNO3
C.30 ℃时,KNO3溶液的溶质质量分数一定大于NaCl溶液的溶质质量分数
D.当KNO3中混有少量NaCl杂质时,可采取冷却KNO3热饱和溶液的方法提纯
A、D
5.(2022·泰安中考)甲、乙、丙三种固体物质的溶解度曲线
如图所示。下列说法正确的是 ( )
A.图中P点表示10 ℃时丙的饱和溶液
B.10 ℃时,甲、乙、丙三种物质的溶解度,甲的溶解度最大
C.20 ℃时,甲、乙、丙饱和溶液降温至10 ℃,甲溶液中析出固体最多
D.20 ℃时,向130 g乙的饱和溶液中加入20 g水,所得溶液的溶质质量分数变为20%
D
6.(2021·济宁中考)为探究硝酸钾的溶解性,进行了如图实验(见图Ⅰ),结合
KNO3溶解度曲线(见图Ⅱ)判断,下列说法错误的是 ( )
B
A.溶液②、溶液④一定是饱和溶液
B.溶液①、溶液③一定是不饱和溶液
C.溶液②、溶液③的质量:③>②
D.溶液②、溶液③、溶液④的溶质质量分数:③>②=④
7.(2021·淄博中考)如图是A物质的溶解度曲线和B物质在不同温度时的溶解度表。
温度/℃ B物质溶解度/g
0 35
20 38
40 43
60 50
80 60
(1)20 ℃时,A物质的溶解度__________B物质的溶解度(填写“大于”“等于”或“小
于”)。观察A物质的溶解度曲线,对于这类物质,工业上常采取______________方
法,使溶质从溶液中结晶析出,得到化工原料和产品。
(2)80 ℃时,向100 g水中加入50 g B物质,充分溶解后得到的是__________
溶液(填写“饱和”或“不饱和”);此温度时,B物质饱和溶液溶质质量分数为
___________(计算结果精确到0.1%)。
小于
降温结晶
不饱和
37.5%
8.(2023·威海中考)典籍里的化学《天工开物》是我国古代劳动人民在长期生产
生活实践中总结出来的宝贵财富,其中蕴含很多化学知识与方法。
(1)颜料制取:“水银入石亭脂(天然硫),同研……得银朱(HgS)。”银朱是古代作画
的红色颜料。请写出制取银朱的化学方程式:_________________。
Hg+S===HgS
氯化钠的溶解度受温度的影响不大,刮风时水蒸发得快,氯化钠蒸发结晶析出;硫
酸镁的溶解度受温度的影响大,刮东北风温度迅速降低,硫酸镁降温结晶析出
(3)生石灰的制取和应用(图3):“每煤饼一层,垒石(石灰石)一层,铺薪其底,灼火燔(灼烧)之,火力到后,烧酥石性。以水沃之,亦自解散……成质之后,入水永劫不坏。”
①“灼火燔之”涉及的化学方程式为________________________,该反应的基本
反应类型是______________。
②“解散”是因为生石灰遇水由块状变成粉末。该粉末的主要成分是_________
(填化学式)。粉末“成质之后,入水永劫不坏”,可用于船只、墙壁的填缝防水。请写出“粉末成质”的化学方程式:_________________________________;根据
“入水永劫不坏”,推测“成质”后的产物具有的性质是_____________________
(写一条即可)。
CaCO3 CaO+CO2↑
分解反应
Ca(OH)2
Ca(OH)2+CO2===CaCO3↓+H2O
难溶于水(合理即可)
基础达标
1.20 ℃时几种物质的溶解度如表:
梯级训练·提素能
物质名称 氯化钠 氢氧化钙 氯酸钾 硝酸钾
溶解度(克) 36.0 0.165 7.4 31.6
下列说法正确的是 ( )
A.20 ℃时氢氧化钙是难溶物质
B.20 ℃时可以配制出20%的硝酸钾溶液
C.20 ℃时氯酸钾是易溶物质
D.20 ℃时硝酸钾的溶解度比氯化钠大
B
D
3.(2023·达州中考)甲、乙、丙三种固体物质的溶解度曲
线如图所示,结合图示判断,下列说法错误的是 ( )
A.P点表示t2 ℃时甲、乙两种物质的溶解度相等
B.甲中含有少量乙,可用降温结晶的方法提纯甲
C.t3 ℃时,甲溶液的溶质质量分数一定等于20%
D.将等质量的甲、乙、丙饱和溶液,从t3 ℃降到t1 ℃,溶液的质量大小关系为丙>乙>甲
C
4.(2023·天津中考)溶液与人类的生产、生活密切相关。
(1)厨房中的下列物质分别放入水中,能形成溶液的是_______(填字母)。
A.白糖 B.花生油 C.面粉
A
(2)如图为硝酸钾和氯化钠的溶解度曲线示意图。
①t1 ℃时,将40 g硝酸钾加入100 g水中,充分搅拌,形成__________(填“饱和”或
“不饱和”)溶液;
②P点表示t1 ℃时,硝酸钾的溶解度__________(填“大于”“等于”或“小于”)氯化钠
的溶解度;
③将t2 ℃时一定质量的硝酸钾饱和溶液降温到t1 ℃,所得溶液的溶质质量分
数__________(填“增大”“不变”或“减小”)。
饱和
等于
减小
(3)在实验室配制一定溶质质量分数的氯化钠溶液,需要用到的玻璃仪器有试剂
瓶、烧杯、____________、量筒、胶头滴管。
(4)20 ℃时,向40 g溶质质量分数为20%的氯化钠溶液中加入68 g水,若得到该温
度下氯化钠的饱和溶液,至少需要再加入________g氯化钠固体(20 ℃时,氯化钠的
溶解度为36 g)。
玻璃棒
28
5.(2023·重庆中考B卷)神奇的“风暴瓶”能“预报天气,冷暖先知”。制作“风暴瓶”
用到以下物质:樟脑、酒精、KNO3、NH4Cl和水等。
(1)将樟脑的酒精饱和溶液滴入水中,出现了明显的浑浊,说明樟脑在水中的溶解
能力__________(填“强于”或“弱于”)其在酒精中的溶解能力。把樟脑的酒精饱和
溶液降温也出现了晶体。除上述方法外,________________也能使樟脑从溶液
中结晶。
弱于
恒温蒸发溶剂
(2)如图1为KNO3和NH4Cl的溶解度曲线。t3 ℃时将等质量的KNO3、NH4Cl
两种物质的饱和溶液降温到t2 ℃,所得溶液中的溶质质量大小关系为KNO3
_______(填“>”“<”或“=”)NH4Cl。
<
(3)已知X是KNO3或NH4Cl中的一种,小敏同学对该物质进行了如图2所示实验,
据图回答问题。
X是____________,②和③中的溶液分别达到饱和状态还需加入X的质量更大的是
________(填“②”或“③”)。
硝酸钾
③
6.溶液在生产、生活中起着十分重要的作用。请回答(1)(2)题。
(1)如图,在木块上滴几滴水,将装有某种固体的大烧杯放置于木块上,向大烧杯
中加水并搅拌,结果木块上的水结冰了,则大烧杯内的固体可能是_______。
A.氯化钠 B.硝酸铵
C.氢氧化钠 D.蔗糖
B
(2)用汽油或加了洗涤剂的水都能除去衣服上的油污,两者去油污的原理分别
是_______。
A.乳化、乳化 B.乳化、溶解
C.溶解、乳化 D.溶解、溶解
C
如图是甲、乙、丙三种固体物质的溶解度曲线。请回答(3)(4)题。
(3)现有t1 ℃时甲、乙、丙三种物质的饱和溶液,将这三种溶液分别升温到
t2 ℃,所得溶液中溶质质量分数大小关系是_______。
A.甲=乙>丙 B.乙>甲=丙
C.乙>甲>丙 D.甲>乙>丙
(4)为了将接近饱和的丙溶液变为饱和溶液,可采用的方法有________(有2~3个
选项符合题意)。
A.加固体丙 B.加水
C.降低温度 D.蒸发浓缩
C
AD
能力提升
1.(2023·广东中考)“盐穴储气”是一种地下储能技术,进气时采集盐水,采集的盐
水主要含NaCl和少量MgSO4。根据图判断,下列说法正确的是 ( )
A.溶解度:MgSO4>NaCl
B.MgSO4的溶解度随温度升高而增大
C.a ℃时,MgSO4溶液的溶质质量分数为50%
D.将盐水蒸发结晶,可得到较纯的NaCl
D
2.(2023·淄博沂源一模)向装有等量水的A、B、C烧杯中分别加入10 g、25 g、
25 g NaNO3固体,充分溶解后,现象如图一所示,甲、乙对应的溶解度曲线如图
二所示。下列说法错误的 ( )
D
A.图一烧杯中的溶液一定属于饱和溶液的是B
B.在图二中,能表示NaNO3溶解度曲线的是甲
C.欲除去混在甲中的少量乙物质可采用的方法是降温结晶
D.依据图二的分析判断,若分别将100 g甲、乙的饱和溶液从t2 ℃降温到t1 ℃,所得溶液的溶质的质量分数:甲=乙
3.(2023·淄博张店区二模)下表是两种硫酸盐在不同温度时的溶解度:
温度/℃ 0 10 20 30 40 50 60 70 80
溶解 度/g 硫酸钠 4.9 9.1 19.5 40.8 48.8 46.2 45.3 44.3 43.7
硫酸铈 24.1 20.0 17.2 14.0 10.0 8.9 8.3 7.1 6.0
下列说法正确的是 ( )
A.随温度升高,物质的溶解度只可能不断增大或不断减小
B.在0~80 ℃间的任何温度下,硫酸钠和硫酸铈的溶解度均不相等
C.某温度下,向等质量水中分别加入等质量硫酸钠和硫酸铈,充分溶解后,前者的溶质质量分数可能大于、等于或小于后者
D.将100 g 30 ℃时的饱和硫酸铈溶液加热到40 ℃(加热过程中水的蒸发忽略不计),从溶液中可析出4 g硫酸铈晶体
C
4.(2023·东营中考)有一种浸洗瓜果的“果蔬洗盐”,其主要成分是氯化钠、碳酸钠
和碳酸氢钠。
(1)从物质类别看,“果蔬洗盐”属于____________(填“纯净物”或“混合物”),“果蔬洗
盐”溶于水配成溶液后的pH_______7(填“>”“=”或“<”),溶液中最多的阳离子的符
号是_________。
(2)瓜果表面残留的农药一般呈酸性,用“果蔬洗盐”溶液浸洗瓜果有助于消除瓜
果表面的残留农药。请从化学反应的角度解释其中的原因:__________________
____________________。
混合物
>
Na+
碳酸钠、碳酸氢
钠会与酸发生反应
(3)一种固体“果蔬洗盐”的质量组成为食盐50%、碳酸钠10%、碳酸氢钠15%、
其他基料25%时,25 ℃时,取这种“果蔬洗盐”100 g加入100 g水中,判断达到饱和
状态最简单的直观现象是________________,根据三种物质的溶解度曲线(如图)判
断,达到饱和状态的物质是______________________。若将上述饱和溶液降温到
20 ℃时,无晶体析出的物质是____________。
有固体剩余
氯化钠、碳酸氢钠
碳酸钠
(4)生活中浸洗瓜果去除农药残留有多种方法:①淘米水浸泡、冲洗 ②洗洁精浸
泡、冲洗 ③开水烫、冲洗 ④“果蔬洗盐”浸泡、冲洗,既保鲜又环保的方法是
________(填数字序号)。
①
5.张老师在讲授溶液时,用固体M做了如下实验,图一中甲、乙、丙、丁是充分搅拌后静置的现象,请回答相关问题(忽略水的挥发):
(1)上述烧杯中,溶液质量最大的是________(填序号)。
(2)上述实验可以判断物质M的溶解度曲线是图二对应的_______(填序号)。
(3)甲、乙、丙烧杯中的溶液一定呈饱和状态的是________(填序号)。
(4)根据图二,若要使丁烧杯中的溶液恰好达到饱和状态,还需要加入_______g
的M固体。
丁
A
乙
8
第二节
物质的溶解性
知识清单·理脉络
溶解度及溶解度曲线
易错辨析
判断下列说法是否正确。
(1)20 ℃时,10 g食盐溶解在100 g水中,所以20 ℃时,食盐的溶解度是10 g。( )
(2)100 g水中溶解了36 g食盐刚好达到饱和,所以食盐的溶解度是36 g。( )
(3)20 ℃时,100 g水里最多溶解了33.3 g氯化铵,则20 ℃时氯化铵的溶解度是33.3。( )
(4)20 ℃时,100 g硝酸钾的饱和溶液含硝酸钾24 g,则20 ℃时硝酸钾的溶解度是
24 g。 ( )
(5)两种物质溶解度曲线的交点表示该温度下两种物质的溶液溶质质量分数
一定相同。( )
(6)氢氧化钙的饱和溶液降温会析出固体。 ( )
×
×
×
×
×
×
追根溯源(教材习题变式)
1.与固体溶解度大小无关的因素是 ( )
A.温度 B.溶剂的多少
C.溶质的种类 D.溶剂的种类
2.夏季下雨之前,天气闷热,水中的含氧量降低,养鱼池中的鱼往往会浮出
水面。下列有关说法错误的是 ( )
A.氧气的溶解度会随压强的减小而减小
B.氧气的溶解度会随温度的升高而增大
C.为了增加养鱼池中的含氧量,可以向养鱼池中通入空气
D.为了增加养鱼池中的含氧量,可以把养鱼池的水喷向空中
B
B
3.下列说法正确的是 ( )
A.氯化钠的溶解度为36克
B.饱和溶液的质量分数一定比不饱和溶液的质量分数大
C.在一定温度下,搅拌不能改变硝酸钾的溶解度
D.固体物质的溶解度都是随着温度的升高而增大
C
4.溶解度曲线所表示的意义是 ( )
①同一种物质在不同温度下溶解度的大小
②不同种物质在同一温度下溶解度的大小
③物质溶解度受温度变化影响的大小
④比较不同物质的溶解度
A.仅①②③ B.①②
C.①②③④ D.①③④
C
5.下表是氯化钠和氯化钾的部分溶解度数据,回答下列问题。
温度/℃ 0 10 20 30 40 50 60
溶解 度/g 氯化钠 35.7 35.8 36.0 36.3 36.6 37.0 37.3
氯化钾 27.6 31.0 34.0 37.0 40.0 42.6 45.5
(1)30 ℃时,氯化钠的溶解度是_________g。
(2)分析表中数据可知,溶解度受温度影响较大的物质是____________。
(3)某同学用氯化钾进行了如图所示实验(实验过程中水分损失忽略不计)。
①A~D中为饱和溶液的是__________(填字母)。
②D中析出晶体的质量是________g。
36.3
氯化钾
BCD
4.5
考点 溶解度曲线及其应用
【示范题1】(2023·永州中考)甲、乙两种物质的溶解度曲线如图所示。
下列说法正确的是 ( )
A.阴影部分的任意点表明甲、乙两种溶液都是饱和溶液
B.P点时,甲、乙两种溶液的溶质质量分数相等
C.t2 ℃时,在100 g水中加入60 g甲,形成不饱和溶液
D.t1 ℃时,甲、乙的饱和溶液升温至t2 ℃,溶液的溶质质
量分数:甲>乙
考点突破·释疑难
B
【示范题2】(2023·滨州中考)如图为甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,请回答下列问题:
(1)当温度为_______℃时;甲物质的溶解度等于丙物质的溶解度;
(2)图中A点表示乙物质在t1 ℃时的____________(填“饱和”或“不饱和”)溶液;
(3)若甲中含有少量乙时,可以采用______________(填“降温结晶”或“蒸发结晶”)
的方法提纯甲;
(4)将t2 ℃时接近饱和的丙溶液变成饱和溶液,下列方法不能达到目的的
是_______;
A.蒸发溶剂 B.降低温度 C.增加溶质 D.升高温度
(5)将t2 ℃时100 g甲的饱和溶液稀释成溶质质量分数为25%的溶液,需加水的
质量为_________g。
t1
不饱和
降温结晶
B
100
【方法点拨】
1.熟悉溶解度曲线中点、线、面的意义:
(1)点:曲线上的点叫饱和点。曲线上任一点表示对应温度下(横坐标)该物质的溶解度(纵坐标);两曲线的交点表示两物质在交点的温度下溶解度相等。
(2)线:溶解度曲线表示物质的溶解度随温度变化的趋势。
(3)面:溶解度曲线下方的面表示不同温度下该物质的不饱和溶液;溶解度曲线上方的面表示相应温度下的饱和溶液且有未溶解的溶质。
2.明确根据溶解度曲线确定分离混合物的方法:
(1)陡升型的物质中混有少量缓升型或缓降型的物质时,可采用降温结晶的方法进行提纯。
(2)缓升型的物质中含有少量陡升型物质时,可采用蒸发结晶的方法进行提纯。
命题点一 溶解性与溶解度
1.( 2019·东营中考 )夏季,鱼虾养殖池内常设置一些水泵,把水喷向空中,
从化学角度分析,喷水的目的是 ( )
A.降低养殖池内水的温度
B.增大与空气的接触面积,便于氧气溶解
C.增加观赏性
D.便于太阳照射,杀灭水中的病菌
五四制地区5年真题
B
2.(2022·济宁中考)利用20 ℃时KNO3溶液(有少量未溶解的KNO3晶体)见图Ⅰ,进行下面实验:
①加入NH4NO3固体后,实验结果见图Ⅱ;
②加入NaOH固体后,实验结果见图Ⅲ。
分析实验过程判断,以下说法错误的是( )
A.硝酸铵溶于水时,吸收热量
B.随温度升高,硝酸钾的溶解度增大
C.图Ⅰ、图Ⅱ中,硝酸钾溶液都是饱和溶液
D.图Ⅲ中,硝酸钾溶液一定是不饱和溶液
D
命题点二 溶解度曲线及其应用
1.(2022·淄博中考)如图为硝酸钾和氯化钠在水中的
溶解度曲线,下列说法错误的是 ( )
A.24 ℃时,硝酸钾和氯化钠的溶解度相等
B.硝酸钾中混有少量氯化钠,可用降温结晶的方法提纯硝酸钾
C.10 ℃时,将20 g硝酸钾放入50 g水中,充分搅拌,得到60 g硝酸钾溶液
D.30 ℃时,硝酸钾溶液中溶质的质量分数一定大于氯化钠溶液中溶质的质量分数
D
2.(2022·威海中考)如图为硝酸钾和氯化钠的溶解度曲线,
下列说法正确的是 ( )
A.氯化钠和硝酸钾的溶解度相等
B.20 ℃时,氯化钠饱和溶液中溶质和溶剂的质量比为36∶100
C.将24 ℃时两种物质的饱和溶液升温至40 ℃,硝酸钾溶液的溶质质量分数大于氯化钠溶液的溶质质量分数
D.10 ℃时,分别将硝酸钾和氯化钠的饱和溶液恒温蒸发等质量的水,析出晶体的质量:硝酸钾>氯化钠
B
3.(2019·淄博中考)如图是A、B、C三种固体物质的溶解度曲线,下列说法
正确的是 ( )
A.t1℃时,三种物质的溶解度为B>A>C
B.t2℃时,三种物质的饱和溶液溶质质量分数为A=B>C
C.t3℃时,三种物质的饱和溶液降温至t1℃,仍为饱和溶液
D.t3℃时,三种物质各b g分别放入100 g水中,所得溶液质量相等
B
4.(双选)(2023·烟台中考)KNO3和NaCl的溶解度曲线如图所示,下列叙述正确
的是 ( )
A.KNO3和NaCl都属于易溶物质
B.20 ℃时,100 g KNO3饱和溶液中溶解了32 g KNO3
C.30 ℃时,KNO3溶液的溶质质量分数一定大于NaCl溶液的溶质质量分数
D.当KNO3中混有少量NaCl杂质时,可采取冷却KNO3热饱和溶液的方法提纯
A、D
5.(2022·泰安中考)甲、乙、丙三种固体物质的溶解度曲线
如图所示。下列说法正确的是 ( )
A.图中P点表示10 ℃时丙的饱和溶液
B.10 ℃时,甲、乙、丙三种物质的溶解度,甲的溶解度最大
C.20 ℃时,甲、乙、丙饱和溶液降温至10 ℃,甲溶液中析出固体最多
D.20 ℃时,向130 g乙的饱和溶液中加入20 g水,所得溶液的溶质质量分数变为20%
D
6.(2021·济宁中考)为探究硝酸钾的溶解性,进行了如图实验(见图Ⅰ),结合
KNO3溶解度曲线(见图Ⅱ)判断,下列说法错误的是 ( )
B
A.溶液②、溶液④一定是饱和溶液
B.溶液①、溶液③一定是不饱和溶液
C.溶液②、溶液③的质量:③>②
D.溶液②、溶液③、溶液④的溶质质量分数:③>②=④
7.(2021·淄博中考)如图是A物质的溶解度曲线和B物质在不同温度时的溶解度表。
温度/℃ B物质溶解度/g
0 35
20 38
40 43
60 50
80 60
(1)20 ℃时,A物质的溶解度__________B物质的溶解度(填写“大于”“等于”或“小
于”)。观察A物质的溶解度曲线,对于这类物质,工业上常采取______________方
法,使溶质从溶液中结晶析出,得到化工原料和产品。
(2)80 ℃时,向100 g水中加入50 g B物质,充分溶解后得到的是__________
溶液(填写“饱和”或“不饱和”);此温度时,B物质饱和溶液溶质质量分数为
___________(计算结果精确到0.1%)。
小于
降温结晶
不饱和
37.5%
8.(2023·威海中考)典籍里的化学《天工开物》是我国古代劳动人民在长期生产
生活实践中总结出来的宝贵财富,其中蕴含很多化学知识与方法。
(1)颜料制取:“水银入石亭脂(天然硫),同研……得银朱(HgS)。”银朱是古代作画
的红色颜料。请写出制取银朱的化学方程式:_________________。
Hg+S===HgS
氯化钠的溶解度受温度的影响不大,刮风时水蒸发得快,氯化钠蒸发结晶析出;硫
酸镁的溶解度受温度的影响大,刮东北风温度迅速降低,硫酸镁降温结晶析出
(3)生石灰的制取和应用(图3):“每煤饼一层,垒石(石灰石)一层,铺薪其底,灼火燔(灼烧)之,火力到后,烧酥石性。以水沃之,亦自解散……成质之后,入水永劫不坏。”
①“灼火燔之”涉及的化学方程式为________________________,该反应的基本
反应类型是______________。
②“解散”是因为生石灰遇水由块状变成粉末。该粉末的主要成分是_________
(填化学式)。粉末“成质之后,入水永劫不坏”,可用于船只、墙壁的填缝防水。请写出“粉末成质”的化学方程式:_________________________________;根据
“入水永劫不坏”,推测“成质”后的产物具有的性质是_____________________
(写一条即可)。
CaCO3 CaO+CO2↑
分解反应
Ca(OH)2
Ca(OH)2+CO2===CaCO3↓+H2O
难溶于水(合理即可)
基础达标
1.20 ℃时几种物质的溶解度如表:
梯级训练·提素能
物质名称 氯化钠 氢氧化钙 氯酸钾 硝酸钾
溶解度(克) 36.0 0.165 7.4 31.6
下列说法正确的是 ( )
A.20 ℃时氢氧化钙是难溶物质
B.20 ℃时可以配制出20%的硝酸钾溶液
C.20 ℃时氯酸钾是易溶物质
D.20 ℃时硝酸钾的溶解度比氯化钠大
B
D
3.(2023·达州中考)甲、乙、丙三种固体物质的溶解度曲
线如图所示,结合图示判断,下列说法错误的是 ( )
A.P点表示t2 ℃时甲、乙两种物质的溶解度相等
B.甲中含有少量乙,可用降温结晶的方法提纯甲
C.t3 ℃时,甲溶液的溶质质量分数一定等于20%
D.将等质量的甲、乙、丙饱和溶液,从t3 ℃降到t1 ℃,溶液的质量大小关系为丙>乙>甲
C
4.(2023·天津中考)溶液与人类的生产、生活密切相关。
(1)厨房中的下列物质分别放入水中,能形成溶液的是_______(填字母)。
A.白糖 B.花生油 C.面粉
A
(2)如图为硝酸钾和氯化钠的溶解度曲线示意图。
①t1 ℃时,将40 g硝酸钾加入100 g水中,充分搅拌,形成__________(填“饱和”或
“不饱和”)溶液;
②P点表示t1 ℃时,硝酸钾的溶解度__________(填“大于”“等于”或“小于”)氯化钠
的溶解度;
③将t2 ℃时一定质量的硝酸钾饱和溶液降温到t1 ℃,所得溶液的溶质质量分
数__________(填“增大”“不变”或“减小”)。
饱和
等于
减小
(3)在实验室配制一定溶质质量分数的氯化钠溶液,需要用到的玻璃仪器有试剂
瓶、烧杯、____________、量筒、胶头滴管。
(4)20 ℃时,向40 g溶质质量分数为20%的氯化钠溶液中加入68 g水,若得到该温
度下氯化钠的饱和溶液,至少需要再加入________g氯化钠固体(20 ℃时,氯化钠的
溶解度为36 g)。
玻璃棒
28
5.(2023·重庆中考B卷)神奇的“风暴瓶”能“预报天气,冷暖先知”。制作“风暴瓶”
用到以下物质:樟脑、酒精、KNO3、NH4Cl和水等。
(1)将樟脑的酒精饱和溶液滴入水中,出现了明显的浑浊,说明樟脑在水中的溶解
能力__________(填“强于”或“弱于”)其在酒精中的溶解能力。把樟脑的酒精饱和
溶液降温也出现了晶体。除上述方法外,________________也能使樟脑从溶液
中结晶。
弱于
恒温蒸发溶剂
(2)如图1为KNO3和NH4Cl的溶解度曲线。t3 ℃时将等质量的KNO3、NH4Cl
两种物质的饱和溶液降温到t2 ℃,所得溶液中的溶质质量大小关系为KNO3
_______(填“>”“<”或“=”)NH4Cl。
<
(3)已知X是KNO3或NH4Cl中的一种,小敏同学对该物质进行了如图2所示实验,
据图回答问题。
X是____________,②和③中的溶液分别达到饱和状态还需加入X的质量更大的是
________(填“②”或“③”)。
硝酸钾
③
6.溶液在生产、生活中起着十分重要的作用。请回答(1)(2)题。
(1)如图,在木块上滴几滴水,将装有某种固体的大烧杯放置于木块上,向大烧杯
中加水并搅拌,结果木块上的水结冰了,则大烧杯内的固体可能是_______。
A.氯化钠 B.硝酸铵
C.氢氧化钠 D.蔗糖
B
(2)用汽油或加了洗涤剂的水都能除去衣服上的油污,两者去油污的原理分别
是_______。
A.乳化、乳化 B.乳化、溶解
C.溶解、乳化 D.溶解、溶解
C
如图是甲、乙、丙三种固体物质的溶解度曲线。请回答(3)(4)题。
(3)现有t1 ℃时甲、乙、丙三种物质的饱和溶液,将这三种溶液分别升温到
t2 ℃,所得溶液中溶质质量分数大小关系是_______。
A.甲=乙>丙 B.乙>甲=丙
C.乙>甲>丙 D.甲>乙>丙
(4)为了将接近饱和的丙溶液变为饱和溶液,可采用的方法有________(有2~3个
选项符合题意)。
A.加固体丙 B.加水
C.降低温度 D.蒸发浓缩
C
AD
能力提升
1.(2023·广东中考)“盐穴储气”是一种地下储能技术,进气时采集盐水,采集的盐
水主要含NaCl和少量MgSO4。根据图判断,下列说法正确的是 ( )
A.溶解度:MgSO4>NaCl
B.MgSO4的溶解度随温度升高而增大
C.a ℃时,MgSO4溶液的溶质质量分数为50%
D.将盐水蒸发结晶,可得到较纯的NaCl
D
2.(2023·淄博沂源一模)向装有等量水的A、B、C烧杯中分别加入10 g、25 g、
25 g NaNO3固体,充分溶解后,现象如图一所示,甲、乙对应的溶解度曲线如图
二所示。下列说法错误的 ( )
D
A.图一烧杯中的溶液一定属于饱和溶液的是B
B.在图二中,能表示NaNO3溶解度曲线的是甲
C.欲除去混在甲中的少量乙物质可采用的方法是降温结晶
D.依据图二的分析判断,若分别将100 g甲、乙的饱和溶液从t2 ℃降温到t1 ℃,所得溶液的溶质的质量分数:甲=乙
3.(2023·淄博张店区二模)下表是两种硫酸盐在不同温度时的溶解度:
温度/℃ 0 10 20 30 40 50 60 70 80
溶解 度/g 硫酸钠 4.9 9.1 19.5 40.8 48.8 46.2 45.3 44.3 43.7
硫酸铈 24.1 20.0 17.2 14.0 10.0 8.9 8.3 7.1 6.0
下列说法正确的是 ( )
A.随温度升高,物质的溶解度只可能不断增大或不断减小
B.在0~80 ℃间的任何温度下,硫酸钠和硫酸铈的溶解度均不相等
C.某温度下,向等质量水中分别加入等质量硫酸钠和硫酸铈,充分溶解后,前者的溶质质量分数可能大于、等于或小于后者
D.将100 g 30 ℃时的饱和硫酸铈溶液加热到40 ℃(加热过程中水的蒸发忽略不计),从溶液中可析出4 g硫酸铈晶体
C
4.(2023·东营中考)有一种浸洗瓜果的“果蔬洗盐”,其主要成分是氯化钠、碳酸钠
和碳酸氢钠。
(1)从物质类别看,“果蔬洗盐”属于____________(填“纯净物”或“混合物”),“果蔬洗
盐”溶于水配成溶液后的pH_______7(填“>”“=”或“<”),溶液中最多的阳离子的符
号是_________。
(2)瓜果表面残留的农药一般呈酸性,用“果蔬洗盐”溶液浸洗瓜果有助于消除瓜
果表面的残留农药。请从化学反应的角度解释其中的原因:__________________
____________________。
混合物
>
Na+
碳酸钠、碳酸氢
钠会与酸发生反应
(3)一种固体“果蔬洗盐”的质量组成为食盐50%、碳酸钠10%、碳酸氢钠15%、
其他基料25%时,25 ℃时,取这种“果蔬洗盐”100 g加入100 g水中,判断达到饱和
状态最简单的直观现象是________________,根据三种物质的溶解度曲线(如图)判
断,达到饱和状态的物质是______________________。若将上述饱和溶液降温到
20 ℃时,无晶体析出的物质是____________。
有固体剩余
氯化钠、碳酸氢钠
碳酸钠
(4)生活中浸洗瓜果去除农药残留有多种方法:①淘米水浸泡、冲洗 ②洗洁精浸
泡、冲洗 ③开水烫、冲洗 ④“果蔬洗盐”浸泡、冲洗,既保鲜又环保的方法是
________(填数字序号)。
①
5.张老师在讲授溶液时,用固体M做了如下实验,图一中甲、乙、丙、丁是充分搅拌后静置的现象,请回答相关问题(忽略水的挥发):
(1)上述烧杯中,溶液质量最大的是________(填序号)。
(2)上述实验可以判断物质M的溶解度曲线是图二对应的_______(填序号)。
(3)甲、乙、丙烧杯中的溶液一定呈饱和状态的是________(填序号)。
(4)根据图二,若要使丁烧杯中的溶液恰好达到饱和状态,还需要加入_______g
的M固体。
丁
A
乙
8
同课章节目录
