2023-2024 人教版化学 九年级下册 第十一单元 课题1 第3课时 酸、碱、盐的化学性质及应用 课件(共33张PPT)
文档属性
| 名称 | 2023-2024 人教版化学 九年级下册 第十一单元 课题1 第3课时 酸、碱、盐的化学性质及应用 课件(共33张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 484.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-25 00:00:00 | ||
图片预览






文档简介
(共33张PPT)
第3课时
酸、碱、盐的化学性质及应用
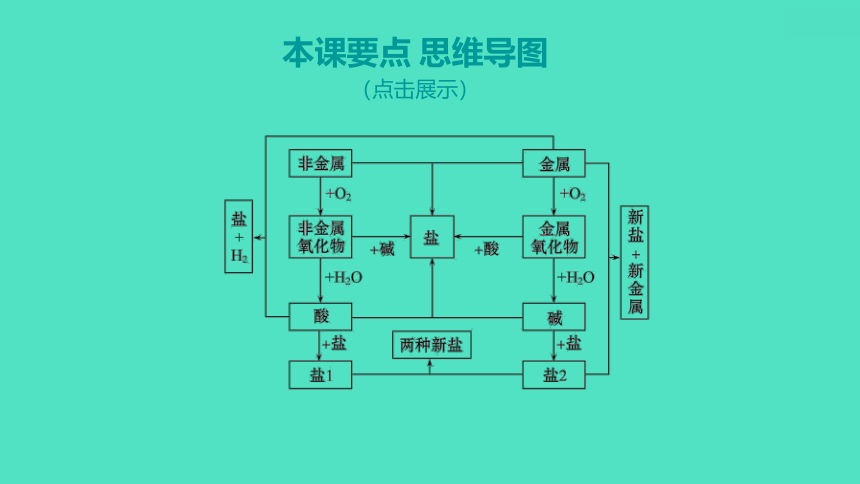
本课要点 思维导图
(点击展示)
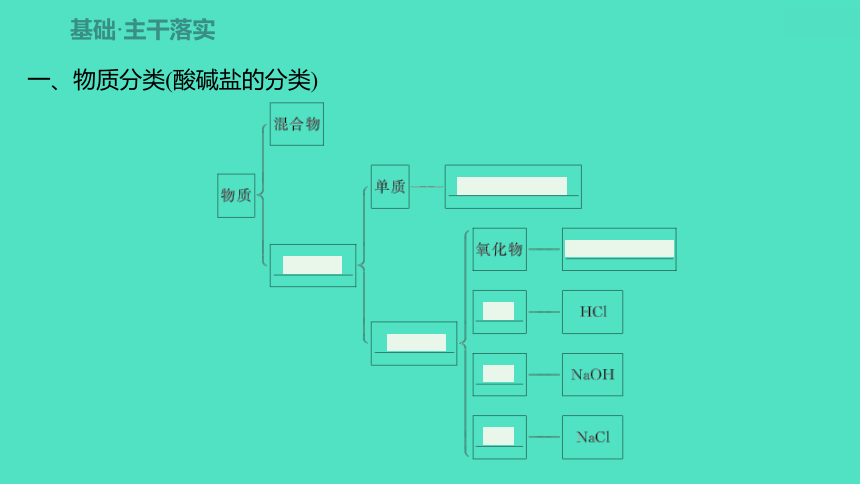
一、物质分类(酸碱盐的分类)
基础·主干落实
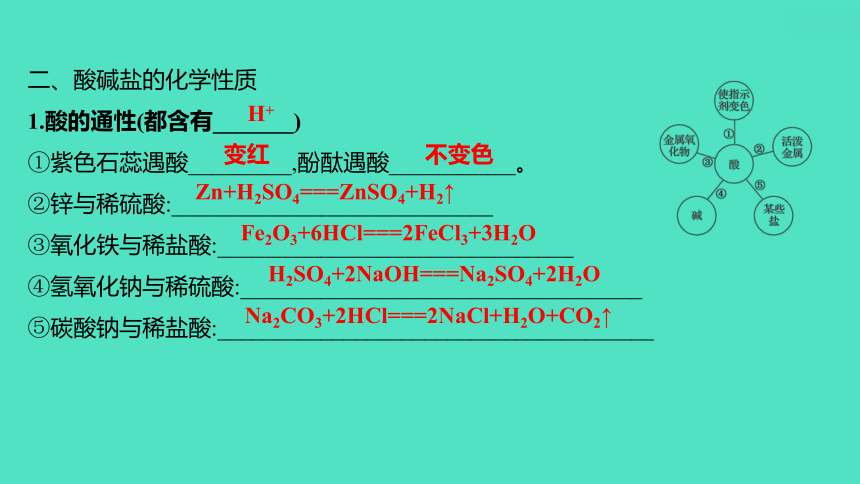
二、酸碱盐的化学性质
1.酸的通性(都含有_______)
①紫色石蕊遇酸_________,酚酞遇酸___________。
②锌与稀硫酸:____________________________
③氧化铁与稀盐酸:_______________________________
④氢氧化钠与稀硫酸:___________________________________
⑤碳酸钠与稀盐酸:______________________________________
H+
变红
不变色
Zn+H2SO4===ZnSO4+H2↑
Fe2O3+6HCl===2FeCl3+3H2O
H2SO4+2NaOH===Na2SO4+2H2O
Na2CO3+2HCl===2NaCl+H2O+CO2↑
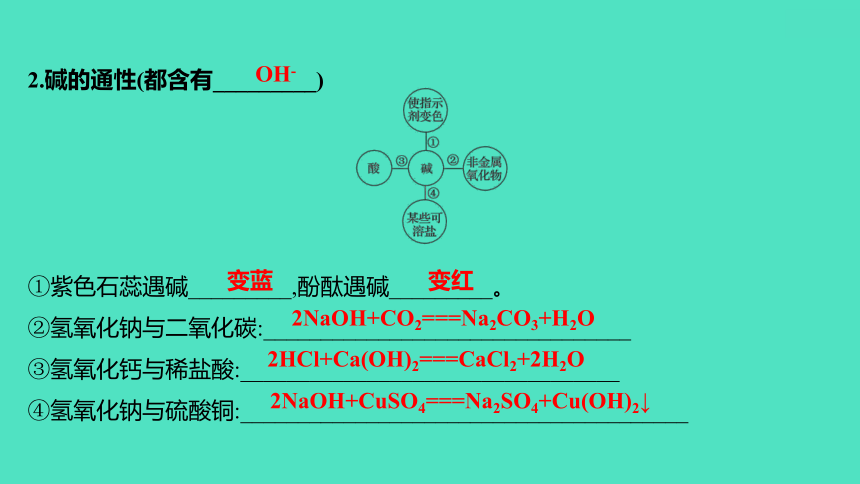
2.碱的通性(都含有_________)
①紫色石蕊遇碱_________,酚酞遇碱_________。
②氢氧化钠与二氧化碳:________________________________
③氢氧化钙与稀盐酸:_________________________________
④氢氧化钠与硫酸铜:_______________________________________
OH-
变蓝
变红
2NaOH+CO2===Na2CO3+H2O
2HCl+Ca(OH)2===CaCl2+2H2O
2NaOH+CuSO4===Na2SO4+Cu(OH)2↓
3.盐的性质
①Fe与CuSO4溶液:___________________________
②氢氧化钙与碳酸钠:_______________________________________
③CaCO3和稀盐酸:_____________________________________
④BaCl2与硫酸钠溶液:___________________________________
Fe+CuSO4===FeSO4+Cu
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
CaCO3+2HCl===CaCl2+H2O+CO2↑
Na2SO4+BaCl2===BaSO4↓+2NaCl
【漫画导学】 “过五关斩六将”,看你能冲到哪一关 (写对化学方程式即可过关)
提示:Zn+H2SO4===ZnSO4+H2↑
Na2CO3+H2SO4===Na2SO4+H2O+CO2↑
H2SO4+2NaOH===Na2SO4+2H2O
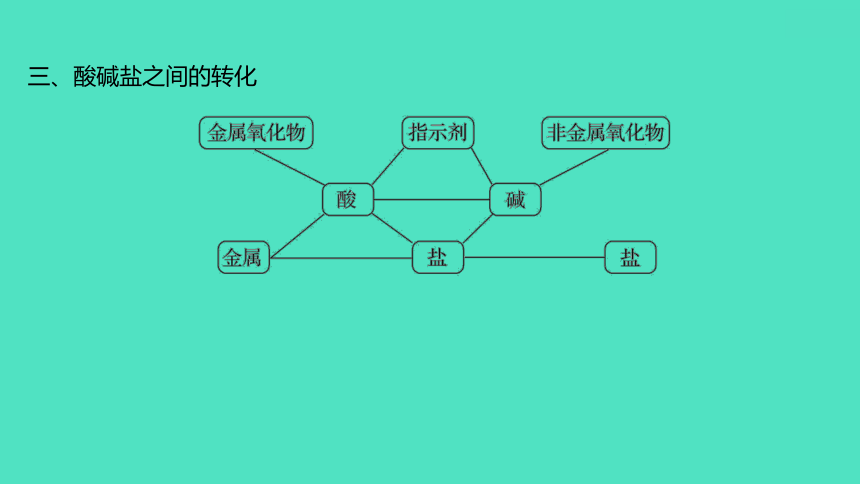
三、酸碱盐之间的转化
【探究主题】对氢氧化钠变质的探究
氢氧化钠与稀硫酸的反应本应无明显现象,小明向敞口放置的氢氧化钠溶液中滴加稀硫酸,却意外看到大量气泡产生,对此进行如下探究。
重点·探究实践
【基础探究】
任务一:检验氢氧化钠是否变质
1.由此可见敞口放置的氢氧化钠中产生了____________,原因是
________________________________,因为反应无明显现象,故不易察觉。
2.小海同学提议可以用无色酚酞溶液验证氢氧化钠是否变质,你同意他的观点吗
___________,原因是_______________________________________。
3.检验氢氧化钠是否变质实际上是检验溶液中__________(填离子符号)的存在。
实验方案:(1)加酸。加入足量的____________________,若_______________,证明氢
氧化钠已经变质。
(2)加碱或盐。加入__________________________或_______________________,若有
白色沉淀生成,证明NaOH已经变质。
Na2CO3
2NaOH+CO2===Na2CO3+H2O
不同意
碳酸钠溶液跟氢氧化钠溶液一样显碱性
稀盐酸(合理即可)
有气泡产生
Ba(OH)2溶液(合理即可)
BaCl2溶液(合理即可)
【深度探究】
任务二:探究已变质氢氧化钠的变质程度
1.变质后成分:全部变质后的成分为Na2CO3;部分变质后的成分为Na2CO3、NaOH。
2.探究的实质:检验溶液中是否存在_________。
3.实验证明变质的氢氧化钠中一定存在Na2CO3,还有可能存在 ___________ 。只有
选足量的___________________________________________________溶液_______
_______________________________________________。
4. 【素养迁移】若将变质的氢氧化钠溶液复原应选择适量的_____________
___________溶液。
OH-
NaOH
氯化钙(或者氯化钡溶液,氯化钙、氯化钡溶液显中性)
充分
反应过滤后才可以用酚酞证明原溶液是否完全变质
Ca(OH)2或
Ba(OH)2
【特别提醒】 变质的情况有三种
①没有变质(变质后的物质不存在),检验时只需证明不存在变质后的物质。
②部分变质(变质前与变质后的物质都存在),检验时需分别证明变质前和变质后的物质都存在,但一定要注意二者在检验时可能存在的相互干扰以及加入的物质对成分检验的干扰。
③全部变质(变质前的物质不存在,只存在变质后的物质),检验时只需证明不存在变质前的物质。
【A层 基础练】
【知识点1】物质分类
1.(2023·株洲中考)2023年5月30日,神舟十六号载人飞船发射取得圆满成功。在飞船太空舱里,常用铁酸镍[Ni(FeO2)2]作催化剂将航天员呼出的二氧化碳气体转化为氧气。Ni(FeO2)2属于 ( )
A.氧化物 B.酸 C.碱 D.盐
素养·分层评价
D
2.运用分类法学习和研究化学物质,能够收到事半功倍的效果,根据如图纯净物的
分类图,回答下列问题:
(1)图中的空白方框内应填___________。
(2)用氢氧化钙、金刚石、汞、三氧化硫、
小苏打的化学式填空:
①属于氧化物的是________。
②属于金属单质的是________。
③属于非金属单质的是_______。
④属于盐的是_____________。
⑤属于碱的是_____________。
化合物
SO3
Hg
C
NaHCO3
Ca(OH)2
【知识点2】酸、碱、盐的化学性质及应用
3.如图为四种物质间的反应关系,两圆相交部分(A、B、C、D)表示主要反应现象,其中描述不正确的是 ( )
A.溶液变蓝
B.溶液变红
C.产生白色沉淀
D.有气泡产生
A
4.小华在学习了酸、碱、盐之间的转化规律后,发现很多酸、碱、盐之间的反应都能生成盐,于是绘制了可以通过一步反应制取ZnSO4的思维导图,其中所选用的物质错误的是 ( )
A.①—Zn(OH)2 B.②—ZnCl2
C.③—H2SO4 D.④—Zn
B
5. 【化学与生活】(2023·唐山期末)酸、碱、盐在工农业生产和日常生活中具有广泛应用,下列说法不合理的是 ( )
A.烧碱既可以改良酸性土壤,又可以作食品干燥剂
B.小苏打既可以治疗胃酸过多,又可以作面点发酵剂
C.高温煅烧石灰石可制得生石灰
D.用石灰乳与硫酸铜溶液混合配制农药波尔多液
A
6.学习小组同学用如图装置进行实验。打开分液漏斗的活塞,将NaOH浓溶液加入
锥形瓶A中,关闭活塞,打开弹簧夹,观察到A中产生白色沉淀,烧杯B中液面降低。
(1)写出CO2与NaOH溶液发生反应的化学方程式:
______________________________。
2NaOH+CO2===Na2CO3+H2O
(2)若X是一种碱,其化学式可能是_______________________(只写一种)。
(3)学习小组同学用的X是CaCl2,实验结束后,同学们又分别做了以下三组实验:
①取少量A中溶液测其pH,pH>7
②取少量A中溶液,向其中加入CaCl2溶液,无明显现象,再测其pH,pH>7
③取少量A中溶液,测其pH,pH>7,再向其中加入K2CO3溶液,产生白色沉淀
查阅资料可知CaCl2溶液呈中性。
以上三组实验事实中,能说明A中溶液一定含有NaOH的是_________(填序号)。
Ca(OH)2[或Ba(OH)2]
②③
【易错点】对酸、碱、盐的性质及其互相反应的认知不清
7.(多选)下列有关酸、碱、盐的说法错误的是_____________。
A.酸、碱、盐之间都能发生复分解反应
B.中和反应一定是复分解反应,但复分解反应不一定是中和反应
C.能使无色酚酞变红的一定是碱溶液
D.盐溶液呈中性pH=7
E.酸中一定含有氢元素,不一定含有氧元素
【易错点拨】 发生复分解反应时,生成物中必须有水或气体或沉淀生成,并且盐
与盐、盐与碱发生复分解反应时,要求反应物都溶于水;碳酸钠属于盐,其水溶液
呈碱性。
A、C、D
【B层 能力练】
8. 【化学与生活】某公司生产的融雪剂由NaCl、CaCl2、Na2CO3和CuSO4中的一种或两种物质组成。小洁同学将该融雪剂加水溶解,得到无色溶液,向该溶液中加入K2CO3溶液,有白色沉淀生成。由此可知,该融雪剂的组成可能是 ( )
A.CuSO4 NaCl B.Na2CO3 NaCl
C.CaCl2 NaCl D.CuSO4 CaCl2
C
9.(2022·毕节中考)已知CaCl2溶液显中性。向CaCl2与盐酸混合溶液中逐滴滴加Na2CO3溶液,边加边搅拌,用pH计测得混合溶液pH的变化如图。下列相关叙述正确的是 ( )
A.实验中Cl-个数保持不变
B.A→B对应反应为中和反应
C.B→C对应反应无明显现象
D.C→D表明Na2CO3属于碱
A
10.下列物质间的转化关系,不能实现的是( )
A.C→CO2→CO
B.Mg→MgO→MgSO4
C.KCl→KNO3→K2SO4
D.NaOH→Na2CO3→NaCl
C
11.(2023·新疆中考改编)盐酸和碳酸钠是重要的化工产品,也是实验室中重要的化
学试剂。
(1)碳酸钠俗称纯碱或_________,属于________(填“酸”“碱”或“盐”),广泛用于玻璃、
造纸、纺织和洗涤剂的生产等。
(2)在盐酸中加入一定量碳酸钠固体充分反应。
①此反应的现象是______________________________________。
②如图表示该反应前后溶液中存在的主要离子,用pH试纸测定反应后溶液的酸
碱度,pH______7(填“>”“=”或“<”)。反应
后的图中R代表的离子是________。
苏打
盐
固体粉末逐渐溶解,溶液中有气泡产生
<
Na+
(3)下列物质中能与盐酸发生反应的是___________(填字母)。
A.Pb B.NaHCO3
C.KOH D.NaNO3
E.Al2O3
ABCE
12.构建知识网络,可以帮助我们理解知识间的内在联系。如图是盐酸与不同类别
物质之间反应的知识网络。
(1)写出金属锌与盐酸反应的化学方程式:__________________________。
(2)用盐酸除铁锈(主要成分为Fe2O3)的化学方程式是
_____________________________。
Zn+2HCl===ZnCl2+H2↑
Fe2O3+6HCl===2FeCl3+3H2O
(3)小林觉得你很聪明,是他的良师益友,学完“酸的化学性质”后,他邀请你与他一
起讨论:食醋也是一种酸,和盐酸具有相似的化学性质,请列举两点食醋的化学性
质:_________________________________;______________________________
______。
(4)反思:盐酸、硫酸、食醋具有相似化学性质的原因是它们的水溶液中都含有
_______(填离子符号)。
(5)写出氧化铜与稀硫酸反应的化学方程式:______________________________。
(6)氢氧化铝可用于医疗上,服用它可以治疗胃酸过多,请写出此反应的化学方程
式:________________________________。
能与活泼金属反应生成盐和氢气
能与碱反应生成盐和水(合理即
可)
H+
CuO+H2SO4===CuSO4+H2O
Al(OH)3+3HCl===AlCl3+3H2O
13.(2023·陕西中考)学习小组的同学进行了如图所示的实验,并展开了拓展学习与
探究。
【学习交流】
(1)上述实验A中无明显现象,B中溶液颜色呈_______色。
(2)写出A中发生反应的化学方程式:_________________________________。
红
Ca(OH)2+2HCl===CaCl2+2H2O
【提出问题】
反应后A中溶液的溶质成分是什么
【作出猜想】
猜想一:CaCl2
猜想二:CaCl2、HCl
猜想三:CaCl2、Ca(OH)2
【查阅资料】
CaCl2溶液呈中性。
【讨论交流】在讨论方案时,某些同学认为可以直接将B中滴了无色酚酞的碳酸
钠溶液倒入A中,根据实验现象来验证猜想,其中甲、乙、丙三位同学的观点如表。
你认为上述_______同学依据预测实验现象得出的结论是不合理的。
同学 预测实验现象 结论
甲 产生白色沉淀,溶液为无色 猜想一成立
乙 产生无色气泡,溶液为无色 猜想二成立
丙 产生白色沉淀,溶液为红色 猜想三成立
丙
【实验验证】丁同学将B中溶液倒入A中进行实验,观察到有无色气泡和白色沉
淀生成,溶液为红色,与甲、乙、丙三位同学预测的实验现象有所不同。实验中产
生的白色沉淀是___________(填化学式),丁同学的实验现象能证明猜想_______成
立。
【反思拓展】大家认为还可以选择其他方案来验证猜想。你认为下列方案可行
的是________(填序号)。
①测A中溶液的pH
②向A中溶液中通入CO2气体
③向A中溶液中滴加AgNO3溶液
CaCO3
二
①
【C层 拓展练】
14.(2022·岳阳中考)小明在做课后习题时,看到了化学方程式:BaCl2+H2SO4===BaSO4↓+2HCl,联想到医院在用X射线检查肠胃病时让患者服用的“钡餐”,其主要成分是BaSO4。
【查阅资料】BaSO4不会被人体吸收,对身体无害,但Ba2+是重金属离子,对身体危害较大。
【提出问题】与BaSO4一样,BaCO3也不溶于水,有同学提出BaCO3是否也可用作“钡餐”
【实验探究】模拟胃液环境设计以下方案:
【反思交流】从BaSO4性质角度分析,BaSO4不被人体吸收可作“钡餐”的原因是
_____________________________________。
实验操作 实验现象 实验分析 实验结论
取少量BaCO3粉末 于试管中,向其中 滴加适量 (1)___________ (2)____________ 产生该现象的化学方程 式为(3)_____________ ____________________ BaCO3不可用作
“钡餐”
稀盐酸
有气泡产生
BaCO3+2HCl
===BaCl2+H2O+CO2↑
BaSO4不溶于水,不与胃液中的盐酸反应
第3课时
酸、碱、盐的化学性质及应用
本课要点 思维导图
(点击展示)
一、物质分类(酸碱盐的分类)
基础·主干落实
二、酸碱盐的化学性质
1.酸的通性(都含有_______)
①紫色石蕊遇酸_________,酚酞遇酸___________。
②锌与稀硫酸:____________________________
③氧化铁与稀盐酸:_______________________________
④氢氧化钠与稀硫酸:___________________________________
⑤碳酸钠与稀盐酸:______________________________________
H+
变红
不变色
Zn+H2SO4===ZnSO4+H2↑
Fe2O3+6HCl===2FeCl3+3H2O
H2SO4+2NaOH===Na2SO4+2H2O
Na2CO3+2HCl===2NaCl+H2O+CO2↑
2.碱的通性(都含有_________)
①紫色石蕊遇碱_________,酚酞遇碱_________。
②氢氧化钠与二氧化碳:________________________________
③氢氧化钙与稀盐酸:_________________________________
④氢氧化钠与硫酸铜:_______________________________________
OH-
变蓝
变红
2NaOH+CO2===Na2CO3+H2O
2HCl+Ca(OH)2===CaCl2+2H2O
2NaOH+CuSO4===Na2SO4+Cu(OH)2↓
3.盐的性质
①Fe与CuSO4溶液:___________________________
②氢氧化钙与碳酸钠:_______________________________________
③CaCO3和稀盐酸:_____________________________________
④BaCl2与硫酸钠溶液:___________________________________
Fe+CuSO4===FeSO4+Cu
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
CaCO3+2HCl===CaCl2+H2O+CO2↑
Na2SO4+BaCl2===BaSO4↓+2NaCl
【漫画导学】 “过五关斩六将”,看你能冲到哪一关 (写对化学方程式即可过关)
提示:Zn+H2SO4===ZnSO4+H2↑
Na2CO3+H2SO4===Na2SO4+H2O+CO2↑
H2SO4+2NaOH===Na2SO4+2H2O
三、酸碱盐之间的转化
【探究主题】对氢氧化钠变质的探究
氢氧化钠与稀硫酸的反应本应无明显现象,小明向敞口放置的氢氧化钠溶液中滴加稀硫酸,却意外看到大量气泡产生,对此进行如下探究。
重点·探究实践
【基础探究】
任务一:检验氢氧化钠是否变质
1.由此可见敞口放置的氢氧化钠中产生了____________,原因是
________________________________,因为反应无明显现象,故不易察觉。
2.小海同学提议可以用无色酚酞溶液验证氢氧化钠是否变质,你同意他的观点吗
___________,原因是_______________________________________。
3.检验氢氧化钠是否变质实际上是检验溶液中__________(填离子符号)的存在。
实验方案:(1)加酸。加入足量的____________________,若_______________,证明氢
氧化钠已经变质。
(2)加碱或盐。加入__________________________或_______________________,若有
白色沉淀生成,证明NaOH已经变质。
Na2CO3
2NaOH+CO2===Na2CO3+H2O
不同意
碳酸钠溶液跟氢氧化钠溶液一样显碱性
稀盐酸(合理即可)
有气泡产生
Ba(OH)2溶液(合理即可)
BaCl2溶液(合理即可)
【深度探究】
任务二:探究已变质氢氧化钠的变质程度
1.变质后成分:全部变质后的成分为Na2CO3;部分变质后的成分为Na2CO3、NaOH。
2.探究的实质:检验溶液中是否存在_________。
3.实验证明变质的氢氧化钠中一定存在Na2CO3,还有可能存在 ___________ 。只有
选足量的___________________________________________________溶液_______
_______________________________________________。
4. 【素养迁移】若将变质的氢氧化钠溶液复原应选择适量的_____________
___________溶液。
OH-
NaOH
氯化钙(或者氯化钡溶液,氯化钙、氯化钡溶液显中性)
充分
反应过滤后才可以用酚酞证明原溶液是否完全变质
Ca(OH)2或
Ba(OH)2
【特别提醒】 变质的情况有三种
①没有变质(变质后的物质不存在),检验时只需证明不存在变质后的物质。
②部分变质(变质前与变质后的物质都存在),检验时需分别证明变质前和变质后的物质都存在,但一定要注意二者在检验时可能存在的相互干扰以及加入的物质对成分检验的干扰。
③全部变质(变质前的物质不存在,只存在变质后的物质),检验时只需证明不存在变质前的物质。
【A层 基础练】
【知识点1】物质分类
1.(2023·株洲中考)2023年5月30日,神舟十六号载人飞船发射取得圆满成功。在飞船太空舱里,常用铁酸镍[Ni(FeO2)2]作催化剂将航天员呼出的二氧化碳气体转化为氧气。Ni(FeO2)2属于 ( )
A.氧化物 B.酸 C.碱 D.盐
素养·分层评价
D
2.运用分类法学习和研究化学物质,能够收到事半功倍的效果,根据如图纯净物的
分类图,回答下列问题:
(1)图中的空白方框内应填___________。
(2)用氢氧化钙、金刚石、汞、三氧化硫、
小苏打的化学式填空:
①属于氧化物的是________。
②属于金属单质的是________。
③属于非金属单质的是_______。
④属于盐的是_____________。
⑤属于碱的是_____________。
化合物
SO3
Hg
C
NaHCO3
Ca(OH)2
【知识点2】酸、碱、盐的化学性质及应用
3.如图为四种物质间的反应关系,两圆相交部分(A、B、C、D)表示主要反应现象,其中描述不正确的是 ( )
A.溶液变蓝
B.溶液变红
C.产生白色沉淀
D.有气泡产生
A
4.小华在学习了酸、碱、盐之间的转化规律后,发现很多酸、碱、盐之间的反应都能生成盐,于是绘制了可以通过一步反应制取ZnSO4的思维导图,其中所选用的物质错误的是 ( )
A.①—Zn(OH)2 B.②—ZnCl2
C.③—H2SO4 D.④—Zn
B
5. 【化学与生活】(2023·唐山期末)酸、碱、盐在工农业生产和日常生活中具有广泛应用,下列说法不合理的是 ( )
A.烧碱既可以改良酸性土壤,又可以作食品干燥剂
B.小苏打既可以治疗胃酸过多,又可以作面点发酵剂
C.高温煅烧石灰石可制得生石灰
D.用石灰乳与硫酸铜溶液混合配制农药波尔多液
A
6.学习小组同学用如图装置进行实验。打开分液漏斗的活塞,将NaOH浓溶液加入
锥形瓶A中,关闭活塞,打开弹簧夹,观察到A中产生白色沉淀,烧杯B中液面降低。
(1)写出CO2与NaOH溶液发生反应的化学方程式:
______________________________。
2NaOH+CO2===Na2CO3+H2O
(2)若X是一种碱,其化学式可能是_______________________(只写一种)。
(3)学习小组同学用的X是CaCl2,实验结束后,同学们又分别做了以下三组实验:
①取少量A中溶液测其pH,pH>7
②取少量A中溶液,向其中加入CaCl2溶液,无明显现象,再测其pH,pH>7
③取少量A中溶液,测其pH,pH>7,再向其中加入K2CO3溶液,产生白色沉淀
查阅资料可知CaCl2溶液呈中性。
以上三组实验事实中,能说明A中溶液一定含有NaOH的是_________(填序号)。
Ca(OH)2[或Ba(OH)2]
②③
【易错点】对酸、碱、盐的性质及其互相反应的认知不清
7.(多选)下列有关酸、碱、盐的说法错误的是_____________。
A.酸、碱、盐之间都能发生复分解反应
B.中和反应一定是复分解反应,但复分解反应不一定是中和反应
C.能使无色酚酞变红的一定是碱溶液
D.盐溶液呈中性pH=7
E.酸中一定含有氢元素,不一定含有氧元素
【易错点拨】 发生复分解反应时,生成物中必须有水或气体或沉淀生成,并且盐
与盐、盐与碱发生复分解反应时,要求反应物都溶于水;碳酸钠属于盐,其水溶液
呈碱性。
A、C、D
【B层 能力练】
8. 【化学与生活】某公司生产的融雪剂由NaCl、CaCl2、Na2CO3和CuSO4中的一种或两种物质组成。小洁同学将该融雪剂加水溶解,得到无色溶液,向该溶液中加入K2CO3溶液,有白色沉淀生成。由此可知,该融雪剂的组成可能是 ( )
A.CuSO4 NaCl B.Na2CO3 NaCl
C.CaCl2 NaCl D.CuSO4 CaCl2
C
9.(2022·毕节中考)已知CaCl2溶液显中性。向CaCl2与盐酸混合溶液中逐滴滴加Na2CO3溶液,边加边搅拌,用pH计测得混合溶液pH的变化如图。下列相关叙述正确的是 ( )
A.实验中Cl-个数保持不变
B.A→B对应反应为中和反应
C.B→C对应反应无明显现象
D.C→D表明Na2CO3属于碱
A
10.下列物质间的转化关系,不能实现的是( )
A.C→CO2→CO
B.Mg→MgO→MgSO4
C.KCl→KNO3→K2SO4
D.NaOH→Na2CO3→NaCl
C
11.(2023·新疆中考改编)盐酸和碳酸钠是重要的化工产品,也是实验室中重要的化
学试剂。
(1)碳酸钠俗称纯碱或_________,属于________(填“酸”“碱”或“盐”),广泛用于玻璃、
造纸、纺织和洗涤剂的生产等。
(2)在盐酸中加入一定量碳酸钠固体充分反应。
①此反应的现象是______________________________________。
②如图表示该反应前后溶液中存在的主要离子,用pH试纸测定反应后溶液的酸
碱度,pH______7(填“>”“=”或“<”)。反应
后的图中R代表的离子是________。
苏打
盐
固体粉末逐渐溶解,溶液中有气泡产生
<
Na+
(3)下列物质中能与盐酸发生反应的是___________(填字母)。
A.Pb B.NaHCO3
C.KOH D.NaNO3
E.Al2O3
ABCE
12.构建知识网络,可以帮助我们理解知识间的内在联系。如图是盐酸与不同类别
物质之间反应的知识网络。
(1)写出金属锌与盐酸反应的化学方程式:__________________________。
(2)用盐酸除铁锈(主要成分为Fe2O3)的化学方程式是
_____________________________。
Zn+2HCl===ZnCl2+H2↑
Fe2O3+6HCl===2FeCl3+3H2O
(3)小林觉得你很聪明,是他的良师益友,学完“酸的化学性质”后,他邀请你与他一
起讨论:食醋也是一种酸,和盐酸具有相似的化学性质,请列举两点食醋的化学性
质:_________________________________;______________________________
______。
(4)反思:盐酸、硫酸、食醋具有相似化学性质的原因是它们的水溶液中都含有
_______(填离子符号)。
(5)写出氧化铜与稀硫酸反应的化学方程式:______________________________。
(6)氢氧化铝可用于医疗上,服用它可以治疗胃酸过多,请写出此反应的化学方程
式:________________________________。
能与活泼金属反应生成盐和氢气
能与碱反应生成盐和水(合理即
可)
H+
CuO+H2SO4===CuSO4+H2O
Al(OH)3+3HCl===AlCl3+3H2O
13.(2023·陕西中考)学习小组的同学进行了如图所示的实验,并展开了拓展学习与
探究。
【学习交流】
(1)上述实验A中无明显现象,B中溶液颜色呈_______色。
(2)写出A中发生反应的化学方程式:_________________________________。
红
Ca(OH)2+2HCl===CaCl2+2H2O
【提出问题】
反应后A中溶液的溶质成分是什么
【作出猜想】
猜想一:CaCl2
猜想二:CaCl2、HCl
猜想三:CaCl2、Ca(OH)2
【查阅资料】
CaCl2溶液呈中性。
【讨论交流】在讨论方案时,某些同学认为可以直接将B中滴了无色酚酞的碳酸
钠溶液倒入A中,根据实验现象来验证猜想,其中甲、乙、丙三位同学的观点如表。
你认为上述_______同学依据预测实验现象得出的结论是不合理的。
同学 预测实验现象 结论
甲 产生白色沉淀,溶液为无色 猜想一成立
乙 产生无色气泡,溶液为无色 猜想二成立
丙 产生白色沉淀,溶液为红色 猜想三成立
丙
【实验验证】丁同学将B中溶液倒入A中进行实验,观察到有无色气泡和白色沉
淀生成,溶液为红色,与甲、乙、丙三位同学预测的实验现象有所不同。实验中产
生的白色沉淀是___________(填化学式),丁同学的实验现象能证明猜想_______成
立。
【反思拓展】大家认为还可以选择其他方案来验证猜想。你认为下列方案可行
的是________(填序号)。
①测A中溶液的pH
②向A中溶液中通入CO2气体
③向A中溶液中滴加AgNO3溶液
CaCO3
二
①
【C层 拓展练】
14.(2022·岳阳中考)小明在做课后习题时,看到了化学方程式:BaCl2+H2SO4===BaSO4↓+2HCl,联想到医院在用X射线检查肠胃病时让患者服用的“钡餐”,其主要成分是BaSO4。
【查阅资料】BaSO4不会被人体吸收,对身体无害,但Ba2+是重金属离子,对身体危害较大。
【提出问题】与BaSO4一样,BaCO3也不溶于水,有同学提出BaCO3是否也可用作“钡餐”
【实验探究】模拟胃液环境设计以下方案:
【反思交流】从BaSO4性质角度分析,BaSO4不被人体吸收可作“钡餐”的原因是
_____________________________________。
实验操作 实验现象 实验分析 实验结论
取少量BaCO3粉末 于试管中,向其中 滴加适量 (1)___________ (2)____________ 产生该现象的化学方程 式为(3)_____________ ____________________ BaCO3不可用作
“钡餐”
稀盐酸
有气泡产生
BaCO3+2HCl
===BaCl2+H2O+CO2↑
BaSO4不溶于水,不与胃液中的盐酸反应
同课章节目录
