2024届高三化学二轮复习化学工艺流程题解题模型建立课件(共18张PPT)
文档属性
| 名称 | 2024届高三化学二轮复习化学工艺流程题解题模型建立课件(共18张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 5.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-25 14:00:28 | ||
图片预览






文档简介
(共18张PPT)
黄铁矿FeS2
菱铁矿 FeCO3
铝士矿
赤铁矿
Fe2O3
赤铜矿 Cu2O
孔雀石 Cu2(OH)2CO3
化学工艺流程题
解题模型建立
化学工艺流程题的结构
题干:一般是简单介绍工艺生产的原材料和工艺生产的目的(包括副产品);
流程图:主要用框图形式将操作或物质转换之间的关系或原料到产品的主要生产工艺流程表示出来;
问题:主要是根据流程中涉及到的化学知识设置成系列问题,构成一道完整的化学试题。
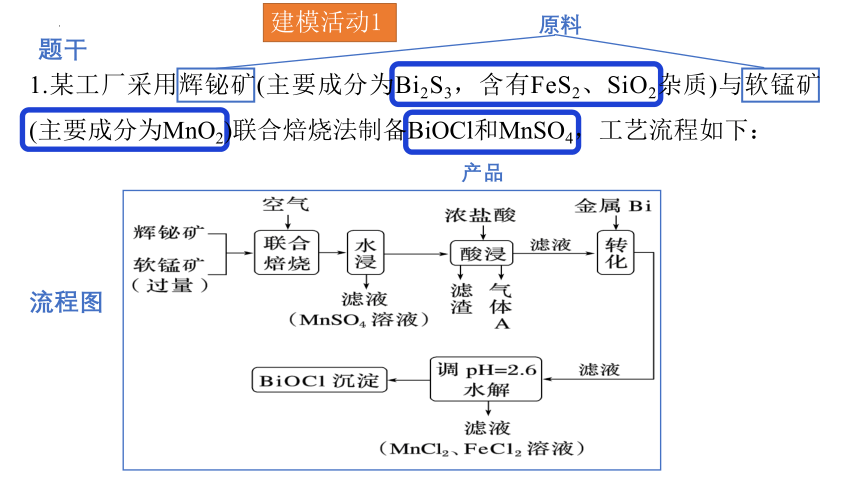
建模活动1
原料
产品
题干
流程图
1.某工厂采用辉铋矿(主要成分为Bi2S3,含有FeS2、SiO2杂质)与软锰矿(主要成分为MnO2)联合焙烧法制备BiOCl和MnSO4,工艺流程如下:
思考:下列问题主要考查了工业流程中哪些方面的内容?
(1)为了提高焙烧效率,可采取的措施为_____。
a.进一步粉碎矿石 b.鼓入适当过量的空气 c.降低焙烧温度
(2)Bi2S3在空气中单独焙烧生成Bi2O3,反应的化学方程式为
__________________________________。
(3)“酸浸”中过量浓盐酸的作用为:①充分浸出Bi3+和Mn2+; ②__________________。
(4)滤渣的主要成分为______(填化式)。
(5)生成气体A的离子方程式为___________________________。
(6)加入金属Bi的目的是__________________。
建模活动2
yaunlia原原料料o
原料
核心过程
产品
思考:原料的预处理有哪些方法
①烧灼(煅烧、焙烧):
改变结构,是一些物质能溶解。并使一些杂质高温下氧化分解;
②溶解:包括水浸取、酸溶、碱溶、醇溶等;
③粉碎、研磨:
增大表面积,加快后续过程溶解或反应速率。
MnO2 Mn2O3 Mn2+
MnSO4
FeS2 Fe2O3 Fe3+ Fe2+
Bi2S3 Bi2O3 Bi3+ BiOCl
在此流程中锰、铁、铋元素的转化过程有哪些?
将各
元素
转化
成氧
化物
Bi2S3
Bi2S3、FeS2、
SiO2、MnO2
Bi2O3、SO2
Fe2O3、SiO2
Mn2O3、MnSO4
已知:①焙烧时过量的MnO2
分解为Mn2O3,FeS2转变为Fe2O3;
②金属活动性:Fe>(H)>Bi>Cu;
核心过程
O2
O2
O2
HCl
SO2
HCl
Bi
HCl
H2O
开始沉淀pH 完全沉淀pH
Fe2+ 6.5 8.3
Fe3+ 1.6 2.8
Mn2+ 8.1 10.1
yaunlia原原料料o
工业流程题的解题模型
原料
核心过程
产品
预处理
分离分元素
转化分离提纯
分离分分离
提纯分离提纯
分离分条件
控制分离提纯
核心过程的建模建构
核心过程
陌生问题
元素转换
条件控制
试剂的选择
溶液PH
深挖题干信息
物质本身性质
非氧化还原反应
氧化还原反应
温度
洗涤剂的选择
沉淀剂的选择
分离提纯
蒸发结晶趁热过滤
过滤
重结晶
蒸发浓缩冷却结晶
分液
[2021·全国乙卷,26]磁选后的炼铁高钛炉渣,主要成分有TiO2、SiO2、Al2O3、MgO、CaO以及少量的Fe2O3。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表
金属离子 Fe3+ Al3+ Mg2+ Ca2+
开始沉淀的pH 2.2 3.5 9.5 12.4
沉淀完全(c=1.0×10-5 mol·L-1)的pH 3.2 4.7 11.1 13.8
“焙烧”中,TiO2、SiO2几乎不发生反应,MgO、CaO、Fe2O3转化为相应的硫酸盐,Al2O3转化为硫酸铝铵。
变式训练----练一练
(1)“焙烧”中,TiO2、SiO2几乎不发生反应,Al2O3、MgO、CaO、Fe2O3转化为相应的硫酸盐,写出Al2O3转化为NH4Al(SO4)2的化学方程式____。
(2)“水浸”后“滤液”的pH约为2.0,在“分步沉淀”时用氨水逐步调节pH至11.6,依次析出的金属离子是___________________。
(3)“母液①”中Mg2+浓度为__________ mol·L-1。
(4)“水浸渣”在160 ℃“酸溶”,最适合的酸是_________,“酸溶渣”的成分是______________。
(5)“酸溶”后,将溶液适当稀释并加热,TiO2+水解析出TiO2·xH2O沉淀,
该反应的离子方程式是________________________________________。(6)将“母液①”和“母液②”混合,吸收尾气,经处理得__,循环利用。
金属离子 Fe3+ Al3+ Mg2+ Ca2+
开始沉淀的pH 2.2 3.5 9.5 12.4
沉淀完全(c=1.0×10-5 mol·L-1)的pH 3.2 4.7 11.1 13.8
“焙烧”中,TiO2、SiO2几乎不发生反应,MgO、CaO、Fe2O3转化为相应的硫酸盐,Al2O3转化为硫酸铝铵。
讨论:在此流程中铝、镁、铁、钙、钛元素的转化过程有哪些?
yaunlia原原料料o
原料
核心过程
产品
(1)“焙烧”中,TiO2、SiO2几乎不发生反应,Al2O3、MgO、CaO、Fe2O3转化为相应的硫酸盐,写出Al2O3转化为NH4Al(SO4)2的化学方程式__________________________。
(2)“水浸”后“滤液”的pH约为2.0,在“分步沉淀”时用氨水逐步调节pH至11.6,依次析出的金属离子是___________________。
(3)“母液①”中Mg2+浓度为__________ mol·L-1。
(4)“水浸渣”在160 ℃“酸溶”,最适合的酸是_________,“酸溶渣”的成分是______________。
(5)“酸溶”后,将溶液适当稀释并加热,TiO2+水解析出TiO2·xH2O沉淀,
该反应的离子方程式是________________________________________。
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得________, 循环利用。
(NH4)2SO4
硫酸
SiO2、CaSO4
Fe3+、Al3+、Mg2+
1.0×10-6
高温
Al2O3+4(NH4)2SO4====2NH4Al(SO4)2+6NH3↑+3H2O
我国是世界上最早制得和使用金属锌的国家,一种以闪锌矿(ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:
金属离子 Fe3+ Fe2+ Zn2+ Cd2+
开始沉淀的pH 1.5 6.3 6.2 7.4
沉淀完全的pH 2.8 8.3 8.2 9.4
环节一:请同学们以小组为单位,根据流程图设计问题。
环节二:我是小小审题专家,对小组展示的问题进行审核评价。
环节三:我是答卷人,对审核后的问题进行解答!
变式拓展----我能行
黄铁矿FeS2
菱铁矿 FeCO3
铝士矿
赤铁矿
Fe2O3
赤铜矿 Cu2O
孔雀石 Cu2(OH)2CO3
化学工艺流程题
解题模型建立
化学工艺流程题的结构
题干:一般是简单介绍工艺生产的原材料和工艺生产的目的(包括副产品);
流程图:主要用框图形式将操作或物质转换之间的关系或原料到产品的主要生产工艺流程表示出来;
问题:主要是根据流程中涉及到的化学知识设置成系列问题,构成一道完整的化学试题。
建模活动1
原料
产品
题干
流程图
1.某工厂采用辉铋矿(主要成分为Bi2S3,含有FeS2、SiO2杂质)与软锰矿(主要成分为MnO2)联合焙烧法制备BiOCl和MnSO4,工艺流程如下:
思考:下列问题主要考查了工业流程中哪些方面的内容?
(1)为了提高焙烧效率,可采取的措施为_____。
a.进一步粉碎矿石 b.鼓入适当过量的空气 c.降低焙烧温度
(2)Bi2S3在空气中单独焙烧生成Bi2O3,反应的化学方程式为
__________________________________。
(3)“酸浸”中过量浓盐酸的作用为:①充分浸出Bi3+和Mn2+; ②__________________。
(4)滤渣的主要成分为______(填化式)。
(5)生成气体A的离子方程式为___________________________。
(6)加入金属Bi的目的是__________________。
建模活动2
yaunlia原原料料o
原料
核心过程
产品
思考:原料的预处理有哪些方法
①烧灼(煅烧、焙烧):
改变结构,是一些物质能溶解。并使一些杂质高温下氧化分解;
②溶解:包括水浸取、酸溶、碱溶、醇溶等;
③粉碎、研磨:
增大表面积,加快后续过程溶解或反应速率。
MnO2 Mn2O3 Mn2+
MnSO4
FeS2 Fe2O3 Fe3+ Fe2+
Bi2S3 Bi2O3 Bi3+ BiOCl
在此流程中锰、铁、铋元素的转化过程有哪些?
将各
元素
转化
成氧
化物
Bi2S3
Bi2S3、FeS2、
SiO2、MnO2
Bi2O3、SO2
Fe2O3、SiO2
Mn2O3、MnSO4
已知:①焙烧时过量的MnO2
分解为Mn2O3,FeS2转变为Fe2O3;
②金属活动性:Fe>(H)>Bi>Cu;
核心过程
O2
O2
O2
HCl
SO2
HCl
Bi
HCl
H2O
开始沉淀pH 完全沉淀pH
Fe2+ 6.5 8.3
Fe3+ 1.6 2.8
Mn2+ 8.1 10.1
yaunlia原原料料o
工业流程题的解题模型
原料
核心过程
产品
预处理
分离分元素
转化分离提纯
分离分分离
提纯分离提纯
分离分条件
控制分离提纯
核心过程的建模建构
核心过程
陌生问题
元素转换
条件控制
试剂的选择
溶液PH
深挖题干信息
物质本身性质
非氧化还原反应
氧化还原反应
温度
洗涤剂的选择
沉淀剂的选择
分离提纯
蒸发结晶趁热过滤
过滤
重结晶
蒸发浓缩冷却结晶
分液
[2021·全国乙卷,26]磁选后的炼铁高钛炉渣,主要成分有TiO2、SiO2、Al2O3、MgO、CaO以及少量的Fe2O3。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表
金属离子 Fe3+ Al3+ Mg2+ Ca2+
开始沉淀的pH 2.2 3.5 9.5 12.4
沉淀完全(c=1.0×10-5 mol·L-1)的pH 3.2 4.7 11.1 13.8
“焙烧”中,TiO2、SiO2几乎不发生反应,MgO、CaO、Fe2O3转化为相应的硫酸盐,Al2O3转化为硫酸铝铵。
变式训练----练一练
(1)“焙烧”中,TiO2、SiO2几乎不发生反应,Al2O3、MgO、CaO、Fe2O3转化为相应的硫酸盐,写出Al2O3转化为NH4Al(SO4)2的化学方程式____。
(2)“水浸”后“滤液”的pH约为2.0,在“分步沉淀”时用氨水逐步调节pH至11.6,依次析出的金属离子是___________________。
(3)“母液①”中Mg2+浓度为__________ mol·L-1。
(4)“水浸渣”在160 ℃“酸溶”,最适合的酸是_________,“酸溶渣”的成分是______________。
(5)“酸溶”后,将溶液适当稀释并加热,TiO2+水解析出TiO2·xH2O沉淀,
该反应的离子方程式是________________________________________。(6)将“母液①”和“母液②”混合,吸收尾气,经处理得__,循环利用。
金属离子 Fe3+ Al3+ Mg2+ Ca2+
开始沉淀的pH 2.2 3.5 9.5 12.4
沉淀完全(c=1.0×10-5 mol·L-1)的pH 3.2 4.7 11.1 13.8
“焙烧”中,TiO2、SiO2几乎不发生反应,MgO、CaO、Fe2O3转化为相应的硫酸盐,Al2O3转化为硫酸铝铵。
讨论:在此流程中铝、镁、铁、钙、钛元素的转化过程有哪些?
yaunlia原原料料o
原料
核心过程
产品
(1)“焙烧”中,TiO2、SiO2几乎不发生反应,Al2O3、MgO、CaO、Fe2O3转化为相应的硫酸盐,写出Al2O3转化为NH4Al(SO4)2的化学方程式__________________________。
(2)“水浸”后“滤液”的pH约为2.0,在“分步沉淀”时用氨水逐步调节pH至11.6,依次析出的金属离子是___________________。
(3)“母液①”中Mg2+浓度为__________ mol·L-1。
(4)“水浸渣”在160 ℃“酸溶”,最适合的酸是_________,“酸溶渣”的成分是______________。
(5)“酸溶”后,将溶液适当稀释并加热,TiO2+水解析出TiO2·xH2O沉淀,
该反应的离子方程式是________________________________________。
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得________, 循环利用。
(NH4)2SO4
硫酸
SiO2、CaSO4
Fe3+、Al3+、Mg2+
1.0×10-6
高温
Al2O3+4(NH4)2SO4====2NH4Al(SO4)2+6NH3↑+3H2O
我国是世界上最早制得和使用金属锌的国家,一种以闪锌矿(ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:
金属离子 Fe3+ Fe2+ Zn2+ Cd2+
开始沉淀的pH 1.5 6.3 6.2 7.4
沉淀完全的pH 2.8 8.3 8.2 9.4
环节一:请同学们以小组为单位,根据流程图设计问题。
环节二:我是小小审题专家,对小组展示的问题进行审核评价。
环节三:我是答卷人,对审核后的问题进行解答!
变式拓展----我能行
同课章节目录
