2023—2024学年人教版化学九年级下册第八单元 金属和金属材料 基础训练题(含答案)
文档属性
| 名称 | 2023—2024学年人教版化学九年级下册第八单元 金属和金属材料 基础训练题(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 436.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-25 00:00:00 | ||
图片预览




文档简介
2023—2024学年人教版化学九年级下册第八单元 金属和金属材料 基础训练题(含答案)
一、选择题。
1、我们的生活离不开金属材料,下列金属材料的使用,主要是利用其导热性的是( )
A.铂金戒指 B.铜导线 C.铁制门把手 D.不锈钢炒锅
2、下列关于“金属之最”的说法中正确的是( )
A.硬度最高的金属是铁 B.目前,世界年产量最高的金属是铝
C.导电性最好的金属是钨 D.熔点最低的金属是汞
3、高铁车厢使用的铝合金材料属于( )
A.合成材料 B.金属材料 C.天然材料 D.复合村料
4、有A,B两种金属分别放入等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,下列结论合理的是( )
A.金属活动性A>B B.生成氢气的质量A>B
C.反应的硫酸质量A<B D.反应的金属质量A<B
5、铁在海水中容易生锈,通常在轮船的吃水线以下焊接比铁更活泼的金属块,用于保护铁质船壳。该金属块的材料可以是 ( )
A.金 B.银 C.铜 D.锌
6、钯(Pd)是一种稀有的贵金属,钯镍合金在电子工业等有广泛应用。已知钯、铜、镍三种金属的活动性强弱顺序是Ni>Cu>Pd,下列可以验证三者金属活动性强弱的实验组合是( )
A.①③ B.①② C.②④ D.③④
7、下列关于生铁和钢的说法中错误的是( )
A.钢的性能比生铁优越
B.将生铁和钢加入足量的稀硫酸中可全部溶解
C.生铁与钢的性能有很大的差别,主要是由于生铁和钢中的含碳量不同
D.生铁可以通过铁矿石冶炼制得
8、金属资源与社会生活密切相关。下列说法正确的是( )
A.不能用特种塑料代替金属制造机器的零部件,这样会影响机器的寿命
B.回收利用一个铝质易拉罐的成本比新造一个要高,所以不用回收
C.回收利用废旧电池中的铅、汞等可减少对环境的污染
D.有效防止金属制品锈蚀是保护金属资源的唯一途径
9、下列关于资源、能源的叙述正确的是( )
A.地球上的总水储量很大,且淡水约占全球水储量的96.5%
B.空气是一种宝贵的资源,其中稀有气体的体积分数约为78%
C.防止金属的腐蚀是保护金属资源的唯一途径
D.人们正在利用和开发许多其他能源,如氢能、太阳能、生物质能等
10、分类法在科学研究中具有广泛的应用.下列说法正确的是( )
A. 铝、银均属于金属单质,它们都能与稀硫酸反应
B. 金刚石和石墨都是由碳元素组成的单质,它们的原子排列方式相同
C. 盐酸、硫酸均属于酸,它们都能使紫色石蕊试液变红
D. 一氧化碳、三氧化硫均属于非金属氧化物,它们都能与氢氧化钠溶液反应
11、化学是你,化学是我,化学深入我们的生活。下列说法或做法正确的是( )
A.鱼、虾能在水中生存仅利用了氧气的物理性质
B.焊接金属时可用氧气作保护气,使焊接更牢固
C.为增加节日氛围,大量燃放烟花爆竹
D.将稀有气体制成多种用途的电光源,如航标灯、霓虹灯
12、下列与金属材料有关的说法中,正确的是( )
A.常温下所有的金属都是固体
B.钢是纯净物,生铁是混合物
C.银的导电性比铜、铝都好,所以最好常用银制作电线
D.铝合金被广泛用于火箭、飞机、轮船等制造业
13、在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出的固体中滴加稀盐酸,没有气泡产生.下列判断正确的是( )
A.滤出的固体中一定含有铜,可能含有铁和镁
B.滤出的固体一定含有铜和铁,一定不含镁
C.滤液中一定含有氯化镁和氯化亚铁,可能含有氯化铜
D.滤液中一定含有氯化镁、氯化亚铁、氯化铜
14、随着人们生活质量的不断提高,废电池必须集中处理的问题被提上议事日程,其主要原因是( )
A.可以卖钱,增加经济收入
B.回收电池中的石墨
C.防止电池中汞、镉和铅等金属离子对土壤和水源的污染
D.利用电池外壳的金属材料
15、现有甲、乙、丙、丁四种颗粒大小相同的金属,分别投入相同的稀硫酸中,只有甲、乙表面有气泡产生,且甲产生气泡较快;再把丙和丁投入相同的硝酸银溶液中,过一会儿,丙的表面有银析出,而丁没变化,则四种金属的活动性顺序是( )
A. 甲>乙>丙>丁 B. 丁>乙>丙>甲
C. 丙>乙>丁>甲 D. 乙>甲>丁>丙
16、化学趣味小组在学习了金属的化学性质后,对金属R的活动性进行探究发现:将金属R放入稀盐酸中,观察到有气泡产生(该反应的化学方程式可表示为:R+2HCl=RCl2+H2↑),将R放入ZnSO4溶液中无任何变化。下列化学方程式书写错误的是( )
A.R+MgSO4=RSO4+Mg B.R+CuSO4=RSO4+Cu
C.R+H2SO4=RSO4+H2↑ D.2Al+3RSO4=Al2(SO4)3+3R
二、填空题。
17、人类最早大规模利用的金属是________,然后是_______。
【答案】铜 铁
18、全国很多城市都已经开通了地铁,迈入了地铁线网时代,下图为地铁列车图。回答下列问题:
(1)图中所示材料中,属于金属材料的是 钢(或钛合金)(填一种即可)塑料。
(2)冶炼钛时,将铁矿石转化为下TiCl4,TiCl4再与Na在一定条件下置换反应生成Ti,请写出后一步反应的化学方程式(不要求标出反应条件):
TiCl4+4Na=Ti+4NaCl 。
19、铁锈的主要成分是________,将一枚生锈的铁钉放入足量的稀盐酸中,你首先观察到的现象是________,过一会儿,你还可以观察到的现象是________请写出有关反应的化学方程式________ 。
20、常见的金属有铜、铁、铝,写出下列反应的化学方程式。
(1)在加热或点燃的条件下,它们与O2反应:
(2)与稀硫酸的反应:
(3)与盐酸的反应:
(4)与硫酸铜溶液的反应:
21、在Fe2O3+3CO2Fe+3CO2的反应中,Fe2O3发生了 反应,其中还原剂是 。
三、综合应用题。
22、高铁是中国制造的代表。
(1)建筑铁路所需的大量钢铁是以铁矿石为主要原料冶炼而得。写出用一氧化碳和赤铁矿(主要成分是氧化铁)炼铁的化学方程式 。
(2)防止铁轨生锈的措施有 (写一条)。
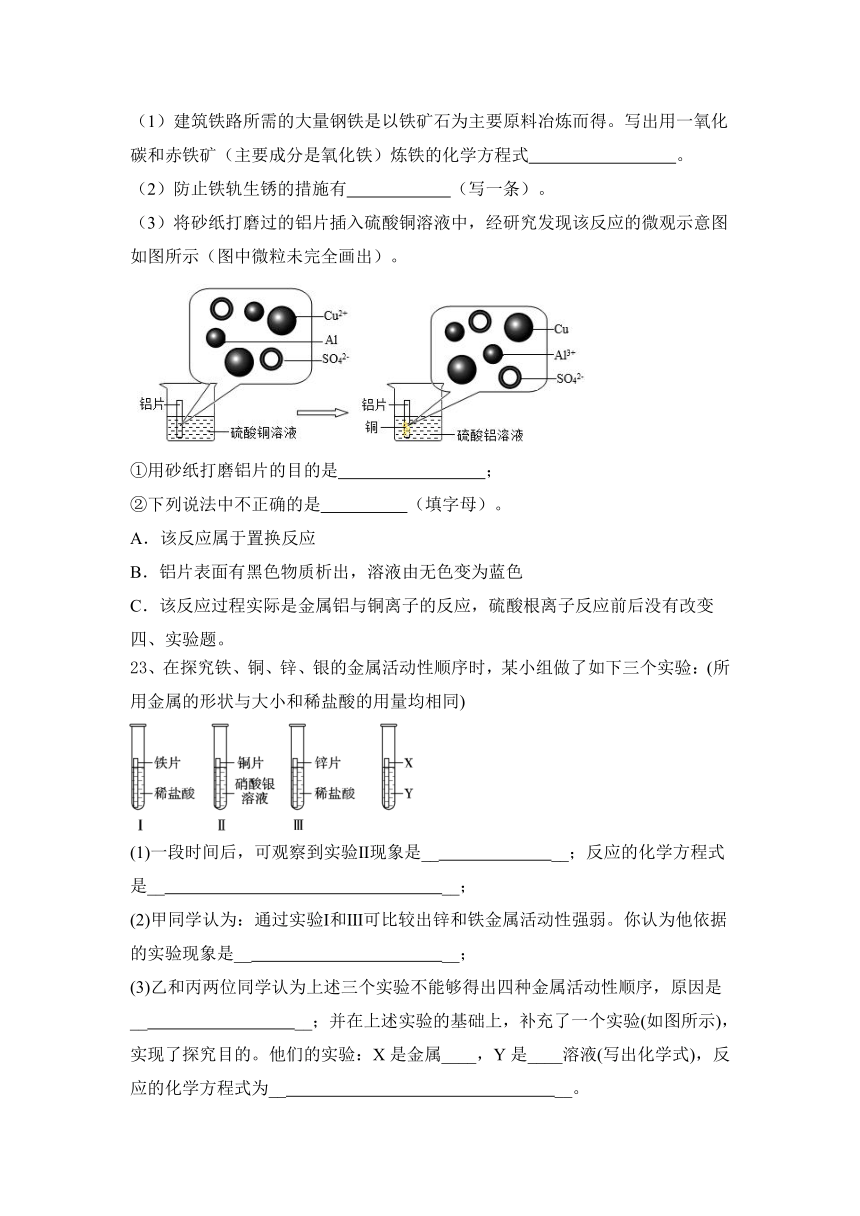
(3)将砂纸打磨过的铝片插入硫酸铜溶液中,经研究发现该反应的微观示意图如图所示(图中微粒未完全画出)。
①用砂纸打磨铝片的目的是 ;
②下列说法中不正确的是 (填字母)。
A.该反应属于置换反应
B.铝片表面有黑色物质析出,溶液由无色变为蓝色
C.该反应过程实际是金属铝与铜离子的反应,硫酸根离子反应前后没有改变
四、实验题。
23、在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:(所用金属的形状与大小和稀盐酸的用量均相同)
(1)一段时间后,可观察到实验Ⅱ现象是__ __;反应的化学方程式是__ __;
(2)甲同学认为:通过实验Ⅰ和Ⅲ可比较出锌和铁金属活动性强弱。你认为他依据的实验现象是__ __;
(3)乙和丙两位同学认为上述三个实验不能够得出四种金属活动性顺序,原因是__ __;并在上述实验的基础上,补充了一个实验(如图所示),实现了探究目的。他们的实验:X是金属____,Y是____溶液(写出化学式),反应的化学方程式为__ __。
24、进行如下实验,研究金属的性质。补全实验报告。
序号 操作或装置 现象 结论或解释
(1) 黄铜片在纯铜片表面刻画出明显痕迹 黄铜的硬度比纯铜 (填“大”或“小”)
(2) 铁的金属活动性比铜强
(3) 。 A、B中均无明显变化,C中铁钉表面有红色固体生成 铁与氧气和水同时接触时易生锈
五、计算题。
25、将铁粉和铜粉混合物10.0 g投入盛100.0 g稀盐酸(足量)的烧杯中,充分反应后,称得剩余物质的总质量为109.8 g,求:
(1)生成氢气的质量是多少克;
(2)该混合物中铜粉的质量分数。
2023—2024学年人教版化学九年级下册第八单元 金属和金属材料 基础训练题(含答案)
一、选择题。
1、我们的生活离不开金属材料,下列金属材料的使用,主要是利用其导热性的是( )
A.铂金戒指 B.铜导线 C.铁制门把手 D.不锈钢炒锅
【答案】D
2、下列关于“金属之最”的说法中正确的是( )
A.硬度最高的金属是铁 B.目前,世界年产量最高的金属是铝
C.导电性最好的金属是钨 D.熔点最低的金属是汞
【答案】D
3、高铁车厢使用的铝合金材料属于( )
A.合成材料 B.金属材料 C.天然材料 D.复合村料
【答案】B
4、有A,B两种金属分别放入等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,下列结论合理的是( )
A.金属活动性A>B B.生成氢气的质量A>B
C.反应的硫酸质量A<B D.反应的金属质量A<B
【答案】B
5、铁在海水中容易生锈,通常在轮船的吃水线以下焊接比铁更活泼的金属块,用于保护铁质船壳。该金属块的材料可以是 ( )
A.金 B.银 C.铜 D.锌
【答案】D
6、钯(Pd)是一种稀有的贵金属,钯镍合金在电子工业等有广泛应用。已知钯、铜、镍三种金属的活动性强弱顺序是Ni>Cu>Pd,下列可以验证三者金属活动性强弱的实验组合是( )
A.①③ B.①② C.②④ D.③④
【答案】A
7、下列关于生铁和钢的说法中错误的是( )
A.钢的性能比生铁优越
B.将生铁和钢加入足量的稀硫酸中可全部溶解
C.生铁与钢的性能有很大的差别,主要是由于生铁和钢中的含碳量不同
D.生铁可以通过铁矿石冶炼制得
【答案】B
8、金属资源与社会生活密切相关。下列说法正确的是( )
A.不能用特种塑料代替金属制造机器的零部件,这样会影响机器的寿命
B.回收利用一个铝质易拉罐的成本比新造一个要高,所以不用回收
C.回收利用废旧电池中的铅、汞等可减少对环境的污染
D.有效防止金属制品锈蚀是保护金属资源的唯一途径
【答案】C
9、下列关于资源、能源的叙述正确的是( )
A.地球上的总水储量很大,且淡水约占全球水储量的96.5%
B.空气是一种宝贵的资源,其中稀有气体的体积分数约为78%
C.防止金属的腐蚀是保护金属资源的唯一途径
D.人们正在利用和开发许多其他能源,如氢能、太阳能、生物质能等
【答案】D
10、分类法在科学研究中具有广泛的应用.下列说法正确的是( )
A. 铝、银均属于金属单质,它们都能与稀硫酸反应
B. 金刚石和石墨都是由碳元素组成的单质,它们的原子排列方式相同
C. 盐酸、硫酸均属于酸,它们都能使紫色石蕊试液变红
D. 一氧化碳、三氧化硫均属于非金属氧化物,它们都能与氢氧化钠溶液反应
【答案】C
11、化学是你,化学是我,化学深入我们的生活。下列说法或做法正确的是( )
A.鱼、虾能在水中生存仅利用了氧气的物理性质
B.焊接金属时可用氧气作保护气,使焊接更牢固
C.为增加节日氛围,大量燃放烟花爆竹
D.将稀有气体制成多种用途的电光源,如航标灯、霓虹灯
【答案】D
12、下列与金属材料有关的说法中,正确的是( )
A.常温下所有的金属都是固体
B.钢是纯净物,生铁是混合物
C.银的导电性比铜、铝都好,所以最好常用银制作电线
D.铝合金被广泛用于火箭、飞机、轮船等制造业
【答案】D
13、在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出的固体中滴加稀盐酸,没有气泡产生.下列判断正确的是( )
A.滤出的固体中一定含有铜,可能含有铁和镁
B.滤出的固体一定含有铜和铁,一定不含镁
C.滤液中一定含有氯化镁和氯化亚铁,可能含有氯化铜
D.滤液中一定含有氯化镁、氯化亚铁、氯化铜
【答案】C
14、随着人们生活质量的不断提高,废电池必须集中处理的问题被提上议事日程,其主要原因是( )
A.可以卖钱,增加经济收入
B.回收电池中的石墨
C.防止电池中汞、镉和铅等金属离子对土壤和水源的污染
D.利用电池外壳的金属材料
【答案】C
15、现有甲、乙、丙、丁四种颗粒大小相同的金属,分别投入相同的稀硫酸中,只有甲、乙表面有气泡产生,且甲产生气泡较快;再把丙和丁投入相同的硝酸银溶液中,过一会儿,丙的表面有银析出,而丁没变化,则四种金属的活动性顺序是( )
A. 甲>乙>丙>丁 B. 丁>乙>丙>甲
C. 丙>乙>丁>甲 D. 乙>甲>丁>丙
【答案】A
16、化学趣味小组在学习了金属的化学性质后,对金属R的活动性进行探究发现:将金属R放入稀盐酸中,观察到有气泡产生(该反应的化学方程式可表示为:R+2HCl=RCl2+H2↑),将R放入ZnSO4溶液中无任何变化。下列化学方程式书写错误的是( )
A.R+MgSO4=RSO4+Mg B.R+CuSO4=RSO4+Cu
C.R+H2SO4=RSO4+H2↑ D.2Al+3RSO4=Al2(SO4)3+3R
【答案】A
二、填空题。
17、人类最早大规模利用的金属是________,然后是_______。
【答案】铜 铁
18、全国很多城市都已经开通了地铁,迈入了地铁线网时代,下图为地铁列车图。回答下列问题:
(1)图中所示材料中,属于金属材料的是 钢(或钛合金)(填一种即可)塑料。
(2)冶炼钛时,将铁矿石转化为下TiCl4,TiCl4再与Na在一定条件下置换反应生成Ti,请写出后一步反应的化学方程式(不要求标出反应条件):
TiCl4+4Na=Ti+4NaCl 。
【答案】(1)钢(或钛合金); (2)TiCl4+4Na=Ti+4NaCl;
19、铁锈的主要成分是________,将一枚生锈的铁钉放入足量的稀盐酸中,你首先观察到的现象是________,过一会儿,你还可以观察到的现象是________请写出有关反应的化学方程式________ 。
【答案】氧化铁;溶液由无色变成黄色;产生气泡;
Fe2O3+6HCl═2FeCl3+3H2O,Fe+2HCl═FeCl2+H2↑
20、常见的金属有铜、铁、铝,写出下列反应的化学方程式。
(1)在加热或点燃的条件下,它们与O2反应:
(2)与稀硫酸的反应:
(3)与盐酸的反应:
(4)与硫酸铜溶液的反应:
【答案】(1)Cu+O22CuO、3Fe+2O2Fe3O4、
4Al+3O22Al2O3。
(2)Fe+H2SO4===FeSO4+H2↑、2Al+3H2SO4===Al2(SO4)3+3H2↑。
(3)Fe+2HCl===FeCl2+H2↑、2Al+6HCl===2AlCl3+3H2↑。
(4)Fe+CuSO4===FeSO4+Cu、2Al+3CuSO4===Al2(SO4)3+3Cu。
21、在Fe2O3+3CO2Fe+3CO2的反应中,Fe2O3发生了 反应,其中还原剂是 。
【答案】还原 一氧化碳(或CO)
三、综合应用题。
22、高铁是中国制造的代表。
(1)建筑铁路所需的大量钢铁是以铁矿石为主要原料冶炼而得。写出用一氧化碳和赤铁矿(主要成分是氧化铁)炼铁的化学方程式 。
(2)防止铁轨生锈的措施有 (写一条)。
(3)将砂纸打磨过的铝片插入硫酸铜溶液中,经研究发现该反应的微观示意图如图所示(图中微粒未完全画出)。
①用砂纸打磨铝片的目的是 ;
②下列说法中不正确的是 (填字母)。
A.该反应属于置换反应
B.铝片表面有黑色物质析出,溶液由无色变为蓝色
C.该反应过程实际是金属铝与铜离子的反应,硫酸根离子反应前后没有改变
【答案】(1)Fe2O3+3CO2Fe+3CO2;
(2)刷漆(答案合理即可);
(3)①除去铝片表面的氧化膜; ②B。
四、实验题。
23、在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:(所用金属的形状与大小和稀盐酸的用量均相同)
(1)一段时间后,可观察到实验Ⅱ现象是__ __;反应的化学方程式是__ __;
(2)甲同学认为:通过实验Ⅰ和Ⅲ可比较出锌和铁金属活动性强弱。你认为他依据的实验现象是__ __;
(3)乙和丙两位同学认为上述三个实验不能够得出四种金属活动性顺序,原因是__ __;并在上述实验的基础上,补充了一个实验(如图所示),实现了探究目的。他们的实验:X是金属____,Y是____溶液(写出化学式),反应的化学方程式为__ __。
【答案】(1)铜片表面有银白色固体析出,溶液由无色变为蓝色
Cu+2AgNO3===2Ag+Cu(NO3)2
(2)锌与酸反应的程度要比铁剧烈
(3)无法比较铁与铜的活动性 Fe CuSO4
Fe+CuSO4 ===FeSO4+Cu
24、进行如下实验,研究金属的性质。补全实验报告。
序号 操作或装置 现象 结论或解释
(1) 黄铜片在纯铜片表面刻画出明显痕迹 黄铜的硬度比纯铜 (填“大”或“小”)
(2) 铁的金属活动性比铜强
(3) 。 A、B中均无明显变化,C中铁钉表面有红色固体生成 铁与氧气和水同时接触时易生锈
【答案】大;铁片表面有气泡产生溶液变为浅绿色,铜片无现象;如图所示:
五、计算题。
25、将铁粉和铜粉混合物10.0 g投入盛100.0 g稀盐酸(足量)的烧杯中,充分反应后,称得剩余物质的总质量为109.8 g,求:
(1)生成氢气的质量是多少克;
(2)该混合物中铜粉的质量分数。
【答案】(1)0.2g (2)混合物中铜粉的质量分数为44.0%。
一、选择题。
1、我们的生活离不开金属材料,下列金属材料的使用,主要是利用其导热性的是( )
A.铂金戒指 B.铜导线 C.铁制门把手 D.不锈钢炒锅
2、下列关于“金属之最”的说法中正确的是( )
A.硬度最高的金属是铁 B.目前,世界年产量最高的金属是铝
C.导电性最好的金属是钨 D.熔点最低的金属是汞
3、高铁车厢使用的铝合金材料属于( )
A.合成材料 B.金属材料 C.天然材料 D.复合村料
4、有A,B两种金属分别放入等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,下列结论合理的是( )
A.金属活动性A>B B.生成氢气的质量A>B
C.反应的硫酸质量A<B D.反应的金属质量A<B
5、铁在海水中容易生锈,通常在轮船的吃水线以下焊接比铁更活泼的金属块,用于保护铁质船壳。该金属块的材料可以是 ( )
A.金 B.银 C.铜 D.锌
6、钯(Pd)是一种稀有的贵金属,钯镍合金在电子工业等有广泛应用。已知钯、铜、镍三种金属的活动性强弱顺序是Ni>Cu>Pd,下列可以验证三者金属活动性强弱的实验组合是( )
A.①③ B.①② C.②④ D.③④
7、下列关于生铁和钢的说法中错误的是( )
A.钢的性能比生铁优越
B.将生铁和钢加入足量的稀硫酸中可全部溶解
C.生铁与钢的性能有很大的差别,主要是由于生铁和钢中的含碳量不同
D.生铁可以通过铁矿石冶炼制得
8、金属资源与社会生活密切相关。下列说法正确的是( )
A.不能用特种塑料代替金属制造机器的零部件,这样会影响机器的寿命
B.回收利用一个铝质易拉罐的成本比新造一个要高,所以不用回收
C.回收利用废旧电池中的铅、汞等可减少对环境的污染
D.有效防止金属制品锈蚀是保护金属资源的唯一途径
9、下列关于资源、能源的叙述正确的是( )
A.地球上的总水储量很大,且淡水约占全球水储量的96.5%
B.空气是一种宝贵的资源,其中稀有气体的体积分数约为78%
C.防止金属的腐蚀是保护金属资源的唯一途径
D.人们正在利用和开发许多其他能源,如氢能、太阳能、生物质能等
10、分类法在科学研究中具有广泛的应用.下列说法正确的是( )
A. 铝、银均属于金属单质,它们都能与稀硫酸反应
B. 金刚石和石墨都是由碳元素组成的单质,它们的原子排列方式相同
C. 盐酸、硫酸均属于酸,它们都能使紫色石蕊试液变红
D. 一氧化碳、三氧化硫均属于非金属氧化物,它们都能与氢氧化钠溶液反应
11、化学是你,化学是我,化学深入我们的生活。下列说法或做法正确的是( )
A.鱼、虾能在水中生存仅利用了氧气的物理性质
B.焊接金属时可用氧气作保护气,使焊接更牢固
C.为增加节日氛围,大量燃放烟花爆竹
D.将稀有气体制成多种用途的电光源,如航标灯、霓虹灯
12、下列与金属材料有关的说法中,正确的是( )
A.常温下所有的金属都是固体
B.钢是纯净物,生铁是混合物
C.银的导电性比铜、铝都好,所以最好常用银制作电线
D.铝合金被广泛用于火箭、飞机、轮船等制造业
13、在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出的固体中滴加稀盐酸,没有气泡产生.下列判断正确的是( )
A.滤出的固体中一定含有铜,可能含有铁和镁
B.滤出的固体一定含有铜和铁,一定不含镁
C.滤液中一定含有氯化镁和氯化亚铁,可能含有氯化铜
D.滤液中一定含有氯化镁、氯化亚铁、氯化铜
14、随着人们生活质量的不断提高,废电池必须集中处理的问题被提上议事日程,其主要原因是( )
A.可以卖钱,增加经济收入
B.回收电池中的石墨
C.防止电池中汞、镉和铅等金属离子对土壤和水源的污染
D.利用电池外壳的金属材料
15、现有甲、乙、丙、丁四种颗粒大小相同的金属,分别投入相同的稀硫酸中,只有甲、乙表面有气泡产生,且甲产生气泡较快;再把丙和丁投入相同的硝酸银溶液中,过一会儿,丙的表面有银析出,而丁没变化,则四种金属的活动性顺序是( )
A. 甲>乙>丙>丁 B. 丁>乙>丙>甲
C. 丙>乙>丁>甲 D. 乙>甲>丁>丙
16、化学趣味小组在学习了金属的化学性质后,对金属R的活动性进行探究发现:将金属R放入稀盐酸中,观察到有气泡产生(该反应的化学方程式可表示为:R+2HCl=RCl2+H2↑),将R放入ZnSO4溶液中无任何变化。下列化学方程式书写错误的是( )
A.R+MgSO4=RSO4+Mg B.R+CuSO4=RSO4+Cu
C.R+H2SO4=RSO4+H2↑ D.2Al+3RSO4=Al2(SO4)3+3R
二、填空题。
17、人类最早大规模利用的金属是________,然后是_______。
【答案】铜 铁
18、全国很多城市都已经开通了地铁,迈入了地铁线网时代,下图为地铁列车图。回答下列问题:
(1)图中所示材料中,属于金属材料的是 钢(或钛合金)(填一种即可)塑料。
(2)冶炼钛时,将铁矿石转化为下TiCl4,TiCl4再与Na在一定条件下置换反应生成Ti,请写出后一步反应的化学方程式(不要求标出反应条件):
TiCl4+4Na=Ti+4NaCl 。
19、铁锈的主要成分是________,将一枚生锈的铁钉放入足量的稀盐酸中,你首先观察到的现象是________,过一会儿,你还可以观察到的现象是________请写出有关反应的化学方程式________ 。
20、常见的金属有铜、铁、铝,写出下列反应的化学方程式。
(1)在加热或点燃的条件下,它们与O2反应:
(2)与稀硫酸的反应:
(3)与盐酸的反应:
(4)与硫酸铜溶液的反应:
21、在Fe2O3+3CO2Fe+3CO2的反应中,Fe2O3发生了 反应,其中还原剂是 。
三、综合应用题。
22、高铁是中国制造的代表。
(1)建筑铁路所需的大量钢铁是以铁矿石为主要原料冶炼而得。写出用一氧化碳和赤铁矿(主要成分是氧化铁)炼铁的化学方程式 。
(2)防止铁轨生锈的措施有 (写一条)。
(3)将砂纸打磨过的铝片插入硫酸铜溶液中,经研究发现该反应的微观示意图如图所示(图中微粒未完全画出)。
①用砂纸打磨铝片的目的是 ;
②下列说法中不正确的是 (填字母)。
A.该反应属于置换反应
B.铝片表面有黑色物质析出,溶液由无色变为蓝色
C.该反应过程实际是金属铝与铜离子的反应,硫酸根离子反应前后没有改变
四、实验题。
23、在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:(所用金属的形状与大小和稀盐酸的用量均相同)
(1)一段时间后,可观察到实验Ⅱ现象是__ __;反应的化学方程式是__ __;
(2)甲同学认为:通过实验Ⅰ和Ⅲ可比较出锌和铁金属活动性强弱。你认为他依据的实验现象是__ __;
(3)乙和丙两位同学认为上述三个实验不能够得出四种金属活动性顺序,原因是__ __;并在上述实验的基础上,补充了一个实验(如图所示),实现了探究目的。他们的实验:X是金属____,Y是____溶液(写出化学式),反应的化学方程式为__ __。
24、进行如下实验,研究金属的性质。补全实验报告。
序号 操作或装置 现象 结论或解释
(1) 黄铜片在纯铜片表面刻画出明显痕迹 黄铜的硬度比纯铜 (填“大”或“小”)
(2) 铁的金属活动性比铜强
(3) 。 A、B中均无明显变化,C中铁钉表面有红色固体生成 铁与氧气和水同时接触时易生锈
五、计算题。
25、将铁粉和铜粉混合物10.0 g投入盛100.0 g稀盐酸(足量)的烧杯中,充分反应后,称得剩余物质的总质量为109.8 g,求:
(1)生成氢气的质量是多少克;
(2)该混合物中铜粉的质量分数。
2023—2024学年人教版化学九年级下册第八单元 金属和金属材料 基础训练题(含答案)
一、选择题。
1、我们的生活离不开金属材料,下列金属材料的使用,主要是利用其导热性的是( )
A.铂金戒指 B.铜导线 C.铁制门把手 D.不锈钢炒锅
【答案】D
2、下列关于“金属之最”的说法中正确的是( )
A.硬度最高的金属是铁 B.目前,世界年产量最高的金属是铝
C.导电性最好的金属是钨 D.熔点最低的金属是汞
【答案】D
3、高铁车厢使用的铝合金材料属于( )
A.合成材料 B.金属材料 C.天然材料 D.复合村料
【答案】B
4、有A,B两种金属分别放入等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,下列结论合理的是( )
A.金属活动性A>B B.生成氢气的质量A>B
C.反应的硫酸质量A<B D.反应的金属质量A<B
【答案】B
5、铁在海水中容易生锈,通常在轮船的吃水线以下焊接比铁更活泼的金属块,用于保护铁质船壳。该金属块的材料可以是 ( )
A.金 B.银 C.铜 D.锌
【答案】D
6、钯(Pd)是一种稀有的贵金属,钯镍合金在电子工业等有广泛应用。已知钯、铜、镍三种金属的活动性强弱顺序是Ni>Cu>Pd,下列可以验证三者金属活动性强弱的实验组合是( )
A.①③ B.①② C.②④ D.③④
【答案】A
7、下列关于生铁和钢的说法中错误的是( )
A.钢的性能比生铁优越
B.将生铁和钢加入足量的稀硫酸中可全部溶解
C.生铁与钢的性能有很大的差别,主要是由于生铁和钢中的含碳量不同
D.生铁可以通过铁矿石冶炼制得
【答案】B
8、金属资源与社会生活密切相关。下列说法正确的是( )
A.不能用特种塑料代替金属制造机器的零部件,这样会影响机器的寿命
B.回收利用一个铝质易拉罐的成本比新造一个要高,所以不用回收
C.回收利用废旧电池中的铅、汞等可减少对环境的污染
D.有效防止金属制品锈蚀是保护金属资源的唯一途径
【答案】C
9、下列关于资源、能源的叙述正确的是( )
A.地球上的总水储量很大,且淡水约占全球水储量的96.5%
B.空气是一种宝贵的资源,其中稀有气体的体积分数约为78%
C.防止金属的腐蚀是保护金属资源的唯一途径
D.人们正在利用和开发许多其他能源,如氢能、太阳能、生物质能等
【答案】D
10、分类法在科学研究中具有广泛的应用.下列说法正确的是( )
A. 铝、银均属于金属单质,它们都能与稀硫酸反应
B. 金刚石和石墨都是由碳元素组成的单质,它们的原子排列方式相同
C. 盐酸、硫酸均属于酸,它们都能使紫色石蕊试液变红
D. 一氧化碳、三氧化硫均属于非金属氧化物,它们都能与氢氧化钠溶液反应
【答案】C
11、化学是你,化学是我,化学深入我们的生活。下列说法或做法正确的是( )
A.鱼、虾能在水中生存仅利用了氧气的物理性质
B.焊接金属时可用氧气作保护气,使焊接更牢固
C.为增加节日氛围,大量燃放烟花爆竹
D.将稀有气体制成多种用途的电光源,如航标灯、霓虹灯
【答案】D
12、下列与金属材料有关的说法中,正确的是( )
A.常温下所有的金属都是固体
B.钢是纯净物,生铁是混合物
C.银的导电性比铜、铝都好,所以最好常用银制作电线
D.铝合金被广泛用于火箭、飞机、轮船等制造业
【答案】D
13、在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出的固体中滴加稀盐酸,没有气泡产生.下列判断正确的是( )
A.滤出的固体中一定含有铜,可能含有铁和镁
B.滤出的固体一定含有铜和铁,一定不含镁
C.滤液中一定含有氯化镁和氯化亚铁,可能含有氯化铜
D.滤液中一定含有氯化镁、氯化亚铁、氯化铜
【答案】C
14、随着人们生活质量的不断提高,废电池必须集中处理的问题被提上议事日程,其主要原因是( )
A.可以卖钱,增加经济收入
B.回收电池中的石墨
C.防止电池中汞、镉和铅等金属离子对土壤和水源的污染
D.利用电池外壳的金属材料
【答案】C
15、现有甲、乙、丙、丁四种颗粒大小相同的金属,分别投入相同的稀硫酸中,只有甲、乙表面有气泡产生,且甲产生气泡较快;再把丙和丁投入相同的硝酸银溶液中,过一会儿,丙的表面有银析出,而丁没变化,则四种金属的活动性顺序是( )
A. 甲>乙>丙>丁 B. 丁>乙>丙>甲
C. 丙>乙>丁>甲 D. 乙>甲>丁>丙
【答案】A
16、化学趣味小组在学习了金属的化学性质后,对金属R的活动性进行探究发现:将金属R放入稀盐酸中,观察到有气泡产生(该反应的化学方程式可表示为:R+2HCl=RCl2+H2↑),将R放入ZnSO4溶液中无任何变化。下列化学方程式书写错误的是( )
A.R+MgSO4=RSO4+Mg B.R+CuSO4=RSO4+Cu
C.R+H2SO4=RSO4+H2↑ D.2Al+3RSO4=Al2(SO4)3+3R
【答案】A
二、填空题。
17、人类最早大规模利用的金属是________,然后是_______。
【答案】铜 铁
18、全国很多城市都已经开通了地铁,迈入了地铁线网时代,下图为地铁列车图。回答下列问题:
(1)图中所示材料中,属于金属材料的是 钢(或钛合金)(填一种即可)塑料。
(2)冶炼钛时,将铁矿石转化为下TiCl4,TiCl4再与Na在一定条件下置换反应生成Ti,请写出后一步反应的化学方程式(不要求标出反应条件):
TiCl4+4Na=Ti+4NaCl 。
【答案】(1)钢(或钛合金); (2)TiCl4+4Na=Ti+4NaCl;
19、铁锈的主要成分是________,将一枚生锈的铁钉放入足量的稀盐酸中,你首先观察到的现象是________,过一会儿,你还可以观察到的现象是________请写出有关反应的化学方程式________ 。
【答案】氧化铁;溶液由无色变成黄色;产生气泡;
Fe2O3+6HCl═2FeCl3+3H2O,Fe+2HCl═FeCl2+H2↑
20、常见的金属有铜、铁、铝,写出下列反应的化学方程式。
(1)在加热或点燃的条件下,它们与O2反应:
(2)与稀硫酸的反应:
(3)与盐酸的反应:
(4)与硫酸铜溶液的反应:
【答案】(1)Cu+O22CuO、3Fe+2O2Fe3O4、
4Al+3O22Al2O3。
(2)Fe+H2SO4===FeSO4+H2↑、2Al+3H2SO4===Al2(SO4)3+3H2↑。
(3)Fe+2HCl===FeCl2+H2↑、2Al+6HCl===2AlCl3+3H2↑。
(4)Fe+CuSO4===FeSO4+Cu、2Al+3CuSO4===Al2(SO4)3+3Cu。
21、在Fe2O3+3CO2Fe+3CO2的反应中,Fe2O3发生了 反应,其中还原剂是 。
【答案】还原 一氧化碳(或CO)
三、综合应用题。
22、高铁是中国制造的代表。
(1)建筑铁路所需的大量钢铁是以铁矿石为主要原料冶炼而得。写出用一氧化碳和赤铁矿(主要成分是氧化铁)炼铁的化学方程式 。
(2)防止铁轨生锈的措施有 (写一条)。
(3)将砂纸打磨过的铝片插入硫酸铜溶液中,经研究发现该反应的微观示意图如图所示(图中微粒未完全画出)。
①用砂纸打磨铝片的目的是 ;
②下列说法中不正确的是 (填字母)。
A.该反应属于置换反应
B.铝片表面有黑色物质析出,溶液由无色变为蓝色
C.该反应过程实际是金属铝与铜离子的反应,硫酸根离子反应前后没有改变
【答案】(1)Fe2O3+3CO2Fe+3CO2;
(2)刷漆(答案合理即可);
(3)①除去铝片表面的氧化膜; ②B。
四、实验题。
23、在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:(所用金属的形状与大小和稀盐酸的用量均相同)
(1)一段时间后,可观察到实验Ⅱ现象是__ __;反应的化学方程式是__ __;
(2)甲同学认为:通过实验Ⅰ和Ⅲ可比较出锌和铁金属活动性强弱。你认为他依据的实验现象是__ __;
(3)乙和丙两位同学认为上述三个实验不能够得出四种金属活动性顺序,原因是__ __;并在上述实验的基础上,补充了一个实验(如图所示),实现了探究目的。他们的实验:X是金属____,Y是____溶液(写出化学式),反应的化学方程式为__ __。
【答案】(1)铜片表面有银白色固体析出,溶液由无色变为蓝色
Cu+2AgNO3===2Ag+Cu(NO3)2
(2)锌与酸反应的程度要比铁剧烈
(3)无法比较铁与铜的活动性 Fe CuSO4
Fe+CuSO4 ===FeSO4+Cu
24、进行如下实验,研究金属的性质。补全实验报告。
序号 操作或装置 现象 结论或解释
(1) 黄铜片在纯铜片表面刻画出明显痕迹 黄铜的硬度比纯铜 (填“大”或“小”)
(2) 铁的金属活动性比铜强
(3) 。 A、B中均无明显变化,C中铁钉表面有红色固体生成 铁与氧气和水同时接触时易生锈
【答案】大;铁片表面有气泡产生溶液变为浅绿色,铜片无现象;如图所示:
五、计算题。
25、将铁粉和铜粉混合物10.0 g投入盛100.0 g稀盐酸(足量)的烧杯中,充分反应后,称得剩余物质的总质量为109.8 g,求:
(1)生成氢气的质量是多少克;
(2)该混合物中铜粉的质量分数。
【答案】(1)0.2g (2)混合物中铜粉的质量分数为44.0%。
同课章节目录
